Обзор литературы
Резюме
В обзоре освещена подробная информация об исторических шагах, которые прошла нейрохирургия для того, чтобы лечить болезнь Паркинсона (БП). В статье описаны методики, принятые в начале попыток хирургии двигательных расстройств, также после изобретения и начала применения стереотаксиса на людях. Также рассказано о людях, внесших неоценимый вклад в развитие стереотаксической и функциональной нейрохирургии.
Ключевые слова: стереотаксическая хирургия, история нейрохирургии, болезнь Паркинсона.
Фундамент хирургического лечения двигательных расстройств была заложен во второй половине XIX века. Концепция локализации активности коры головного мозга была основана на исследованиях электрической стимуляции Fritsch и Hitzig, а также клинических наблюдениях Jackson о потери двигательных и чувствительных функций при патологии коры и Broca с аналогичными исследованиями выпадения речи. Функция базальных ганлиев не была исследована из-за сложностей экспериментальных манипуляций на субкортикальных структурах [1].
Первым нейрохирургом, кто решился оперировать двигательные расстройства был сэр Виктор Горслей (SirVictorHorsley) из Национального госпиталя неврологии и нейрохирургии, Лондон, Великобритания. Он предполагал, что атетоз может быть вызван патологическим процессом во фронтальной коре, в связи с чем предпринял попытку удаления зоны коры, соматотопически связанной с вовлеченной конечностью. В 1890 году он выполнил первую кортикальную абляцию для лечения атетоза [2]. В 1909 году он успешно оперировал 15-летнего пациента с геми-атетозом, удалив часть прецентральной извилины, ценой апраксии и гемипареза [3].
В 1932 году Бьюси (Bucy) и Буханан (Buchanan) опубликовали результаты серии операций по удалению первичной моторной коры и окружающих тканей для лечения хореоатетоза. Они получили стойкий послеоперационный эффект [4]. Немного позже Bucy утверждал о возможности лечения тремора путем пересечения пирамидных путей, несмотря на то, что в послеоперационном периоде наблюдался выраженный неврологический дефицит [5]. В 1937 году Поленов пересек пирамидные волокна во внутренней капсуле [6].
В 1933 году Путнам (Putnam) пересек проприоцептивные пути, выполнив постеролатеральнуюхордотомию с целью уменьшения хореоатетоза с меньшим риском [7]. В 1937 году Н.Н. Бурденко предложил пересекать руброспинальные и покрышечные пути в продолговатом мозге [8]. Уокер (Walker) в 1949 году предложил рассекать ножку мозга для лечения экстрапирамидных расстройств [9].
Особую роль в истории хирургии двигательных расстройств занимает американский нейрохирург из Университета Айовы Рассел Мейерс (RusselMeyers), который проанализировав ранние исследования Dendy [10], произвел удачную экстирпацию головки хвостатого ядра трансвентрикулярным доступом пациенту с болезнью Паркинсона в 1939 году. Он был воодушевлен данным случаем и разработал сложный нестереотаксический межполушарный и трансвентрикулярный доступ для рассечения ansaventricularis в основании бледного шара, который он
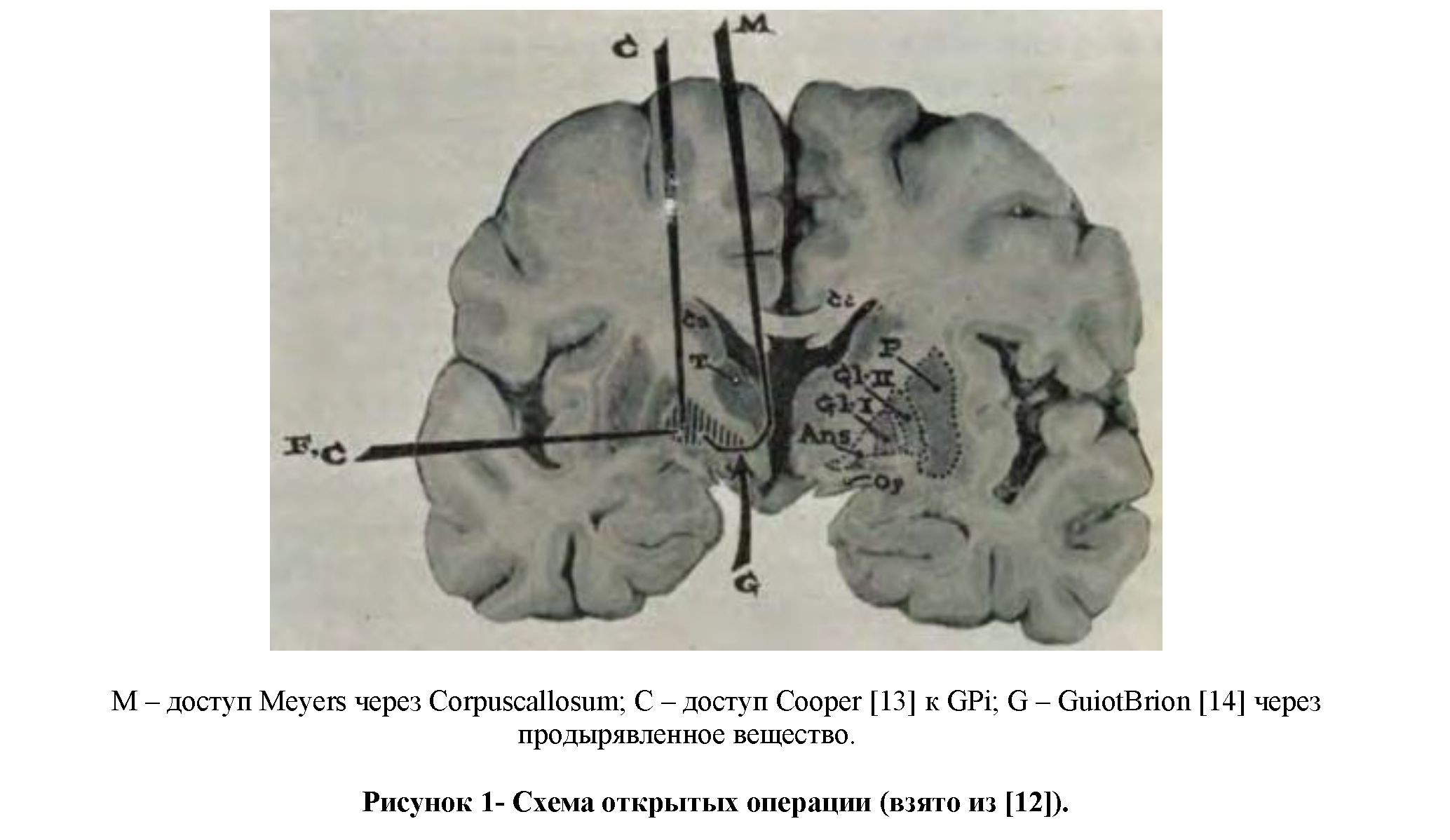
опубликовал в 1942 году [11]. Появилось четкое понимание, что прерывание в экстрапирамидной системе может помочь пациентам с двигательными расстройствами, особенно с болезнью Паркинсона (Рисунок 1). Из-за того, что в то время не было другой альтернативы, данная хирургия была довольно распространенной, но в последующем запрещенной самим Мейерсом из-за высокого уровня летальности (15,6%) [12].
Большой вклад в развитие хирургии двигательных расстройств внес американский нейрохирург Ирвин Купер (IrvingCooper). Во время проведения педункулотомии по Уолкеру по поводу болезни Паркинсона, он ненароком повредил переднюю хороидальную артерию, вследствие чего он заклипировал артерию и завершил операцию. Пациент проснулся с значительным уменьшением симптомов и отсутствием какого-либо дефицита. Купер опубликовал этот случай в 1953 году [15]. Он пришел к заключению, что в этом случае произошел инсульт в зоне, где образуются паркинсонические симптомы.
Основываясь на этом наблюдении, он стал проводить химиопаллидотомию алкоголем [16]. Он не использовал стереотаксическую технику, а методику, которая была основана ни на Декартовых координатах, ни на мозговой локализации. Траектория проходила через височную долю в верхнюю часть паллидума. После гибели одного пациента от других причин, было произведено вскрытие места процедуры и было выявлено, что на самом деле деструкция была в вентролатеральном таламусе, который был предложен Хасслером и Райхартом ранее. Купер опубликовал в 1958 году довольно широкую серию из 700 пациентов [17], которая к 1960 году увеличилась до 1000 человек [18]. В 1961 году Купер внедрил деструкцию криозондом, что значительно уменьшало побочные эффекты, которые возникали от применения химических реагентов [19].
Однако, по мнению некоторых исследователей, несмотря на большое число проведенных операций, исследования Cooper отличались поверхностным анализом данных, нестандартизирован- ным подходом к результатам, низким уровнем подтверждения таргета, ненаучным подходом к оценке результатов лечения. Все это привело к некоторому снижению его репутации, несмотря на его колоссальный труд по популяризации хирургии двигательных расстройств [1].
Стереотаксическая хирургия берет свое начало в 1908 году, когда Сэр Виктор Горслей (SirViktorHorsley) и Роберт Кларк (RobertClark) представили свой новый аппарат, который позволял вводить датчики, электроды, иглы под точным контролем в субкортикальные структуры обезьян или других экспериментальных животных. Они приспособили Декартовую систему координат, которая позволила им определить точку в пространстве, используя три координаты: передне-заднюю, латеральную и вертикальную [20].
Сэр Виктор Горслей (Рисунок 2) был нейрохирургом и нейрофизиологом, и обычно представляется отцом основателем функциональной нейрохирургии человека. Он работал совместно с Робертом Кларком, математиком и хирургом, который был вовлечен в работу по созданию стереотаксического аппарата.
Дизайн и математические расчеты аппарата были проведены Кларком, а детали использования его в практике были разработаны Горслеем (Рисунок 3). Первый отчет об экспериментальном использовании аппарата был посвящен электролитной деструкции зубовидного ядра мозжечка обезьян для исследования его структуры и функции.
В 1908 году вышла данная статья, содержащая великолепные иллюстрации. Статья была разделена на 4 части. В первой части описывался первый стереотаксический аппарат для животных, который остается основой для всех современных стереотаксических аппаратов. Также впервые описывался принцип применения Декартовых координат. Вторая часть статьи посвящена технике применения стереотаксического атласа в системе Декартовых координат и принципы определения стереотаксических координат каждой отдельной структуры. Третья часть посвящена технике проведения электролитной абляции, а четвертая непосредственно эксперименту.
Кларк предложил Горслею использовать аппарат на людях. Однако оба ученых не осуществили эту идею в силу разных других разногласий, и идея применения стереотаксиса на людях была оставлена на будущее. В 1918 году инженер по фамилии Мюссен (Mussen), который был задействован в разработке аппарата Горслея-Кларка, разработал подобный аппарат для использования на людях. Однако нет никаких доказательств, что кто-либо из нейрохирургов применил его по назначению. Аппарат был найден на чердаке его дома спустя 60 лет после его конструкции, которую определили по газете, в которую он был завернут [21]. И только по прошествии почти 40 лет после первого опубликования концепции стереотаксиса, после того, как знания о физиологии человека стали достаточными, история с применением стереотаксиса продолжилась.
До внедрения стереотаксического аппарата Горслея-Кларка были попытки применения аппаратов для исследования головного мозга, но ни один из них не был основан на применении Декартовых координат.
Например, известна система, изобретенная Диттмаром в 1873 году, где использовался направляемый датчик для внедрения его в продолговатый мозг крыс с целью нейрофизиологических
 5 6исследований [22]. Также известен аппарат Зернова, который в 1989 году описал энцефаломер [23], который помогал локализовать кортикальные зоны, который был клинически применен Алтуховым спустя 2 года [24]. Он не был основан на Декартовых координатах и не был предназначен для локализации глубинных структур.
5 6исследований [22]. Также известен аппарат Зернова, который в 1989 году описал энцефаломер [23], который помогал локализовать кортикальные зоны, который был клинически применен Алтуховым спустя 2 года [24]. Он не был основан на Декартовых координатах и не был предназначен для локализации глубинных структур.
Проблему определения стабильных внутримозговых ориентиров, от которых могут быть точно вычислены те или иные анатомические структуры мозга стали активно изучать Эрнест Шпигель (ErnestA. Spiegel) и Генри Вайцис (Henry T. Wycis) (Рисунок 4). Шпигель был неврологом и нейрофизиологом, который эмигрировал из нацисткой Германии в TempleMedicalSchool в Филадельфии и работал там профессором Экспериментальной Неврологии. Вайцис начал работу в лаборатории Шпигеля, когда был еще студентом медицинского университета и их сотрудничество продолжалось в течение его нейрохирургической резидентуры и дальнейшей карьеры.
В 1947 году они доложили о первом использовании разработанного ими стереотаксического аппарата на людях [25]. Это было отличное время для развития стереотаксической хирургии. Префронтальная лоботомия была весьма популярной процедурой и проводилась в большинстве случаев до применения антипсихотической терапии, тем самым злоупотребляя ее применение. Поэтому одной из мотивационных причин развития стереотаксической хирургии было применение щадящих контролируемых лоботомий с низким риском нежелательного неврологического дефицита. Однако первое использование стереотаксической хирургии было при двигательных расстройствах, а применение в психохирургии было отложено на несколько лет.
Другой толчок был со стороны широко внедрявшейся в медицинскую практику применение интраоперационной рентгенографии с быстрой печатью. Проводимая вентрикулография была использована для определения внутримозговых ориентиров для последующего вычисления локализации любой структуры. Это позволило использовать мозговые ориентиры, расположенные возле третьего желудочка для вычисления трех координат, каждая из которых была основана на одной из трех Декартовых плоскостей. Локализация специфических структур головного мозга предполагает обращение к специальному стереотаксическому атласу, который был разработан ранее. Также немаловажным фактором для развития стереотаксической хирургии стало бурное развитие нейрофизиологии экстрапирамидной системы. Были выявлено, что большинство двигательных расстройств можно лечить, воздействуя на этот цикл.
За основу аппарата Шпигеля и Вайциса был взят аппарат Горслея-Кларка. Изначально были выбраны два внутримозговых ориентира: передняя комиссура и шишковидная железа и разработанный атлас был основан на расчетах между этими ориентирами и нужными целями.
 5 7
5 7
Использование передней и задней комиссур было начато гораздо позже французским нейрохирургом Талайрахом (Talairach) и его группой [26]. С некоторыми изменениями данная методика была принята большинством стереотаксических нейрохирургов.
При помощи стереотаксической техники стали проводить деструкции определенных участков головного мозга, задействованных в передачи двигательного импульса. Изначально деструкция производилась введением алкоголя, который теоретически был более применим для воздействия на нейроны нужного ядра. Однако распространение алкоголя была непрогнозируемым, поэтому стали применять тот же электролитный раствор, который применялся Горслеем и Кларком полвека назад. Также использовались другие техники, такие как введение масло-прокаина и масло-прокаин-воска [27,28], баллонные канюли, коагулирующие субстанции, механическое разрушение с помощью лейкотома [29.30], позже радиочастотный ток [31] и криозонды [32].
Стереотаксический аппарат для человека был впервые продемонстрирован в статье в журнале Science(25). Он состоял из аппратаГорслея-Кларка, монтированного на кольцо, которое фиксировалось на пластмассовый колпак, который изготавливался индивидуально для каждого пациента. Электрод мог двигаться в переднезаднем и поперечном направлениях и мог погружаться вглубь с помощью простого микропривода. Было произведено несколько модификаций аппарата, но к применению был допущена Модель V.
Первые стереотаксические случаи были паллидотомии для лечения хореи Хантингтона, потому что Шпигель и Вайцис первоначально сопротивлялись выполнять процедуру для лечения болезни Паркинсона, боясь, что гипокинезия, которая появлялась после экспериментальной паллидотомии могла ухудшить и акинезию при болезни Паркинсона. Первому человеку, которому была проведена стереотаксическая операция в 1947 году, провели деструкцию алкоголем одновременно бледного шара и дорзомедиального таламуса (Рисунок 5). Предполагалось прервать экстрапирамидную циркуляцию в бледном шаре и уменьшить эмоциональный фон, прервав таламические пути в лобную долю. Хотя пациент получил средний и временный эффект, это продемонстрировало, что пути могут быть прерваны с минимальным риском и хорошим улучшением двигательного контроля, облегчая насильственные движения. Пациент прожил 15 лет и Вайцис после его смерти провел посмертные исследования головного мозга и оплатил его похороны.
Оригинальный доклад Шпигеля и Вайциса завершался перечислением списка потенциальных показаний для стереотаксической хирургии. Авторами был сделан комментарий «последующее применение стереотаксической техники изучается. Это может быть прерывание спиноталамических тактов при некоторых видах боли, проведение деструкции бледного шара для лечения насильственных движений, электрокоагуляция Гассерова узла при трегименальной невралгии, удаление жидкости из патологических полостей, кистозных опухолей». Должно быть известно, что Шпигель был очень секретным человеком и боялся, что кто-нибудь украдет его идею и разовьет ее первым, поэтому он особо не распространялся о нем. Очевидно, что они выполняли новую процедуру при всех перечисленных показаниях до первой их публикации.
Хасслер (Hassler) и Райхарт (Reichart) опубликовали в 1954 году серию успешно проведенных вентролатеральных таламотомий для лечения болезни Паркинсона [33]. Это подстегнуло Шпигеля и Вайциса проводить деструкцию ansalenticularis, в том месте, где она выходит из бледного шара, которую они назвали паллидо-анзотомией [34]. Нарабаяши (Narabayashi) и Окума (Okuma) в то же время проводили инъекции прокаина и масла в бледный шар [27].
Наиболее частое показание для стереотаксической хирургии стала болезнь Паркинсона. Это было до эпохи леводопы, поэтому медикаментозное лечение было весьма малоэффективным. Соответственно, пациенты направлялись к нейрохирургу в более раннем этапе заболевания, но симптомы были гораздо выраженные. Брадикинезия, как симптом более поздней стадии болезни, встречался реже, нежели тремор, как первичный симптом. Не было таких симптомов, как леводопа- индуцированная дискинезия, а пациенты конца 60-х годов выглядели совсем по-другому, нежели пациенты нашего времени.
Первая декада после внедрения стереотаксической нейрохирургии было весьма продуктивной. Большой поток нейрохирургов со всего мира направлялись к Шпигелю и Вайцису в TempleMedicalSchool в Филадельфию для освоения новой методики. Они возвращались домой, разрабатывали и производили новые собственные стереотаксические аппараты. Было внедрено много новых аппаратов. Среди них один из самых известных был разработан Ларсом Лекселлом (LarsLeksell) в 1948 году после возвращения из Филадельфии домой в Швецию [35]. Бэйли и Штайн (BaileyandStein) в США представили аппарат, крепящийся к трефинационному отверстию [36], Нарабаяши (Narabayashi) из Японии несколько усовершенствовал систему Шпигеля и Вайциса [37].
В первую декаду после рождения стереотаксической хирургии много нейрохирургических центров стали заниматься данной процедурой. Лекселл в Швеции [35], Талайрах с коллегами во Франции [26], Райхерт и Мундингер (ReichertandMundinger) в Германии [38], Гиллингэм (Gillingham) в Великобритании, Лайтинен (Laitinen) и Тойвакка (Toivakka) в Финляндии [39], Росси (Rossi) в Италии, Бертанд (Bertand) и коллеги в Канаде, Веласко Суарес (VelascoSuarez) и Эскобедо (Escobedo) в Мексике, Обрадор (Obrador) в Испании [40], Бехтерева и Кандель в СССР [32] и ряд других. Каждый исследователь добавлял в метод что-то свое и тем самым метод развивался быстро и качественно. За 20 лет стереотаксическая хирургия распространилась практически по всему миру. Было подсчитано, что к 1965 году было произведено более 25000 стереотаксических процедур по всему миру, а к 1969 году количество составляло 37000.
Необходимость к взаимным коммуникациям среди стереотаксических нейрохирургов привело к созданию стереотаксического общества. Первый конгресс Международного Общества Исследований в Стереоэнцефалотомии, которое в последующем было переименовано в 1973 во Всемирное Общество Стереотаксической и Функциональной нейрохирургии, прошел в 1966 году, через 20 лет после первой стереотаксической процедуры на человеке [21].
Хаслер и Райхерт выявили, что таламус как таргет более практичный и что Vop рекомендован для лечения тремора и Voa для лечения ригидности. Это позволило Хаслеру разделить таламус на части, что помогло коррелировать результаты деструкций с клиническими результатами. Шпигель и Вайцис все еще предпочитали паллидотомию как таргет и в 1958 году выявили, что деструкиция заднего паллидума более эффективно для лечения ригидности, чем на границе с ansalenticularis [41]. Исследования шведских нейрохирургов (Svennilson) также подтвердили эту догадку, что привело к вентропостеропаллидотомии [42].
В 1961 году Альбе-Фессард (Albe-Fessard) предложил использовать микроэлектродрекординг для уточнения положения цели [43].
Как таламотомия, так и паллидотомия были популярны для лечения дистоний. Результаты были более вариабельные, чем при паркинсонизме, но более чем 50% пациентов с генерализованной и цервикальной дистонией получали улучшение.
Все изменилось в 1968 году, когда в широкую практику поступила леводопа. В течение нескольких месяцев количество оперируемых пациентов с болезнью Паркинсона сократилось в разы. Также значительно уменьшилось количество функциональных нейрохирургов. Их осталось несколько человек, которые занимались дельнейшими исследованиями в специальных академических центрах.
Однако, в начале 80-х годов мировая медицинская общественность пришла к неутешительному выводу, что лечение леводопой не является решением проблемы лечения болезни Паркинсона. После длительного применения леводопы болезнь не только прогрессировала, но и вызывала побочные эффекты в виде рефрактерности лечения, появления дискинезий, флюктуаций. И на арену вновь вышла хирургия.
Стали появляться альтернативные методы хирургического лечения болезни Паркинсона. В 1985 году Баклунд (Backlund) с коллегами доложил результаты первого клинического исследования аутологической трансплантации ткани надпочечников в хвостатое ядро головного мозга двум пациентам [44]. Два года спустя, Мадразо (Madrazo) с коллегами доложил о двух пациентах и получил некоторые положительные результаты [45]. Позже он доложил 18 случаев лечения. Это привело к росту интереса к данной теме и несколько крупных лабораторий занялось этой проблемой. Однако, результаты оказались не столь впечатляющими, и большое количество побочных эффектов, привели к тому, что к 1991 году данная тема была полностью закрыта.
Идея трансплантации тканей продолжила свое существование, и вылилась в идею трансплантации фетальных клеток. В конце 80-х после проведения испытания на животных, Линдваллом (Lindvall) была проведено трансплантация двум пациентам c болезнью Паркинсона [46]. Далее были организованы межинституциональные исследования, но в связи со сложившимися многими проблемами, интерес к технологии стал идти на убыль.
Период затишья в функциональной нейрохирургии продолжался в 1970-1980 годах, за исключением длительных исследований по хирургии боли и эпилепсии. Немного проводились психохирургические операции, но совсем мало из-за появления новых психотропных препаратов и этических запретов.
В начале 90-х годов, стало наиболее очевидным, что успешная терапия болезни Паркинсона с помощью леводопы имеет ряд побочных эффектов, которые порой становятся более значимыми, чем сама болезнь. В связи с этим вновь встал вопрос об альтернативных методах лечения. И тогда возродился интерес к нейрохирургическому лечению болезни Паркинсона. Шведский нейрохирург Лайтинен (Laitinen), основываясь на технике Ларса Лекселла, Шпигеля и Вайциса, провел исследование положительного влияния паллидотомии на лечение симптомов болезни Паркинсона и осложнений леводопотерапии – лекарственной дискинезии, и в 1992 году опубликовал первую за последние два десятилетия статью [39]. Это был шаг к возврату к стереотаксической паллидотомии для лечения болезни Паркинсона. Уже стали использоваться современные методы визуализации, микроэлектродрекординг, что позволило более точно определять координаты. Первую «современную» паллидотомию в США провел Майкл Догали (MichaelDogali) из Нью-Йорка в декабре 1991 года, под руководством Латинена и Таскера (Tasker). В течение последующих 5 лет, паллидотомия стала весьма распространенной и популярной процедурой, также благодаря тому, что в нейрофизиологический мониторинг во время операций были задействованы неврологи, которые затем стали основными популяризаторами данного метода.
Первая хроническая стимуляция глубинных структур головного мозга для лечения болезни Паркинсона была выполнена в Институте экспериментальной медицины в Ленинграде в 1963 году под руководством Натальи Петровны Бехтеревой. Она назвала метод «терапевтической электростимуляцией», используя «электрическую высокочастотную сверхпороговую стимуляцию». В тот год она опубликовала работу по использованию нескольких имплантируемых электродов в субкортикальные структуры для лечения гиперкинезов [47]. Однако, из-за того, что статья была опубликована на русском языке, ее работа не была признана за рубежом. «Превосходные результаты исследований» были опубликованы в зарубежной литературе на английском языке в 1975 году [48]. Ее пациенты с болезнью Паркинсона приходили ежедневно в течение нескольких недель, все это время она наблюдала их и отмечала положительные результаты. Однако дальше исследования не пошли из-за отсутствия технологий имплантированных стимуляторов, а также возникших этических вопросов. Первый доклад о имплантированном нейростимуляторе для глубинной стимуляции головного мозга для лечения двигательных расстройств был сделан Брайс (Brice) и МакЛеллан (McLellan) в 1980 году [49]. Они использовали таламическую стимуляцию для лечения тремора при рассеянном склерозе.
В 1987 году французский нейрохирург Бенабид (Benabid) с соавторами описали подавление тремора у пациентов, которым была проведена хроническая таламическая стимуляция [50]. Длительный эффект от стимуляции VIM заключался в подавлению тремора, но не других паркинсонических симптомов, при этом доза допаминергической терапии не изменялась и качество жизни пациентов тоже. Тогда Зигфрид (Siegfried), Липиц (Lippitz), основываясь на работах Лайтинена предложили стимулировать бледный шар, что показало свою высокую эффективность в лечении, на ряду с тремором, брадикинезии, ригидности и дискинезий [51]. После изобретения методики моделирования паркинсонизма с помощью специальных химических веществ, в 1989 году были успешно проведены опыты на животных, используя субталамическое ядро как таргет для абляции. Основываясь на эти данные, Бенабид и его группа впервые предложила стимулировать субталамическое ядро при болезни Паркинсона и получила отличные результаты, опубликовав их в 1994 году, положив начало широкому применению данного метода во всем мире [52]. Метод стал называться Deepbrainstimulation (DBS).
В Соединенных Штатах Америки данный метод был утвержден Foodand Drug Administration и официально разрешен к применению в 2002 году. Таким образом, учитывая высокую эффективность метода, низкую вероятность осложнений, метод глубинной стимуляции стал прочно завоевывать позиции в лечении болезни Паркинсона.
Программа нейрохирургического лечения при двигательных расстройствах в Республике Казахстан существует с 2013 года, когда были произведены первые имплантации систем глубинной стимуляции головного мозга и аблятивные операции. Прооперировано более 200 пациентов с БП и другими двигательными расстройствами. За это время значительно продвинулся уровень оказания помощи пациентам с этой болезнью, собственный опыт диагностики и лечения позволил открыть первый Кабинет двигательных расстройств, что привело к новому и осмысленному взгляду на проблему лечения двигательных расстройств, включая БП в Республике Казахстан.
Дальнейшее развитие нейрохирургии БП и двигательных расстройств непрерывно связано с улучшением качества неврологической помощи пациентам, организацией непрерывного цикла диагностики, лечения, в том числе нейрохирургического, а также качественной нейрореабилитации, основанной на доказательной медицине. Открытие новых специализированных клиник в Казахстане по оказанию медицинской помощи пациентам с двигательными расстройствами позволит концентрировать больных у обученных специалистов, проводить тщательное обследование, наблюдение и качественный отбор на нейрохирургическое лечение.
Литература
- Bakay R. Movement Disorders Surgery. The Essentials. Thieme, 2009.
- Horsley V. remarks on the surgery of the central neurvous system. BMJ 1890; 2:1286-1292.
- Horsley V. The function fo so-called motor area of the brain. BMJ 1909; 2:125-132.
- Bucy PC, Buchanan DN. Athetosis. Brain 1932; 55:479-492.
- Bucy PC, Case TJ. Tremor. Physiologic mechanism and abolition by surgical means. Arch Neurol Psychiatry 1939; 41:721-746.
- Polenov AL. New developments in surgery of central neurvous system. VestnKhir 1937; 49:223227.
- Putnam TJ. Treatment of athetosis and dystonia by section of the extrapyramidal motor tracts. Arch Neurol Psychiatry 1933; 29:504-521.
- Burdenko NN, Klosovski BN, Bulbectomy, Report I: Ceasing of hyperkinetic phenomena by cutting the extrapyramidal tract in the medulla oblongata. VoprNeirokhir 1937; 1:5-16.
- Walker AE. Cerebral pedunculotomy for the relief of involuntary movement; hemiballismus. ActaPsichiatrNeurolScand 1979; 24:723-729.
- Dandy WE. Changes in our conceptions of localization of certain functions in the brain. Am J Physiol 1930; 93:643-7.
- Meyers R. The modification of alternating tremors, rigidity and festination by surgery of the basal ganglia. ResPubl Ass Res NervMent Dis 1942; 21:602-65.
- Meyers R. Historical background and personal experiences in the surgical relief of hyperkinesia and hypertonus. In: Fields W. ed. Pathogenesis and Treatment of Parkinsonism. Springfield, IL: Chas C Thomas; 1958:229-270.
- Cooper IS. Chemopallidectomy: an investigating technique in geriatric parkinsonians. Science 1955; 121:217.
- Guiot G, Brion S. Traitmentneurochirurgical de syndrome choreoathetosique et parkinsoniens. Sem Hop Paris 1952; 49:2095-2099.
- Cooper IS. Ligation of the anterior choroidal artery for involuntary movements of parkinsonism. Psychiat Quart 1953; 27:317-9.
- Cooper IS. Chemopallidectomy and chemothalamectomy for parkinsonism and dystonia. Proc R Soc Med 1959; 52:47-60.
- Cooper IS, Bravo GJ. Implications of a five year study of 700 basal ganglia operations. Neurology 1958; 8:701-17.
- Cooper IS. Results of 1000 consecutive basal ganglia operations for parkinsonism. Ann Intern Med 1960; 52:483-99.
- Cooper IS, St Lee AJ. Cryostatic congelation. J NervMent Dis 1961; 133:259-63.
- Horsley V, Clarke RH. The structure and functions of the cerebellum examined by a new method. Brain 1908; 31:45-124.
- Lozano A, GildenbergPh, Tasker R. eds. Textbook of Stereotactic and Functional Neurosurgery. Springer‐ Verlag Berlin Heidelberg 2009
- Dittmar C. Ueber die Lage des sogenanntenGefaesszentrums in der Medulla oblongata. BersaechsGesWiss Leipzig (Math Phys) 1873; 25:449-69.
- Zernov DN. Encephalometer. Device for estimation of parts of brain in human (Russian). Proc SocPhysicomed, Moscow Univ 1889; 2:70-80.
- Altukhov NV. Encephalometric investigations of the brain relative to the sex, age and skull indexes. Moscow; 1891.
- Spiegel EA, Wycis HT, Marks M, Lee AS. Stereotaxic apparatus for operations on the human brain. Science 1947; 106:349-50.
- Talairach J, He ́caen M, David M, Monnier M, Ajuriaguerra J. Recherches sur la coagulation therapeu- tique des structures sous-corticales chez l’homme. Rev Neurol 1949; 81:4-24.
- Narabayashi H, Okuma T. Procaine oil blocking of the globus pallidus for the treatment of rigidity and tremor of parkinsonism. Proc JpnAcad 1953; 29:310-8.
- Narabayashi H, Shimazu H, Fujita Y, et al. Procaine-oil-wax pallidotomy for double athetosis and spastic states in infantile cerebral palsy. Neurology 1960; 10:61-9.
- Guiot G, Pecker J. Tractotomiemesencephaliqueanterieure pour tremblementparkinsonien. Rev NeurolSuppl 1949; 1:387.
- Uchimura Y, Narabayashi H. Stereoencephalotom. PsychiatrNeurolJpn 1951; 52:265.
- Cosman ER, Nashold BS, Jr, Bedenbaugh P. Stereotactic radiofrequency lesion making. Appl Neurophysiol 1983; 46:160-6.
- Kandel EI. Experience with the cryosurgical method in production of lesions of the extrapyramidal system. confinneurol 1965; 26:306-9.
- Hassler R, Riechert T. Indikationen und Lokalisationsmethode der gezieltenHirnoperationen. Nervenarzt 1954; 25:441-7.
- Spiegel EA, Wycis HT, Baird HW, Long-range effects of electropallido-ansotomy in extrapyramidal and convulsive disorders. Neurology 1958; 8:734-40.
- Leksell L. A stereotaxic apparatus for intracerebral surgery. Actachirscand 1949; 99:229-33.
- Bailey P, Stein SN. A stereotaxic apparatus for use on the human brain. Atlantic City: AMA Scientific Exhibit; 1951.
- Narabayashi H. Stereotaxic instrument for operation on the human basal ganglia. PsychiatrNeurolJpn 1952; 54:669-71.
- Mundinger F, Riechert T. Die stereotaktischen Hirnoperationenzur Behandlungextrapyramidaler Bewegungssto ̈rungen (Parkinsonismus und Hyperkinesen) und ihreResultate. Postoperative und Langzeitergebnisse der stereo- taktischen Hirnoperationenbeiextrapyramidalmotorischen
Bewedunasstro ̈rungen. TeilB.Fortschr Neurol Psychiatr 1963; 31:69-120.
- Laitinen LV, Bergenheim AT, Hariz MI. Leksell’sposteroventralpallidotomy in the treatment of Parkinson’s disease. J Neurosurg 1992; 76:53-61.
- Obrador S. A simplified neurosurgical technique for approaching and damaging the region of the globus pallidus in Parkinson’s disease. J NeurolNeurosurgPsychiatr 1957; 20:47-9.
- Gildenberg Ph. The birth of stereotactic surgery: a personal retrospective Neurosurgery 54:198-208, 2004 DOI: 10.1227/01.NEU.0000100180.55117.3E
- Svennilson E, Torvik A, Lowe R, Leksell L. Treatment of parkinsonism by stereotactic thermolesions in the pallidal region. A clinical evaluation of 81 cases. ActaPsychiatrNeurolScand 1960; 35:358-77.
- Albe-Fessard D, Arfel G, Guiot G, et al. Identification et delimitation precise de certaines structures souscorticales de l’homme par l’electrophysiologie. cr acadsci (Paris) 1961; 243:2412-4.
- Backlund EO, Granberg PO, Hamberger B, et al. Transplantation of adrenal medullary tissue to striatum in parkinsonism. First clinical trials. J Neurosurg 1985; 62:169-73.
- Madrazo I, Drucker-Colin R, Diaz V. Open microsurgical autograft of adrenal medulla to the right caudate nucleus in two patients with intractable Parkinson’s disease. N Engl J Med 1987; 316:831-4.
- Lindvall O, Rehncrona S, Brundin P, et al. Human fetal dopamine neurons grafted into the striatum in two patients with severe Parkinson’s disease. A detailed account of methodology and a 6-month follow-up. Arch Neurol 1989; 46:615-31.
- Bechtereva NP, Bondarchuk AN, Smirnov VM. Therapeutic electrostimulations of the deep brain structures. VoprNeirokhir 1972; 1:7-12.
- Bechtereva NP, Bondartchuk AN, Smirnov VM, Meliutcheva LA, Shandurina AN. Method of electrostimulation of the deep brain structures in treatment of some chronic diseases. ConfinNeurol 1975; 37:136-40.
- Brice J, McLellan L. Suppression of intention tremor by contingent deep-brain stimulation. Lancet 1980; 1:1221-2.
- Benabid AL, Pollak P, Gervason C, Hoffmann D, Gao DM, Hommel M, Perret JE, de Rougemont J. Long-term suppression of tremor by chronic stimulation of the ventral intermediate thalamic nucleus. Lancet 1991; 337:403-6.
- Siegfried J, Lippitz B. Chronic electrical stimulation of the VL-VPL complex and of the pallidum in the treatment of movement disorders: personal experience since 1982. StereotactFunctNeurosurg 1994; 62:71-5.
- Benabid AL, Pollak P, Gross C, et al. Acute and long-term effects of subthalamic nucleus stimulation in Parkinson’s disease. StereotactFunctNeurosurg 1994; 62:76-84.