Введение. Одним из компонентов суммы экстрактивных веществ (от 2 до 5%) некоторых видов произрастающих в Средней Азии растений рода Lagochilus (семейство Губоцветные - Labiatae Juss) является дитерпеноидный спирт - лагохилин, C20H36O5. Кроме того, в этих растениях встречаются и его другие природные производные. Наличие в молекуле лагохилина четырёх гидроксильных групп позволяет на его основе синтезировать с альдегидами ацетальные. Так, с ацетоном лагохилин образует 3,18-О-изопопилиденлагохилин [1].
При изучении гемостатической активности 3,18-О-изопропилиденлагохилина ранее нами было установлено, что его модулирующее действие на свертывание крови связано с проявлением им мембранной активности в липидных бислоях [2].
Цель исследования. Целью исследования является изучение взаимодействия молекул 3,18- О-изопропилиденлагохилина с липидными системами из димиристоилфосфатидилхолина для получения подтверждения его встраивания в бислои при разных значениях pH среды методом дифференциальной сканирующей калориметрии.
Материалы и методы. Определение термодинамических параметров фазовых превращений мультиламеллярных дисперсий проводились на дифференциальном сканирующем микрокалориметре при скорости записи 1°С/мин. Мультиламеллярные бислои для
калориметрических измерений готовили высушиванием раствора липидов в спирте под вакуумом. Далее к высушенному остатку липидов добавлялся соответствующий буфер и необходимое количество исследуемого вещества. Температуры фазовых переходов определяли по положению максимумов соответствующих пиков с точностью до 0,02°С.
Результаты и обсуждения. Выбор димиристоилфосфатидилхолина в качестве липидной системы связан с тем, что он является основным структурообразующим компонентом липидного бислоя биологических мембран тромбоцитов, так как наружный слой этих кровяных клеток формируется в основном из димиристоилфосфатидилхолина при разных значениях pH среды [3].
При введении молекул 3,18-О-изопропилиденлагохилина в липидные бислои из димиристоилфосфатидилхолина при различных значениях pH (от 5 до 10), в термограмме плавления наблюдалась корреляционная трансформация температуры основного фазового перехода липида (рис. 1).
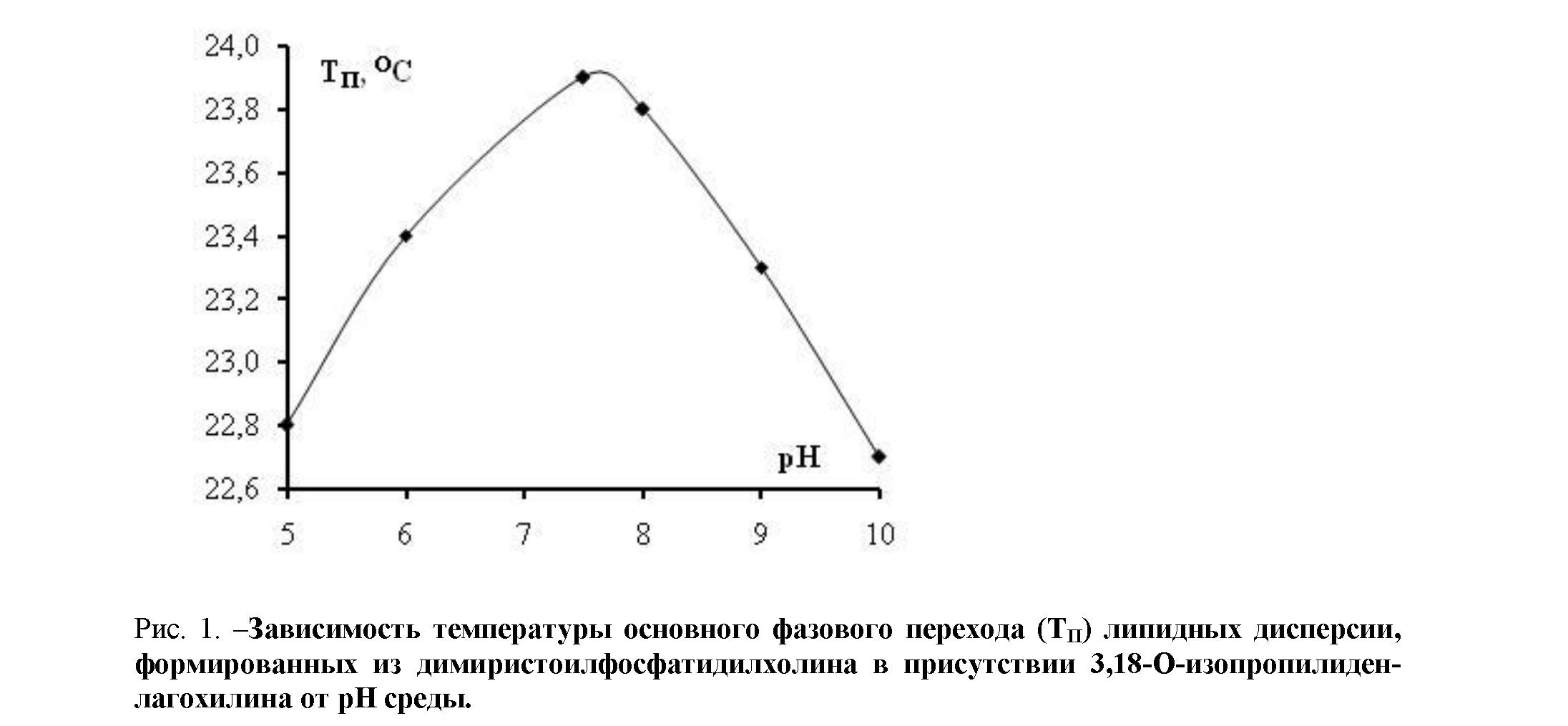
Как видно из рис. 1, максимальное значение температуры основного фазового перехода для димиристоилфосфатидилхолина в присутствии 3,18-О-изопропилиденлагохилина наблюдается при pH 7,5.
Вывод. Полученные результаты свидетельствует о том, что оптимальное взаимодействие молекул 3,18-О-изопропилиденлагохилина с липидными бислоями из димиристоилфосфатидилхолина происходит именно при значении pH среды 7,5.
Список литературы
- Косымбетов П.Г., Р.Х.Зиятдинова, С.В.Бессонова, Б.А.Салахутдинов, Дж.Зиямов, У.Н.Зайнутдинов, Т.Ф.Арипов. Ионофорные и комплексообразующие свойства производных лагохилина. /Химия природных соединений, 2004, №3, стр. 199-203.
- П.Г.Косымбетов, Д.С.Казанцева, Р.Х.Зиятдинова, Б.А.Салахутдинов, У.Н.Зайнутдинов, Т.Ф.Арипов. Влияние лагохилина и его производных на скорость свертывания оксалатной плазмы // Доклады АН РУз, 2006, №1, стр. 58-61.
- Ивков В.Г., Берестовский Г.Н. Липидный бислой биологических мембран. Москва, «Наука», 1982. 224 с.