АННОТАЦИЯ
В данной статье представлены результаты фармакокинетического исследования нового противотуберкулезного лекарственного средства тиозонида. Разработана методика определения препарата тиозонида в плазме крови человека методом ВЭЖХ с масс-селективным детектором. Методика была валидирована по следующим валидационным параметрам: специфичность, линейность, правильность, прецизионность, предел количественного определения, стабильность и перенос пробы. Аналитический диапазон методики составил 1-1000 нг/мл. Разработанная методика была применена для изучения фармакокинетики препарата тиозонида, капсулы 100 мг (ЗАО «Фарм-Синтез») при однократном пероральном приеме возрастающих доз различными группами здоровых добровольцев в рамках клинического исследования I фазы.
Цель исследования:провести разработку и валидацию методики определения инновационного противотуберкулезного препарата тиозонидав плазме крови с целью количественного определения тиозонидав плазме крови на стадии клинических и фармакокинетических исследований данного препарата.
Ключевые слова: тиозонид, ВЭЖХ-МС, валидация, фармакокинетика, плазма.
Туберкулез (ТБ) остается одной из основных проблем здравоохранения, не смотря на наличие эффективных методов противотуберкулезной терапии. Ключевыми барьерами на пути к улучшению исходов заболевания являются: длительность лечения (что приводит к снижению контроля за соблюдением терапии пациентами), сложные схемы лечения, которые включают дорогостоящие и токсичные препараты, выраженные токсические побочные эффекты при введении антиретровирусной терапии, и множественная лекарственная устойчивость [1-3].
Динамика основных эпидемиологических показателей по туберкулезу в России в течение последнего десятилетия свидетельствует об улучшении эпидемической ситуации, однако на фоне снижения заболеваемости и распространенности туберкулеза сохраняются негативные тенденции к дальнейшему росту лекарственно-устойчивых форм туберкулеза, сочетанных с другими сопутствующими заболеваниями. В настоящее время проблема туберкулеза в сочетании с ВИЧ- инфекцией является одной из самых актуальных[4,5]. В этих условиях становится очевидной необходимость разработки инновационных лекарственных препаратов для борьбы с устойчивыми штаммами микобактерий туберкулёза.
Материалы и методы. Проведена разработка и валидация методики определения противотуберкулезного препарата тиозонида в плазме крови. Тиозонид - {1R,2S + 1S,2R}-1-(6- Бром-2-хлорхинолил-3-ил)-4-(диметиламино)-2-(нафталин-1-ил)-1-фенилбутан-2-ол, субстанция- порошок (ЗАО «Фарм-Синтез», Россия). Пробоподготовку проводили путем осаждения белков ацетонитрилом. Количественное определение проводили методом ВЭЖХ с масс-селективным детектором.
Валидацию методики проводили согласно требованиям «Руководства по экспертизе лекарственных средств» под.ред. проф. А.Н. Миронова. Том I [6], а также на основании руководства по валидациибиоаналитических методик FDA [7] и EMA [8] по следующим характеристикам: селективность; линейность; правильность (на уровнях inter-day и intra-day); прецизионность (на уровнях inter-day и intra-day); предел количественного определения;- стабильность растворов; перенос пробы.
Селективность. Проводили анализ 9 образцов чистой плазмы, образца чистой плазмы с прибавлением стандартного растворатиозонида в диапазоне концентраций 1нг/мл - 1000 нг/мл. На хроматограммах образцов чистой плазмы не наблюдалось пиков со временем удерживания, соответствующим времени удерживания тиозонида.
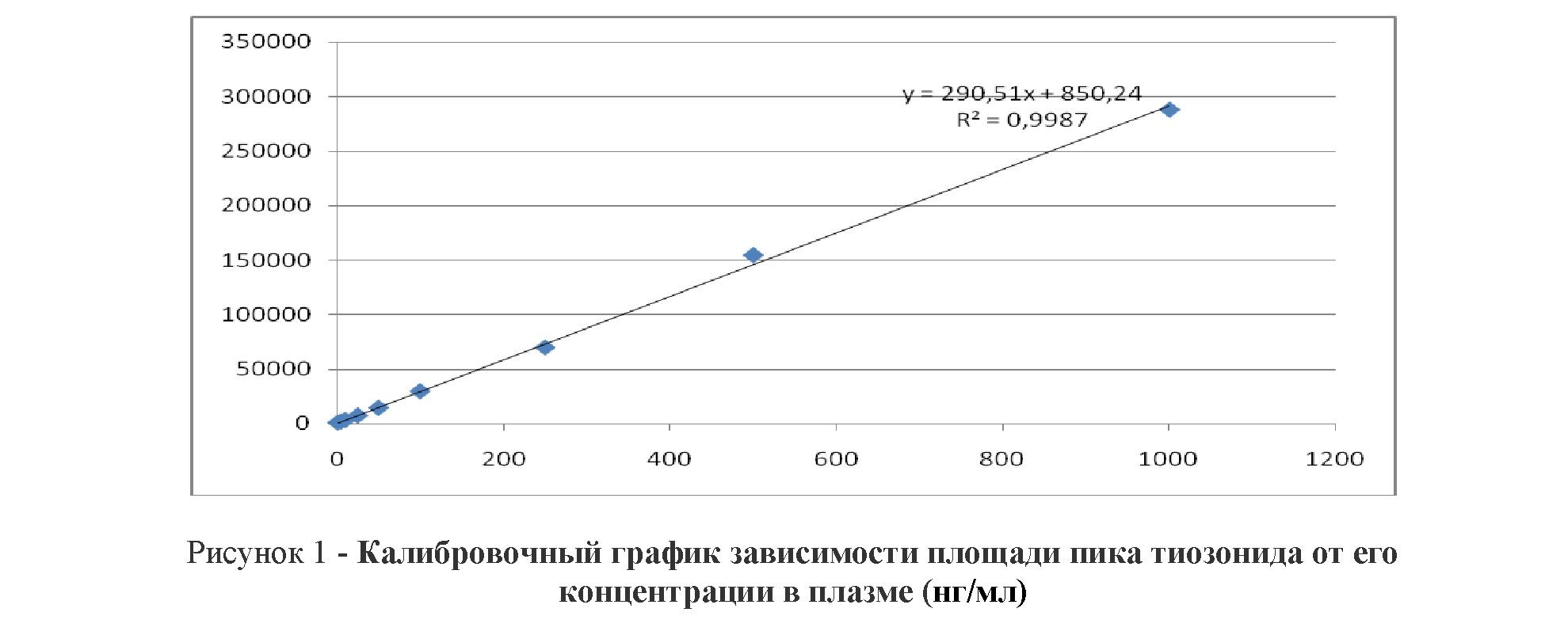
Линейность. Проводили анализ 9 образцов чистой плазмы с прибавлением раствора стандартного образца тиозонида до получения концентраций: 1 нг/мл, 5 нг/мл, 10 нг/мл, 25 нг/мл, 50 нг/мл, 100 нг/мл, 250 нг/мл, 500 нг/мл и 1000 нг/мл. По полученным значениям был построен калибровочный график (r2> 0,999) совместно с уравнением калибровочной кривой, представленные на рисунке 1.
Полученные отклонения соответствуют нормам FDA и EMA (не более 20 % для нижней точки линейности, не более 15 % - для остальных точек). Исходя из полученных данных, методику можно считать линейной в пределах от 1 нг/мл до 1000 нг/мл.
Правильность и прецизионность
Проводили анализ 4 отдельно приготовленных образцов чистой плазмы с прибавлением стандартного раствора тиозонида до получения концентраций: 1 нг/мл, 10 нг/мл, 100 нг/мл, 1000 нг/мл. Каждый раствор хроматографировали по 5 раз. Исследование проводили в течение 1-го дня (intra - day) и 2-го дня (inter-day). Для полученных значений концентраций были рассчитаны величины относительного стандартного отклонения (RSD, %) и относительной погрешности (е, %).
Полученные величины относительного стандартного отклонения (прецизионность) и относительной погрешности (правильность) соответствуют нормам FDA и EMA (не более 20 % для нижней точки линейности, не более 15 % - для остальных точек).
Предел количественного определения
Предел количественного определения (ПКО) методики на основании данных линейности, правильности и прецизионности. За ПКО методики принималась минимальная концентрация тиозонида в плазме, для которой возможно определение тиозонида со значениями RSD и е не более 20 % в диапазоне линейной зависимости. Предел количественного определения методики составил 1 нг/мл.
Хроматограмма, демонстрирующая ПКО методики, приведена на Рисунке 2.
Стабильность растворов
Стабильность была подтверждена для стандартных растворов тиозонида (при хранении раствора в течение 14 дней при температуре от 2 0 до 8 о С), кратковременная стабильность (для приготовленных проб в течение 24 и 48 ч при анализе на следующий день при температуре 15 оС), на уровнях концентраций 1 нг/ мл и 1000 нг/мл. Образцы выдерживали 3 цикла заморозки- разморозки. Площадь пика при повторных анализах не менялась более чем на 10 %.
Для исследования долговременной стабильности образцы плазмы на уровне концентрации 100 нг/мл были помещены в морозильник при температуре от -750 до -80о С для последующего анализа спустя 1 месяц после заморозки. Площадь пика при повторных анализах не менялась более чем на 10 %.
Перенос пробы
При последовательном вводе пробы с концентрацией тиозонида1000 нг/мл и чистой плазмы на хроматограмме чистой плазмы отсутствовали пики, соответствующие тиозониду. Перенос пробы отсутствовал.
Аналитический диапазон методики составил 1 нг/мл -1000 нг/мл тиозонида в плазме крови.
На основании разработанной методики проводили изучениефармакокинетики препарата тиозонид, капсулы 100 мг (ЗАО «Фарм-Синтез») при однократном пероральном приеме возрастающих доз различными группами здоровых добровольцев в рамках клинического
 98
98
исследования I фазы. В исследовании приняли участие4 группы добровольцев (по 10 добровольцев в каждой группе), которые принимали препарат в дозировке 25, 200, 400 и 600 мг.
Для каждого добровольца рассчитаны следующие фармакокинетические параметры: 1. Значения площади под кривыми "концентрация-время" (AUC0-t). 2. Максимальная концентрация в плазме (Стах). 3. Время достижения максимальной концентрации (tmax). 4. Общая площадь под кривой AUC0 -да. 5. Период полувыведения (ТУ). 6. Соотношение AUC0-t и AUCO-да. 8. Показатель скорости всасывания (Cmax/AUC0-t). 9. Константа элиминации (kel)
Результаты и обсуждения. В ходе биоаналитического исследования была проведена разработка и валидация (по параметрам: специфичность, линейность, правильность, прецизионность, предел количественного определения,стабильность, перенос пробы) методики определения тиозонида в плазме крови. Аналитический диапазон составил 1 нг/мл -1000 нг/мл.
Разработанная методика была применена для изучения фармакокинетики препарата Тиозонид, капсулы 100 мг (ЗАО «Фарм-Синтез»)при однократном пероральном приеме возрастающих доз различными группами здоровых добровольцев в рамках клинического исследования I фазы.
В результате данного фармакокинетического исследования были рассчитаны индивидуальные значения концентраций тиозонида в плазме крови во времени, а также индивидуальные и усредненные фармакокинетические параметры тиозонида, была показана линейность фармакокинетики препарата в интервале доз 25-600 мг. Сопоставление значений AUC0-168 с общим AUCO-да (их отношение составляло значительно больше 80%) свидетельствовало о том, что выбранный регламент фармакокинетического исследования обеспечивает необходимую надежность оценки фармакокинетических параметров тиозонида.
Период полувыведения составил 25 часов, что показывает медленное выведение препарата из плазмы крови. Согласно полученным данным было установлено, что тиозонид постепенно всасывался в системный кровоток при пероральном приеме (Tmax около 4,5 часа), а также определен возможный режим дозирования препарата 1-2 раза в сутки для изучения в последующих клинических исследованиях.
Выводы. Противотуберкулезные препараты, применяемые в настоящее время во всем мире, не решают всех проблем, существующих в сфере лечения туберкулеза. Всё это делает необходимым выведением на рынок новых противотуберклезных препаратов, способных расширить возможности для лечения больных туберкулезом с множественной лекарственной устойчивостью, повысить эффективность, сократить сроки лечения и снизить частоту нежелательных эффектов этиотропной терапии
СПИСОК ЛИТЕРАТУРЫ
- Доклад ВОЗ о глобальной борьбе с туберкулезом, 2013 г. URL: http://www.who.int/tb/publications/global_report/ru/
- Шилова М.В. Взгляд на эпидемическую ситуацию с туберкулезом в Российской Федерации (в современных социально-экономических условиях). REJR. 1. 2014: 34-41.
- Alimuddin I Zumla, Prof Stephen H Gillespie, Michael Hoelscher, Patrick P J Philips, Stewart T Cole, Ibrahim Abubakar, Timothy D McHugh, Marco Schito, Markus Maeurer, Prof Andrew J Nunn . New antituberculosis drugs, regimens, and adjunct therapies: needs, advances, and future prospects // The Lancet Infectious Diseases. - 2014. - Vol.14. - Issue 4. - P. 327 - 340.
- Мишин В.Ю. Диагностика и химиотерапия туберкулёза органов дыхания // Проблемы туберкулеза № 3. - 2005. - С. 47-64.
- Аминев Х.К., Бакиров А.А., Гольянова К.И., Аминев Э.Х. Влияние ВИЧ-инфекции на эпидемическую ситуацию по туберкулезу // Фтизиатрия и пульмонология № 1 (8). - 2014. - С. 1821.
- А.Н. Миронова (ред.), Руководство по экспертизе лекарственных средств, Т. I, Гриф и К, М.:Медицина, -2013.
- Guidance for Industry: Bioanalytical method validation. U.S. Department of Health and Human Services, Food and Drug Administration, Center for Drug Evolution and Research (CDER). U.S. Government Printing Office: Washington, DC, (2001).
- Guideline on validation of bioanalytical methods (draft).European Medicines Agency. Committeeformedicinalproducts for human use, London (2009).