АННОТАЦИЯ
Обьектом исследования является высокосернистой нефти Тенгизского месторождения. Хромотографический анализ водно-спиртовой вытяжки из такой серы и ИК-спектроскопия показали наличие в составе серы органических примесей. Исследования по предварительной обработке тенгизской серы различными реагентами, такими как - тиосульфатные растворы, спирты, растворы кислот и щелочей показали, что наиболее благоприятное воздействие на растворимость тенгизской серы оказывают разбавленные растворы гидроксида натрия. Предварительная обработка тенгизской серы 0,3%-ным раствором гидроксида натрия положительно сказывается на скорости реакции, что ускоряющее действие щелочи объясняется способностью гидроксид-ионов активировать атомы серы, с образованием промежуточных соединений - полисульфидов, легко отдающих серу сульфиту натрия. Органические примеси в составе тенгизской серы также оказывают катализирующее действие на процесс образования
тиосульфата натрия, снижая процесс окисления исходных сульфитных растворов, что подтверждается результатами исследований. Выход тиосульфата натрия из тенгизской серы при 60°С в 2-2,5 раза больше, чем из обычной серы. Содержание №^Оз в реакционной смеси в процессе взаимодействия с тенгизской серой уменьшается из-за его расходования, а рост концентрации сульфита натрия в смеси с элементной серой свидетельствует о ее плохой смачиваемости при температуре 60°С. Увеличение температуры до 75, 90°С значительно (в 1,5-2,0) раза увеличивает выход тиосульфата натрия. Полученный продукт, идентифицированный как пентагидрат сульфат натрия, отвечает требованиям ГОСТ 244-76 по высшему сорту.
Ключевые слова: сульфат натрия; гидроксид натрия, горючие сланцы, гипс, природный сера, пентагидрат, полисульфиды.
Введение. Продуктом очистки высокосернистого нефтегазового сырья Тенгизского месторождения является сера, в огромных количествах скопившаяся на месторождении и оказывающая вредное воздействие на окружающую среду [1]. Такая сера содержит следующие элементы и неорганические примеси масс.%: S (78,61), С (8,22), Н (1,95), N (-0,69), Ог (10,51), Сг (0,05), Si (0,01), Mg (0,001), Al (0,001), Си (0,0005), Fe (0,0005) и может быть использована для получения сульфата натрия и серной кислоты. Сера может быть использована в производстве искусственного волокна, сероуглерода, красителей, защитные средства растений, резинотехнических изделий, как промежуточный продукт в бумажной и текстильной промышленности [2].
Сера в природе выделяется из сульфатов, содержащихся в почве, при разложении белков выделяются соединения серы в виде сероводорода и меркаптанов, более 90% серы находится в угле, горючих сланцах и гипсе. Содержание серы в нефти и природном газе оценивается в 2х109 тонн, т.е. в пять раз больше, чем запасы природной серы [3].
Цель работы. Изучение растворимость серы в содо-сульфатном растворе и получение сульфата и тиосульфата натрия из серы Тенгизского месторождения.
Материалы и методы. В процессе изучение растворимости было использована реактивная сера марки «хч» и элементарная сера Тенгизского месторождения. Использование элементарную серу как отхода нефтехимической отрасли позволяет получить сульфат и тиосульфата натрия и сократить её накопления на Тенгизском газоконденсатном месторождении.
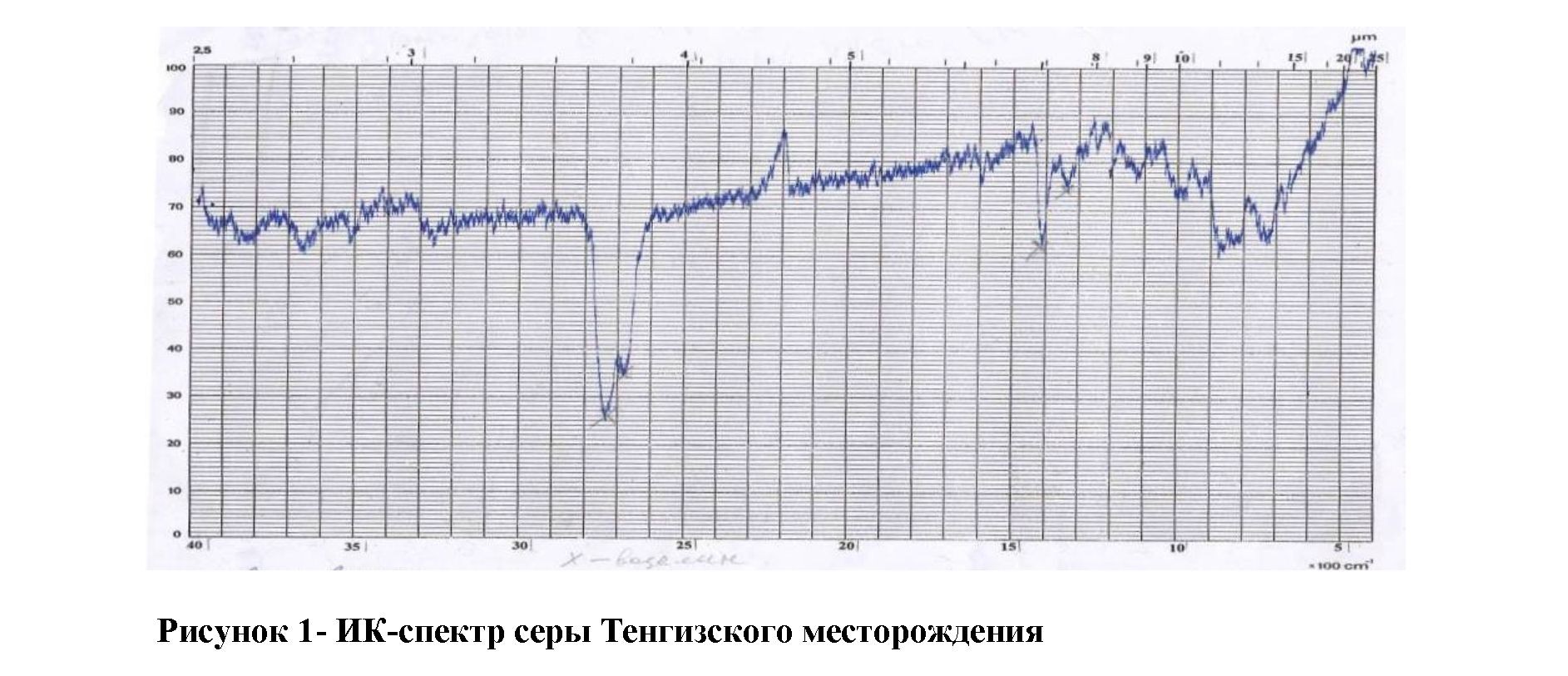
Результаты и их обсуждения. Предварительно проведенный хромотографический анализ водно-спиртовой вытяжки из тенгизской серы и ИК-спектроскопия показали наличие в составе серы органических примесей (1250, 1410 см-1), что видно из рисунка 1.
Исследован процесс взаимодействия сульфита натрия с серосодержащим продуктом - отходом сероочистки нефтегазового сырья Тенгизского месторождения (тенгизской серой) в сравнении с элементарной серой, марки «хч».
Растворимость серы в растворе сульфита натрия невысокая. Процесс взаимодействия сульфита натрия с серой состоит из двух этапов:
-первый характеризуется постепенным смачиванием серы и сопровождается медленным возрастанием скорости реакции;
-второй этап начинается, когда уже закончен процесс смачивания реагирующей серы и в сферу реакции вводится вся поверхность ее частиц.
На этой стадии реакция протекает с максимальной скоростью. Результаты исследования показали, что превращение элементарной серы в тиосульфат натрия возможно в присутствии раствора сульфита натрия.
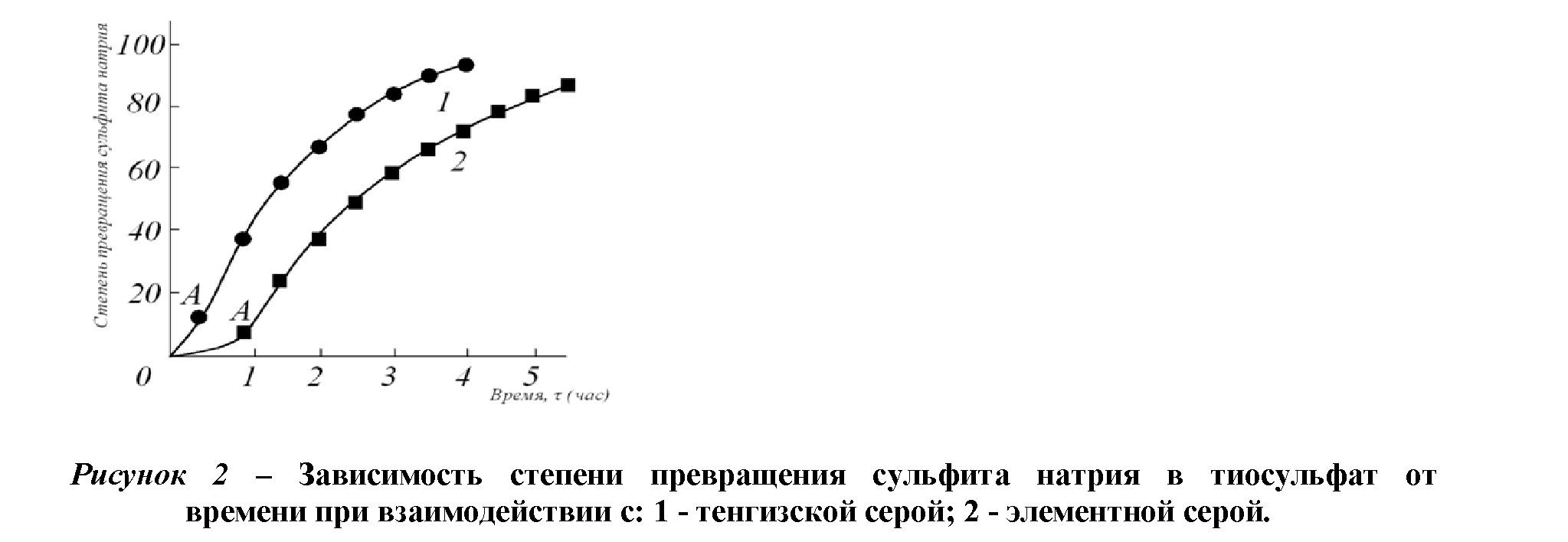
На рисунке 2 показана зависимость степени превращения Тенгизской (кривая 1) и элементарной (кривая 2) серы при взаимодействии с сульфитным раствором натрия.
Участок ОА соответствует первому периоду, второй период начинается в точке А. Из-за плохой смачиваемости Тенгизской серы водными растворами сульфита натрия реакция между ними протекает медленно.
Экспериментальные исследования по предварительной обработке тенгизской серы различными реагентами, такими как тиосульфатные растворы, спирты, растворы кислот и щелочей, показали, что наиболее благоприятное воздействие на растворимость тенгизской серы оказывают разбавленные растворы гидроксида натрия. Нами установлено, что предварительная обработка Тенгизской серы 0,3%-ным раствором гидроксида натрия положительно сказывается на скорости реакции. Ускоряющее действие щелочи объясняется способностью гидроксид-ионов активировать атомы серы, в результате чего образуются промежуточные соединения - полисульфиды, легко отдающие серу сульфиту натрия.
В начале происходит взаимодействие щелочи с серой 6S + 6NaOH = 2Na2S2 + Na2S2O3 + ЗН2О. Образующийся дисульфид Na2S2 способен легко отдавать один атом серы сульфиту натрия с образованием тиосульфата натрия: Na2S2 + Na2SO3= Na2S + Na2S2O3
Сульфид натрия активно взаимодействует кислородом и переходит в сульфат натрия по реакции: Na2S +2О2=№^О.-4.
Образовавшейся тиосульфат натрия при доступе кислорода взаимодействует с гидрооксидом натрия и образуют сульфат натрия 2NaOH + Na2S2O3 +1,5О2= 2Na2SO4 + Н2О
Отдавши серу, дисульфид превращается в сульфид, который затем растворяет новые количества серы и вновь отдает ее сульфиту с образованием тиосульфата. Следовательно, промежуточные соединения (Na2S и Na2S2) находятся в замкнутом цикле (кругообороте). В свою очередь, органические примеси в составе тенгизской серы также могут оказывать катализирующее действие на процесс образования тиосульфата натрия, снижая процесс окисления исходных сульфитных растворов. Это подтверждается результатами исследований процесса взаимодействия тенгизской и элементарной серы с раствором сульфита натрия. Стадия смачивания (участок ОА рисунок 1) у элементарной серы в (2-2,5) раза больше, чем у тенгизской серы. Анализ продуктов реакции взаимодействия, предварительно обработанных 0,3%-ным раствором гидроксида натрия тенгизской и элементной серы с сульфитом натрия при 60°С, 75°С и 90°С, показал присутствие в реакционной смеси тиосульфата, сульфита и бисульфита натрия (таблица1).
Выход тиосульфата натрия из тенгизской серы при 60°С в 2-2,5 раза больше, чем из обычной серы. Содержание №^О3 в реакционной смеси в процессе взаимодействия с тенгизской серой уменьшается из-за его расходования, а рост концентрации сульфита натрия в смеси с элементной серой свидетельствует о ее плохой смачиваемости при температуре 60°С. Увеличение температуры до 75, 90°С значительно (в 1,5-2,0) раза увеличивает выход тиосульфата натрия. При
 119
119
достижении 90°С улучшается смачивание элементной серы, что приводит к ее уменьшению в смеси.
Максимальное значение кажущейся энергии активации, рассчитанное по уравнению Аррениуса из зависимости выхода тиосульфата натрия от температуры в случае применения элементарной серы марки «х.ч.» равно 140,3 кДж/моль и 78,4 кДж/моль при использовании тенгизской серы с предварительной их обработкой 0,3%-ным раствором NaOH. Это свидетельствует о более высокой скорости растворения тенгизской серы в растворе сульфита натрия.
Таблица 1- Продукты реакции взаимодействия тенгизской серы с сульфитом натрия при 60, 75 и 90°С
|
Температ ура, °С |
Время.1 мин. |
С (Na2SO3), г/л |
C(Na2S2O3), г/л |
||
|
S тенгиз. |
S элем. |
S тенгиз |
S элем. |
||
|
1 |
2 |
3 |
4 |
5 |
6 |
|
60 |
10 |
173,46 |
160,12 |
17,94 |
7,17 |
|
25 |
142,33 |
163.09 |
30,49 |
9,86 |
|
|
50 |
133,43 |
212,01 |
35,87 |
11,66 |
|
|
75 |
136,39 |
186,81 |
35,87 |
12,11 |
|
|
100 |
137,88 |
216,46 |
41,25 |
13,45 |
|
|
125 |
137,88 |
183,84 |
50,67 |
17,94 |
|
|
150 |
136,39 |
209,05 |
56,05 |
20,18 |
|
|
75 |
10 |
160,12 |
148,88 |
28J5 |
26,20 |
|
25 |
170,49 |
123,05 |
47,98 |
43,50 |
|
|
50 |
148,26 |
105,26 |
58,29 |
52,60 |
|
|
75 |
203,12 |
97,85 |
56,05 |
51,70 |
|
|
100 |
212,08 |
106,74 |
- |
76,60 |
|
|
125 |
200,15 |
91,72 |
96,41 |
62,50 |
|
|
150 |
209,04 |
97,85 |
98,65 |
75,60 |
|
|
1 |
2 |
3 |
4 |
5 |
6 |
|
90 |
10 |
110,75 |
- |
52,01 |
33,18 |
|
25 |
133,43 |
152,58 |
51,57 |
39,01 |
|
|
50 |
122,76 |
152,58 |
107,62 |
55,15 |
|
|
75 |
- |
80,53 |
74,43 |
49,32 |
|
|
100 |
144,11 |
141,99 |
94,61 |
58,29 |
|
|
125 |
121,42 |
152,58 |
90,58 |
83,40 |
|
|
150 |
216,16 |
150,47 |
104,93 |
94,16 |
|
Полученный раствор тиосульфата натрия содержит сульфит и сульфат натрия. Для выделения из раствора кристаллов пентагидрата тиосульфата раствор, полученный взаимодействием сульфита натрия с серой, упаривают. Упаривание растворов тиосульфата натрия необходимо также для выделения из раствора растворимых в воде примесей - сульфата и сульфита натрия. При кристаллизации тиосульфата натрия эти примеси переходят в продукт и снижают содержание основного вещества, что ухудшает его качество.
Исследования показали, что с увеличением концентрации сульфата и сульфита растворимость тиосульфата снижается и наоборот, т.е. наблюдается эффект высаливания. Таким образом, выбираем такой режим упаривания раствора тиосульфата натрия, чтобы сульфат и сульфит натрия выпадали в осадок, а тиосульфат натрия еще оставался в растворе.

Упаренные растворы отстаиваются, здесь они отделяются от осадка сульфата и сульфита натрия. Раствор тиосульфата натрия циркулируется в системе и подается вместе с гидрооксидом натрия для растворения свежей серы. Раствор тиосульфата натрия циркулируется в системе и подается вместе с гидрооксидом натрия для растворения свежей серы.
По необходимости из упаренного раствора, содержащего - 75% тиосульфата натрия, после отделения примесей при охлаждении до 20-25°С кристаллизуется пентагидрат. Кристаллы, отделяемые от раствора тиосульфата натрия, содержат воду. Сушку продукта проводят при температуре не выше 48°С во избежание обезвоживания, т.к. Na2S2O3*5H2O термически устойчив при нагревании свыше 47°С Полученный продукт, идентифицированный как пентагидрат тиосульфата натрия, отвечает требованиям ГОСТ 244-76 по высшему сорту.
Сульфат натрия получают после фильтрации раствора, отстаивания осадка и сушат при температуре 80-100оС. Полученный сульфат натрия исследовали методом ИК-спектроскопии (рисунок 3).
Полученный продукт, идентифицированный как пентагидрат сульфат натрия, отвечает требованиям ГОСТ 244-76 по высшему сорту.
Выводы.
Таким образом, изучение растворимость серы в сульфит и тиосульфат натрия показали, что с повышением температуры увеличивается растворение, а присутствие гидрооксида натрия способствуют увеличения растворения серы и выхода сульфата и тиосульфата натрия. Причем сера Тенгизского месторождения растворяется лучше чем реактивная сера. Полученная путем растворения серы продукты может быть использована как химический реагент в целлюлозной и стекольной промышленности.
ЛИТЕРАТУРА
- Сатенов К.Г., Сериков Т.П., Мухтаров А.К. и др. Разработка персективных методов утилизации серы на Тенгизе //Доклады вторых Международных научных Надировских чтений «Научно - технологическое развитие нефтегазового комплекса», Алматы-Кызылорда. 2004.-с.280-283
- Химические средства защиты растений (пестициды). Справочник.- М.: Химия, 1980, - с.19
- Получение тонкодисперсной серы / Головлев Ю.И., Бролинский Г.И., Сыпяк О.И. и др. //Технология производства серы. - М.:НИИТЭХИМ, 1980.-С.31-35