АННОТАЦИЯ
Диурез является показателем адекватности искусственного кровообращения(ИК) и препараты влияющие на диурез могут быть потенциальной угрозой и причиной острой почечной недостаточности(ОПН) в раннем послеоперационном периоде. В результате исследования выявлено следующее: 1) аминазин сохраняет диуретическую активность почек, но удлиняет время до экстубации; 2) нитраты являются фактором риска развития острой почечной недостаточности в раннем послеоперационном периоде; 3), севофлуран показал хороший диуретический эффект без осложнений в раннем периоде. Вывод: применение лекарственных средств в комбинации с диуретиками дает лучший эффект, чем только прием диуретиков.
Ключевые слова: искусственное кровообращение, диуретик, острая почечная недостаточность.
Введение. Острая почечная недостаточность после кардиохирургических операции у детей возникает 5-33% и ассоциируется с летальностью от 20-79% в зависимости от результата исследования[1]. Ретроспективное исследование в детской хирургии сердца показывает корреляцию ОПН с удлиненной госпитализацией [2] и развитием хронических почечных заболеваний[3,4,5]. В литературе по результатам различных исследований выявлено что в детской кардиохирургии риском фактора ОПН является периоперационный уровень креатинина, возраст менее одного года, пролонгированное время ИК и постоперационный синдром низкого выброса [6]. Однако на проведенное исследования на сегодняшний день не выявлен не один биомаркер, который мог бы предсказать и предупредить ОПН[7]. Развитие ОПН диагностируется различными центрами по разному. Но в данный момент не существует единого мнения, когда диагностировать ОПН.
Назначение диуретиков бесспорно увеличивает диурез во время искусственного кровообращения, но увеличение дозы петлевых диуретиков вызывает вторичный некроз канальцев почечной ткани, и соответственно увеличивает риск послеоперационной почечной недостаточности [8].
Одним из этих факторов является, патофизиология ОПН после ИК, который имеет сложный механизм развития. Lombardi R. с соавторами выявил, что фуросемид не только оказывает протективное действие, но и в результате является вредным для организма[9]. Однако Lassnigg A. в исследовании [10] показал что прием фуросемида улучшает диурез во время ИК. В исследовании [11] показано низкое влияние психоактивных веществ на уровень развития ОПН. При применении седативных препаратов в раннем послеоперационном периоде снижается риск развития ОПН [12]. Несколько исследований провели по изучению маннитола: Rigden S.P. с соавторами и выявил снижение креатинина после операции [13], однако Fisher A.R. выявил высокие цифры мочевины [14]. Loef B.G. выявил улучшение гломерулярной фильтрации после приема клонидина [15]. Thakar C.V. в своих исследованиях использовал дилтиазем, который не показал улучшение почечной фильтрации [16]. Однако Fansa I. доказал протективное свойство дилтиазема и улучшение почечных показателей [17]. Но в тоже время Bergman A.S. обнаружил в своих исследованиях что применение дилтиазема при имеющейся почечной патологии увеличивает риск развития ОПН [18].
Поэтому исследование поиска биомаркеров все еще продолжается и требует тщательного исследования. Учитывая что диурез является показателем адекватности ИК мы полагаем, что препараты влияющие на диурез могут быть потенциальной угрозой и причиной ОПН в раннем послеоперационном периоде.
Цель работы: выявить влияние лекарственных средств на уровень диуреза во время искусственного кровообращения и оценить ближайшие результаты в раннем
послеоперационном периоде.
Материал и методы исследования. Проспективный клинический раздел работы выполнен на базе Научно-Клинического Центра Кардиохирургии и трансплантологии (г. Тараз) в период с января 2013 года по декабрь 2014 года. В исследование вошли 181 ребенка после коррекции врожденных септальных пороков сердца: дефекта межпредсердной и межжелудочковой перегородки сердца, находившихся на оперативном лечении в кардиохирургическом отделении.
Пациенты были рандомизированы по типу лекарственного препарата для обеспечения адекватной почечной перфузии с массой тела от 5 до 25 кг из-за ограниченных возможностей применяемого оксигенатора, без половых ограничений и не старше 18 лет.
Пациенты были разделены на 3 группы соответственно назначенному лекарственному препарату: 1 группа - применение ингаляционного анестетика севофлурана 0,4-0,9об.% минимальная альвеолярная концентрация (МАК) - 61 больной, 2-группа -применение аминазина с добавлением в оксигенатор 2,5%-0,1-0,3мл\кг - 47больных и 3-группа -ретроспективный анализ комбинированнго применения магния сульфата 25%-1-1,5мл\кг и нитрата 0,1%-0,3мл\кг при добавлении в оксигенатор - 73 больных.
Искусственное кровообращение проводили аппаратом “Stokert SIII. Germany” с применением одноразовых мембранных оксигенаторов различных фирм производителей. Оксигенаторы использованные для проведения процедуры искусственного кровообращения: Lilliput-2 D902 (Dideco, Italy), максимальная объемная скорость перфузии 2,3 л\мин, объем заполнения максимально до 400 мл. и Quadrox (Maquet, Germany), максимальная объемная скорость перфузии 3,2 л\мин, объем заполнения максимально до 450 мл.
Результаты исследований и обсуждение.
В таблице № 1 приведены клинические данные по группам обследуемых.
Таблица 1 - Клинические данные пациентов
|
Параметры |
1-группа |
2-группа |
3-группа |
Оценка-р |
|
Общее число пациентов, n (%) |
61 (100%) |
47 (100%) |
73 (100%) |
р=0,23 |
|
Возраст, лет, M±SD |
3±0,5 |
2±0,7 |
4±1,1 |
р=0,65 |
|
Из них мальчиков, n (%) |
33(54%) |
29(62%) |
42(58%) |
р=0,32 |
|
Вес, кг, M±SD |
11,6±2 |
9,9±4,2 |
15,1±6,7 |
р=0,22 |
|
Рост, м, M±SD |
0,55±0,12 |
0,65±0,23 |
0,65±0,18 |
р=0,12 |
|
Виды врожденных пороков - ДМПП
|
27 (44%) 28 (46%) 6 (10%) |
36 (76%) 7(16%) 4(8%) |
44(61%) 16(21%) 13(18%) |
р=0,023 р=0,0027 р=0,033 |
Учитывая важность искусственного кровообращения и пережатия аорты во время операции, мы решили в первую очередь выявить насколько эти параметры связаны статистически(таб.2).
Таблица 2 - Параметры искусственного кровообращения во время операции
|
Параметры |
1-группа |
2-группа |
3-группа |
Оценка-р |
|
Время ИК |
31±9 |
37±10 |
39±11 |
p<0,001 |
|
Время пережатия аорты (только коррекция дефекта межжелудочковой перегородки) |
21±7 |
21±9 |
24±13 |
p<0,001 |
Как видно из таблицы, время искусственного кровообращения и время пережатия аорты имеют межгрупповое статистически значимое влияние, кроме того определена корреляционная связь между параметрами времени искусственного кровообращения во 2 и 3 группах и пережатия аорты в 1 и 3 группах на диурез у детей перенесших операцию на сердце.
После разжатия аорты сердечная деятельность восстанавливалась: в 1 группе у 59 (97%) самостоятельно и у 2 (3%) больных через АВ блокаду, во 2 группе 46 (7%) самостоятельно и у 1 (3%) через АВ блокаду, и в 3 группе у 70 (95%) самостоятельно и у 3 (5%) через АВ блокаду.
Временный электрокардиостимулятор (ЭКС) был применен в 1-й группе в 2-х случаях; во 2-й группе в 1-м случае и в 3 группе в 3 случаях, которые восстановились самостоятельно в раннем послеоперационном периоде в течении от 1 до 3 суток после операции. За период наблюдения в трех группах не выявлено ни одного случая полной АВ блокады с необходимостью установки постоянного ЭКС.
При проведении дисперсионного анализа между группами, время искусственного кроообращения и пережатия аорты оказались статистически значимы, и у большинства больных был восстановлен синусовый ритм, а АВ блокада не была постоянной и не требовала установки постоянного ЭКС. При применении различных комбинаций лекарственных средств одномоментное применение петлевого диуретика (лазикс 5 мг) во всех случаях показал хороший диуретический эффект. Разные комбинации были назначены для улучшения почечного кровотока и последующего увеличения диуреза. Поэтому дополнительное назначение препаратов улучшающих почечный кровоток и в последующем увеличивающим диурез оправдано, но среди комбинаций препаратов севофлуран смог оказать более хороший эффект.
Комбинации лекарственных препаратов и динамика диуреза показаны в таблице №3.
Таблица № 3. Комбинации использованных лекарственных препаратов и динамика
диуреза
|
Параметры |
Лекарственные средства |
Диурез до ИК, мл |
Диурез во время ИК, мл |
Диурез после ИК, мл |
Диурез в ОРИТ, мл |
Диурез мл\кг\час в общем |
|
1 группа |
Севофлуран 0,4- 0,9об.% МАК |
23±5 |
45±7 |
85±13 |
414±67 |
2,1±0,7 |
|
2 группа |
Аминазин 2,5%- 0,1-0,3мл\кг |
33±6 |
42±9 |
87±21 |
309±81 |
2,0±0,4 |
|
3 группа |
Магнезия сульфат 25%-1-1,5мл\кг +нитраты 0,1%- 0,3мл\кг |
34±7 |
35±5 |
101±19 |
527±104 |
1,8±0,5 |
При проведении множественной регрессии влияния лекарственных препаратов на диурез во время искусственного кровообращения аминазин не показал статистически значимого влияния, тогда как севофлуран и изокет имели статистическое влияние (p<0,05). В результате анализа регрессии одной зависимой переменной на уровень диуреза до и после искусственного кровообращения выявлено, что севофлуран и нитраты (изокет) влияют на диурез, а аминазин не влияет.
Учитывая отсутствие введения аминазина и севофлурана, а так же периодическое спорадическое назначение изокета в отделении реанимации нами было проанализирована корреляционная связь лекарственных препаратов на диурез в раннем послеоперационном периоде, т.е. в отделении реанимации и интенсивной терапии. В результате мы выявили, что при определении влияния на почечный кровоток у детей получавших изокет в раннем послеоперационном периоде диурез больше и отмечена статистическая значимость препарата изокет (р=0,00347) сравнительно с севофлураном (р=1,0000) и аминазином (р=0,48756)
Анализ хирургических показателей. Диурез в течении искуственного кровообращения относительно типа операции по группам исследуемых показана в таблице №4.
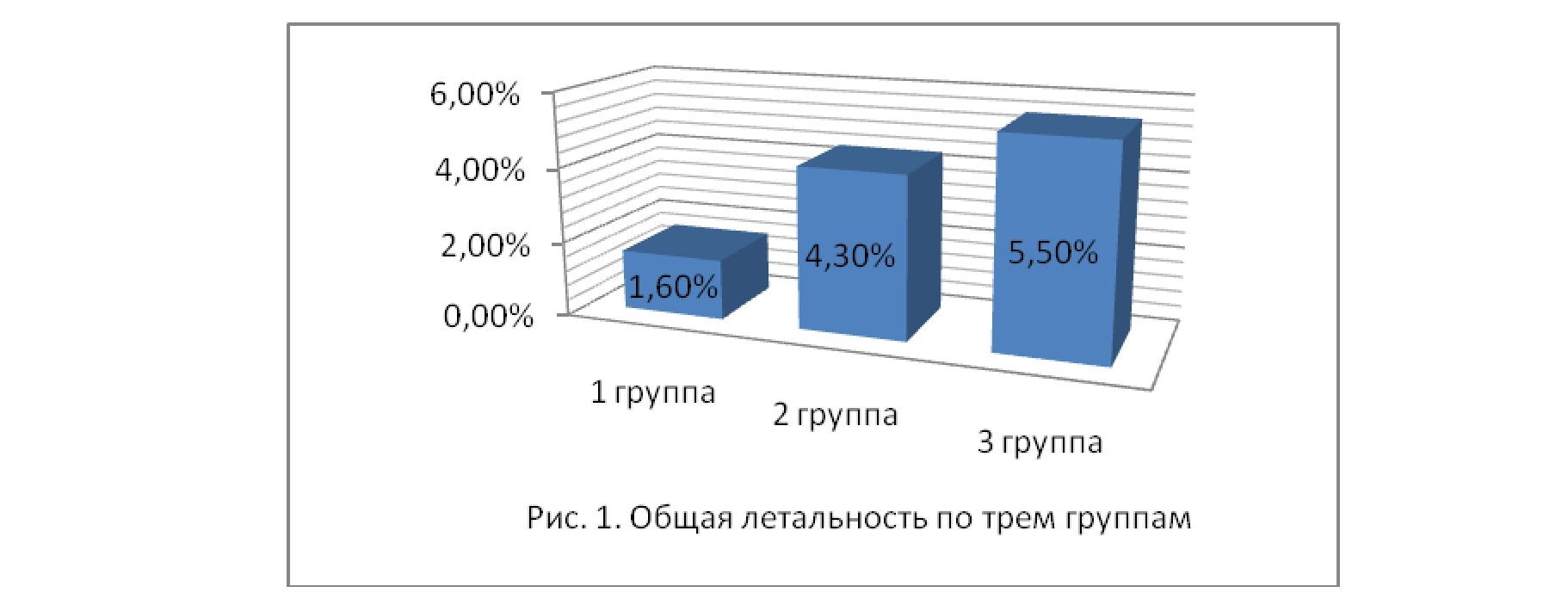
Таблица 4 - Диурез в течении искуственного кровообращения относительно типа
операции
|
Операция |
1 группа |
2 группа |
3 группа |
|
Пластика ДМПП |
54±8,4 мл |
47±7,5 мл |
36±8,9 мл |
|
Пластика ДМЖП |
61±9,1 мл |
48±11,7 мл |
44±4,4 мл |
|
Уровень р |
p<0,001 |
р=0,623 |
p<0,001 |
Как видно из таблицы вид операции имеет статистически значимое влияние (p<0,001) на диурез в период искусственного кровообращения, но применение аминазина не показало статистически значимого влияния (р=0,623).
Среднее пребывание в отделении реанимации и интенсивной терапии в 1, 2 и 3 группах соответственно: 18±7, 21±5, 19±6 часов (p=0,8); время до экстубации 7±3, 12±5, 8±4 часа (p=0,01). В результате мы можем полагать, что при применении аминазина время до экстубации увеличивалось вследствие седатирующего действия препарата, в результате время нахождения в ОРИТ удлинялось.
Среди осложнений в данной группе больных особо важное место отдается острой почечной недостаточности. В раннем послеоперационном периоде у больных 1-группы острая почечная недостаточность не была зафиксирована, тогда как во 2 группе острая почечная недостаточность была у 1 ребенка, а в 3 группе такое осложнение было у 3 детей.
К сожаленью, все дети с острой почечной недостаточностью скончались, 1 ребенку в 3 группе был установлен перитонеальный диализ, но результат был отрицателен. Кроме того причинами летальности были в 1 группе 1 ребенок из-за анафилактического шока, во 2 группе 1 ребенок от острого нарушения ритма, и в третьей группе 1 ребенок от острого легочно-артериального криза( Рис.1).
Выводы. Применение лекарственных средств в комбинации с диуретиками показывает лучший эффект, чем только прием диуретиков. Однако не все препараты действуют положительно. Аминазин сохраняет диуретическую активность почек, но удлиняет время наркозного сна до экстубации. Нитраты являются фактором риска развития ОПН и развитием энцефалопатии у детей в раннем послеоперационном периоде, а вот севофлуран показал хороший диуретический эффект без осложнений после операции.
СПИСОК ЛИТЕРАТУРЫ
- Pedersen KR, Povlsen JV, Christensen S, et al. Risk factors for acute renal failure requiring dialysis after surgery for congenital heart disease in children. Acta Anaesthesiol Scand. 2007; 51:13441349. [PubMed: 17944638]
- Zappitelli M, Bernier PL, Saczkowski RS, et al. A small post-operative rise in serum creatinine predicts acute kidney injury in children undergoing cardiac surgery. Kidney Int. 2009; 76:885-892. [PubMed: 19641482]
- Shaw NJ, Brocklebank JT, Dickinson DF, et al. Long-term outcome for children with acute renal failure following cardiac surgery. Int J Cardiol. 1991; 31:161-165. [PubMed: 1869324]
- Heying R, Seghaye MC, Grabitz RG, et al. Mid-term follow-up after multiple system organ failure following cardiac surgery in children. Acta Paediatr. 1999; 88:1238-1243. [PubMed: 10591426]
- Dimopoulos K, Diller GP, Koltsida E, et al. Prevalence, predictors, and prognostic value of renal dysfunction in adults with congenital heart disease. Circulation. 2008; 117:2320-2328. [PubMed:18443238]
- Rigden SP, Barratt TM, Dillon MJ, et al. Acute renal failure complicating cardiopulmonary bypass surgery. Arch Dis Child. 1982; 57:425-430. [PubMed: 7092306]
- Parikh CR, Devarajan P. New biomarkers of acute kidney injury. Crit Care Med. 2008; 36:S159- S165. [PubMed: 18382188]
- Aravindan N, Natarajan M, Shaw AD. Fenoldopam inhibits nuclear translocation of nuclear factor kappa B in a rat model of surgical ischemic acute renal failure. J Cardiothorac Vasc Anesth 2006;20:179- 186.
- Lombardi R, Ferreiro A, Servetto C: Renal function after cardiac surgery: Adverse effect of furosemide. Ren Fail 25:775-786, 2003
- Lassnigg A, Donner E, Grubhofer G, Presterl E, Druml W, Hiesmayr M: Lack of renoprotective effects of dopamine and furosemide during cardiac surgery. J Am Soc Nephrol11: 97-104, 2000
- Caimmi PP, Pagani L, Micalizzi E, Fiume C, Guani S, Bernardi M, Parodi F, Cordero G, Fregonara M, Kapetanakis E, Panella M, Degasperis C: Fenoldopam for renal protection in patients undergoing cardiopulmonary bypass. J Cardiothorac Vasc Anesth 17: 491-494, 2003
- Ranucci M, Soro G, Barzaghi N, Locatelli A, Giordano G,Vavassori A, Manzato A, Melchiorri C, Bove T, Juliano G,Uslenghi MF: Fenoldopam prophylaxis of postoperative acute renal failure in high-risk cardiac surgery patients. Ann Thorac Surg 78: 1332-1337, 2004
- Rigden SP, Dillon MJ, Kind PR, de Leval M, Stark J, Barratt TM: The beneficial effect of mannitol on postoperative renal function in children undergoing cardiopulmonary bypass surgery. Clin Nephrol 21: 148-151, 1984
- Fisher AR, Jones P, Barlow P, Kennington S, Saville S,Farrimond J, Yacoub M: The influence of mannitol on renalfunction during and after open-heart surgery. Perfusion 13:181-186, 1998
- Loef BG, Henning RH, Epema AH, Rietman GW, van Oeveren W, Navis GJ, Ebels T: Effect of dexamethasone on perioperative renal function impairment during cardiacsurgery with cardiopulmonary bypass. Br J Anaesth 93:793-798, 2004
- Thakar CV, Yared JP, Worley S, Cotman K, Paganini EP:Renal dysfunction and serious infections after open-heart surgery. Kidney Int 64: 239-246, 2003
- Fansa I, Gol M, Nisanoglu V, Yavas S, Iscan Z, Tasdemir O: Does diltiazem inhibit the inflammatory response in bypass? Med Sci Monit 9: PI30-PI36, 2003
- Bergman AS, Odar-Cederlof I, Westman L, Bjellerup P, Hoglund P, Ohqvist G: Diltiazem infusion for renal protection in cardiac surgical patients with preexisting renal dysfunction. J Cardiothorac Vasc Anesth 16: 294-299, 2002