АННОТАЦИЯ
Цель исследования: Изучить клинические показатели течения заболевания и провести комплексную сравнительную оценку эффективности и переносимости монотерапии «традиционными» (вальпроаты, карбамазепин) и «новыми» (топирамат, окскарбазепин, леветирацетам) антиэпилептическими препаратами у взрослых больных симптоматической и криптогенной фокальной эпилепсией. Для исследования больных симптоматической и криптогенной фокальной эпилепсией при монотерапии основными современными АЭП (ВПА, КБЗ, ТПМ, ОКЗ, ЛЕВ) было обследовано 97 больных, жителей Шымкента и ЮжноКазахстанской области , в возрасте от 18 до 65 лет (средний возраст 41,5±0,7 лет), среди них 41 (43,11%) мужчин, 56 (56,89%) женщин. Антиэпилептические препараты (АЭП) «новой» генерации (топирамат, леветирацетам, окскарбазепин) и «традиционные» (вальпроаты, карбамазепин) в равной степени эффективны при рациональной монотерапии симптоматических и криптогенных фокальных эпилепсий у взрослых. Леветирацетам и окскарбазепин отличаются более благоприятным профилем переносимости. Выявлено значимое влияние клинических и социальных показателей на больных эпилепсией. Персистирование приступов любого характера было значимым фактором развития аффективных расстройств, выраженность которых коррелировала с тяжестью приступов.
Ключевые слова: эпилепсия, антиэпилептические препараты, побочные эффекты, качество жизни
Введение. Эпилепсия - самое частое из тяжелых заболеваний головного мозга с распространенностью в популяции до 2% [1], способное оказывать существенное влияние на состояние физического и психического здоровья человека и приводить к снижению качества жизни и социальной дезадаптации больных. В настоящее время в связи с бурным развитием нейрофармакологии эпилепсия рассматривается как потенциально излечимое заболевание и ремиссии имеют место у достаточно большого количества больных: по данным разных авторов от 50 до 80% [2.3]. Но несмотря на значительные успехи, достигнутые в лечении эпилепсии, в определенной части случаев заболевание оказывается резистентным к противосудорожным препаратам, а у части больных эти препараты вызывают побочные эффекты, в значительной степени влияющие на физическое и психическое здоровье, снижающие качество жизни и заставляющие отказаться от их применения. Кроме того, проблема КЖ связана не только с клиническими проявлениями эпилепсии и фармакотерапией, но и с отношением больных к болезни, необходимостью постоянно принимать лекарства, трудовыми ограничениями, запретом на вождение автомобиля, с отношением общества к больным и т.д. [4,5]. В связи с расширением возможностей фармакотерапии эпилепсии, появлением целого ряда новых средств с широким спектром действия для монотерапии неизбежно возникают вопросы, касающиеся сравнительной эффективности традиционных и новых антиэпилептических препаратов, при этом одним из приоритетных направлений является их влияние на качество жизни больных . Имеющиеся данные не дают исчерпывающего ответа на эти вопросы [6].
Цель исследования: Изучить клинические показатели течения заболевания и провести комплексную сравнительную оценку эффективности и переносимости монотерапии «традиционными» (вальпроаты, карбамазепин) и «новыми» (топирамат (ТМП), окскарбазепин (ОКЗ), леветирацетам (ЛЕВ)) антиэпилептическими препаратами у взрослых больных симптоматической и криптогенной фокальной эпилепсией.
Материалы и методы исследования Исследование проводилось на базе кафедры неврологии, психиатрии, психологии ЮКГФА с 2011 по 2014 гг. В исследование включено 97 больных в возрасте от 14 до 65 лет (средний возраст 39,5+2,1 лет) с длительностью заболевания от нескольких месяцев до 48 лет (в среднем 24,5+0,7 лет), страдающих симптоматической и криптогенной фокальной эпилепсией. Диагноз установлен в соответствии с Международной классификацией эпилепсии, эпилептических синдромов и схожих заболеваний (Нью-Дели, 1989г.).
Возраст начала заболевания среди обследованных больных составил от 4 до 55 лет. Дебют заболевания в возрасте до 10 лет отмечен у 15 (16%) больных, в возрастных интервалах 11-20 лет - у 43 (44,44%), 21-30 лет - у 14 (14,67%), 31-40 лет - у 12 (12,89%), 41-50 лет - у 8 (8,89%), более 50 лет - у 3 (3,11%).
Отбор больных симптоматической и криптогенной фокальной эпилепсией проводился путем активного выявления пациентов во время консультативного приема на кафедре неврологии, психиатрии, психологии на основе критериев включения и исключения после проведенных диагностических процедур.
Методы исследования включали: общее клиническое исследование, которое
проводилось по стандартной методике (сбор анамнеза заболевания и жизни, соматический статус, ЭКГ), неврологический статус и электроэнцефалографическое исследование, нейровизуализационное исследование, лабораторные методы включали клинический анализ крови, биохимический анализ крови (билирубин, АЛТ, ACT, ЩФ).
Исследования проводились перед назначением вальпроатов (ВПА) и карбамазепина (КБЗ) с целью определения противопоказаний к их назначению, а также в процессе лечения 1 раз в 3-4 месяца с целью контроля возможных побочных эффектов.
После проведения необходимых диагностических процедур всем больным была назначена терапия впервые или проведена коррекция неадекватной предшествующей терапии в соответствии с рекомендациями ILAE. При лечении больных использовался режим монотерапии.
Эффективность терапии при применении различных антиэпилептических препаратов (АЭП) в режиме монотерапии оценивалась по показателю снижения частоты эпилептических приступов в процентах от исходной частоты не ранее 6 месяцев лечения на основании анализа дневников учета приступов, самостоятельно заполняемых больными. Полное отсутствие приступов на фоне лечения на протяжении всего времени наблюдения мы обозначили как «ремиссия». Снижение частоты приступов на 50% и более определялось как «улучшение». Под отсутствием эффекта мы подразумевали сохранение числа приступов на прежнем уровне, а также снижение их количества менее чем на 50%. Увеличение частоты приступов расценивалось нами как «ухудшение».
Статистическая обработка данных производилась с использованием описательной статистики, корреляционной связи и оценки достоверности различий между средними и относительными величинами при помощи коэффициента корреляции Пирсона (г), коэффициента Стьюдента.
Результаты исследования. У большинства больных (п=54, 56,44%) была диагностирована криптогенная (неустановленной этиологии, предположительно симптоматическая) фокальная эпилепсия, у остальных больных (п=43, 43,56%) - симптоматическая фокальная эпилепсия (с известной этиологией). Длительность заболевания в исследуемой группе пациентов составила от нескольких месяцев до 45 лет (в среднем 8,43 ± 0,76), частота приступов от 1-2 в месяц до нескольких приступов ежедневно.
От нескольких месяцев до 5 лет эпилепсией страдали 47 (49,08%) человек, от 6 до 10 лет - 23 (24,31%), более 10 лет - 27 (26,61%) . Таким образом, половина пациентов (50,92%) имели эпилептические приступы в течение 6 и более лет, что, безусловно, снижало качество их жизни и приводило к социальной дезадаптации. Из установленных и предполагаемых этиологических факторов заболевания основную роль играли: родовая травма (РТ), аномалии развития головного мозга (АГМ), черепно-мозговые травмы (ЧМТ), хроническая ишемия головного мозга (ХИ), опухоли головного мозга и последствия их оперативного лечения (О), нейроинфекции (НИ), последствия ишемического (ИИ) и геморрагического (ГИ) инсультов. Сочетание различных факторов было отмечено у 5 (6,12%) пациентов.
В зависимости от локализации источника эпилептогенеза в коре головного мозга лобная эпилепсия была установлена у 37 (38,22%) больных, височная — у 25 (26,67%), затылочная - у 1 (0,44%), мультифокальная - у 2 (0,89%). Еще у 32 (33,78%) больных локализационную форму заболевания установить не удалось. Неустановленная локализационная форма эпилепсии в большинстве случаев объясняется отсутствием изменений при электроэнцефалографии и нейровизуализации, а также несовпадением вышеуказанных изменений с клинической картиной заболевания.
Ha момент первого обращения ежемесячные эпилептические приступы отмечались у 84 (87,11%), ежедневные - у 13 (12,89%). Лишь 46 (47,56%) больных до консультации регулярно вели учет своих приступов. По нашему мнению, фиксация приступов больными позволяет лечащему врачу получать адекватную информацию о течении заболевания и эффективности проводимого лечения.
Изолированные парциальные приступы отмечались у 15 больных (16%). Исключительно генерализованные приступы были зафиксированы у 36 пациентов (37,33%). Сочетание парциальных и вторично-генерализованных приступов было выявлено у 45 (46,79%)
больных.Таким образом, у исследованных больных преобладали наиболее тяжелые сложные парциальные и вторично-генерализованные судорожные приступы, в значительной степени влияющие на КЖ, психоэмоциональное состояние и социальный статус.
Простые парциальные приступы в большинстве случаев были моторными - у 12 больных. Чаще всего больные отмечали «напряжение», «подергивания», «скручивания» в той или иной части тела. У 6 пациентов наблюдались соматосенсорные приступы: зрительные, обонятельные приступы, парестезии в различных частях тела. Простые парциальные приступы с вегетативно- висцеральными проявлениями отмечались у 3 больных, чаще в виде «восходящего эпигастрального ощущения». Еще у 3 больных наблюдались простые парциальные приступы с психическими симптомами, в большинстве случаев проявлялись ощущением «уже виденного», нереальности происходящего.
Среди сложных парциальных приступов наиболее частыми были аутомоторные приступы (п=23) со стереотипными действиями или бессмысленными движениями, автоматизмами. В большинстве случаев встречались ороалиментарные автоматизмы (чмоканье, сглатывание, сплевывание), повторение слов, продолжение или повторение движений, начатых до приступа (топтание), движения рук (перебирание одежды). Диалептические приступы с выключением сознания и двигательной активности отмечались у 18 больных. У 6 больных отмечались сложные парциальные гипермоторные приступы (боксирование, педалирование).
Данные ЭЭГ-исследования. Патологическая, в том числе эпилептиформная, активность, согласующаяся с диагнозом фокальной эпилепсии, при рутинной ЭЭГ-исследовании была выявлена у 49 (50,67%) пациентов. У 48 (49,33%) больных патологических изменений при данном исследовании обнаружено не было. Частота выявляемости различных патологических изменений на ЭЭГ в общей группе исследуемых больных представлена в таблице .
Таблица 1 - Патологические изменения, выявленные при рутинной ЭЭГ
|
Патологические изменения |
Абс |
% |
|
Региональная эпилептиформная активность |
58 |
60,53 |
|
Региональное замедление основной активности |
17 |
17,54 |
|
- периодическое |
11 |
12,28 |
|
- продолженное |
5 |
5,26 |
|
Диффузное замедление основной активности |
11 |
12,28 |
|
Феномен вторичной билатеральной синхронизации |
23 |
24,56 |
|
Всего |
49 |
50,67 |
Наиболее частой находкой при ЭЭГ являлась региональная эпилептиформная активность и региональное замедление основной активности, являющиеся характерными для фокальных эпилепсий.
Особое внимание уделялось электроэнцефалографическому феномену вторичной билатеральной синхронизации (ВБС), имеющему большое практическое значение. При любой форме эпилепсии появление ВБС на ЭЭГ знаменует возможность ухудшения течения заболевания. Особенно остро эта проблема звучит при выборе АЭП для лечения фокальных эпилепсий. Обнаружение ВБС на ЭЭГ в некоторых случаях диктует необходимость пересмотра тактики лечения. Феномен ВБС наблюдался нами в 15 (16,44%) случаях.
Данные нейровизуализационного исследования. В исследуемой группе больных патологические изменения головного мозга при нейровизуализации выявлены у 50 из 97 пациентов (52,13%). Наиболее частыми патологическими находками были кистозно-глиозная трансформация (КГТ) вещества головного мозга, гидроцефалия (Г)- Реже встречались аномалии развития головного мозга (АР), кисты (К), очаги дистрофии (ОД) вещества головного мозга, атрофии (Атр), мезиальный височный склероз (МВС), опухоли головного мозга (О). Кальцинаты (Ка) и крупные арахноидалъные кисты (АК) встречались в единичных случаях.
Наиболее резистентной к терапии формой фокальной эпилепсии является, как известно, амигдало-гиппокампальная височная эпилепсия, развивающаяся у больных с дисгенезиями головного мозга, большинство из которых, по-видимому, относится к разряду микродисгенезий, обусловленных нарушением нейрональной миграции. К сожалению, частота обнаружения этих поражений при традиционных KT и МРТ-исследовании, использованных у наших пациентов, невысока: 2,66% и 6,91% соответственно. Именно с недостаточной разрешающей способностью нейровизуализационных методик в настоящее время связывают существование большого числа криптогенных (предположительно симптоматических) форм фокальной эпилепсии (Мухин К.Ю. и др., 2004), встречающихся в нашем исследовании у 56,44% больных.
Наиболее часто в исследуемой группе идентифицировались кистозно- глиозные (12,23%), кистозные (6,38%), дистрофические (5,85%) и атрофические (2,13%) изменения резидуального характера после перенесенных родовых травм, ЧМТ, ишемического или геморрагического инсультов, реже воспалительных процессов. В 2,13% отмечены изменения после оперированных опухолевых процессов мозга. У 16,48% констатирована энцефалопатия резидуально- органического генеза с гипертензионно-гидроцефальными изменениями.
Анализ монотерапии. После проведения необходимых диагностических процедур всем больным было назначено впервые или скорректировано предыдущее противоэпилептическое лечение. Лечение назначалось с учетом формы эпилепсии, характера приступов, возраста и веса больного, а также с учетом сопутствующих заболеваний.
В зависимости от принимаемого АЭП все больные были разделены на 5 групп: группу вальпроатов (ВПА) (п=34), карбамазепина (КБЗ) (п=26), топирамата (ТПМ) (п=29), леветирацетама (ЛЕВ) (п=12) и окскарбазепина (ОКЗ) (п=11). Используемые суточные дозировки АЭП соответствовали индивидуальным клинически эффективным или максимальным переносимым дозам: для ВПА 10003000 мг, для КБЗ - 600-1800 ли-, для ТПМ 200-400 мг, для ЛЕВ 1500-3000 мг, для ОКЗ 900-2400 мг. Режим приема для всех АЭП: дважды в день утром и вечером. Препараты ВПА и КБЗ назначались в пролонгированных формах.
Среди больных, получающих лечение «традиционными» АЭП, преобладали лица, у которых терапия эпилепсии была стартовой: 67% в группе ВПА и 73% - КБЗ. Среди больных, получающих новые АЭП, большую часть составляли пациенты, у которых был осуществлен
переход с ранее применяемой терапии в связи с ее неэффективностью или побочными эффектами: 54% в группе ТПМ, 56% - ЛЕВ и 67% - ОКЗ. Более редкое назначение в качестве стартовой монотерапии ЛЕВ (44%) было обусловлено отнюдь не меньшей его эффективностью, а скорее относительной новизной препарата и недостаточным опытом применения в режиме монотерапии, а в отношение ОКЗ (33%) - еще и КБЗ наиболее активно использовался нами при лечении фокальной височной эпилепсии. Кроме того, КБЗ назначался и при других локализационных формах симптоматической и криптогенной эпилепсии при отсутствии на ЭЭГ феномена ВБС. ВПА применялись нами при преобладании вторично- генерализованных приступов. «Новые» АЭП, несмотря на широкий спектр эффективности, чаще назначались при неэффективности или непереносимости лечения «традиционными» АЭП, а также при наличии индивидуальных противопоказаний к использованию ВПА и КБЗ.
У большинства больных во всех выделенных группах отмечалась комбинация различных видов приступов с преобладанием более тяжелых сложных парциальных (СПП) и вторично генерализованных приступов (ВГСП) над простыми парциальными (ППП).
КБЗ наиболее активно использовался нами при лечении фокальной височной эпилепсии. Кроме того, КБЗ назначался и при других локализационньгх формах симптоматической и криптогенной эпилепсии при отсутствии на ЭЭГ феномена ВБС. ВПА применялись нами при преобладании вторично-генерализованных приступов.
Оценка эффективности монотерапии у исследованных больных. Всем пациентам после необходимого обследования и установления диагноза была проведена коррекция ранее получаемого лечения или впервые назначена терапия в соответствии с рекомендациями ILAE. Доза препаратов наращивалась постепенно с целью сведения к минимуму риска возникновения побочных эффектов терапии. Первоначально больным назначалась минимальная терапевтическая доза, которая в дальнейшем увеличивалась под контролем эффективности и переносимости. При постепенной замене терапии мы придерживались тактики назначения второго АЭП до достижения терапевтической дозы с последующей отменой исходно применяемого препарата. Данный подход позволяет более правильно интерпретировать клинический эффект.
Окончательная оценка эффективности терапии проводилась не ранее 6 месяцев лечения, предварительная — 2-3 месяцев в зависимости от скорости титрования АЭП, на основании анализа дневников учета приступов, самостоятельно заполняемых больными. Полное отсутствие приступов на фоне лечения на протяжении всего времени наблюдения мы обозначили как «ремиссия». Снижение частоты приступов на 50% и более определялось нами как «улучшение». Под отсутствием эффекта мы подразумевали сохранение числа приступов на прежнем уровне, а также снижение их количества менее чем на 50%. Увеличение частоты приступов расценивалось нами как «ухудшение».
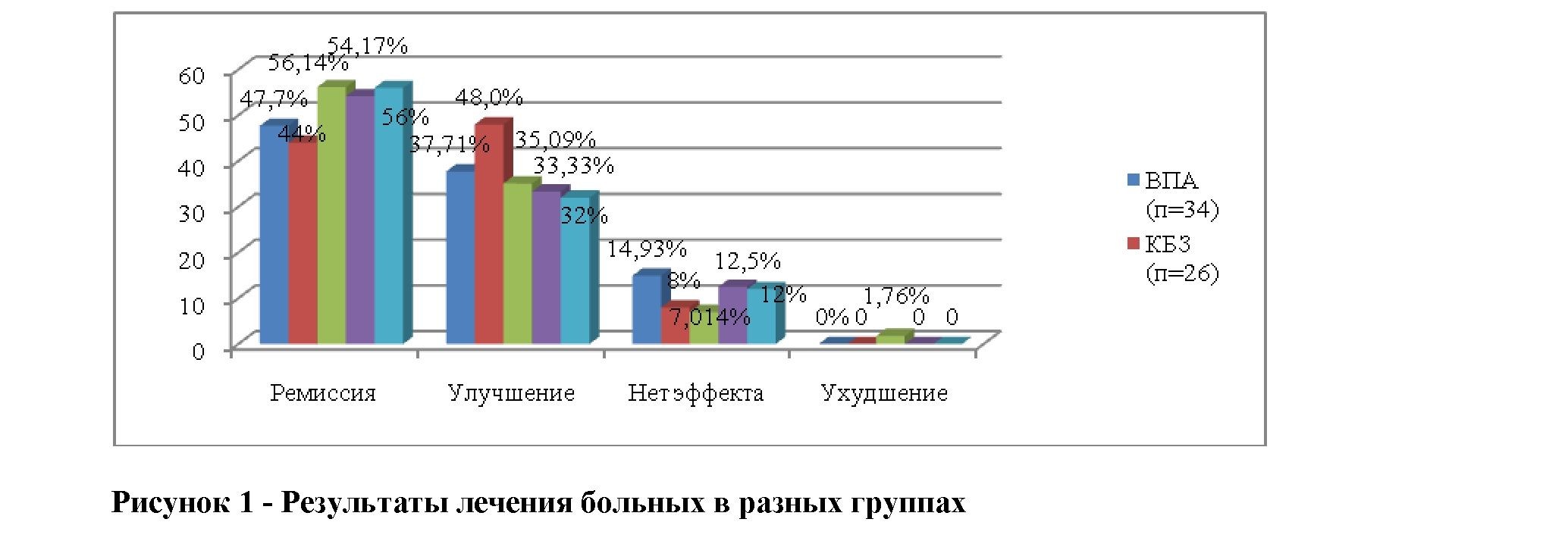
В среднем во всех группах отмечена достаточно высокая эффективность монотерапии симптоматических и предположительно симптоматических фокальных эпилепсий у взрослых: ремиссия заболевания была констатирована в диапазоне от 44 до 56% при использовании разных препаратов. Достоверных различий в эффективности между группами выявлено не было (р>0,05). Максимальная частота достижения ремиссии нами наблюдалась при использовании препаратов новой генерации. Так, в группе ТПМ и ЛЕВ полная редукция приступов отмечалась у 56% больных, в группе ОКЗ - у 54%. Несколько реже ремиссия приступов была достигнута в группах «традиционных» АЭП: при использовании ВПА и КБЗ в 48% и 44% случаев соответственно.
В группе ТПМ в 1 (1,76%) случае мы наблюдали ухудшение течения эпилепсии в форме учащения СП и ВГСП, не зарегистрированное в других группах. Отсутствие аггравации приступов у пациентов, принимающих КБЗ, в нашем исследовании объясняется, прежде всего, активным выявлением на этапе прескрининга при помощи рутинной ЭЭГ и ЭЭГ-мониторинга предикторов этого осложнения терапии - феномена ВБС.
Наибольшая частота неэффективности терапии зафиксирована в группах ВПА (14,93%), ОКЗ (12,5%) и ЛЕВ (12%), несколько реже неэффективность в группах КБЗ (8%) иТПМ (8,77%).
Традиционно КБЗ считается препаратом первой очереди выбора для лечения парциальных приступов. Однако в нашем исследовании его эффективность в отношении парциальных приступов была невысокой (36,58%). Это может быть обусловлено несколькими причинами.
Пациенты, получающие монотерапию препаратами «новой» генерации, оценивали изменения состояния на фоне лечения несколько выше. Однако достоверно выше изменения самочувствия оценили больные в группе ЛЕВ (р<0,05) по сравнению с пациентами, получающими лечение «традиционными» АЭП (ВПА, КБЗ), что, очевидно, связано с лучшей переносимостью препарата.
Побочные эффекты монотерапии различными АЭП. В настоящее время основной принцип лечения эпилепсии может быть сформулирован следующим образом: максимум терапевтической эффективности при минимуме побочных эффектов. Больные, страдающие эпилепсией, вынуждены применять ттротивоэггилептические препараты в течение многих лет. Поэтому назначение антиконвульсантов, их выбор, определение доз должны быть тщательно проанализированы с точки зрения не только терапевтической эффективности, но и возможности проявления побочных эффектов.
Побочные эффекты монотерапии ВПА.Побочные эффекты при лечении вальпроатами нами наблюдались у 12 (37,31%) больных. Наиболее частыми побочными эффектами, о которых сообщали >10% больных, были увеличение веса (17,91%, п=6), тремор (17,91%, п=6), выпадение волос (13,43%, п=4). Реже больные предъявляли жалобы на заторможенность (5,7%, п=2), снижение кратковременной памяти и внимания (5,97%, п=2), дисменорею (4,48%,n=1 ). 1 (4,48%) больной отмечал раздражительность, вялость и апатию. Гепатотоксические эффекты лечения были зафиксированы у 1 (4,48%) больных в виде двукратного повышения трансаминаз крови. Наиболее частым побочным эффектом терапии вальпроатами было увеличение веса (от 3 до 25 кг, в среднем 6,5+3,42 кг) - у 6 (17,91%) больных. Именно это явилось причиной отмены препарата у 2 (5,97%) больных, у которых показатель индекса массы тела значительно
отклонялся от нормативных значений (ИМТ>30 кг/м2). Больные с изменениями веса в результате лечения ВПА (средний показатель итогового КЖ 42,3+1,16) достоверно ниже оценивали КЖ (р<0,05), чем больные, не испытывающие побочные эффекты (средний показатель итогового КЖ 49,65+1,7).
Побочные эффекты монотерапии КБЗ. Из 26 пациентов, получающих монотерапию КБЗ, побочные эффекты отмечались у 6 (23,08%). Чаще всего больные жаловались на появление головокружения (5,77%, п=2), сонливость (5,77%, п=2), реже отмечались снижение кратковременной памяти (3,85%, п=1), головная боль (1,92%, п=1), атаксия (1,92%, п=1), заторможенность (1,92%, п=1). У 2 больных была констатирована дисфункция ЖКТ: боль в животе (1,92%, п=1) и запоры (1,92%, п=1). У 1 (1,92%) больного отмечено увеличение веса на 13 кг.
В 1 (1,92%) наблюдении отмечалась аллергическая сыпь на фазе титрования дозы, потребовавшая немедленной отмены терапии. Гематологические побочные эффекты в виде нейтропении были зафиксированы в 1 (1,92%) случае.
Побочные эффекты монотерапии ТПМ. Побочные эффекты топирамата были зафиксированы у 5 (19,30%) больных. Изменения в психоэмоциональной сфере с приемом топамакса связывали 3 (8,77%) больных: у 2 (5,26%) отмечалась агрессивность и раздражительность, у 1 (1,75%) - апатия и подавленность настроения, у 1 (1,75%) — тревога и страх. Со стороны нервной системы побочные действия были зафиксированы у 2 (3,51%) больных в виде заторможенности. Дополнительно у 7 большее отмечалась легкая заторможенность в начале лечения, которая прошла самостоятельно через 3 месяца лечения.
Специфическим побочным эффектом топирамата, связанным с ингибированием карбоангидразы является возникновение парестезий в конечностях. В нашем исследовании он встречался у 2 (5,26%) больных. У 1 (1,75%) больной парестезии были нестерпимо
мучительными, в результате чего, несмотря на полную редукцию приступов, лечение было отменено. У 1 больной (1,75%) мы наблюдали появление первого в жизни приступа почечной колики в результате развития мочекаменной болезни через 6 месяцев лечения топираматом. Следует отметить, что предварительного исследования на предмет мочекаменной болезни (МКБ) не проводилось. Данный побочный эффект связан с повышением рН мочи из-за снижения секреции лимонной кислоты вследствие торможения карбоангидразы.
Наиболее частым побочным действием топамакса было снижение массы тела от 3 до 25 кг (в среднем 8,31+1,37 кг). В нашем исследовании снижение массы тела констатировалось у 20 (35,09%) пациентов. При сравнении КЖ больных со снижением веса в результате лечения топираматом (итоговое КЖ 53,26+1,99) и КЖ больных, не испытывающих никаких побочных эффектов (итоговое КЖ 52,39+2,27), достоверных различий выявлено не было (р>0,05). Таким образом, ни у одного больного снижение массы тела не привело к ухудшению КЖ и не потребовало отмены лечения, поэтому мы не включили его в список побочных эффектов. Напротив, большинство больных (85%) расценили это действие, как положительное.
Побочные эффекты монотерапии ОКЗ.При лечении окскарбазепином побочные явления отмечались у 2 (20,83%) больных: головокружение и сонливость (12,5%, п=1)
Побочные эффекты монотерапии ЛЕВ. В группе ЛЕВ побочные действия были зафиксированы у 2 (16%) больных: у 1(12%) больных - раздражительность, у 1 (4%) больной - при увеличении дозы препарата - зрительные галлюцинации. Довольно часто ЛЕВ вызывает психические и поведенческие расстройства, которые, по данным КогЬу В. а1. (2003), являются причиной его отмены почти у 9% больных. В нашем исследовании отмена лечения не потребовалась ни у одного больного.
Сравнительная характеристика побочных эффектов при монотерапии различными АЭП. Таким образом, побочные эффекты терапии наиболее часто наблюдались при приеме ВПА (37,31%), несколько реже при лечении КБЗ (23,08%) и ОКЗ (20,83%) (различия статистически недостоверны, р>0,05). При приеме ТПМ и ЛЕВ этот показатель составил 19,30% и 16% соответственно (при сравнении с ВПА достоверность различий по Стьюденту р<0,01, с КБЗ и ОКЗ - различия недостоверны р>0,05). Между тем, частота отмены АЭП в связи с клинически значимыми побочными эффектами практически не различалась для ВПА, КБЗ и ТПМ, составив 1,92-3,51%. Снижение уровня КЖ в качестве единственной причины, потребовавшей отмены принимаемого АЭП, зарегистрировано у 6 (8,96%) пациентов группы ВПА, 1 (1,92%) - КБЗ и 2 (3,51%) - ТПМ. При лечении ЛЕВ и ОКЗ побочные эффекты ни разу не стали причиной прекращения лечения.
Назначение больному конкретного АЭП должно производиться не только в зависимости от типа приступов. Необходимо учитывать и соматическое состояние пациента, а также риск развития тех или иных побочных эффектов терапии (возможная гепатотоксичность ВПА и КБЗ, нарушения сердечного ритма при приеме КБЗ, увеличение веса на фоне лечения ВПА, нефролитиаз и когнитивные расстройства при приеме ТПМ, поведенческие и психоэмоциональные расстройства при приеме ТПМ и ЛЕВ, аггравация приступов при лечении КБЗ).
Обсуждение.Стратегия лечения эпилепсии в настоящее время претерпела изменения. Современный подход к проблеме лечения эпилепсии предусматривает решение ряда вопросов, касающихся не только достижения максимального терапевтического эффекта, но и адекватного функционирования больных в обществе: образование, выбор профессии, трудоустройство, создание семьи (Карлов В.А. и др., 2000). Одним из значимых отрицательных факторов становится необходимость длительного, иногда на протяжении всей жизни, приема антиэпилептических препаратов (АЭП), которые сами могут снижать КЖ, вызывая физические, психические и когнитивные расстройства, обладать тератогенным воздействием (УшкаловаЕ.А., 2003).
После проведения необходимых диагностических процедур всем больным было назначено впервые или скорректировано предыдущее противоэпилептическое лечение. В зависимости от принимаемого АЭП все больные были разделены на 5 групп: группу вальпроатов (ВПА) (п=34), карбамазепина (КБЗ) (п=26), топирамата (ТПМ) (п=29), леветирацетама (ЛЕВ) (п=12) и окскарбазепина (ОКЗ) (п=11). Используемые суточные дозировки АЭП соответствовали индивидуальным клинически эффективным или максимальным переносимым дозам: для ВПА 1000-3000 мг, для КБЗ - 600-1800 мг, для ТПМ 200400 мг, для ЛЕВ 1500-3000 мг, для ОКЗ 9002400 мг. Препараты ВПА и КБЗ назначались в пролонгированных формах.
Среди больных, получающих лечение «традиционными» АЭП, преобладали лица, у которых терапия эпилепсии была стартовой: 67% в группе ВПА и 71% - КБЗ. В группах «новых» АЭП, большую часть составляли пациенты, у которых был осуществлен переход с ранее применяемой терапии в связи с ее неэффективностью или побочными эффектами: 54% в группе ТПМ, 56% - ЛЕВ и 67% - ОКЗ (рис.5.1). Этот факт, безусловно, отражал тенденцию использования «новых», дорогостоящих АЭП лишь в случае обоснованной необходимости. Более редкое назначение ЛЕВ в качестве стартовой монотерапии (44%) было обусловлено не меньшей его эффективностью, а скорее относительной новизной препарата и недостаточным опытом применения, а в отношение ОКЗ (33%) — еще и отсутствием возможности льготного обеспечения.
Во всех группах препаратов отмечалась достаточно высокая эффективность монотерапии симптоматических и предположительно симптоматических фокальных эпилепсий: ремиссия заболевания была констатирована в диапазоне от 44 до 56% при использовании разных препаратов (р>0,05). Однако наибольшая частота достижения ремиссии наблюдалась при использовании препаратов «новой» генерации: в группе ТПМ и ЛЕВ полная редукция приступов отмечалась у 56% больных, в группе ОКЗ - у 54%. Несколько реже ремиссия приступов была достигнута в группах «традиционных» АЭП: при использовании ВПА и КБЗ в 48% и 44% случаев соответственно. Ухудшение течения эпилепсии мы наблюдали у 1 пациента в группе ТПМ в виде учащения СПП и ВГСП. Напротив, в группе КБЗ не было ни одного случая аггравации приступов, что, прежде всего, связано с активным выявлением на этапе прескрининга при помощи ЭЭГ и ЭЭГ-видеомониторинга предикторов этого осложнения терапии - феномена ВБС.
Основные требования, предъявляемые к современным АЭП - максимум терапевтической эффективности при минимуме побочных эффектов [7]. Наиболее часто побочные эффекты терапии наблюдались в группе ВПА - у 37,31% больных. При приеме ТПМ и ЛЕВ, напротив, отмечена наименьшая частота побочных эффектов: у 19,30% и 16% больных соответственно (при сравнении с группой ВПА р<0,05). В группах КБЗ и ОКЗ этот показатель составил 23,08% и 20,83% соответственно (при сравнении с другими группами р>0,05). При лечении ЛЕВ и ОКЗ побочные эффекты ни разу не стали причиной прекращения лечения. Напротив, частота отмены в связи с клинически значимыми побочными эффектами практически не различалась для ТПМ и «традиционных» АЭП (ВПА, КБЗ), составив от 1,92 до 3,51%. Снижение уровня КЖ в качестве единственной причины, потребовавшей отмены принимаемого АЭП, несмотря на отсутствие клинической значимости побочных эффектов наиболее часто регистрировалось у пациентов группы ВПА (8,96%, п=6), реже в группах КБЗ (1,92%, п=1) и ТПМ (3,51%, п=2). Таким образом, по клинической эффективности «новые» АЭП оказались сопоставимы с традиционно использующимися представителями этого класса лекарственных веществ и превосходили последние по переносимости, что согласуется с данными литературы [9,10]. Топирамат продемонстрировал наиболее высокую противоприступную эффективность, однако частота отмены лечения из-за побочных эффектов приближали его к группе «традиционных» АЭП.
Выводы. Антиэпилептические препараты (АЭП) «новой» генерации (топирамат, леветирацетам, окскарбазепин) и «традиционные» (вальпроаты, карбамазепин) в равной степени эффективны при рациональной монотерапии симптоматических и криптогенных фокальных эпилепсий у взрослых. Леветирацетам и окскарбазепин отличаются более благоприятным профилем переносимости. Выявлено значимое влияние клинических и социальных показателей на больных эпилепсией. Персистирование приступов любого характера было значимым фактором развития аффективных расстройств, выраженность которых коррелировала с тяжестью приступов.
СПИСОК ЛИТЕРАТУРЫ
- Аванцини Д. Клинические формы и классификация эпилепсии // Сб., «Эпилепсия - медико-социальные аспекты, диагностика и лечение». М. —2004. - С. 29-46.
- Алиханов А.А., Петрухин А.С., Мухин К.Ю. и др. Магнитно-резонансная томография с высоким разрешением в оценке эпилепогенных поражений мозга // Русский журнал детской неврологии. Том I, выпуск 1. 2006, с. 18-24.
- Беги Э., Монтичелли М.Л. Социальные аспекты эпилепсии. Диагностика и лечение эпилепсии у детей. — М. - Можайск-Терра - 1997. - С. 656.
- Белоусова Е.Д., Харламов Д. А. Противоэпилептическая фармакотерапия и познавательные функции // Альманах клинической медицины. Т. VIII, часть 3. Тематический выпуск: Современные технологии диагностики и лечения неврологических заболеваний». — М., МОНИКИ. —2005. - с. 59-62.
- Берно-Бекуллер И.В. Качество жизни больных эпилепсией —пациентов диспансерного учета // Обозрение психиатрии и медицинской психологии / Санкт-Петербургский НИ психоневрологический институт им. В.М. Бехтерева (СПб). - 2005. -№2. - С. 16-18.
- Вассерман Л.И. Психодиагностическая шкала для оценки уровня социальной фрустрированности // Обозрение психиатрии и медицинской психологии. - 1995. -№2. - С. 73-79.
- Вассерман Л.И., Громов С.А., Михайлов В.А., Лынник С.Д., Флерова И.Л. Концепции реабилитации и качества исизни: преемственность и различия в современных подходах // Психосоциальная реабилитация и качество жизни. Сборник научных трудов. - Том 137. - СПб.: Санкт- Петербургский научно-исследовательских психоневрологических институт им. В.М. Бехтерева, 2001. - С. 103 - 115.
- Вейн А.М., Воробьева О.В. Оптимизация тактики терапии симптоматических парциальных эпилепсии с использованием ретарднои формы карбамазепина. В кн.: ЕРГ2000 // Восточноевропейская конференция "Эпилепсия и клиническая нейрофизиология", Крым, Гурзуф.2000. С. 193-194.
- Гехт А.Б. Качество жизни больных эпилепсией // Сб. Международная конференция «Эпилепсия - диагностика, лечение, социальные аспекты». М.-2005.-С. 120-124.
- Глухова Л.Ю., Мухин К.Ю., Петрухин А.С., Миронов М.Б. Топамакс в лечении симптоматической лобной эпилепсии // Журнал неврологии ипсихиатрии. - 2003. - Т. 103X12. - С. 51-52.