АННОТАЦИЯ
Цель работы: изучить высвобождение антиретровирусного лекарственного препарата в условиях in vitro.
Изучали высвобождение ритонавира из зарегистрированных капсул, содержащих 100 мг. Исследование проводили на аппарате «вращающаяся корзинка» при скорости вращения 100 об/мин при температуре 37 ± 0,5 оС. Среда растворения - 1 % раствор натрия додецилсульфата. Временные точки отбора проб: 15 мин, 30 мин, 45 мин, 60 мин, 90 мин. Количественное определение высвободившегося ритонавира проводили методом ВЭЖХ.
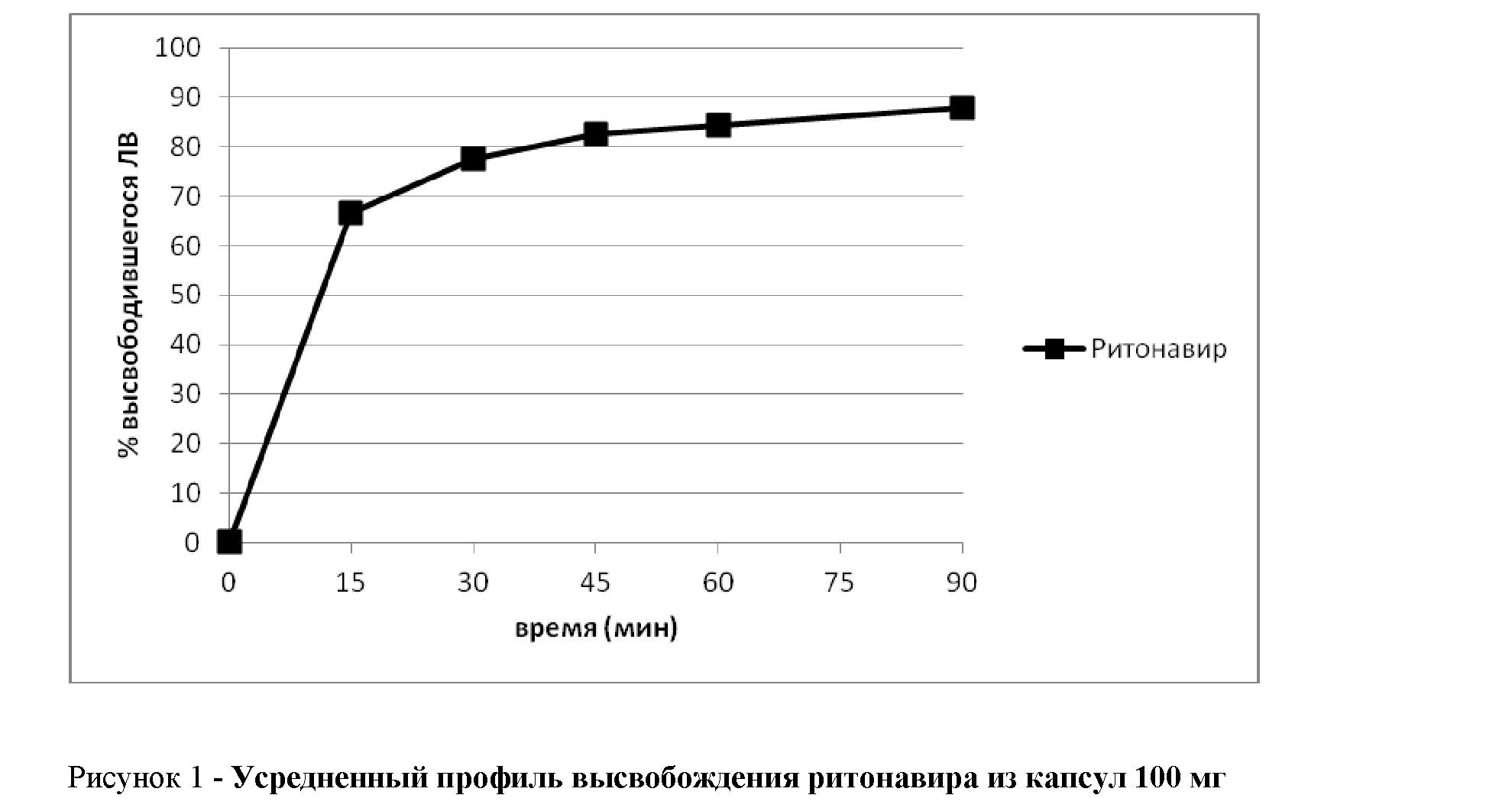
Выводы: по результатам исследования высвобождение ритонавира из капсул 100 мг в условиях in vitro характеризуется быстрым и плавным поступлением вещества в среду растворения (67 % через 15 мин, 78 % через 30 мин, 83 % через 45 мин, 84 % через 60 мин и 88 % через 90 мин).
Ключевые слова: ВЭЖХ, кинетика растворения, антиретровирусные лекарственные прапараты, высвобождение лекарственных прапаратов.
Введение.
ВИЧ-инфекция является одной из наиболее серьезных проблем общественного здравоохранения в Европе и мире. Каждый день в мире выявляется и регистрируется приблизительно 7400 случаев ВИЧ-инфекции, а 5500 человек умирают от заболеваний, вызванных СПИДом [1].
В 2012 г. 131202 новых случая ВИЧ-инфекции были зарегистрированы в 52 из 53 стран Европейского региона [2]. Большинство новых случаев ВИЧ-инфекции (37%) зарегистрировано в возрастной группе 30-39 лет, и 10% - в возрастной группе 15-24 года [2].
В настоящее время эпидемиологическая ситуация по ВИЧ-инфекции в России, по мнению Федерального научно-методического центра по профилактике и борьбе со СПИДом, признается как стабильно ухудшающаяся. Продолжается распространение ВИЧ среди населения и увеличивается кумулятивное число инфицированных больных [3]. Несмотря на меры, предпринимаемые по предоставлению лечения нуждающимся, увеличивается число смертей среди ВИЧ-инфицированных. За весь период эпидемии зарегистрировано 130245 случаев смертей среди ВИЧ-инфицированных лиц, в том числе 20302 смертей за 2012 год [4].
В соответствии со Стратегией развития фармацевтической промышленности Российской Федерации на период до 2020 года, необходимо увеличить обеспечение населения жизненно необходимыми и важнейшими лекарственными препаратами отечественного производства, а также лекарственными препаратами для лечения редких заболеваний [5]. Исходя из вышесказанного поставлена цель: изучить высвобождение воспроизведенного антиретровирусного лекарственного препарата, содержащего ритонавир в условиях in vitro (по тесту кинетики растворения).
Методы и материалы.
Исследование высвобождения (кинетики растворения) проводили в соответствии с требованиями Методических Указаний Минздравсоцразвития России «Оценка биоэквивалентности лекарственных средств», приложение 4, 2008 г.[6].
Тест «Растворение» проводили согласно ОФС 42-0003-04 «Растворение» на аппарате «вращающаяся корзинка» при скорости вращения 100 об/мин при температуре 37 ± 0,5 оС. Среда растворения - 1% раствор натрия додецилсульфата. Объем среды растворения - 900 мл.
Временные точки отбора проб: 15 мин, 30 мин, 45 мин, 60 мин, 90 мин.
Количественное определение проводили методом ВЭЖХ при длине волны УФ 240 нм, в качестве подвижной фазы использовали буферный раствор 0,03 М раствор калия фосфата однозамещенного : ацетонитрил (1:1).
Результаты и обсуждение.
Индивидуальные и усредненные значения количеств ритонавира, высвободившихся в раствор приведены в Таблице 1. Профиль растворения приведен на Рисунке 1.
Таблица 1- Индивидуальные и усредненные значения ритонавира, высвободившегося в раствор из капсул 100 мг
|
№ пробы |
15 |
30 |
45 |
60 |
90 |
|
1 |
68,02 |
74,68 |
81,24 |
85,35 |
89,45 |
|
2 |
67,70 |
84,41 |
83,07 |
85,65 |
87,54 |
|
3 |
66,00 |
72,94 |
75,83 |
80,96 |
83,24 |
|
4 |
61,84 |
74,55 |
83,12 |
83,69 |
86,82 |
|
5 |
66,36 |
77,57 |
82,86 |
85,06 |
90,99 |
|
6 |
69,77 |
82,18 |
89,23 |
86,23 |
90,06 |
|
Среднее, % |
66,62 |
77,72 |
82,56 |
84,49 |
88,02 |
|
RSD, % |
4,05 |
5,95 |
5,20 |
2,28 |
3,19 |
Согласно требованиям Методических Указаний Минздравсоцразвития России «Оценка биоэквивалентности лекарственных средств», приложение 4, 2008 г. величина относительного стандартного отклонения (RSD, %) не должна превышать 20 % для первой временной точки и 10 % - для остальных временных точек. Таким образом, полученные результаты являются достоверными.
Как видно из представленных данных, профиль высвобождения ритонавира из капсул 100 мг в условиях (in vitro) в целом соответствует профилю для лекарственных форм с немедленным высвобождением (полное высвобождение (т.е. более 85 %) достигается спустя 90 мин после начала теста), при этом отмечается быстрое и плавное поступление вещества в среду растворения (67 % через 15 мин, 78 % через 30 мин, 83 % через 45 мин, 84 % через 60 мин и 88 % через 90 мин).
Выводы.
Высвобождение ритонавира из зарегистрированных капсул 100 мг в условиях (in vitro) в целом соответствует профилю для лекарственных форм с немедленным высвобождением, при этом отмечается быстрое и плавное поступление вещества в среду растворения.
СПИСОК ЛИТЕРАТУРЫ
- Использованы материалы The Henry J. Kaiser Family Foundation http://kff.org/global-health- policy/fact-sheet/the-global-hivaids-epidemic/#footnote-UNAIDSGlobalReport
- Использованы материалы Европейского регионального бюро ВОЗ: http://www.euro.who.int/ru/media-centre/sections/press-releases/2013/11/hiv-infections-up-by-8-across- europe.-more-testingand-better-treatment-coverage-recommended
- Единая межведомственная информационно-статистическая система Федеральной службы государственной статистики Российской Федерации - «Число зарегистрированных больных с впервые в жизни установленным диагнозом ВИЧ-инфекции» http://www.fedstat.ru/indicator/ data.do?id= 41719 &referrerId=946905&referrerType=0, по состоянию на 25 октября 2013 г. http://www.fedstat.ru/indicator/data.do
- Письмо Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека от 4 июля 2013 г №01/7570-13-32 «О мерах по противодействию распространения эпидемии ВИЧ-инфекции в Российской Федерации»
- Приказ Минпроторга России № 956 от 23.10.2009 «Об утверждении Стратегии развития фармацевтической промышленности Российской Федерации на период до 2020 года».
- Методические указания «Оценка биоэквивалентности лекарственных средств». М., МЗСР РФ, 2008.- 32 c.