АННОТАЦИЯ
Методами квантовой химии и спектроскопии ЯМР 1H и 13C проведено исследование взаимодействия клеточного фосфатидилхолина с молекулами гистамина. Показано формирование комплекса лецитин - гистамина, изменение электронного строения, конформационных состояний, возникающих при комплексообразовании.
Ключевые слова: квантово-химическое вычисление, 13С ЯМР спектроскопия, химический сдвиг, фосфатидилхолин, гистамин, молекулярный механизм
Фундаментальные достижения квантовой физики и успехи спектроскопии в решении аналитических задач обусловили быстрый прогресс, открыли ранее недоступные возможности для синтеза новых соединений.
Непрерывно возрастающая, по интенсивности, деятельность человечества на данном этапе развития науки и технологий, обусловили возникновение в биосфере земли огромных масс веществ, которые отсутствовали в период эволюции. Основная масса этих веществ является синтезированным или выделенным из природного сырья в новейшее время. Эта масса, в последние годы, возрастает со скоростью 105 новых молекул в год. Принято считать, что все химические соединения обладают какой-то формой биоактивности.[1,2,3]
Среда обитания человека испытывает все возрастающие нагрузки от влияния новых соединений, синтез которых не всегда вызывает осознанной необходимостью и в настоящее время возникла настоятельная необходимость прогнозирования длительного, безопасного существования человека в этой все более насыщаемой биоактивными соединениями в среде обитания.[4,5]
Эти ставшие реальностью проблемы, связанные с условием жизни человека ставят проблемы создания теории биологической активности, способной дать возможность выбора необходимых лекарственных препаратов, из имеющихся синтезированных молекул, и направленного синтеза соединений с необходимыми свойствами.
На данном этапе развития науки, решение этой чрезвычайно сложной задачи нуждается в экспериментальном исследовании молекулярного механизма действия отдельных групп биоактивных соединений. В частности, их влияния на электронное строение и, как следствие, на биологические функции биологических молекул. В настоящем сообщении приводятся результаты исследовании взаимодействия молекулы (4-(2 - аминоэтил) имидазола, (гистамина) с клеточным
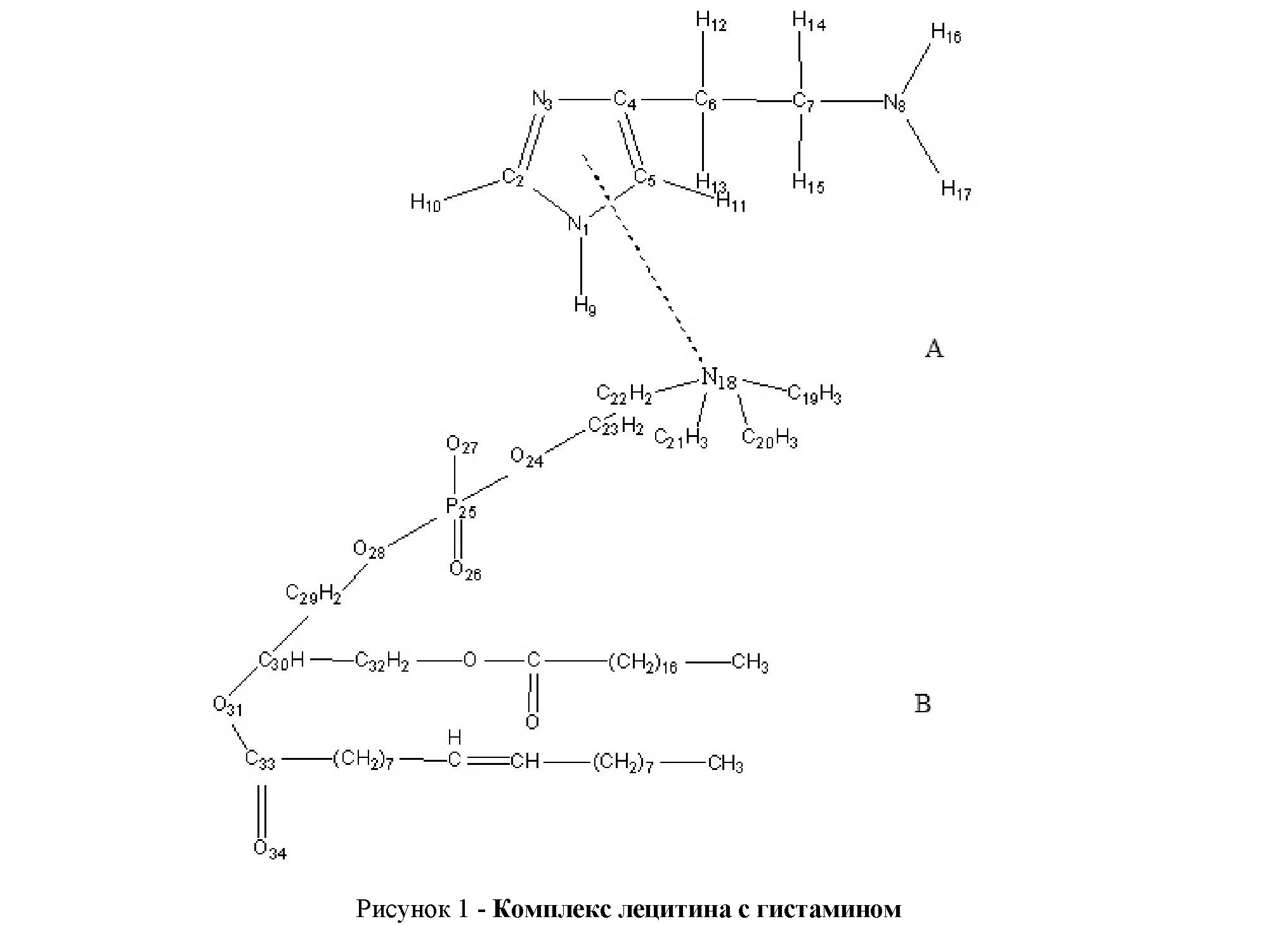
фосфатидилхолином (лецитином),, которая является одной из я структурообразующих молекул клеточной мембраны в Гистамин соединение из группы имидазолов, обладающий широким спектром физиологического действия, в том числе, служит регулятором важных функций организма (рис.1).[6]
Материалы и методы. Работа проведена методами квантовой химии и спектроскопии ЯМР 13С и 1Н.
В расчетах использовались методы AM1 и DFT для исследования комплексов, для сокращения времени расчетов использовался смешение методов AM1 и DFT.[7] Метод функционала плотности применялся для расчета активных фрагментов лецитина. Углеводородные цепи рассчитывались в приближении AM1.[8] Начальные конфигураций молекул, формирующий комплекс, в состоянии изолированных молекул методом молекулярной механики приводились в наиболее устойчивое расположение.
Полученная конфигурация комплекса уточнялась указанными методами. Результаты расчетов показывают, что возникают несколько комплексов, из них наиболее устойчивым и наибольшей энергией комплексообразование является положение, когда гетероцикл гистамина связан посредством Л - системы электронов с холиновой группой и взаимодействует с фосфатной группой. Изменение электронного строения молекулы лецитина при комплексообразовании представлена в таблице.
Как видно из таблицы, наиболее заметное изменение населенности происходит на Pz орбитали атома азота и Px орбитали ближайшего к гетероциклу гистамина атома углерода C20 холиновой головки.
S орбитали атомов азота и углерода меняются незначительно. Полученная из расчетов величина энергии комплексообразование равна 9,13 ккал/моль это значение энергии соответствует взаимному расположению молекул, когда гетероцикл гистамина посредством Л - системы электронов взаимодействует с холиновой головкой, а N(8)H2 группа связана с фосфатной. Необходимо отметить. что это значение энергии получается как малая разность больших величин и имеет заметную погрешность.[9] Применяемые при эксперименте растворители имели индекс ЧДА значение PH растворов поддерживали равным 7,1. Такая величина PH дает минимальное влияние среды на химический сдвиг. Концентрация фосфатидилхолина при значении спектров была равным 0,005М. При такой величине концентрации лецитин еще не образует мицеллы.
При большей концентрации точки связывания остаются внутри мицелл и спектральные линии умеряются. Точность определения химических сдвигов уменьшается.[10]
Спектры ЯМР 13C и 1H регистрировались на спектрометре Bruker Avance III с рабочей частотой 500,13 Мгц 1H при температуре 30°C.
В эксперименте использовался пятимиллиметровый датчик с Z градиентом PABBO при постоянной температуре образца. С целью увеличения цифрового разрешения применялось дополнение нулями и умножение Фурье-образа спектра на экспоненциальную функцию.
(Ie=0,1 Гц для 1H и 1 Гц для 13C). Спектры 13C с развязкой от протонов переменной мощности (powergated) с использованием составных импульсов WALTZ регистрировались при следующих условиях:
Спектральное окно - 29,8 кГЦ, количество точек - 64 к, длительность возбуждающего импульса составляла 3.2 МКС(30°), релаксационная задержка - 2 с, количество прохождений
достигало 2048, такое число прохождений обеспечивает соотношение сигнал/шум не менее 60. Редактирование спектров от ЯМР 13C проводилось на основании экспериментов DERT-90 и DERT- 135. Цифровой метод измерения химических сдвигов дет возможность определить их значение с точностью до 0,001 м.д. Точки отсчета на ядрах 13C служила спектральная линия TMS. Все эксперименты проведены под аргоновой защитой.
Результаты и обсуждение. Структура комплекса представлена рис. 1. При взаимодействии фосфатидилхолина с 4-(2-Аминоэтил) имидазола образует достаточно большое число комплексов. В предыдущих работах нами было показано, что в сопряженных циклических системах при комплексообразовании одновременно с хорошо изученными водородными связями возникают комплексы посредством Л - системы электронов [10]. В данной работе основное внимание уделяется комплексу, возникающему при взаимодействии Л - системы электронов гетероцикла гистамина с холиновой группой лецитина.
Изменения электронного строения молекул лецитина под действием гистамина, полученные в результате квантово-химических расчетов, представлены в табл. Как видно из таб. наименьшие изменения наблюдаются в населенности s-орбитали. s-орбитали атома N остаются практически неизмененными. Комплексообразование сопровождается значительным изменением в р-орбиталях. Расчеты показывают, что гистамин с холиновой группой лецитина образует несколько комплексов.
Приведенные в таб. данные соответствуют случаю, когда гетероцикл гистамина расположен ближе к атому C20, чем к другим атомам углерода. Изменения электронной плотности на ядрах углерода холиновой группы также наиболее значительны на ядре C20. Электронная плотность на этом ядру возрастает на 0,1026 а.е.
Рассчитанное значение энергии комплексообразования посредством Л - системы электронов составляет 9,1 ккал/моль. При одновременном взаимодействии группы N8H2 с фосфатной группой лецитина необходимо отметить, что энергия комплексообразования получается меньше разности больших величин и поэтому содержит значительную погрешность. Комплексообразование лецитина с гистамином вызывает изменение конформационных состояний фосфатидилхолина, для определения которого исследовали изменения конформационных характеристик изолированного фосфатидилхолина.
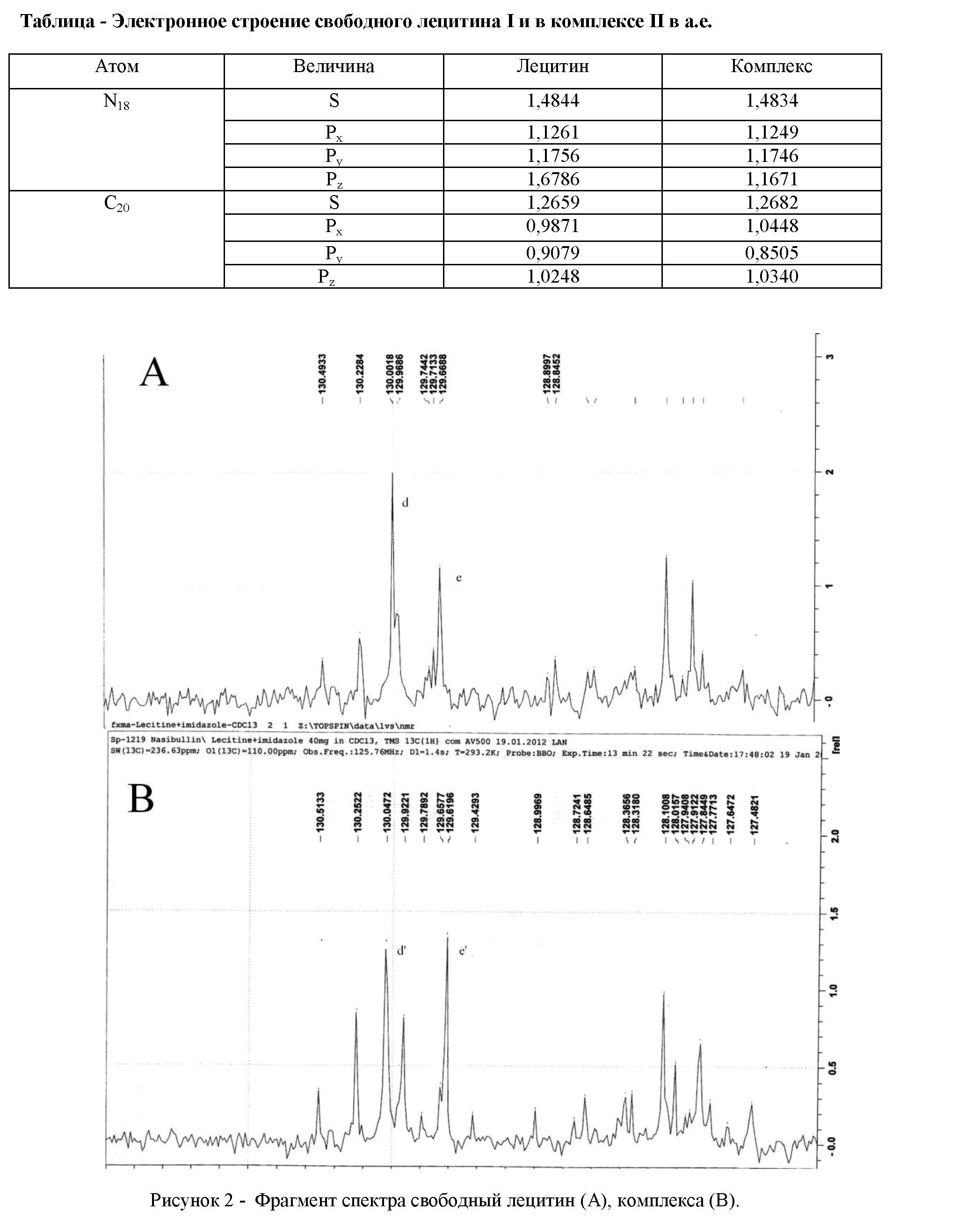
Полученные квантово-химическими методам результаты согласуются с экспериментальными данными ЯМР - спектроскопии. Химический сдвиг (XC) от ядер 13C метильных групп холиновой головки равной 54,3094 при комплексообразовании смещается в сторону сильного поля на 0,1809 м.д. Знак смещения соответствует возрастанию электронной плотности на ядре C20.
Однако, измененная величина XC не отражает истинное значение XC, обусловленное комплексообразованием. Как видно из спектральных данных и в растворе гистамина, и лецитина одновременно формируются несколько комплексов, между которыми происходит в быстрой шкале времени ЯМР обмен, приводящий к усреднению наблюдаемых значений XC. В данном случае, как видно из рис. 2, к комплексам, формирующимся посредством хорошо изученных водородных связей, добавляется комплекс, образующийся при взаимодействии атомов углерода, формирующих двойные связи с гистамином. При формировании этого типа комплекса, XC с (130,0472) смещается на 0,045 м.д. в сторону сильного поля. Одновременно наблюдается небольшое изменение XC от ядер углерода в двойных связях. У свободного лецитина спектральные линии от ядер углерода в двойных связях наблюдаются слитно ( линия d рис.2 ). При образовании комплекса сигнал от правого ядра смещается в сторону сильного поля на 0,4276 м.д. ( линия е рис.2 ) и сигналы от левого и правого ядра углерода различаются, что показывает переход данного звена цепи из транс в цис конформацию..
Анализ конформационных состояний комплекса показывает, что возрастание плотности электронов на узловом ядре углерода C30 приводит к увеличению среднего расстояния между углеводородными хвостами лецитина, следовательно, к возрастанию коэффициента проницаемости мембран. Это обстоятельство, по-видимому, является одной из причин расширения капилляров.
СПИСОК ЛИТЕРАТУРЫ
- Маленков А.Г. Биологически активные вещества. М. Наука, 1986.
- Васильев Ю.М, Маленков А.Г. Клеточная поверхность и реакции клеток, Л. Медицина 1965.
- Н.В. Кохина, Л.А. Валеева, Л.И. Биктимирова. Действие препаратов женских половых гамонов на гистаминовые рецепторы сердца при хирургической минопаузе. Медицинский вестник Башкортостана. 2006 №1. С. 244.
- Setchtnkov M.S., Usmanova S.I., Afanas’eva Yu.G., Nasibullin R.S. Complexing of some biologically active molecules with phosphatidylcholine // Russian Physics Journal. 2009. V. 52, № 4. P. 417-420.
- Breitmaier E., Spohn K.-N. P11-Hbhangigkeit der 13C-Chemischen Verschiebungen Sechsgliedriger stickstoffheteroaromate // Tetrahedron. 1973. V. 29, is. 8. P. 1145-1152.
- Насибуллин Р.С., Спирихин Л.В., Пономарева В.А. Образование комплексов молекулы пиразола с фосфолипидами // Биофизика 1991. Т. 36, № 4. С. 594-597.
- Насибуллин Р.С., Галеева Р.И., Юсупова З.Д. Молекулярный механизм и комплексообразование апигенина с клеточным фосфатидилхолином // Бутлеровские сообщения. 2012. Т. 32, № 10. С. 68-71.
- Буркерт У., Эллинджер Н.Х. Молекулярная механика / пер. с англ. М. : Мир, 1986. 364 с.
- Арташян О.С., Юшков Б.Г., Мухлынина Е.А. Изучение функциональной активности тучных клеток при иммобилизационном стрессе // Цитология. 2006. Т. 48, № 8. С. 665-669.
- Насибуллин Р.С., Кузницова М.В., Фахритдинова Д.И. Воздействия гистамина на клеточный фосфатидилхолин. Химическая физика и мезоскопия. 2013, Т. 15, №4. 627.
- Афанасьева Ю.Г., Насибуллин Р.С. Изменение структуры фосфолипидов клеточных мембран под действием флавоноидов // Вопросы биологической медицины и фармацевтической химии. 2010. № 5. С. 41-45.
- Dawson R.M. On the mechanism of action of phospholipase A // Biochem. J. 1963. V. 88, part 3. P. 414-423.
- Насибуллин Р.С., Усманова С.И., Сетченком М.С., Афанасьева Ю.Г., Фахретдинова Е.Р. О молекулярном механизме биоактивности рутина // Химическая физика и мезоскопия. 2008. Т. 10, № 2. С. 228-231.
- Иогансен А.В. Водородная связь. М. Наука, 1981. 134 с.