АННОТАЦИЯ
Цель работы: является стандартизация сухого экстракта валерианы лекарственный, входящего в состав нового оригинального седативного препарата «Седарем» таблетки, покрытые оболочкой и «Седарем» форте капсулы.
В состав препарата «Седарем» таблетки, покрытые оболочкой и «Седарем» форте в капсулах входят 4 вида растительных экстракты: 1.Сухой экстракта валерианы лекарственной, 2. Сухой экстракт пустырник туркестанский, 3. Сухой экстракт мяты перечной, 4. Сухой экстракт мелиссы лекарственный. Ранее проводилась стандартизация других субстанций, входящих в состав указанных препаратов, в частности сухих экстрактов пустырника Туркестанского, мелиссы лекарственной и мяты перечной [1,2,3].
Ключевые слова: стандартизация, валериана, ВЭЖХ, экстракт, сексвитерпеновых кислот.
Введение: Как известно, исследования по созданию комплексных профилактических средств из растительного сырья, обладающих мягким седативным действием, доступных широким слоям населения, эффективных и безопасных при их длительном применении, являются актуальной задачей фармацевтической науки и клинической медицины. Разработан оригинальный состав из четырех видов лекарственных растений, являющийся основой для получения седативных средств, при этом учитывались данные о применении препаратов лекарственных растений для лечения и профилактики неврозов и неврозоподобных состояний в традиционной и научной медицине, принципы составления многокомпонентных препаратов, сырьевые ресурсы и результаты фармакологического скрининга. На сегодняшний день аналогов по составу препаратов «Седарем» таблетки, покрытые оболочкой и «Седарем» форте в капсулах, в Республике Узбекистан и странах СНГ не имеется [4].
Методы и материалы. Стандартизация сухого экстракта валерианы была проведена согласно требованиям ГФ XI по показателям: описание, подлинность, потеря в массе при высушивании, тяжелые металлы, микробиологическая чистота и количественное определение.
Сухой экстракт валерианы лекарственный представляет собой сухой порошок от светлокоричневого до темно-коричного цвета, сильного своеобразного запаха, с высокой
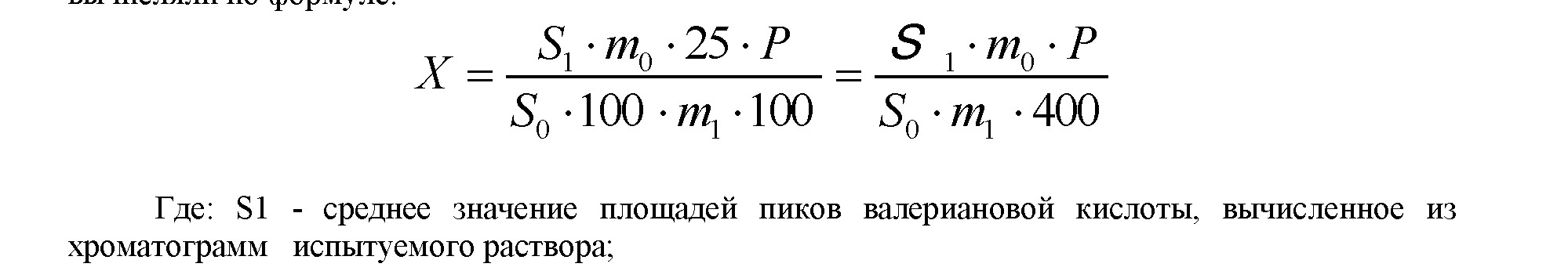
гигроскопичностью. Сухой экстракт валерианы лекарственный легко растворим в спирте и мало растворим в воде.
Потеря в массе при высушивании определялась в соответствие с требованиями ГФ XI, вып. 1, с. 176. Сушили при температуре 60 0С, при давлении 1 атм. в течение часа. Потеря в массе при высушивании составили не более 6,0 %.
Определение тяжелых металлов проводили по методике, описанной в ГФ XI. Все исследованные серии экстрактов выдерживали общее требования (не более 0,01 %).
Микробиологическую чистоту полученной субстанции проверяли на соответственное требованиям, указанным в ГФ XI, вып, 2, с. 193 и изменения №2 от 12.10.2005 г, категория 3.2 согласно которого в 1 г субстанций допускалось наличие общего число аэробных бактерий не более 104 общего числа грибов не более 102, энтеробактерий и некоторых других грамотрицательных бактерий не более 102 при отсутствии Esherichia coli, Pseudomonas aeriginosa, Staphylococcus aureus, при отсутствии и Salmonella 1 г субстанций. Все опытней серии выдерживали указанные требования.
Определение количественного содержания сесквитерпеновых кислот на пересчете на валериановую кислоту проводили методом высокоэффективной жидкостной хроматографии
Приготовление испытуемого раствора: Около 50 мг (точная навеска) испытуемого препарата помещали в мерную колбу вместимостью 25 мл, прибавляли 12 мл метанола,
подвергали обработке на УЗ-бане в течение 10 мин, объем раствора доводили до метки тем же растворителем, перемешивали. Полученный раствор фильтровали через бумажный фильтр «синяя лента».
Приготовление раствора рабочего стандартного образца (РСО) валериановой кислоты: Около 10 мг (точная навеска) РСО валерианой кислоты помещали в мерную колбу вместимостью 100 мл, растворяли в метаноле, (при необходимости подвергали обработке на УЗ-бане), объем раствора доводили до метки тем же растворителем, перемешивали [5].
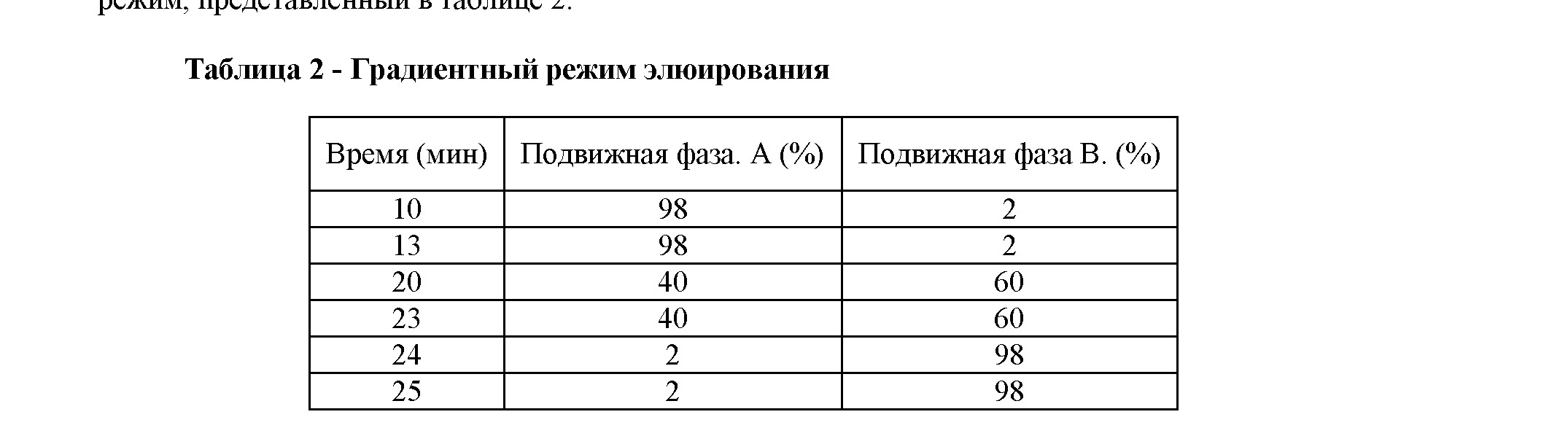
Использовали хроматографическую колонка Zorbax Eclipse,размером 4 * 100мм наполненную сорбентом С 18, Nucleosil 4*100мм с размером частиц 5 мкм . Подвижной фаза А являлся - 0,1 % раствор фосфорный кислоты, подвижной фазой В- Ацетонитрил 2-пропанол (3:7) содержащий 0,1% кислоты фосфорный. Для получения результатов использовали градиентный
УФ детектирование проводили при длине волны 230 нм; скорость потока подвижный фазы: 1,5 мл/ минут, объем вводимой пробы 20 мкл, температура термостата колонок составила 25 0С.
По 20 мкл испытуемого раствора и раствора РСО валериановой кислоты попеременно хроматографировали , получая не менее 5 хроматограмм для каждого из растворов, результаты которые представлены на рисунке 1.
Содержание сексвитерпеновых кислот (Х,%) в пересчете на валериановую кислоты RRTMUrTTCTTTU ТТЛ Thrm/TVITP"
95
S0 - среднее значение площадей пиков валериановой кислоты, вычисленное из
хроматограмм раствора РСО валериановой кислоты;
P - содержание валериановой кислоты в РСО валериановой кислоты в процентах;
m1 - масса навески препарата в граммах;
m0 - масса навески РСО валериановой кислоты в миллиграммах [6].
Результаты количественного определения сексвитерпеновых кислот в экстракте валерианы лекарственной подвергались статической обработке. (табл.3).
Таблица 3 - Результаты количественного определения сексвитерпеновых кислот в экстракте валерианы лекарственной
|
Содержание суммы сесквитерпеновых кислот в пересчете на валериановую кислоту, % |
Хср |
S2 |
S |
t(98%,4) |
А X |
А Хср |
Е |
E |
|
5,55 5,55 5,54 5,55 5,56 |
5,548 |
0,0037 |
0,008 |
2,78 |
0,0083 |
0,008 |
0,56% |
0,25% |
На основе полученные данных нормой содержания сесквитерпеновых кислот в сухом экстракте валерианы лекарственной установлен не менее 4 %.
Выводы. Впервые проведены исследования по стандартизации сухого экстракта валерианы лекарственной методом ВЭЖХ. На основании полученных данных разработаны и представлены на утверждение фармакопейные статьи предприятия на указанные препараты.
СПИСОК ЛИТЕРАТУРЫ
- Арипова Н.Б., Комилов Х.М. Стандартизация сухого экстракта пустырника туркестанского, используемого в составе препаратов. // Фармацевтический журнал, Ташкент.- 2013. -№4- С.39-42.
- Арипова Н.Б., Комилов Х.М. Стандартизация лекарственных форм мяты перечной. // Фармацевтический журнал, Ташкент. 2014. №2- С.52-56.
- Арипова Н.Б., Комилов Х.М. Стандартизация новых лекарственных форм меллисы лекарственный// Вестник КГМА, Бишкек. 2014. № 3- С.134-139.
- Государственный Реестр лекарственных средств и медицинской техники. №14. - 2014 г.
- Государственная фармакопея. изд. XI. - М.: Медицина, 1990. Вып.2. - С. 144.
- Helen Stimson. The Essential chromatography & spectroscopy catalog // 2011-2012 гг. - С. 1344.