АННОТАЦИЯ
Последняя актуализация правил надлежащего производства лекарственных средств и внедрение требований фармацевтической системы качества расширило нормативы GMP на все этапы жизненного цикла лекарственных средств, включая этап масштабирования процессов и трансфера технологии при внедрении в производство. Этот подход, в свою очередь, требует документирования всех процедур, которые должны быть основаны на структурировании (схематизации) процесса масштабирования и трансфера технологии в целом, чему и посвящены исследования, изложенные в данной статье.
Ключевые слова: лекарственное средство, жизненный цикл лекарственного средства, масштабирование процесса, трансфер технологии, фармацевтическая система качества, твердые лекарственные формы.
Цель исследования.
Современная система обеспечения качества лекарственных средств базируется на фармацевтической системе качества (PQS - Pharmaceutical Quality System), которая установлена ICH (International Conference on Harmonization of Technical Requirements for Registration of Pharmaceuticals for Humane Use) [1,2]. Основополагающий принцип системы PQS - качество каждого лекарственного средства может быть гарантировано для конечного потребителя только при условии, что оно встраивается и обеспечивается на каждом этапе жизненного цикла продукта. В соответствии с последней актуализацией правил надлежащего производства требования GMP распространены (расширены) на все этапы жизненного цикла лекарственного средства [1,2].
Одним из этапов жизненного цикла лекарственного средства, предшествующего его рутинному серийному промышленному выпуску, является масштабирование процесса производства до уровня промышленного и трансфер технологии (Technology Transfer) [2]. Выработка единообразных (стандартизованных) процедур в рамках общего процесса трансфера технологии позволит регламентировать и унифицировать их применительно к любому продукту, а также реально на практике обеспечить качество лекарственного средства на следующем этапе его жизненного цикла - производстве коммерческих серий продукции (Commercial Manufacturing).
Задачами данной работы являлось: схематизация подходов к процедурам
масштабирования процессов и трансфера технологии при внедрении в производство лекарственных средств, применительно к производству твердых дозированных лекарственных форм, а так же определение основных направлений разработки письменных процедур (методик, SOPs) для полноценной письменной регламентации этого процесса.
Материалы и методы.
Разработка процедур для этапа масштабирования процесса и трансфера технологии, как отдельного процесса в рамках PQS, возможна, если существуют (разработаны) процедуры встраивания качества в лекарственное средство на предыдущем этапе его жизненного цикла - в рамках процесса фармацевтической разработки (Pharmaceutical Development) [2,3].
Один из основополагающих принципов фармацевтической системы качества, который регламентирован последней актуализированной редакцией правил GMP EU: «управление продукцией и знаниями должны осуществляться на всех этапах жизненного цикла продукта» [1]. Применение системы управления знаниями (Knowledge Management) на этапе масштабирования техпроцесса и трансфера технологии должно позволить не только не потерять полученные и накопленные на этапе фармразработки знания, но и максимально полно использовать их для решения следующих задач (в рамках системы PQS):
- сформировать программу мероприятий по переносу технологии (Technology Transfer), включая испытания по масштабированию технологии (в лабораторных условиях, на «пилотном» участке, в условиях промышленного производства) с учетом требований ICH;
- составить и обосновать программу мониторингов параметров процесса получения (производства) и качества продукта (Process Performance and Product Quality Monitoring System), в соответствии с требованиями PQS и основываясь на системе управления рисками (QRM - Quality Risk Management) [4];
- провести масштабирование технологического процесса до стандартизованных размеров коммерческих серий продукта (с учетом производственной рецептуры / формулы, приводимой в регистрационном досье на продукт), осуществить перенос технологии на реальные производственные мощности производственного участка, а также обзор (мониторинг, анализ) предварительно оцененных рисков (Risk Review);
- разработать программу проверки правильности, воспроизводимости и стабильности процесса промышленного производства продукта и схему валидации технологического процесса (Process Validation Scheme), если это необходимо и допустимо (например, при формировании регистрационного досье в формате CTD) [5];
- провести валидацию технологического процесса (Process Validation), как проверку его правильности, воспроизводимости и стабильности (в соответствии с разработанной программой и схемой) согласно традиционных требований GMP EU (annex 15) [1] и/или актуализированных подходов к валидации процессов (Process Validation: General Principles and Practices) [6].
Как результат - обеспечить внедрение продукта, введя в действие окончательно утвержденные версии основной производственной документации и системы мониторингов качества каждой коммерческой серии продукта.
Специфика производства твердых дозированных лекарственных форм - таблеток и твердых желатиновых капсул - требует особого внимания при переносе технологии (масштабировании процессов и трансфере технологии) из-за сложности самого технологического процесса производства. Наиболее значимым, для воспроизводимости процессов при их масштабировании и трансфере, является применение стрессовых, в отношении действующих и вспомогательных веществ, технологических операций. К таким операциям можно отнести: получение смеси компонентов (аспекты совместимости, стабильность), получение гранул (воздействие влаги, температуры, кислорода воздуха), получение массы для таблетирования или инкапсулирования (аспекты обеспечения однородности распределения гранулята и опудривающих компонентов), получение лекарственной формы (механические воздействия) и др. Каждая из этих операций характеризуется значительным количеством регулируемых и изменяемых параметров, что способствует возникновению риска ухудшения показателей качества ... как промежуточных продуктов, так и готового лекарственного средства, поддержания стабильности качественных показателей при установленном сроке хранении. Правильный подбор параметров ведения каждой из операций процесса, а также правильная программа мониторингов этих параметров, обоснованные результатами оценивания рисков (Risk Assessment) - залог успешной практики масштабирования технологических процессов и трансфера технологии этого вида фармацевтической продукции.
Результаты и обсуждение.
В результате проведенной работы для последующей организации практических и систематизированных мероприятий по масштабированию процесса и трансферу технологии, нами: - обоснована необходимость выделения комплекса процедур по масштабированию процессов и трансферу технологии как отдельной самостоятельной системы/процесса в рамках требований PQS и с учетом системного/процессного подхода;
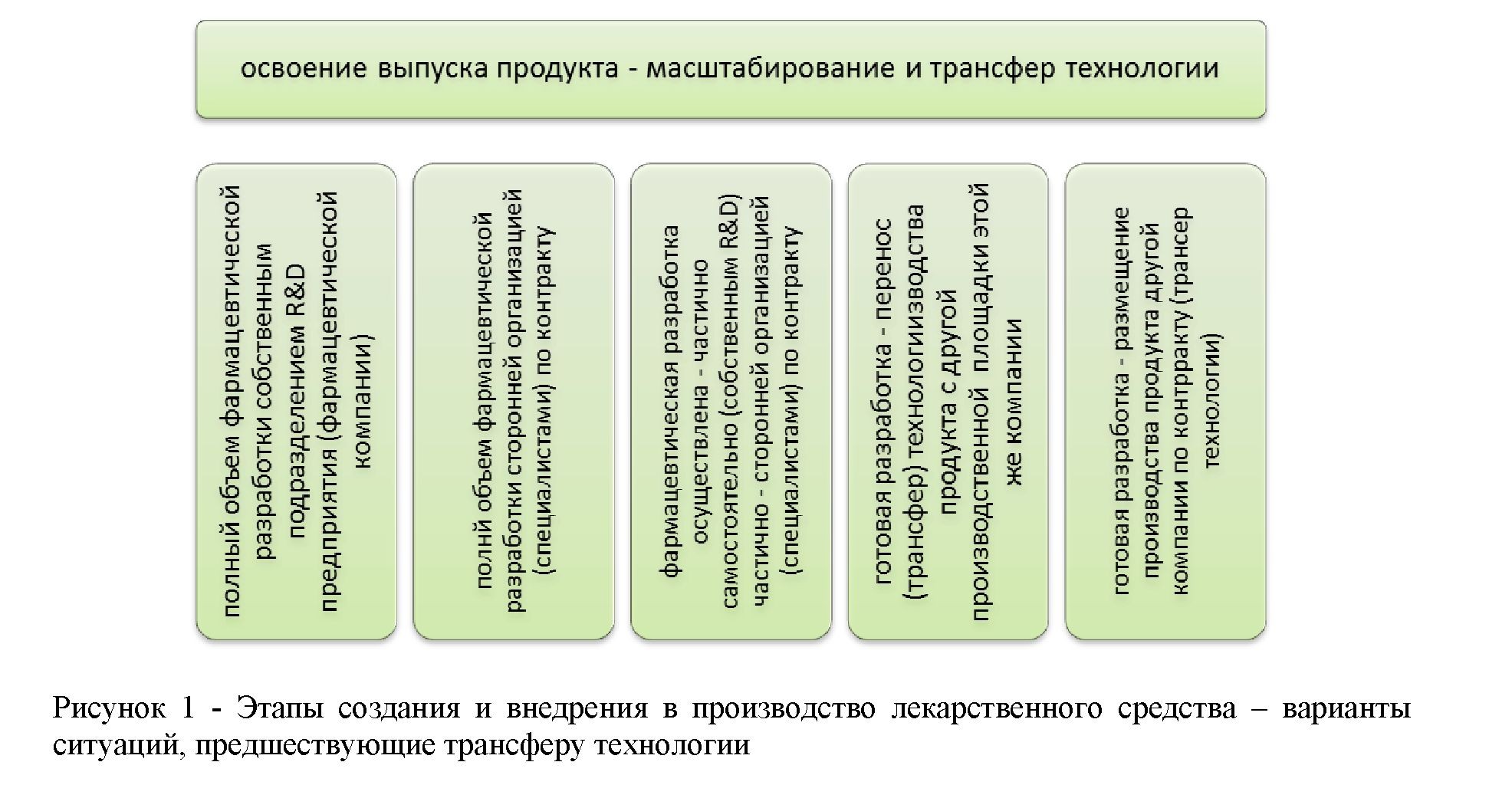
- определены варианты ситуаций, предшествующие трансферу (переносу) технологии на промышленный производственный участок, как факторы, определяющие вариабельность процедур масштабирования и трансфера технологии (схематично представлена на Рис.1);
- сформулирована и схематично визуализирована систематизация основных групп мероприятий в рамках процесса масштабирования и трансфера технологи (схематично представлена на Рис.2 - с отображением основных составляющих процесса и ожидаемых документально оформляемых результатов по каждой из этих составляющих), а так же блок- схема этого процесса.
Предложенная схематизация процесса масштабирования и трансфера технологии обеспечивают рациональный алгоритм создания (разработки) системы документации, детально регламентирующей соответствующие процедуры. Документирование процедур в рамках системы масштабированию процесса и трансфера технологии позволит, в свою очередь, стандартизовать соответствующие действия и их последовательность, распределить ответственность между подразделениями и отдельными специалистами (персонал), максимально на практике оптимизировать весь процесс. В конечном итоге, в соответствии с требованиями современной системы PQS - обеспечить встраивание качества в продукт на данном этапе жизненного цикла продукта и, соответственно, повысить гарантии для конечного потребителя в качестве, безопасности и эффективности лекарственного средства, производимого в промышленных масштабах и реализуемого в коммерческих объемах.
ВЫВОДЫ.
Таким образом, в результате проведенной работы была предложена схематизация подходов к процедурам масштабирования процессов и трансфера технологии при внедрении в производство лекарственных средств (применительно к производству твердых дозированных лекарственных форм), а также определены основные процедуры, для которых потребуются письменно прописанные методики (SOPs).
СПИСОК ЛИТЕРАТУРЫ
- The Rules Governing Medicinal Products in the European Union. Volume 4. EU Guidelines to Good Manufacturing Practice Medicinal Products for Human and Veterinary Use. - 2013. - Chapter 1. Pharmaceutical Quality System.
- Document ICH Q10. Pharmaceutical Quality System. 2009.
- Document ICH Q8(R2). Pharmaceutical Development. 2009.
- Document ICH Q9. Quality Risk Management. 2006.
- The rules governing medicinal products in the European Union. - V.2B. - Notice to applicants. Medicinal products for human use. Common Technical Document. - 2008.
- Guideline on Process Validation. - 2013 - EMA/CHMP/CVMP/QWP/70278/2012.