АННОТАЦИЯ
Представлены данные литературы и результаты собственных исследований по морфологическому изучению биоптатов яичка у больных сгипергонадотропнымгипогонадизмом, азооспермией. Приведены виды мужского бесплодия и нарушений сперматогенеза, а также указаны морфологические критерии их диагностики.
Ключевые слова: первичный гипогонадизм, азооспермия, сперматогенез, биоптаты яичка, Сертоли-клеточный синдром.
Мужское бесплодие, которое развивается вследствие ряда заболеваний или суммарных патологических воздействий на репродуктивную систему мужчин, является весьма актуальным в настоящее время во всем мире. Его патогенез, структура, диагностика продолжают оставаться предметом многих дискуссий [1,2]. Статистика ВОЗ из года в год предоставляет неутешительную информацию о том, что в 45% случаев бесплодных пар «виновником» является мужчина, а в 40% - женщина, оставшиеся случаи связаны с несовместимостью партнеров [3].
К сожалению, в большинстве наблюдений применение эндокринологических и генетических методов исследований не позволяет достоверно дифференцировать причину отсутствия сперматозоидов в эякуляте — нарушение сперматогенеза или нарушение проходимости семявыводящих путей. Многообразие факторов, приводящих к мужскому бесплодию, возможность их сочетания затрудняют выбор необходимых методов диагностики и лечения.
Восстановление репродуктивной функции растягивается во времени и негативно отражается на эффективности лечения [4,5,7,13].
К наиболее тяжелым причинам мужского бесплодия относится азооспермия, проявляющаяся отсутствием сперматозоидов в эякуляте. По данным разных авторов это состояние может бать выявлено у 10% бесплодных пациентов.
Следует дифференцировать обструктивную азооспермию, когда сперматозоиды из яичка и придатка не попадают в сперму вследствие обструкции семявыносящих путей и необструктивную, когда сперматозоиды не вырабатываются или не созревают должным образом. Обструктивная азооспермия обычно развивается на фоне хронических воспалительных заболеваний, вызывающих облитерацию просвета семявыносящих путей, в редких случаях - в результате врожденной аномалии семявыносящих путей и ятрогении. Причинами необструктивной азооспермии могут быть гормональные нарушения, варикоцеле, лучевоевоздействие, опухолевые процессы в яичках, влияние химиотерапии и др.
Остановка развития герменативных клеток также может быть вызвана генетическими факторами, такими как трисомия, аутосомные аномалии (транслокации, инверсии) или делециивҮ-хромосоме (Yqll) [13]. Дифференцировать эти патологические процессы может помочь только проведение морфологического исследования биоптата яичка, позволяющее определить патологию и уровень повреждения сперматогенеза [4,5]. Анализ гистологических препаратов включает в себя оценку гистологических изменений в каждом, отдельно взятом семенном канальце путем раздельного подсчета количества имеющихся клеток (сперматогоний, сперматоцитов, округлых и вытянутых сперматид, клеток Сертоли), состояния собственной пластинки (базальной мембраны) состояния и состава интерстициальной ткани. При выявлении в семенном канальце половых клеток следует определить стадию сперматогенеза.
Термином «сперматогенез» обозначают период развития мужских гамет в эпителии семенных канальцев из диплоидных сперматогоний, имеющих контакт с базальной мембраной, до высвобождения дифференцированных гаплоидных половых клеток в просвет семенных канальцев. Данный процесс включает пролиферацию и дифференцировку сперматогониев, мейотическое деление первичных и вторичных сперматоцитов и трансформацию гаплоидных ранних округлых сперматид в сперматозоиды. Последний этап называется «спермиогенез». Высвобождение вытянутых (зрелых) сперматид в просвет семенных канальцев обозначается термином «спермиация». При этом гаплоидные клетки в эпителии семенных канальцев называются «сперматидами», а гаплоидные мужские гаметы после спермиации — «сперматозоидами».
Большинство исследователей выделяют 6 стадий сперматогенеза, представляющих собой несколько одновременно развивающихся волн сперматогенеза в эпителии семенных канальцев.
Стадия I характеризуется наличием ранних округлых сперматид с акросомальным (апикальным) пузырьком после второго мейотического деления. На этой стадии выявляются сперматогонии типа А и В, сперматоциты 1-го порядка на стадии пахитены, округлые и вытянутые сперматиды.
Стадия II представлена сперматогониями типа А и В сперматоцитами 1-го порядка на стадии пахитены, округлыми и вытянутыми сперматидами, а также резидуальными тельцами, образовавшимися в клетках Сертоли из разрушенных сперматид.
Стадия III характеризуется началом конденсации ядер сперматид и вступлением сперматогоний типа В в мейоз (фаза прелептотена).
На стадиях IV и V отмечаются дальнейшая конденсация ядер сперматид и первичные сперматоциты на стадии пахитены. Выявление сперматоцитов 1-го порядка в фазу лептотены свидетельствует о стадии IV, а в фазу зиготены — стадии V. После стадии V первичные сперматоциты в фазу пахитены подвергаются диакенезу (последний этап профазы мейоза) и вступают в первое мейотическое деление.
Стадия VI характеризуется наличием сперматоцитов 2-го порядка. Эти сперматоциты подвергаются второму мейотическому делению после короткой (около 6 ч) интерфазы, вследствие чего стадия VI обнаруживается крайне редко [6,13,14,18] .
Если в большинстве семенных канальцев определяются практически все стадии сперматогенеза, то такая гетерогенная картина расценивается как «нормальный сперматогенез», как в качественном, так и в количественном аспекте. Так, если в семенных канальцах уменьшено число вытянутых сперматид или наблюдается неполный клеточный состав, то речь идет о «гипосперматогенезе» [8].
Важным этапом микроскопического изучения биоптата яичка является, на наш взгляд, количественная оценка степени нарушений сперматогенеза. Впервые такая бальная система для оценки качества сперматогенеза была предложена в 1970 г. S. Johensen [8], позже она была модифицирована D. DeKretser и A. Holstein [9]. Согласно последней, на гистологических препаратах должен быть оценен каждый семенной каналец. Такая система наиболее значима для пациентов с олигоастенозооспермией, поскольку имеется сильная зависимость между бальной оценкой сперматогенеза при гистологическом исследовании и количеством обнаруженных сперматозоидов.
Цель исследования: Определить морфологические нарушения сперматогенеза в биоптатах яичек у мужчин с гипергонадотропнымгипогонадизмом, осложненным азооспермией.
Материалы и методы. На базе кафедры урологии и нефрологии ОНМедУ г. Одессы проведено морфологическое исследования 24 биоптатов яичка, полученных у мужчин 26-40 лет, страдающих гипергонадотропным гипогонадизмом, азооспермией. Участки ткани яичка размером 0,25-0,4см фиксировали 10% забуференым формалином, заливали впарафин и изготавливали срезы толщиной 5 мкм споследующей обзорной окраской гематоксилиноми эозином, гистохимической окраской для визуализации соединительной ткани с применением пикриновой кислоты и кислого фуксина (Ван Гизон) постандартной методике. В результате гистохимической реакции коллагеновые волокна окрашивались вкрасный цвет. Подсчет клеток осуществляли с помощью программ статистических методов исследования, так же выясняли уровень половых и гонадотропных гормонов.
Результаты исследований и их обсуждение.
с целью изучения оценки морфо-функционального состояния ткани яичка использовали систему гистологического счета, описанную S.G.Johensen и модифицированную DeKretserandHolstein, согласно рекомендациям Европейского урологического общества.
Для изучения андрогенной функции яичек у 24 пациентов с первичным гипогонадизмом проведена оценка гипотоламо-гипофизарно-гонадной системы, включающая исследование содержания тестостерона (Т), ФСГ, ЛГ, пролактина (ПРЛ) и эстрадиола (Э). В процессе обследования нами отмечено, что практически у всех обследованных нами пациентов имелись нарушения уровня половых и гонадотропных гормонов.
Средний возраст больных составил(33,64±0,48) лет. Уровень Т крови колебался от 1,3 до 9,9 нмоль/л (в среднем составил 4,5±1,3нмоль/л), уровень ЛГ определялся от 2,1 до 14,1 МО/л (в среднем 13,4±5,3) МО/л). Уровень ФСГ равнялся от 4,4до 45,3 МО/л (в среднем составил 37,43±11,32) МО/л). Уровень ПРЛ крови составлял от 107,3 до 338,1 МО/л л (в среднем 266,1± 67,4) МО/л). Уровень Э крови состовлял от 37,2 до 101,7 пг/мл. (в среднем 64,21± 23,13 пг/мл.)
Нормальный сперматогенез, что соответствовал 100% согласно шкале D. DeKretser и A. Holstein, классифицировался наличием семенных канальцев, которые имеют тонкую базальную мембрану и последовательно расположенный сперматогенный эпителий. На внутренней стороне базальной мембраны располагаются сперматогонии, сперматоциты первого и второго порядков, единичные клетки Сертоли, группы сперматид и зрелых сперматозоидов.
Среди 24 обследованных, нормальный сперматогенез нами не выявлен. Наряду с этим анализ разновидностей половых клеток в семенных канальцах позволяет выделить ряд вариантов нарушения сперматогенеза.
Среди изученного нами материала гипосперматогенез был диагностирован в 6 (25%) биоптатах. Из них в 2 (8,3%) биоптатах канальцы сперматогенного эпителия частично десквамированы и располагались хаотично. Имеет местоочаговая гиперплазия клеток Лейдига, локализующихся в межканальцевой зоне. Процентная доля семенных канальцев согласно шкалеD. DeKretser и A. Holstein, нами оценена в 87%.(табл.1).
Таблица 1 - Количественная оценка степени нарушения сперматогенеза по шкале D. DeKretser и A. Holstein.
|
доля семенных канальцев содержащие вытянутые сперматиды, (%) |
n |
С%)биоптатов |
|
100-90 |
||
|
80-90 |
2 |
8,3 |
|
70-80 |
||
|
60-70 |
4 |
16,6 |
|
50-60 |
7 |
29,4 |
|
40-50 |
5 |
20,8 |
|
30-40 |
2 |
8,3 |
|
20-30 |
3 |
12,5 |
|
10-20 |
||
|
1-10 |
1 |
4,1 |
|
Всего |
24 |
100% |
Ослабленный сперматогенез наблюдали в 4 (16,6%) случаев,доля семенных канальцев, содержащих вытянутые сперматиды составила от 65 до70%. При этом клеточный состав зародышевых клеток уменьшен на всехстадиях развития
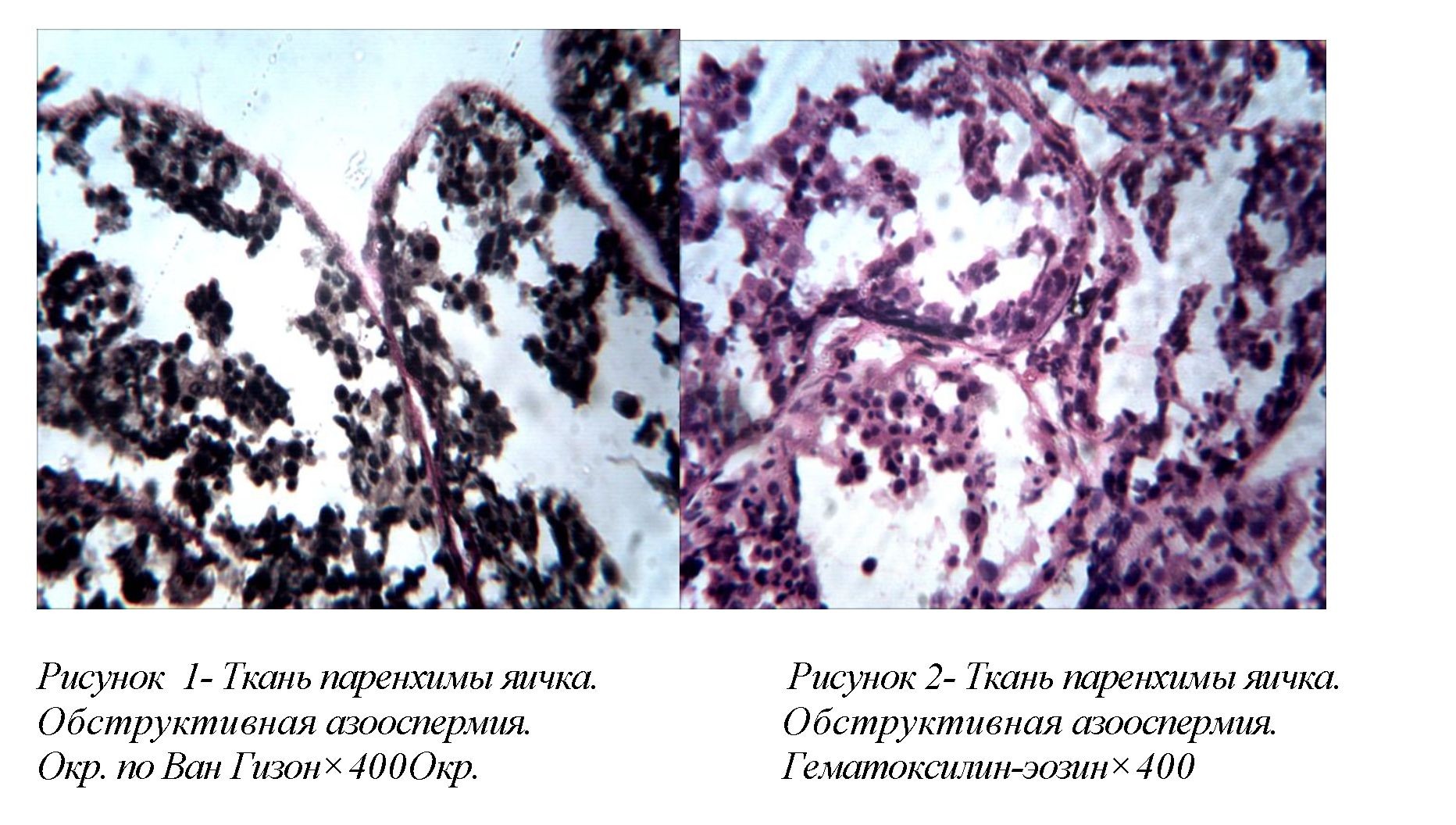
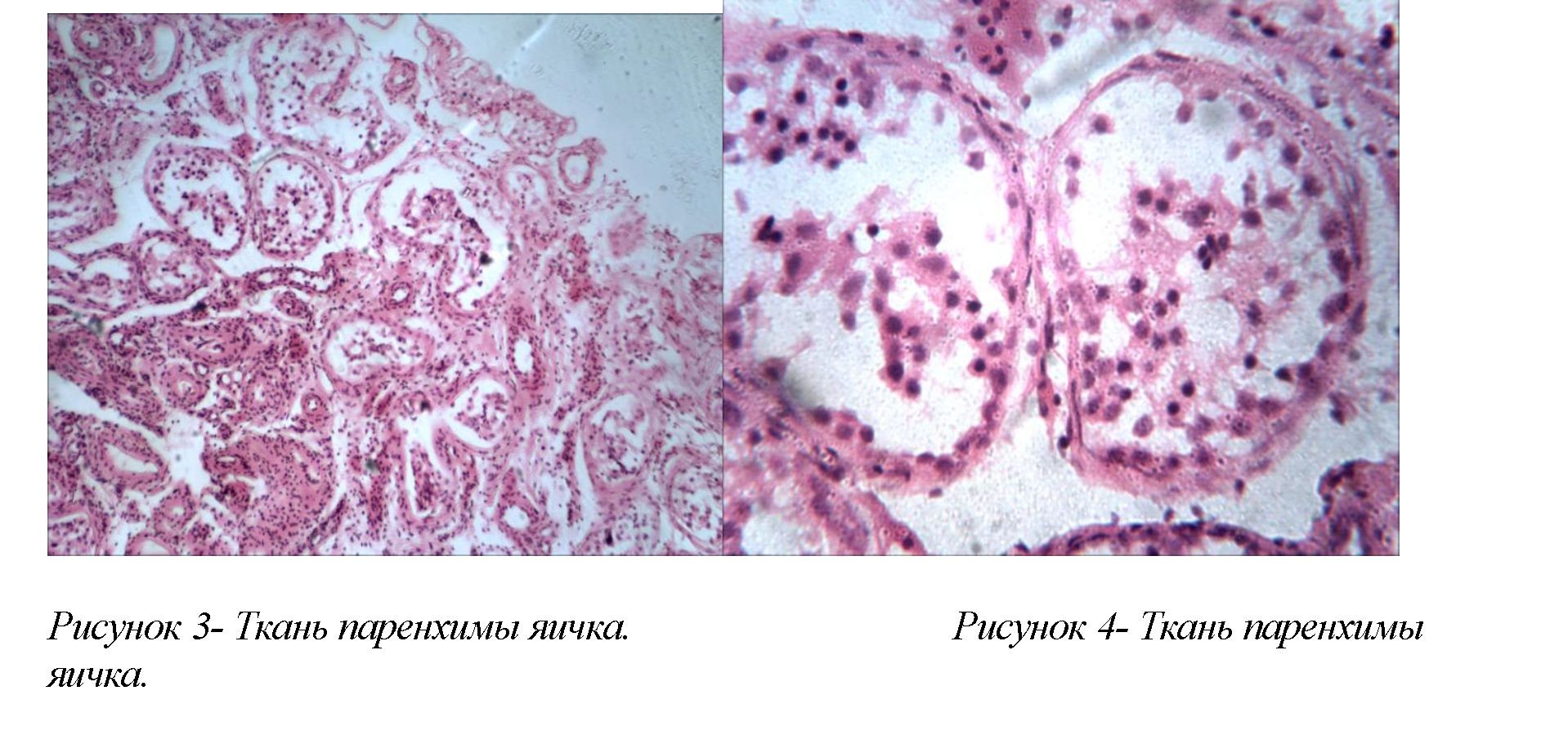
сперматогенеза. В строме отмечается очаговый фиброз и лимфогистиоцитарная инфильтрация. Такая морфологическая картина наблюдается при обструктивной азооспермии (рис. 1,2.).
Ткань яичка с нормальным количеством клеток Сертоли. В части канальцев клеточный пролиферат представлен обычным количеством сперматогониев, сперматоцитов первого и второго порядка и уменьшенным количеством ранних сперматид, часть из которых с умеренно выраженным полиморфизмом и фигурами митозов, а так же их десквамацией в просвет канальца. В канальцах признаки гипосперматогенеза.
В 75% случаев обнаруживали необструктивную азооспермию, связанную с нарушением сперматогенеза на каком то из этапов развития сперматогенеза. Из них у 7 (29,4%) биоптатов наблюдали блокаду развития зародышевых клеток на уровне сперматид, (рис.3,4).
Ткань яичка представлена с некоторым уменьшением количества клеток Сертоли. Уменьшением количества сперматоцитов первого и второго порядка. Ранние и поздние сперматоциты отсутствуют. Количество сперматогониев не изменено. Отмечается сужение просвета семенных канальцев с отсутствием признаков сперматогенеза. Согласно шкале D. DeKretser и A. Holstein, доля семенных канальцев, содержащих вытянутые сперматиды, оценивалась от 57% до 60%.
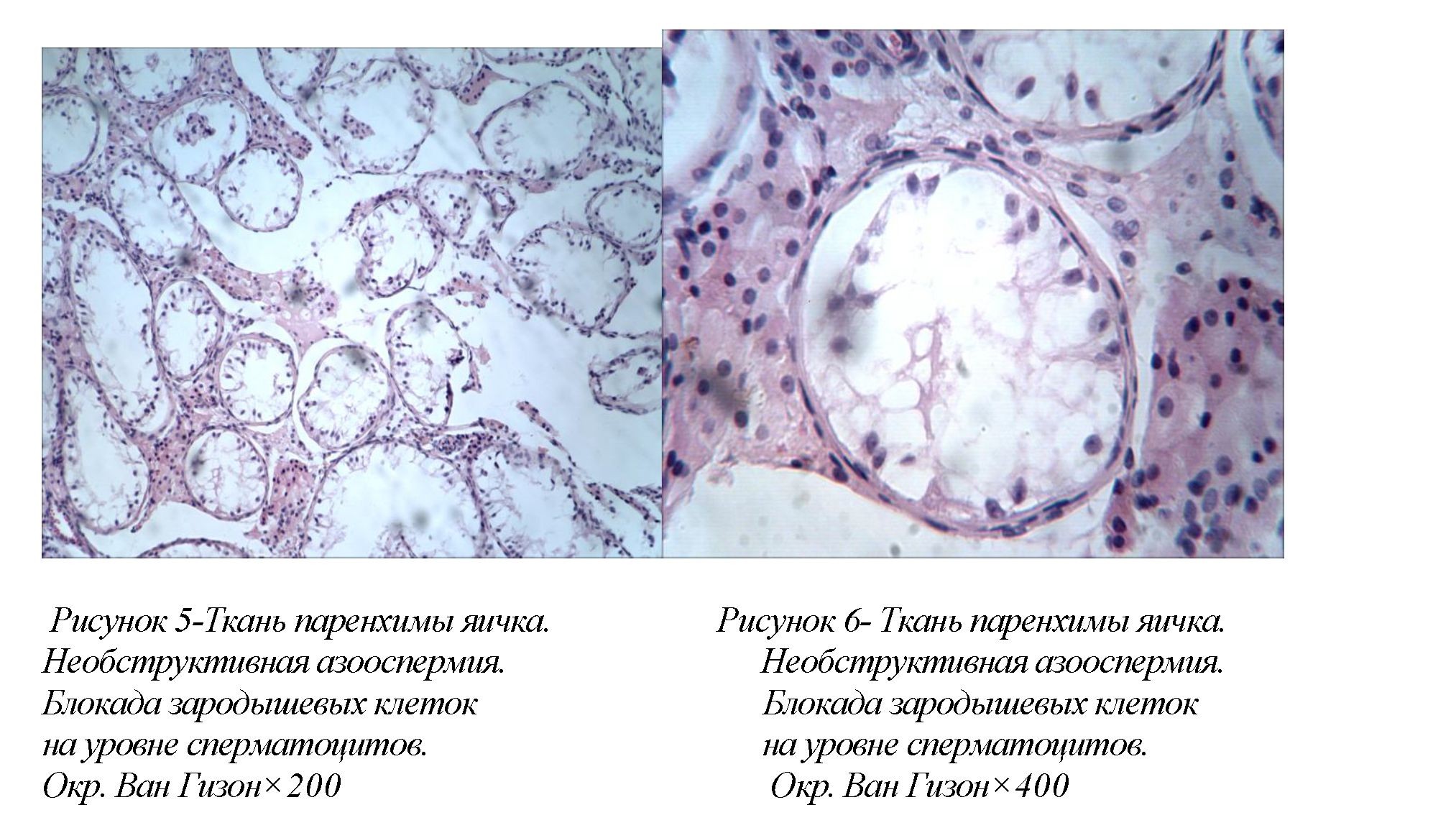
В 5 (20,8%) случаев обнаруживали необструктивную азооспермию, связанную сблокадой развития зародышевых клеток на уровне сперматоцитов, согласно шкале D. DeKretser и A. Holstein, оценена от 40 до 50 %. (рис.5,6).
Ткань яичка представлена с некоторым уменьшением количества клеток Сертоли. Уменьшение количества сперматоцитов первого и второго порядка. Ранние и поздние сперматоциты отсутствуют. Уменьшение количества сперматогониев. Склероз стенок семенных канальцев, очагово, до сужения их просвета с отсутствием признаков сперматогенеза.Слабо выраженный артериосклероз.
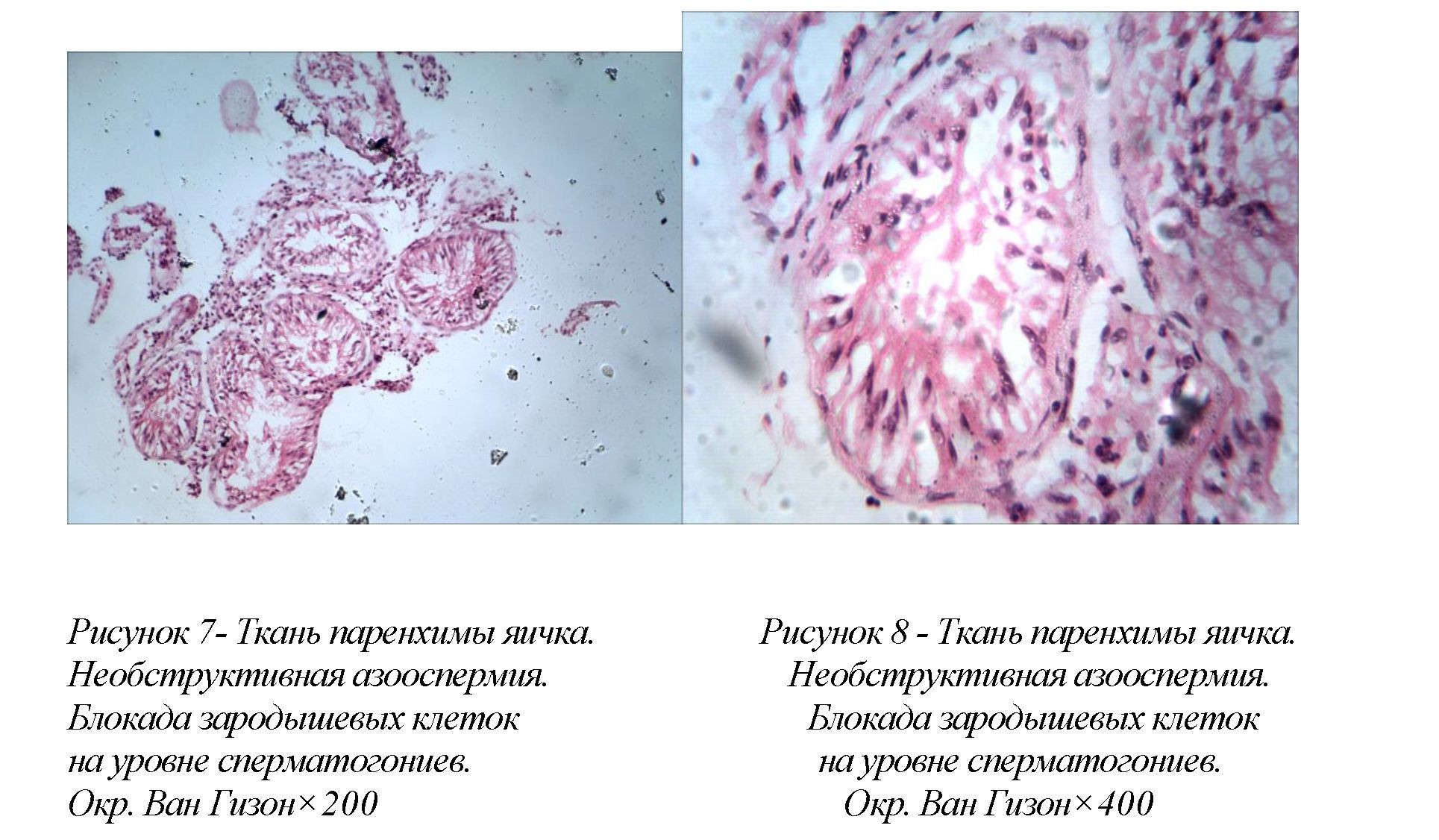
В 2(8,3%)случаев обнаруживалинеобструктивную азооспермию, связанную сблокадой развития зародышевых клеток на уровне сперматогониев. По критериям гистологического счета согласно модифицированной шкале D. DeKretser и A. Holstein, оценивается нами от 30% до 35% (смотрите рисунки 7,8).
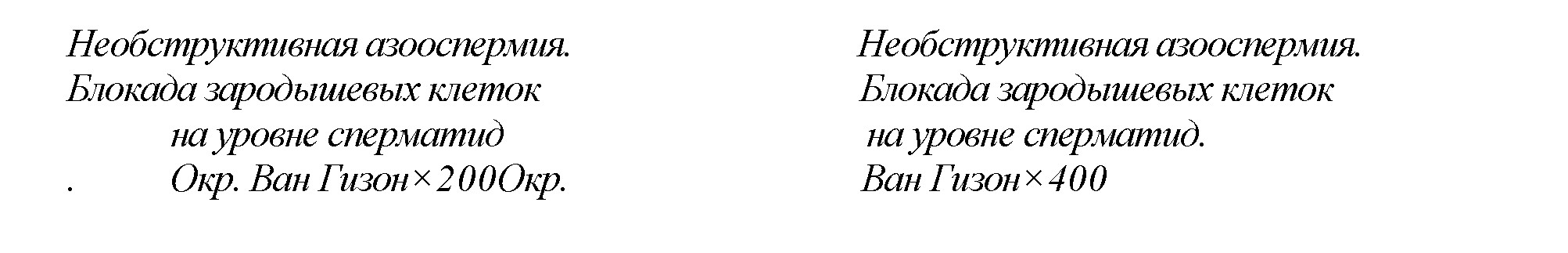
 11
11
Гистологически, диаметр семенных канальцев уменьшен, зародышевые клетки отсутствуют. В некоторых семенных канальцах сохранялось некоторое количество зародышевых клеток. Базальные мембраны таких канальцев несколько утолщены. В интерстиции - гиперплазия клеток Лейдига. Просвет семенных канальцев уменьшен, зародышевые клетки отсутствуют.Склероз и фиброз стенок семенных канальцев, очагово, до сужения их просвета с отсутствием признаков сперматогенеза.Склероз и очаговый фиброз интерстициальной ткани с лимфоидной инфильтрацией. Артериосклероз.
 12
12
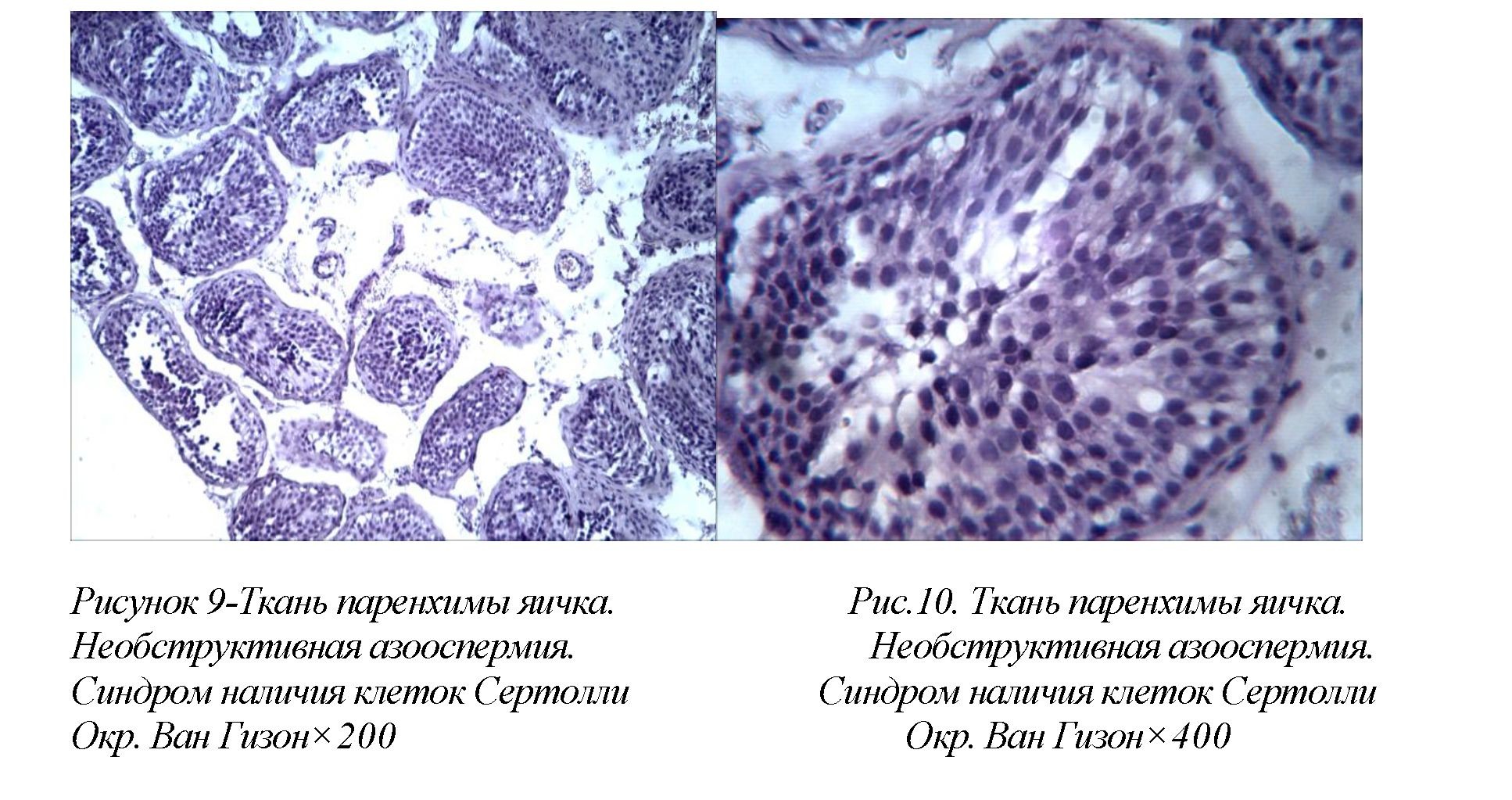
Полный Сертоли-клеточный синдром отмечался в 3(12,5%) случаев, согласно шкалеD. DeKretser и A. Holstein, нами оценен от 25% до 20% и менее,т.е присутствие только клеток Сертоли в канальцах,что явилось основанием для постановки диагноза «синдром наличия только клеток Сертоли» (смотрите рисунки 9, 10)
Ткань яичка, семенные канальцы которой выстланы только клетками Сертоли. Обнаруживаются умеренное уменьшение размеров извитых канальцев семенников. Канальцевыйпролиферат состоит из единичных сперматогониев и сперматоцитов первого порядка. Сперматоциты второго порядка, ранние и поздние сперматиды отсутствуют. Слабо выраженный фиброз интерстиция, собственной оболочки семенного канальца. Подобные наблюдения представляют особую сложность при планируемой аспирации сперматозоидов из яичка и интрацитоплазматической инъекции сперматозоидов.
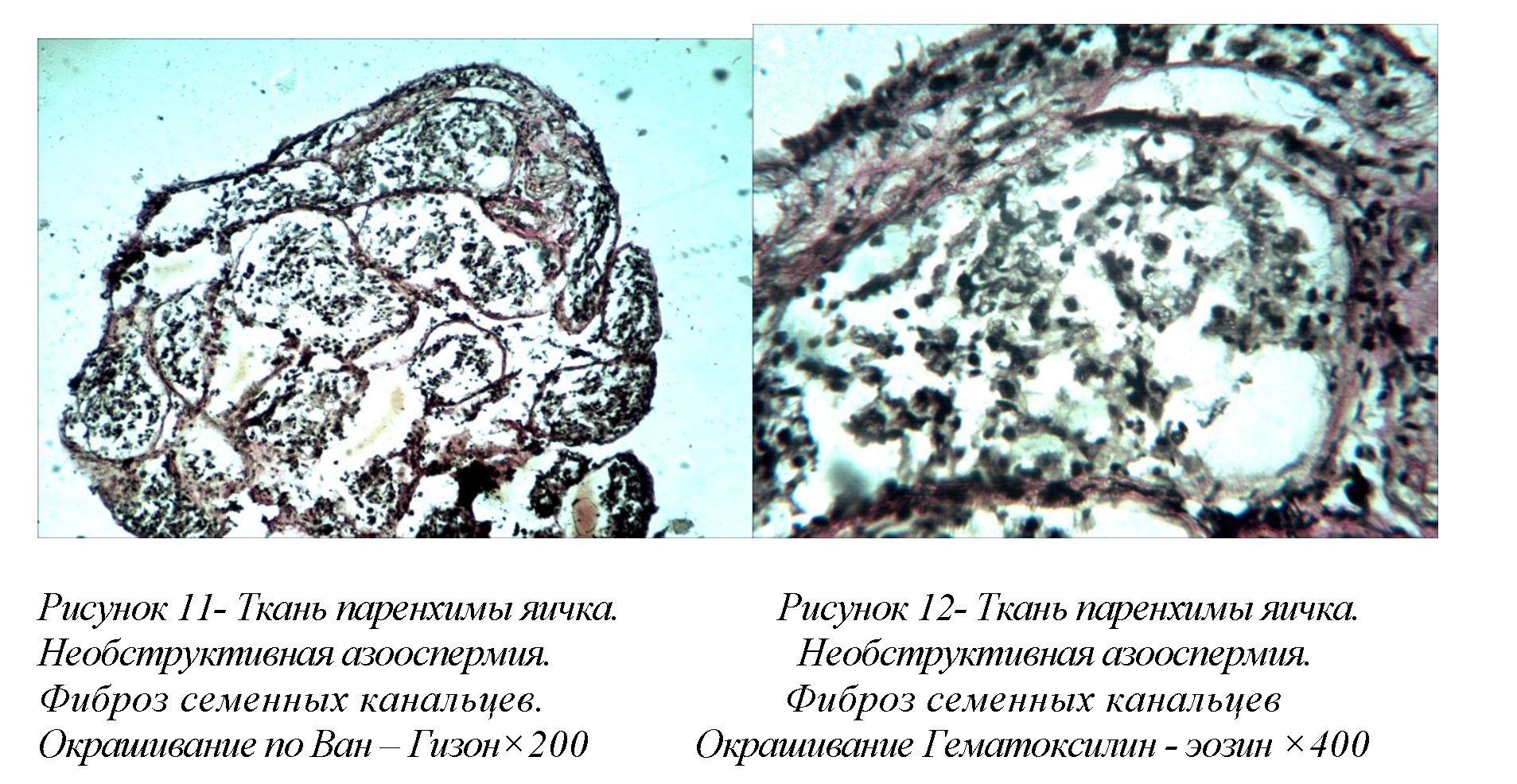
Выраженная атрофия, фиброз и гиалиноз семенных канальцев, определялись только в 1 биоптате (4,1%), доля семенных канальцев, содержащих вытянутые сперматиды согласно шкале D. DeKretser и A. Holstein ниже 10%. (рис.11,12).
При гистологическом исследовании канальцы резко уменьшеныв диаметре, базальная мембрана утолщена. В просвете канальцев зародышевые клетки отсутствуют или обнаруживаются единичные дегенеративные клеткиСертоли. В строме - фиброз и лимфогистиоцитарнаяинфильтрация с уменьшенным содержанием клетокЛейдига.
Таким образом, анализ полученных нами результатов выявил, что преобладающим фактором бесплодия является необструктивная форма азооспермии, при котором нарушение созревания сперматозоидов определяется на различных стадиях развитиязародышевых клеток от сперматогоний до сперматид, что свидетельствует об увеличении роликак генетических факторов необструктивной азооспермии, так и экзогенных воздействий на сперматогенез.
Благоприятный прогноз имеют мужчины с сохранным сперматогенезом, характерным для обструктивной азооспермии. Несмотря на то, что сперматозоиды в семенной жидкости не определяются, сперматогенез у таких больных может сохраняться в течение длительного времени благодаря компенсаторным механизмам, что дает возможность проведения экстракции сперматозоидов с последующим эффективным проведением ВРТ.
 13
13
Учитывая научные сообщения и результаты проведения нами гистологических исследований можно считать, что проведение биопсии яичка является целесообразным не только в плане диагностики состояния сперматогенеза, но и оценки перспективы проведенного лечения, в том числе и по программе ЭКО-ИКСИ пациентов с необструктивными формами бесплодия.
ВЫВОДЫ.
- Морфологические исследования ткани яичка с особенностями гормонального метаболизма позволяют установить степень нарушения сперматогенеза, выяснить возможности репродуктивной функции и целесообразности этиопатогенетического лечения.
- У больных азооспермией имеются нарушения регуляции гипотоламо- гипофизарно - гонадной системы, что обусловлено первичной тестикулярной недостаточностью.
- Наличие очагового и тотального Сертоли-клеточного синдрома определяется ролью генетического фактора.
Благоприятным при азооспермии, на наш взгляд, является установленный морфологический гипосперматогенез, характерный для обструктивной азооспермии, что согласно шкале D. DeKretser и A. Holstein, оценен нами в 87%.
ЛИТЕРАТУРА
- Горпинченко И.И. Мужской гипогонадизм: клиника и лечение// Здоровье мужчины. - 2005. - №1. - С. 7 - 9.
- Горпинченко И.И., Имшинецкая Л.П. Ложныйкрипторхизм - фактор мужскогобесплодия. В: Социальные и клинические проблемы сексологии и сексопатологии: Материалы конференции М., 2003: 47.
- Бойко Н.И., Борисенко Ю.А., Быстров A.A., и др. Сексология и андрология.- К.: Абрис.- 1997.- 870с
- Имшинецкая Л. П., Юнда И. Ф., Горпинченко И. И., Романенко А. М.
- Клинические проблемы сексологии и сексопатологии: Материалы конференции М., 2005: с. 152-157.
- Горбов В. Г. Клинико-морфологические аспекты аспермии // Урология и нефрология. — 1991. — № 4. — С. 58-62.
- Гаспаров А.С. Репродуктивное здоровье. Бесплодие как медико-социальная проблема /А.С. Гаспаров, Т.А.Назаренко //Практическое руководство. - М., 2000. - 56 с.
- Altay B. The effects of female age on the outcomeof testicular sperm extraction and intracytoplasmicsperminjection in infertile patients with azoospermia / B. Altayet al. // Int. Urol. Nephrol. - 2002. - No 33(1). - Р. 95-99.
- Thomas J.O. Histological pattern of testicular biopsiesin infertile males in Ibadan, Nigeria / J.O. Thomas //. EastAfrican Medical Journal - 1990. - No 67. - Р. 578-584.
- Schoor R.A. The role of testicular biopsy in themodern management of male infertility / R.A. Schoor,S.Elhanbly et al. //J. urol. - 2002. - Vol. 167. - No1. - Р. 197-200.
- Clermont Y.The cycle of the seminiferous epithelium in man.Am. J. Anat. 1963; 112: 35—51.
- Bergmann M., KlieschS.Hodenbiopsie. In: Krause W., Weidner W., eds. Andrologie. Stuttgart: EnkeVerlag; 1998: 66—71.
- Johnson L., Chaturvedi P.K., Williams J.D. Missing generations of spermatocytes and spermatids in seminiferous epithelium contribute to low efficiency of spermatogenesis in humans. Biol. Reprod.1992; 47: 1091—8.
- Holstein A.F., Schirren C., Roosen-RungeE.C.Illustrated pathology of human spermatogenesis. Berlin: Grosse Verlag; 1988.
- Amer M., Zohdy W., El Naser T.A. etal.Single tubule biopsy: A new objective microsurgical advancement for testicular sperm retrieval in patients with nonobstructiveazoospermia. Fertil.Steril. 2008 (89): 592—6.
- McLachlan R.I., Raijpert-De Meyts E., Hoi-Hansen C.E. etal.Histological evaluation of the testis — approaches to optimizing the clinical value of the assessment: mini review. Hum. Reprod. 2007; 22: 2—16.
- Dieckmann K.P., Kulejewski M., Pichlmeier U., LoyV.Diagnosis of contralateral testicular intraepithelial neoplasia (TIN) in patients with testicular germ cell cancer: Systematic two-site biopsies are more sensitive than a single random biopsy. Eur. Urol. 2007; 51: 175—83.
- Van Casteren N.J., Boellaard W.P.A., Dohle G.R. etal.Heterogenous distribution of ITGCNU in an adult testis: consequences for biopsy-based diagnosis. Int. J. Surg. Pathol. 2008; 16: 21-4.
- Nieschlag E., Behre H.M., NieschlagS.Andrology. Male reproductive health and dysfunction.3rd ed. Berlin; Heidelberg: Springer-Verlag; 2010.