РЕЗЮМЕ
В статье исследовано изучение взаимосвязи интенсивности признаков воспаления и неоангиогенеза на основе патоморфологического анализа тканей матки крыс в условиях экспериментальной модели спаечного процесса. Исследования выполнены на самках беспородных белых крыс с массой тела 200-250 г (n=22). Индукцию спаечного процесса (n=15) обеспечивали внутрибрюшинным введением 0,5 мл 20% водной суспензии талька. Через 7 суток крыс выводили из эксперимента путем декапитации под легкой эфирной анестезией и собирали пробы тканей матки для дальнейших патоморфологических исследований в сравнении с контрольной группой животных (n=7). Показано, что выбранная экспериментальная модель формирования посттравматических спаек обеспечивает надежное воспроизведение посттравматического спаечного процесса. Установлено, что, при формировании посттравматических спаек, процесс инфильтрации лейкоцитов в периметрии крыс сочетается с патологическими изменениями существующих кровеносных сосудов и активно протекающим неоваскулогенезом.
Ключевые слова: спаечный процесс, белые крысы, матка.
Интраабдоминальные перитонеальные сращения, или спайки, имеют место после большинства хирургических вмешательств. В некоторых случаях спаечный процесс протекает бессимптомно, но в 25% случаев послеоперационные спайки приводят к развитию хронических тазовых болей, бесплодия, кишечной непроходимости [1,2]. Несмотря на множество проведенных исследований и клинических испытаний, надежный метод профилактики послеоперационного спайкообразования в клинической практике отсутствует. Возможность разработки эффективных, патогенетически обоснованных методов профилактики формирования послеоперационных саек, лежит в изучении механизмов этого процесса в условиях экспериментальной модели [3]. Феномен неоангиогенеза занимает одно из центральных мест в патогенезе ряда заболеваний женской репродуктивной сферы, включая процессы формирования постхирургических спаек [4]. Вызванная хирургическим вмешательством ишемия тканей активирует секрецию индуцируемого гипоксией фактора- 1альфа (HIF-1alpha), усиливающего локальную продукцию эндотелиального фактора роста сосудов (VEGF), с одной стороны, стимулирующего восстановление поврежденных кровеносных сосудов, с другой стороны, являющегося важным условием формирования постхирургических спаек [5].
Патогенетическая роль ишемии травмированной ткани в процессах формирования спаек у женщин [6] не вызывает существенных возражений. При этом, некоторые исследователи признают важное значение гипоксии и неоангиогенеза в процесс формирования спаек [5]. Однако, высказываются мнения и о том, что дефицит кислорода в травмированной пери- и миометрии иницирует образование спаек через иммунопатологические механизмы [7] и модуляцию фенотипа перитонеальных фибробластов [8]. Следовательно, усиление неоангиогенеза - естественный процесс, сопутствующий регенерации поврежденной ткани [9]. В патогенезе постхирургических спаек несколько точек инициации процесса, сопряженных с ишемией травмированного органа, фиброзом ткани и наличием устойчивых очагов воспаления, обеспечивающих стимуляцию васкулогенеза через продукты реакций перекисного оксиления и выработку провоспалительных цитокинов [10,11].
Таким образом, значение неоангиогенеза для формирования постхирургических спаек у женщин изучено недостаточно. Также недостаточно изучена роль воспаления в механизмах активации неоангиогенеза, сопутствующего формированию спаек после гинекологических операций. Поэтому, целью работы было изучение взаимосвязи интенсивности признаков лейкоцитарной инфильтрации и неоангиогенеза на основе патоморфологического анализа тканей матки крыс в условиях экспериментальной модели спаечного процесса.
Материалы и методы. В эксперимент отбирали самок беспородных белых крыс с массой тела 200-250 г (n=22). Животные получали стандартный рацион питания при свободном доступе к питьевой воде. Формирование спаек у животных (n=15) вызвали внутрибрюшинным введением 0,5 мл 20% водной суспензии талька [12]. Через 7 суток крыс выводили из эксперимента путем декапитации под легкой эфирной анестезией и собирали пробы тканей матки для дальнейших патоморфологических исследований, затем сравнивали с контрольной группой животных (n=7). Полученные образцы ткани фиксировали в 10% растворе формалина.
Далее материал обрабатывали по общепринятой методике с последующей заливкой в парафин [13]. Срезы тканей толщиной 5-7 мкм окрашивали гематоксилином и эозином. Для выявления протеинов соединительной ткани использовался метод окраски срезов по Ван-Гизон.
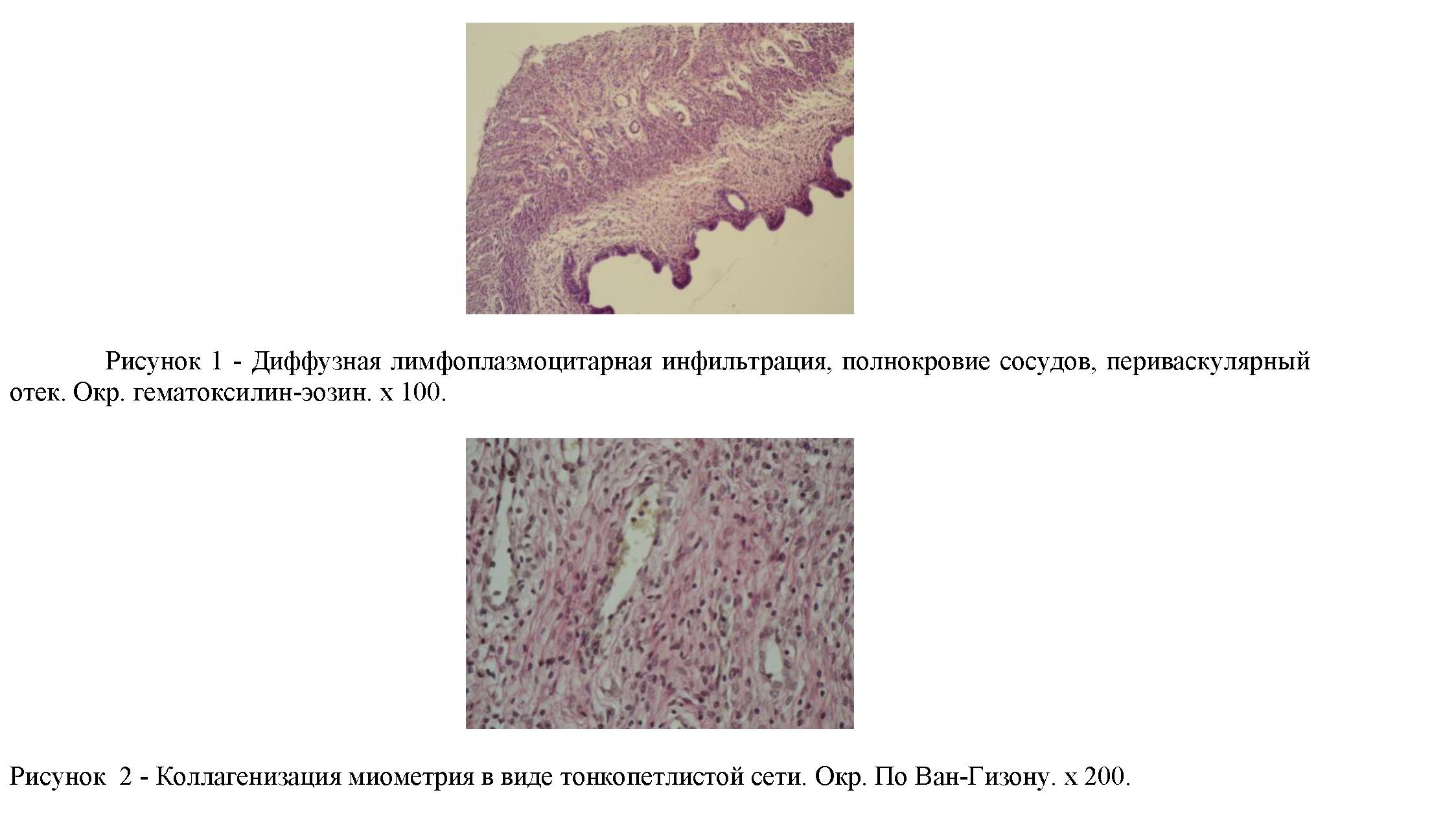
Результаты исследования и их обсуждение. В ходе макроскопического исследования брюшной полости крыс, подвергавшихся воздействию талька, надежно регистрировалось спайкообразование у всех исследованных животных. Спайки были в виде рыхлых, легко разделимых сращений матки и прямой кишки, рогов матки с тонким кишечником, либо тела и рогов матки. В 33,33% случаев регистрировали инкапсулированные частички талька без признаков перифокальной воспалительной реакции. Отмечена отчетливо выраженная гиперемия париетальной брюшины и периметрия в 93,33%. Результаты патоморфологического исследования выявили признаки острого воспаления, которые проявляются диффузной и локальной лейкоцитарной инфильтрацией стенок влагалища, эндометрия, миометрия (рис. 1), расстройствами кровообращения в виде гиперемии и мелких кровоизлияний и развитием выраженного отека тканей. В эндометрии, кроме спиральных артерий, выявляются многочисленные кровеносные сосуды на фоне густой лейкоцитарной инфильтрации, имеющие прямой ход и значительный калибр. В некоторых случаях коллагеновая сеть образуется преимущественно в базальном слое эндометрия, охватывая тонкими волокнами эндометриальные железы и не распространяется при этом на мышечный слой.
Использование окраски по Ван-Гизон позволило установить, что большинство кровеносных сосудов окружены ярко окрашенными коллагеновыми волокнами. Коллагенизация эндометрия, миометрия (рис. 2) и адвентиция сосудов матки и маточной брыжейки, очаговая лимфогистиоцитарная инфильтрация фиброзномышечного слоя влагалища, а также новообразование сосудов в тканях влагалища и эндометрия экспериментальных животных является свидетельством длительного воспалительного процесса и началом склерозирования. Полученные результаты позволяют утверждать, что в условиях выбранной экспериментальной модели удалось добиться надежного воспроизведения постравматического спаечного процесса в брюшной полости. Кроме того, сопоставление результатов патоморфологического анализа проб тканей животных экспериментальной и контрольной группы указывает на отчетливое усиление неоангиогенеза с признаками лейкоцитарной инфильтрации, сопутствующее спайкообразованию.
Признавая роль эстрогенов в HIF-lalpha-зависимой стимуляции синтеза VEGF [8], некоторые авторы указывают на тот факт, что процессы воспаления являются наиболее актуальным звеном активации неоангиогенеза, детерминирующим динамику репаративных механизмов тканей матки и брюшины, определяющим состояние обмена соединительнотканных протеинов и интенсивность неоангиогенеза [14]. Подчеркивая тесную взаимосвязь механизмов воспаления и ангиогенеза, авторы указывают, что полиморфноядерные гранулоциты и перитонеальные макрофаги, обладающие способностью секретировать VEGF, могут усиливать патологические ростовые процессы в тканях [15]. Инициация иммунных реакций на повреждение матки и брюшины протекает параллельно с запуском механизмов репарации поврежденных тканей, демонстрируя в перитонеальной жидкости высокие уровни основных провоспалительных цитокинов — фактора некроза опухоли-альфа и интерлейкина-1бета [14, 15]. Также установлено, что фактор некроза опухоли-альфа (ФНО-альфа) in vivo стимулирует секрецию VEGF, миграцию эндотелиоцитов и неоангиогенез, в то время, как генетически детерминированный дефицит рецепторов 1 к ФНО-альфа резко ослабляет проангиогенный эффект хемокина [11].
Кроме того, ряд исследователей не исключают, что VEGF может стимулировать миграцию лейкоцитов в зону повреждения ткани, дополнительно усиливая роль иммунного фактора в процессах неоваскулогенеза. Поэтому, с одной стороны, регионарное увеличение уровня ФНО-альфа способствует притоку лейкоциов и росту их функциональной активности. С другой стороны, мигирующие к поврежденному участку ткани нейтрофилы и макрофаги являются важным источником ряда физиологически активных молекул, необходимых для полноценного формирования кровеносных сосудов. Действительно, результаты патоморфологических исследований образцов «зрелых» постхирургических спаек указывают на четко структурированную систему кровоснабжения вновь образованных участков ткани, включающую в себя артериолы, венулы, капилляры, а также нервные волокна [5]. Баланс уровней цитокинов в перитонеальной жидкости в начале патологического процесса, может иметь важное значение для последующего течения заболевания, указывая на анти- ангиогенный эффект цепочки хемокинов, индуцируемой интерфероном-гамма [11].
Правомерность такого вывода подкрепляют данные экспериментальных исследований, подчеркивающие влияние предварительной активации иммунной системы на процессы неоангиогенеза [4]. Ффизиологические и патофизиологические механизмы ангиогенеза, воспаления и репарации раневых поверхностей — тесно взаимосвязаны [3]. Показатели темпов миграции лейкоцитов в поврежденные участки тканей могут служить индикаторами воспалительной реакции, определяющей, как активность ростовых процессов, так и интенсивность иммунных механизмов повреждения уже существующих кровеносных сосудов. Особенностью процесса заживления раневых поверхностей в брюшной полости является довольно стремительное увеличение уровня провоспалительных и склерозирующих цитокинов в перитонеальной жидкости, омывающей значительные поверхности, вследствие чего, могут наблюдаться несовпадения мест локализации раневой поверхности и формирования спаек [11]. Действительно, результаты собственных
наблюдений показывают, что образование спаек регистрируется в участках матки отдаленных от места нанесения травмы. Тем не менее, выбранные образцы органа, содержащие спайки, характеризуются отчетливыми признаками воспаления и неоваскулогенеза. Полученные данные свидетельствуют о том, что имеет место топологическая совместимость очагов воспаления и участков неоангиогенеза. Наиболее выраженные признаки фиброза существующих сосудов регистрируются на фоне четко выраженного воспалительного процесса. Такие результаты не противоречат данным литературы о том, что повреждения кровеносных сосудов, вызванные ишемией и реперфузионными механизмами могут играть существенную роль в процессах образования постхирургических спаек [7]. Кроме того клетки эндотелия кровеносных сосудов выполняют важную функцию в системе контроля миграции лейкоцитов в ткани [13].
Кроме того, проникновение лейкоцитов через сосудистый барьер сопровождается закономерной перестройкой активности генов эндотелиальных факторов [16]. При этом, ФНО-альфа играет ключевую роль, как в процессах адгезии и миграции лейкоцитов, так и в стимуляции синтеза провоспалительных и склерозирующих цитокинов, сопутствующих активации лейкоцитов [16]. В целом, приведенные факты указывают, что повреждение кровеносных сосудов на этапе острой фазы воспаления, в дальнейшем, является стимулом для неоангиогенеза, протекающего на фоне хронического воспаления и ремоделирования тканей сосудов [3,4]. С позиции изложенных фактов, сведения о том, что VEGF-А является ключевым гуморальным индуктором неоангиогенеза, связанного со спайкообразованием в гинекологии [9,22], можно дополнить предположением о том, что наряду с функцией репарации поврежденных участков ткани, а так же вовлеченности в патофизиологические механизмы неоваскуляризации соединительнотканных спаечных тяжей, VEGF-А принимает участие в процессах защиты эндотелия на этапе острой фазы воспаления [6], предотвращая тем самым дальнейшее нарастание ишемии травмированной ткани и усиление неоангиогенеза в очагах хронического воспаления [3,4].
Выводы. 1. Использованная экспериментальная модель формирования спаечного процесса у крыс, индуцированного способствует активному образованию элементов соединительной ткани и неоангиогенезу, что способствует спайкообразованию органов брюшной полости. 2. Постхирургические спайки представляют четко структурированную систему кровоснабжения вновь образовавшихся участков ткани, включающую в себя артериолы, венулы, капилляры, а также нервные волокна. 3. При моделировании посттравматических спаек внутрибрюшным введением талька, в тканях матки определяются отчетливые признаки воспаления и неоваскулогенеза. Процесс инфильтрации лейкоцитами в периметрии крыс сочетается с патологическими изменениями уже существующих кровеносных сосудов и активно протекающим неоваскулогенезом.
ЛИТЕРАТУРА
- Гладчук И.З., Рожковская Н.Н., Латий К.В., Волянская А.Г. Прогнозирование спайкообразования у больных с миомой матки и наружным генитальным эндометриозом после хирургического лечения. / Одесский медицинский журнал..-2009.-№5.-С.39-44
- Nappi C., Di Spiezio Sardo A., Greco E. et al. Prevention of adhesions in gynaecological endoscopy//\Human Reproduction Update.-2007.-V.13,№4.-P.379-394
- Attard J.-A., MacLean A. R. Adhesive small bowel obstruction: epidemiology, biology and prevention//Can. J. Surg.-2007.-V.50,№4.-P.291-300
- Frantz S., Vincent K.A., Feron O., Kelly R.A. Innate Immunity and Angiogenesis//Circulation Research.- 2005.-V.96.-P.15-26
- Laschke M.W., Elitzsch A., Vollmar B. et al. Combined inhibition of vascular endothelial growth factor (VEGF), fibroblast growth factor and platelet-derived growth factor, but not inhibition of VEGF alone, effectively suppresses angiogenesis and vessel maturation in endometriotic lesions//Human Reproduction.- 2006.-V.21,N1.-P.262-268
- Chegini N. TGF—вІ System: The Principal Profibrotic Mediator of Peritoneal Adhesion Formation//Semin Reprod. Med.-2008.-V.26.-P.298-312
- Matsuzaki S., Canis M., Bazin J.-E. et al. Effects of supplemental perioperative oxygen on post-operative abdominal wound adhesions in a mouse laparotomy model with controlled respiratory support//Human Reproduction.-2007.-V.22,№10.-P.2702-2706
- Rout U.K., Saed G. M., Diamond M.P. Expression pattern and regulation of genes differ between fibroblasts of adhesion and normal human peritoneum//Reprod. Biol. Endocrinol.-2005.-V.3.-P.1-9
- Rout U.K., Oommen K., Diamond M.P. Altered expressions of VEGF mRNA splice variants during progression of uterine-peritoneal adhesions in the rat\\Am. J. Reprod. Immunol.-2000.-V.43.№5.-P.299-304
- Sainson R.C., Johnston D.A., Chu H.C. et al. TNF primes endothelial cells for angiogenic sprouting by inducing a tip cell phenotype//Blood.-2008.-V. 111,№10.-Р.4997-5007
- Secchiero P., Corallini F., di Iasio M.G. et al. TRAIL counteracts the proadhesive activity of inflammatory cytokines in endothelial cells by down-modulating CCL8 and CXCL10 chemokine expression and release//Blood.-2005.-V.105,N9.-P.3413-3419
- Волянська А.Г., Сивоконюк О.В. Порівняльний аналіз впливу сульфату барію і тальку на інтенсивність спайкового процесу у самок білих щурів // Інтегративна антропологія.- 2012.-№ 1(19).-С.58-61.
- Горальский Л.П. , Хомич В.Т., Кононський О.І. Основи гістологічноі техніки і морфофункціональні методи досліджень у нормі та при патологіх. Навчальний посібник. - Житомир: «Полісся», 2005. с. 7071
- Becker Ch. M., Rohwer N. , Funakoshi T. et al. 2-Methoxyestradiol Inhibits Hypoxia-Inducible Factor-1a and Suppresses Growth of Lesions in a Mouse Model of Endometriosis//American Journal of Pathology.-2008.- V.172.-P.534-544
- Peterson J.M., Feeback K.D., Baas J.H., Pizza F.X. Tumor necrosis factor-а promotes the accumulation of neutrophils and macrophages in skeletal muscle//J. Appl. Physiol.-2006.-V.101.-P.1394-1399
- Wu S.-Q., Aird W.C. Thrombin, TNF-alpha, and LPS exert overlapping but nonidentical effects on gene expression in endothelial cells and vascular smooth muscle cells//Am. J. Physiol. Heart Circ. Physiol.-2005.- V.289.-P.H873-H885
- Roy S., Clark C.J., Mohebali K. et al. Reactive oxygen species and EGR-1 gene expression in surgical postoperative peritoneal adhesions\\World J. Surg.-2004.-V.28,№3.-P.316-320