РЕЗЮМЕ
Проанализирован опыт минимально инвазивных операций при эхинококкозе печени нескольких ведущих клиник России. За период с 1985 по 2012 г. сберегающие методики были использованы при лечении 395 взрослых пациентов и 87 детей. Показания основывались на ультразвуковых признаках эхинококковых кист. Диагностика включала серологические реакции, УЗИ и МРТ с MPXlll'. В качестве гермицидного препарата использовали 85-87% раствор глицерина. В 20% наблюдений были выявлены цистобилиарные свищи, ни в одном наблюдении традиционной операции не потребовалось. В 1,7% наблюдений отмечено нагноение остаточной полости, излечено минимально инвазивно. У одной пациентки был рецидив по ходу стояния дренажа, что составило 0.3%. Послеоперационную противорецидивную химиотерапию альбендазолом проводили во всех случаях.
Ключевые слова: эхинококкоз, гидатидный эхинококкоз, минимально инвазивные методы, УЗИ, МРТ, видеолапароскопия, альбендазол, диагностика, лечение эхинококкоза.
Актуальность. До сих пор в литературе широко обсуждается возможность использования минимально инвазивных методов лечения при гидатидном эхинококкозе, при этом большинство хирургов до сих пор скептически относятся к чрескожным и видеолапароскопическим методам лечения. Трудности дифференциальной диагностики, особенно при малых размерах кист, требуют получения материала для морфологического подтверждения диагноза. Однако, чрескожные диагностические пункции, при подозрении на эхинококкоз, вплоть до последних лет, считались противопоказанными, в связи с опасностью обсеменения зародышевыми элементами паразита пункционного канала и брюшной полости[1-6].
Состояние проблемы. Определение стратегии, разработка техники безопасного чрескожного вмешательства и создание для этого специального инструментария, предотвращающего развитие осложнений, позволило широко внедрить сберегающую хирургию лечения эхинококкоза в повседневную практику. В настоящее время в мире накоплен большой опыт чрескожных вмешательств в лечении кистозного эхинококкоза печени - у некоторых авторов более 1000 наблюдений[7,8]. Первая операция под ультразвуковым (УЗ) и рентгенотелевизионным (РТВ) контролем по поводу эхинококкового поражения печени в России, была успешно проведена А.Н. Лотовым в 1986 году в клинике 1 Московского медицинского института им. И.М. Сеченова [9] и, независимо, А.В. Гаврилиным в Институте хирургии им. А.В. Вишневского [10].
Чрескожные вмешательства, несмотря на кажущуюся простоту, при отсутствии опыта и специального оборудования опасны и чреваты серьезными интра- и послеоперационными осложнениями вплоть до летального исхода во время манипуляции. Описаны тяжелые анафилактические реакции и даже несколько случаев смерти при пункции эхинококковых кист[11]. При этом авторы признают, что осложнения и летальные исходы были обусловлены нарушением техники вмешательства. В настоящее время признана целесообразность использования для дифференциальной диагностики в специализированных лечебных учреждениях прицельных чрескожных пункций эхинококковых кист. Доказана их безопасность при квалифицированном выполнении манипуляции с тщательным соблюдением методики.
Традиционные хирургические вмешательства до сих пор считают «золотым» стандартом лечения эхинококкоза [12-17]. Используют три основных метода традиционного хирургического лечения эхинококкоза:
- Удаление элементов эхинококковой кисты без фиброзной оболочки (эхинококкэктомия);
- Удаление паразита вместе с фиброзной оболочкой (перицистэктомия);
- Удаление эхинококковой кисты путем резекции органа.
Соответственно внутри каждого из методов также выделяют:
- идеальную эхинококкэктомию - удаление паразита без вскрытия хитиновой оболочки;
- закрытую эхинококкэктомию - после удаления элементов паразита ушивание полости фиброзной капсулы без дренажа;

- полузакрытую эхинококкэктомию - оставление дренажа в остаточной полости после ее капитонажа;
- оментопластику - тампонирование полости фиброзной капсулы прядью большого сальника;
- открытую эхинококкэктомию (марсупиализацию) - подшивание краев полости фиброзной капсулы к ране передней брюшной стенки с тампонированием полости кисты мазевыми тампонами и/или оставление толстой дренажной трубкой. Указанный вид операции применяют крайне редко.
В настоящее время вышеупомянутая терминология еще встречается в литературе, в связи с чем, мы сочли целесообразным упомянуть о ней, однако, сейчас правомерно выполнение лишь субтотальной перицистэктомии, резекции печени или пункционно-дренажного лечения. Капитонаж, марсупиализация и тампонирование полости кисты остались в истории и не могут быть рекомендованы в современной хирургии печени в виду большого числа осложнений.
Остается немало сторонников резекции органа или его удаление вместе с кистой [16], но мы не должны забывать о паразитарной природе болезни и реальной возможности повторного заражения. Однако, несмотря на усовершенствование методики вмешательства, апаразитарности выполнения операции, внедрение различных химических и физических методов воздействия на паразита, частота рецидивов заболевания при открытых вмешательствах достигает 12-33% [18]. Повторные оперативные вмешательства при рецидиве заболевания еще более травматичны, более того, у каждого 2-го больного в последующем вновь выявляют эхинококковые кисты.
Большое число рецидивов заболевания обусловило необходимость проведения дальнейших экспериментальных исследований с целью выяснения причин их возникновения.
Известны два вида зародышевых элементов эхинококковой кисты - протосколексы и ацефалоцисты. Протосколексам придавали основное значение при рецидиве заболевания и по воздействию на них in vitro и in vivo определяли эффективность гермицидов. Вероятно, это было обусловлено тем, что зародышевые элементы кисты представлены преимущественно протосколексами, они легко выявляются при микроскопии. Ацефалоцисты в кисте обычно единичные, в связи с чем их часто не выявляют и их роль до последнего времени оставалась неясной.
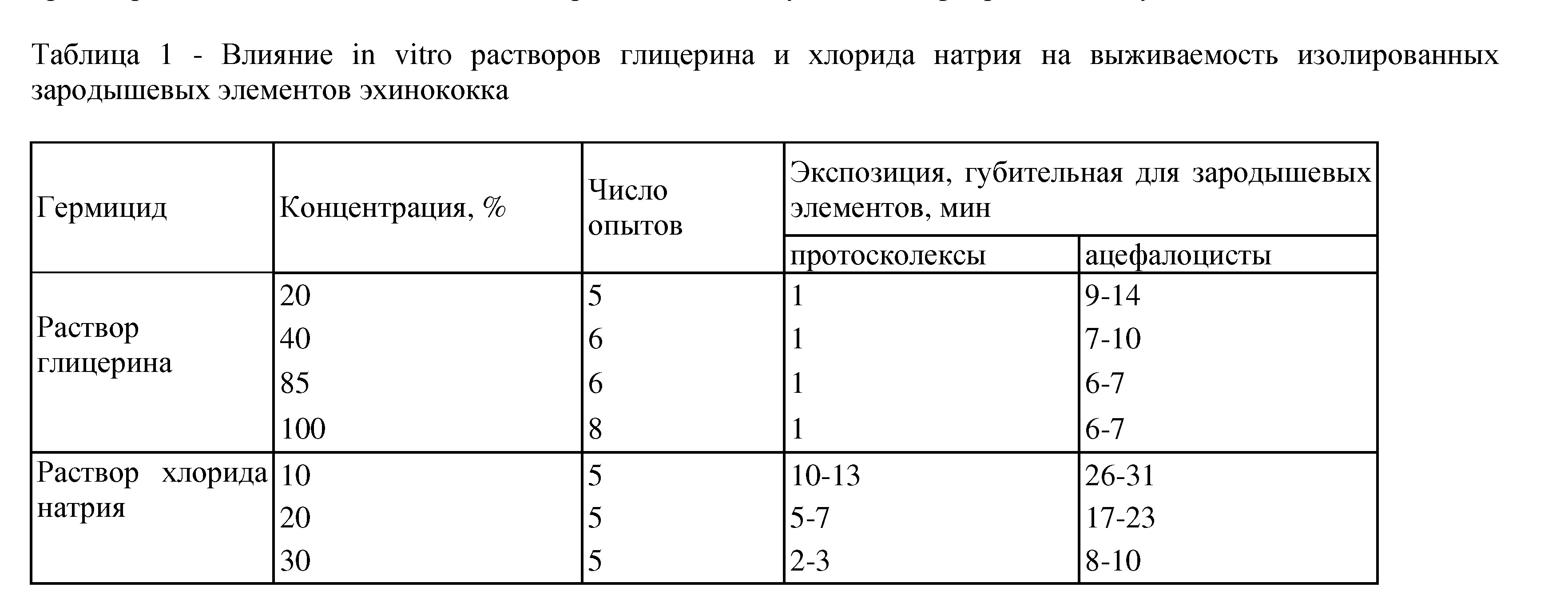
В ходе экспериментальных исследований Ф.П. Коваленко[19] было выяснено, что протосколексы эхинококка погибают на 1-й минуте воздействия химических агентов. Чрезвычайно устойчивыми к действию гермицидных препаратов оказались ацефалоцисты, которым до этой работы не придавали значения. Более того, общепринятые в хирургии эхинококкоза гермициды - формалин и 10-20% растворы хлорида натрия оказались малоэффективными, так как не приводили к гибели ацефалоцист даже при экспозиции 10-15 мин. Увеличение экспозиции (особенно формалина) повышает токсическое действие препарата на организм человека.
Последующие исследования показали, что в большинстве наблюдений именно ацефалоцисты приводят к рецидиву заболевания после хирургических вмешательств.
Доказано также массовое формирование микроскопических ацефалоцист из герминативных клеток ножки протосколекса (рис. 1). Это означает, что при определенных условиях число ацефалоцист в кисте может увеличиваться, что делает кисту очень агрессивной в плане инвазии и устойчивой к воздействию гермицидов, повышая риск рецидива после лечения.
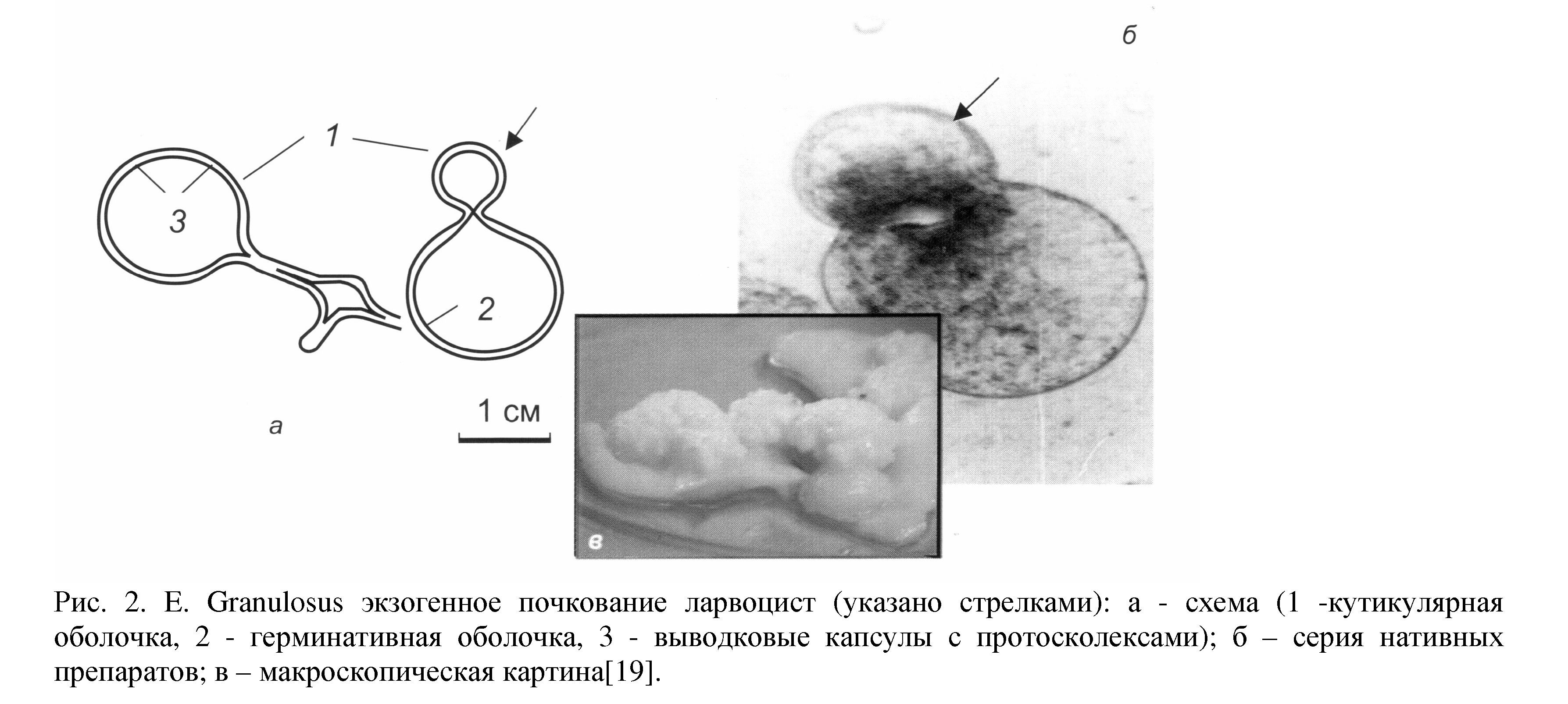
Впервые у человека была выявлена еще одна чрезвычайно важная особенность паразита - экзогенное почкование эхинококка по типу, характерному для альвеококкоза. Это означает, что паразит способен к инфильтративному росту, хотя и менее выраженному, чем у альвеококка (рис. 2).
Таким образом, протосколексы являются наиболее уязвимым элементом паразита и не могут служить критерием отбора гермицидов. Для интраоперационной обработки гидатидных кист необходимы высокоэффективные гермициды, губительные именно для ацефалоцист эхинококка, как наиболее устойчивого звена и самого важного фактора в возникновении послеоперационных рецидивов заболевания.
Было изучено воздействие различных химических агентов на зародышевые элементы паразита, особенно на ацефалоцисты эхинококка, in vitro и на лабораторных животных. Наиболее надежными и пригодными для практического применения оказались 80-100% глицерин и 30% раствор хлорида натрия (табл.1). Однако, применение 30% раствора хлорида натрия сопряжено с возможностью разведения его тканевой жидкостью до неэффективной концентрации. Глицерин активен даже при значительном разведении, что гарантирует его большую надежность. Патоморфологические исследования показали, что глицерин воздействует не только на содержащиеся в кисте зародышевые элементы, но даже проникает на глубину 2-5мм - обычная толщина фиброзной капсулы моновезикулярной кисты. Это свидетельствовало о возможности применения глицерина при оперативных вмешательствах, не сопровождавшихся удалением фиброзной капсулы кисты.
До начала 90-х годов, в лечении больных эхинококкозом, в клиниках применяли преимущественно традиционные оперативные вмешательства без удаления фиброзной капсулы. Рецидивный или резидуальный эхинококкоз имел место в 17%-22,3% наблюдений, в качестве антипаразитарных препаратов использовали 1020% раствор поваренной соли и 2-10% формалин, причем химиотерапия не проводилась [17,20]. Хирург был вынужден идти на небезопасную и травматичную операцию даже при солитарной эхинококковой кисте небольших (30-40 мм) размеров в глубине паренхимы органа. Это потребовало разработки новых сохраняющих методов хирургии эхинококкоза.
 26
26
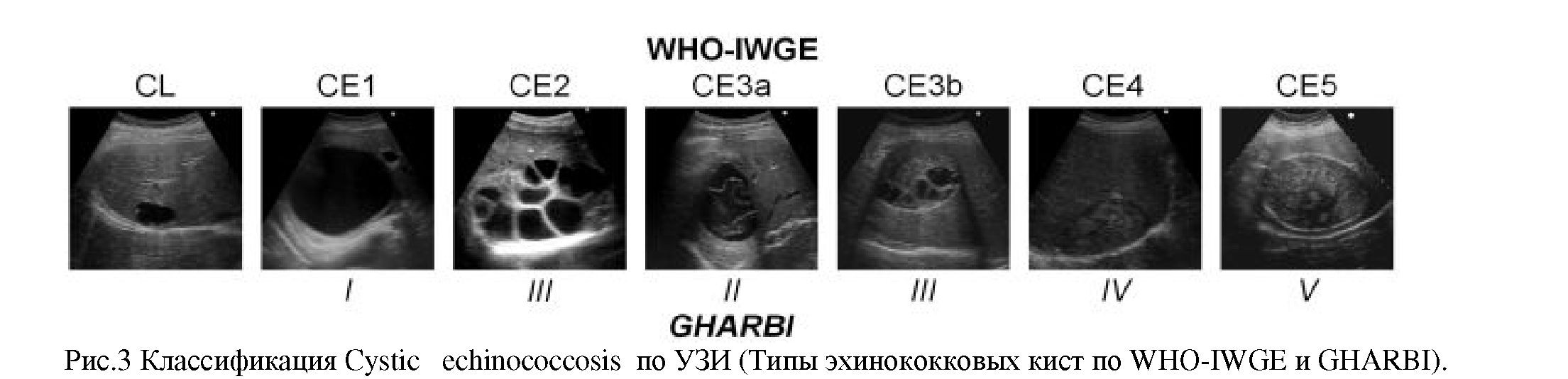
В основу показаний к сохраняющим методам лечения гидатидного эхинококка печени легли УЗИ и MPT признаки состояния эхинококковых кист, в зависимости от стадии жизнедеятельности паразита в организме человека, описанные в работах отечественных и зарубежных авторов [8,20-28]. Минимально инвазивные методики не должны быть дискредитированы (В.А.Кубышкин и соавт., 2002) и в основном применимы при неосложненных формах эхинококкоза, высоком операционном риске и отказе больного от открытого оперативного лечения. Разрабатывая показания к минимально инвазивным операциям, нами взяты за основу ультразвуковые классификации эхинококкоза печени Gharbi H. et al.1981 года и ВОЗ 2003 года[21,22] (рис.3).
Показаниями к минимально инвазивным вмешательствам являются: кистозная форма ацефалоцисты(СЕ); моновезикулярная кистаЩБЦ); множественные моновезикулярные кисты(СЕ1,1); моновезикулярная киста с отслойкой хитиновой оболочки(CE3a,II); погибшая киста без кальциноза стеноЦСБТДУ); нагноение моновезикулярной кисты(СЕ1, I); рецидивная и резидуальная моновизикулярная киста(СЕ1Д).
Противопоказаниями к проведению минимально инвазивных вмешательств являются: мультивезикулярные кисты (CE2,III); множественные дочерние кисты в полости материнской кисты (CE3b,III); кальциноз стенок эхинококковой кисты(СЕ5,У); все типы кист с экзогенной пролиферацией;
все типы кист с эндогенной пролиферацией; кисты, прорвавшиеся в желчные пути, брюшную или плевральную полости; отсутствие безопасного доступа.
Относительным противопоказанием для минимально инвазивного лечения может служить наличие моновезикулярной кисты с единичными дочерними пузырями(СЕ1Д).
Основными задачами, которые решали специалисты при разработке минимально инвазивных хирургических вмешательств, была возможность герметичного удаления жидкости с предупреждением ее попадания в брюшную полость и обсеменения, противопаразитарной обработки кисты с гарантированной гибелью всех зародышевых элементов эхинококка. Решение этих вопросов возможно при скрупулезном соблюдении показаний, технологии пункции кисты, обработки полости и содержащихся в ней элементов 8587% раствором глицерина с обязательным проведением противорецидивной химиотерапии.
Материалы и методы;
Проанализированы результаты диагностики и минимально инвазивных вмешательств у 482(395 взрослых, 87 детей) пациентов из 5 крупных лечебных учреждений. Возраст больных составил от 3 до 79 лет. В основной группе пациентов были лица трудоспособного возраста от 25 до 45лет. При этом кисты располагались в правой доле у 317 больных (66%), левой - у 91 (20%), в обеих долях печени - у 69 пациентов (14 %). Множественные кисты были диагностированы у 143 больных (30 %). Сочетанный эхинококкоз печени и других органов был отмечен у 57 больных (12%). Размеры кист колебались от 5мм до 220 мм. В 64,3% наблюдений были выявлены кисты среднего размера (40-150 мм), малые кисты (до 40 мм) - в 21,5% наблюдении, у а остальных 14,2 % наблюдений диагностированы крупные кисты размером 150-220 мм.
Всем больным проводили комплекс клинических и инструментальных исследований, включающих общеклинические и биохимические анализы крови, серологические реакции, рентгенографию грудной клетки, УЗИ, MPT с MPXl IT. Обязательным считаем сбор эпидемиологического анамнеза. Серологические реакции: иммуноферментного анализа (ИФА) и антительных единиц (АЕ), определяли в Институте медицинской паразитологии и тропической медицины им. Е.М.Марциновского. От 1 до 30 АЕ считали как слабоположительную реакцию, от 31 до 70 АЕ - как положительную и выше 71 АЕ как резкоположительную.
УЗИ является одним из наиболее перспективных методов диагностики эхинококкоза печени (в сочетании с серологическими реакциями на эхинококкоз), позволяющим в большинстве случаев установить диагноз заболевания[8,21,26,27].
Нередко больные обращаются за медицинской помощью, когда паразитарная киста достигает значительных размеров или имеются осложнения (нагноение, прорыв в желчные пути, брюшную или плевральную полости и т.д.). Чаще при профилактическом ультразвуковом исследовании (УЗИ) обнаруживают однополостное анэхогенное или гипоэхогенное образование с четкими, ровными стенками и симптомом «дистального усиления эхосигнала». Однако, подобное УЗ-изображение ассоциируется с простой кистой печени, а типичное УЗ-изображение эхинококковой кисты - с многокамерным жидкостным образованием. В
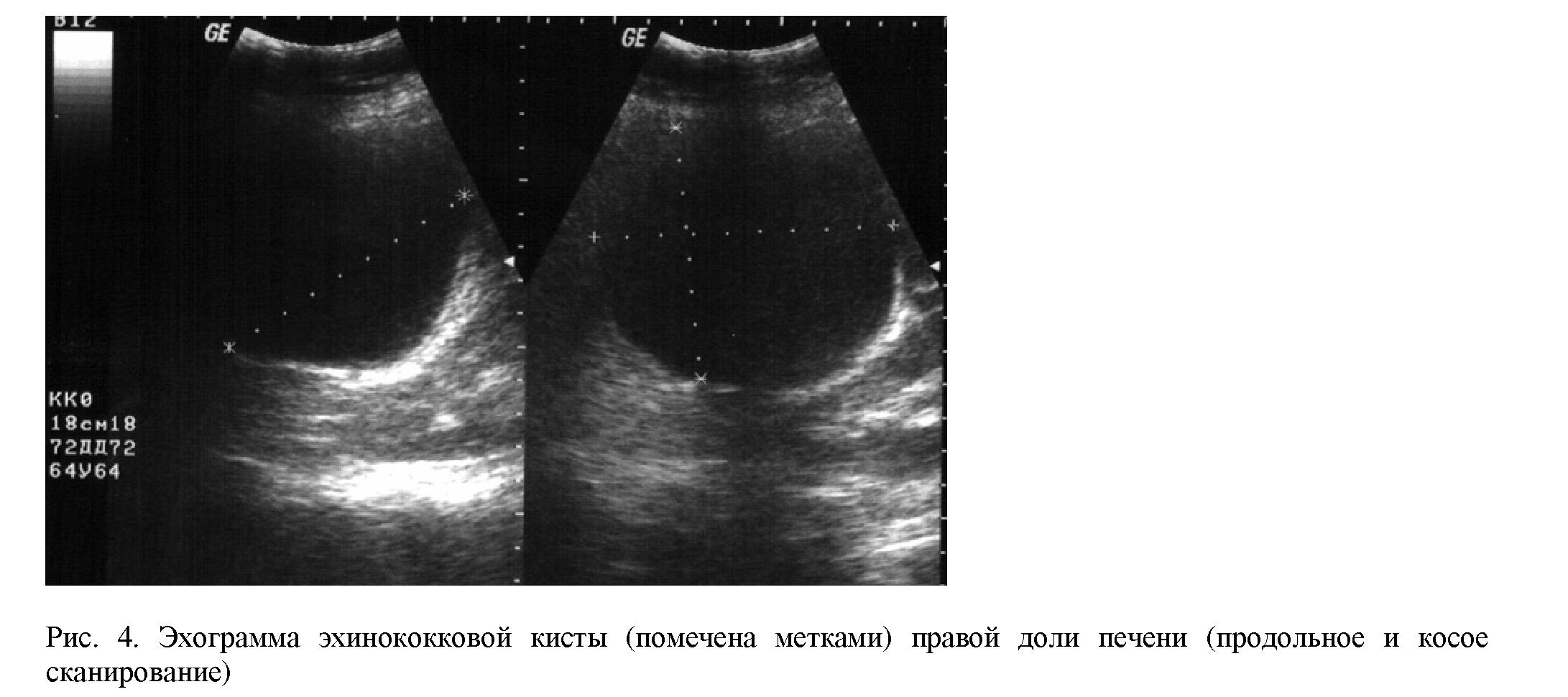
 27действительности, живая эхинококковая киста (рис. 4) однополостное жидкостное образования, а возникновение дополнительных кист свидетельствует о проблемах с материнской кистой. Поэтому выявив при первичном УЗИ жидкостное образования надо бить тревогу и лучше пусть она будет учебной.
27действительности, живая эхинококковая киста (рис. 4) однополостное жидкостное образования, а возникновение дополнительных кист свидетельствует о проблемах с материнской кистой. Поэтому выявив при первичном УЗИ жидкостное образования надо бить тревогу и лучше пусть она будет учебной.
Это ставит на первый план визуальные методы диагностики, в первую очередь УЗИ. Метод позволяет диагностировать паразитарные кисты небольших размеров, что дает возможность чаще выполнять сберегающие вмешательства. Современные ультразвуковые аппараты с высокой разрешающей способностью, цветовым доплеровским картированием и возможностью трехмерной реконструкции УЗ-изображения позволяют специалистам выявить саму кисту и оценить её характерные признаки.
Эхинококковая киста гипо- или анэхогенное образование имеет многослойное строение стенки. Хитиновая оболочка определяется как гиперэхогенная структура, часто имеющая гипоэхогенную прослойку между герминативным слоем и кутикулярным слоем. На внутренней поверхности хитиновой оболочки нередко определяются множественные гиперэхогенные включения - «эхинококковый песок». Фиброзная капсула при УЗИ определяется, как гиперэхогенный ободок. Она отделена от хитиновой оболочки гипоэхогенным слоем, представляющим собой лимфатическую «щель».
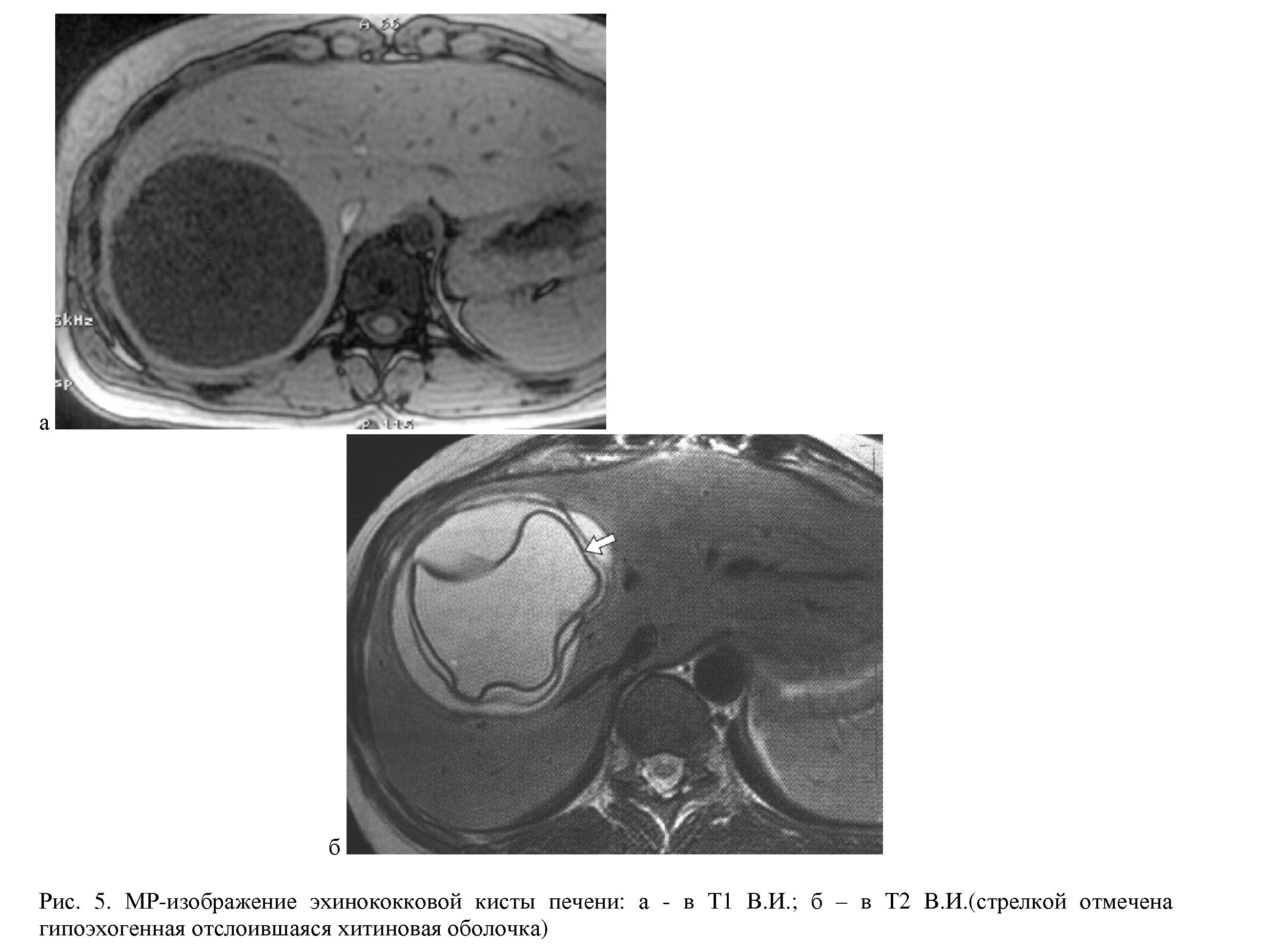
При размерах до 50 мм в диаметре стенка кисты слабо выражена (свидетельство молодого возраста), что чрезвычайно затрудняет дифференциальную диагностику. Наш опыт показывает высокую информативность МРТ с МРХ1П' в диагностике эхинококковых кист даже при их малых размерах. Одним из важнейших преимуществ МРТ является отсутствие лучевой нагрузки, что наряду с УЗИ делает его незаменимым в детской хирургии. Получение четкого изображения о взаимоотношениях с желчными протоками и крупными сосудистыми структурами печени, окружающими органами и тканями, выявление признаков экзогенного почкования, создает условия для планирования вида хирургического вмешательства [28].При МРТ на Т1 взвешенном изображении (В.И.) эхинококковые кисты характеризуются выраженным гипоинтенсивным сигналом (рис. 5а) и гиперинстенсивным - на Т2 В.И. (рис. 5б). Перегородки в просвете кисты, стенки дочерних и внучатых кист имеют гипоинтенсивный сигнал. Хитиновая оболочка кисты даёт гипоинтсивный сигнал на Т1 и Т2 В.И. При этом различие гипоинтенсивности фиброзной капсулы и хитиновой оболочки паразита создаёт на томограммах двуслойное изображение стенки кисты (рис. 5б). Линейные участки снижения интенсивности сигнала в просвете характерны для погибшей кисты и представляют собой отслоившуюся хитиновую оболочку. Кальцинаты в стенке кисты определяются как области отсутствия МР- сигнала, то есть как тёмные участки в стенках с низкой или очень низкой интенсивностью сигнала, Отхождение мелких кист от основного образования выглядит как периферическое повышение сигнала на Т2 В.И. и в STIR последовательности и отражает активность заболевания [28].
 28
28
MPT в различных режимах выполнения повышает эффективности дифференциальной диагностики паразитарных заболеваний с широким диапазоном первичных и вторичных очаговых поражений печени. MPT оказывает большую помощь в определении органной принадлежности гигантских кист и при их множественном числе. Целесообразно использовать модифицированный режим гидрографии - «сильно взвешенная» или «умеренно взвешенная» гидрография [28], при которых даже при маленьких размерах кисты удаётся выявить двуконтурность строения оболочки за счёт деления её на хитиновый и фиброзный слои, а также наличие дочерних кист (рис. 6).
 29
29
Рис. 6. MP-изображение эхинококковой кисты в режиме жесткой гидрографии, четко определяется многослойность стенки кисты
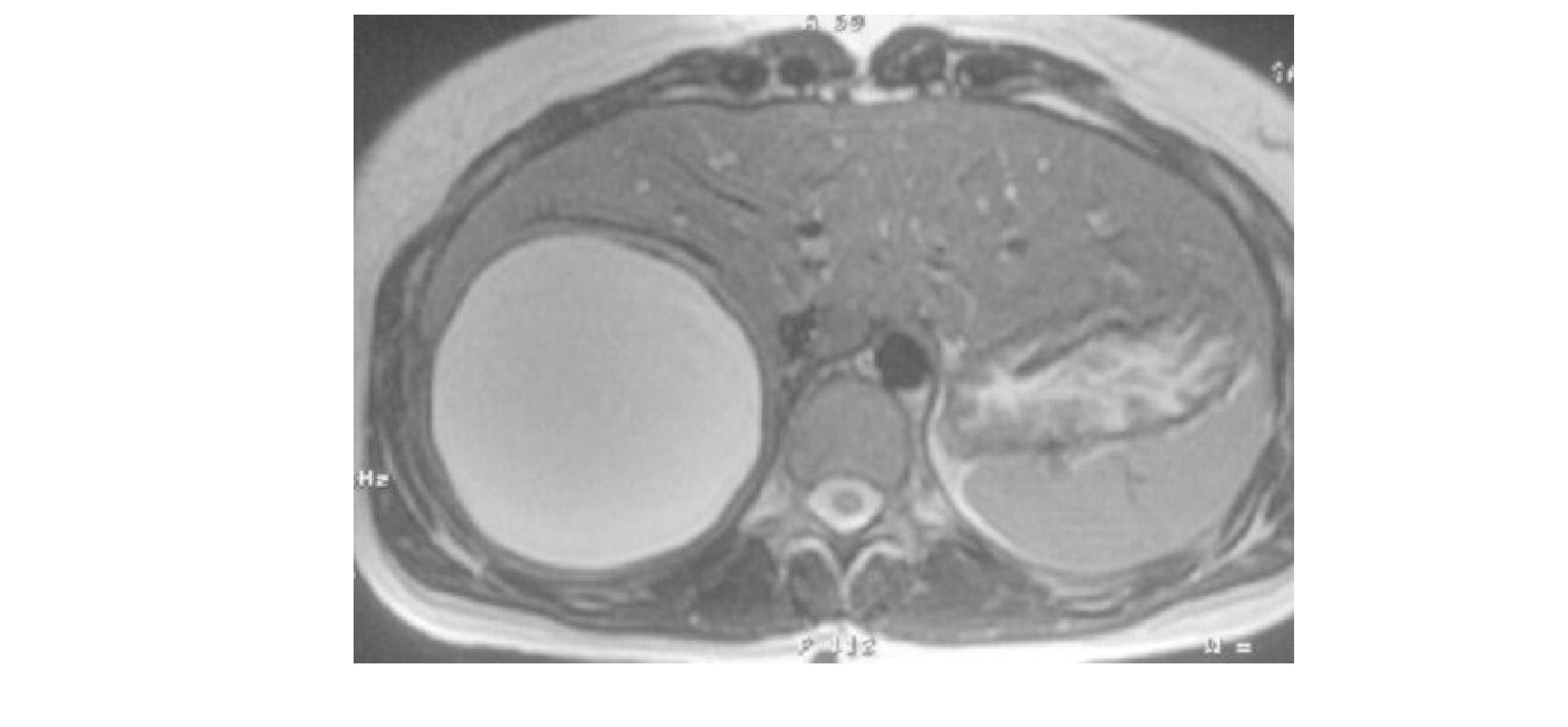
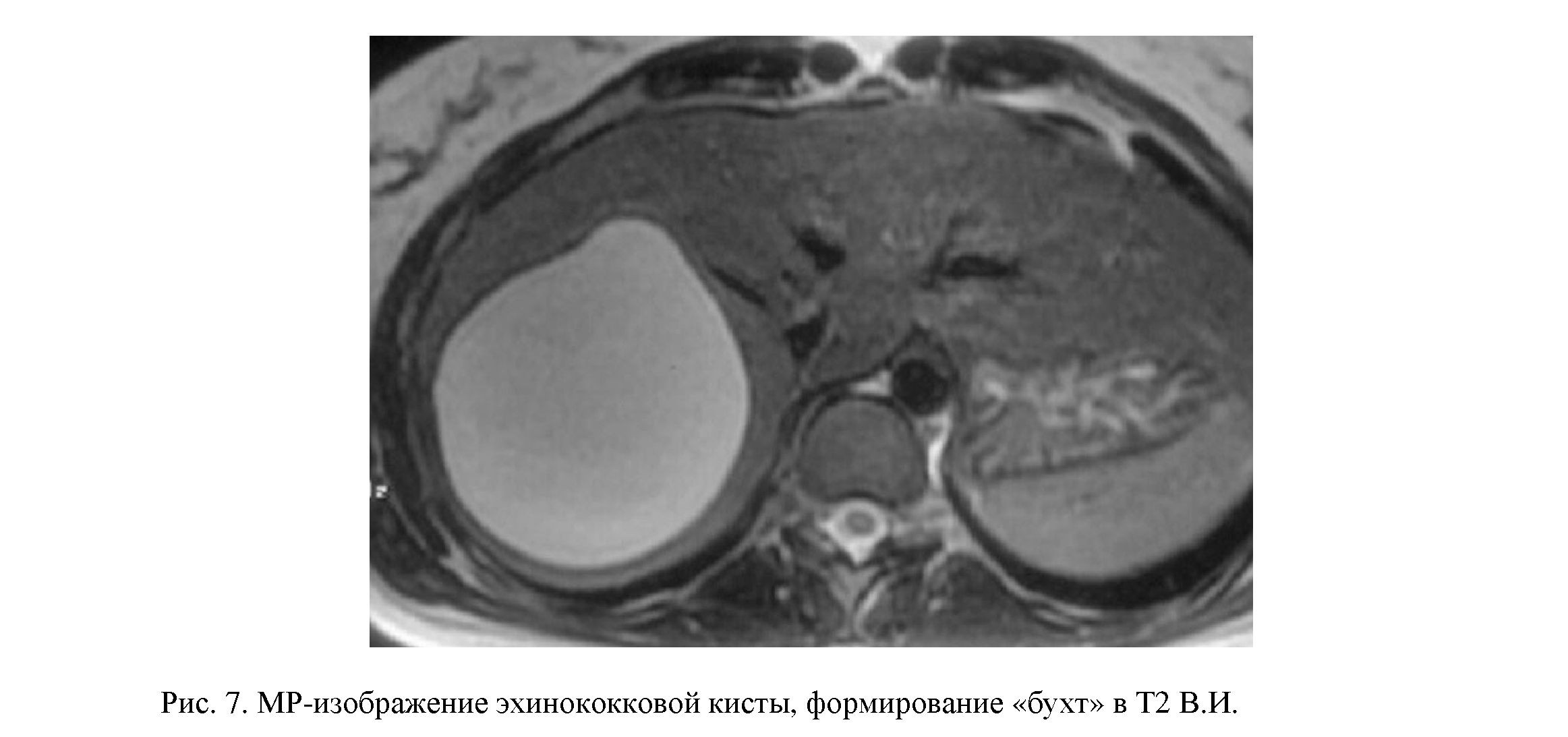
Эхинококковые кисты всегда имеют округлую форму, что связанно с активной жизнедеятельностью, ведущей к повышению давлению в полости кисты. Это приводит к возникновению слабых мест в фиброзной капсуле окружающей эхинококковую кисту. При MPT это проявляется виде бухт, вдающихся в паренхиму окружающей печени (рис. 7). Данная особенность приводит к ряду частых осложнений эхинококковых кист.
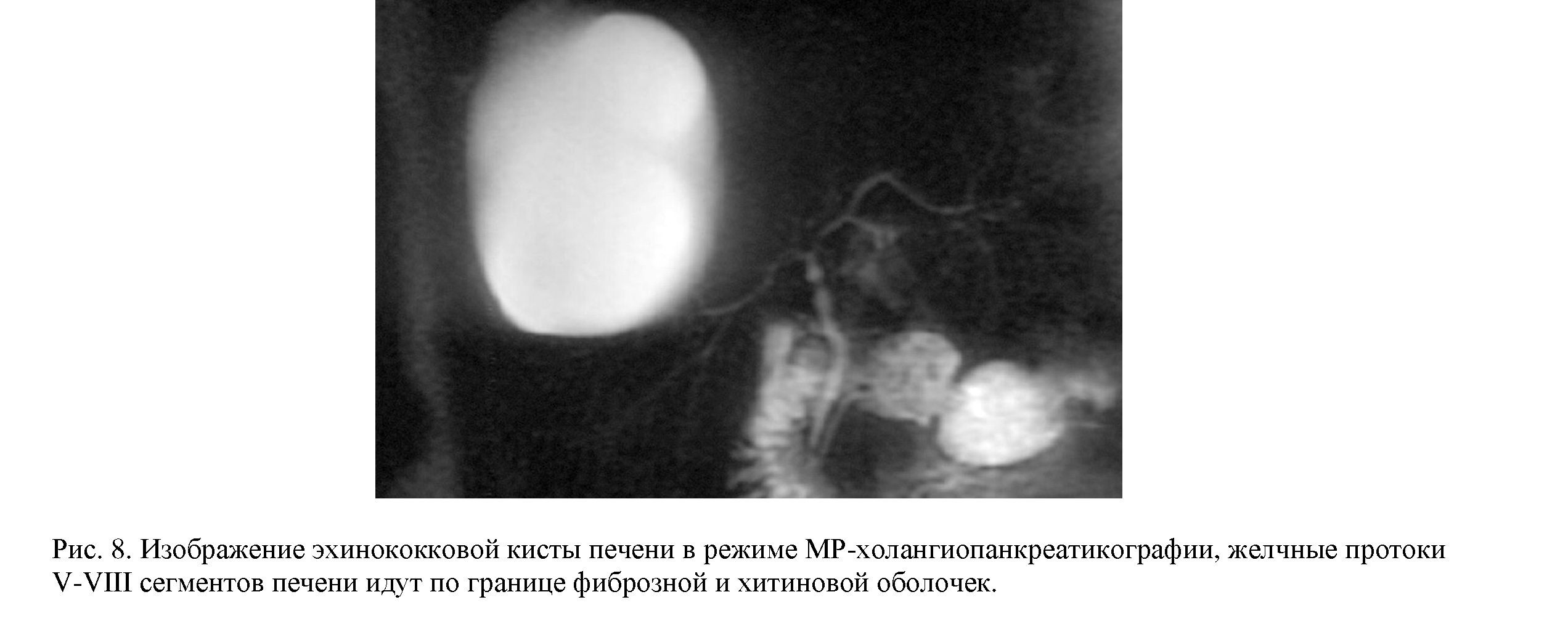
Увеличение размеров кист ведет к атрофии окружающей паренхимы и повышению риска возникновения дефекта в желчевыводящих протоках. MPT в режиме холангиопанкреатикографии (рис. 8) позволяет с большой степенью вероятности, что важно для планирования и осуществления неинвазивных методов лечения, заподозрить формирование желчного свища.
Все минимально инвазивные вмешательства выполнялись в условиях операционной с обязательным анестезиологическим пособием. При чрескожных вмешательствах под УЗ- и РТВ-наведением, при пункции и дренировании эхинококковой кисты, обязательными условиями были, прохождение инструмента через максимальную толщу паренхимы печени, в обход синуса, желчного пузыря, крупных сосудов и желчных протоков. Для дренирования использовали комплекс игла-катетер, исключающий попадание гидатидной жидкости вдоль пункционного канала. После аспирации гидатидной жидкости полость кисты обрабатывали 8587% раствором глицерина в объеме, адекватном эвакуированной жидкости. Обработка глицерином приводит к гибели герминативного слоя хитиновой оболочки, зародышевых элементов внутри и в стенке кисты, что обеспечивало отсутствие рецидива заболевания. На этапе разработки методики в каждом наблюдении проводили интраоперационный микроскопический контроль, который показал, что экспозиция глицерина в течение 7 мин была во всех случаях достаточна для гибели зародышевых элементов эхинококка, что исключает
 30
30
обсеменение и позволяет выполнять дальнейшие манипуляции. Для удаления хитиновой оболочки кисты применяли либо однокатетерный, либо двухкатетерный способ.
В первом случае пункционный канал расширяли до 12-14F с использованием специального инструментария, после чего выполняли дефрагментацию и удаление отслоившейся в процессе противопаразитарной обработки хитиновой оболочки паразита. Контроль полноты удаления хитиновой оболочки осуществляли рентгенологически. При подозрении на неполное удаление хитиновой оболочки или на цистобилиарный свищ, через специальную гильзу 16F в полость кисты вводили эндоскоп, под контролем которого удаляли остатки хитиновой оболочки и при необходимости обрабатывали свищевое отверстие. Операция заканчивалась оставлением в кисте тонкого страховочного дренажа для последующего закрытия остаточной полости.
Во втором случае, после установки дренажа и противопаразитарной обработки по методике Сельдингера, вводили дополнительный дренаж типа Малекот 12-16F. Дефрагментация оболочки осуществлялась с помощью проводника и создания турбулентных потоков внутри кисты, быстрым введением 20-ти граммовым шприцем физиологического раствора в тонкий дренаж и одновременным удалением его через толстый дренаж с фрагментами хитиновой оболочки.
Видеолапароскопические методы применяли при экстрапаренхиматозной локализации кист. Ограничением для видеолапароскопических операций служили кисты с локализацией в I, IVa, VII сегментах. Следует подчеркнуть, что одномоментная видеолапароскопическая эхинококкэктомия весьма опасна. Использование различных насадок, вакуум-присосок на лапароскопический инструмент, не позволяет добиться полной герметичности при аспирации гидатидной жидкости, чревато попаданием зародышевых элементов паразита в брюшную полость, высоким риском интраоперационных осложнений и послеоперационного рецидива заболевания. В связи с этим операцию осуществляли с применением двух методик. При первой методике дренировали кисту, вводили 85-87% раствор глицерина с экспозицией 7 мин, затем заменяли его физиологическим раствором. Далее осуществляли видеолапароскопическую операцию, а катетер использовали в качестве страховочного дренажа. Вторая методика включала интраоперационную пункцию эхинококковой кисты через сохраненную паренхиму печени, аспирацию содержимого, противопаразитарную обработку 8587% раствором глицерина в течение 7 минут, реаспирацию через канюлю вакуум отсоса диаметром 9мм. После удаления хитиновой оболочки максимально иссекали фиброзную капсулу, оставшуюся стенку изнутри обрабатывали плазменно-аргоновым коагулятором, что дополнительно обеззараживало полость и исключало открытие цисто-билиарных фистул. Выявленные при осмотре желчные свищи ушивали.
Применение минимально инвазивных технологий позволило повысить эффективность лечения у наиболее тяжелой категории больных с сочетанным эхинококкозом, чаще при поражении легких. Первым этапом выполняли эхинококкэктомию миниторакотомным доступом, вторым этапом осуществляли минимально инвазивное вмешательство на паренхиматозных органах
Результаты;
Чувствительность обнаружения сывороточных антител при РИГА, ИФА и AE достигает 85-87% для кист печени. Комбинация серологических реакций с УЗИ, когда определяется двухконтурность стенки, отслоение хитиновой оболочки, дочерние кисты в полости, кальциноз стенки кисты, позволяет в 93-95% поставить диагноз эхинококкоза печени. Трудностями в интерпретации УЗИ в 10% наблюдений оказались небольшие (до 50мм) кисты. Магнитно-резонансное исследование в Т2-взвешенных изображениях дает возможности выявить двойное строение стенки и диагностировать эхинококкоз.
Взятая за основу ультразвуковая классификация ВОЗ и Gharbi H.[21,22] позволила нам выработать показания и противопоказания к минимально инвазивным операциям в лечение эхинококкоза печени.
Чрескожные чреспеченочные эхинококкэктомии под УЗ- и РТВ-наведением были выполнены у 233(59%) взрослых и 12(14%) детей, чрескожное пункционное лечение - у 87(22%) взрослых и 16(18%) детей. Видеолапароскопические вмешательства с предварительным дренированием и обработкой полости кисты 8587% глицерином - у 76(19%) взрослых и 9(10%) детей, изолированные видеолапароскопические операции с интраоперационной пункцией и обработкой полости 85-87% глицерином - у 49(56%) детей. Один ребенок (1,2%) оперирован по методике М.И. Прудкова. При небольших размерах кисты (до 40 мм) нет необходимости удалять оболочку, в последующем она подвергается кальцификации или резорбции. Поэтому в этих случаях выполняли пункционное лечении эхинококковой кисты. Результаты экспериментальных и
патоморфологических исследований, внедрения глицерина в клиническую практику показали, что оставление хитиновой оболочки в полости предварительно обработанной кисты вполне допустимо.
Следует подчеркнуть, что выбор варианта вмешательства был основан на тщательном анализе ультразвуковой семиотики и данных МРТ с МРХПГ. Совершеннолетним пациентам и родителям детей разъяснялись возможные варианты операций, получали информированное согласие для проведения определенного минимально инвазивного метода. При этом акцентировали внимания на преимуществах и недостатках каждого метода, возможных осложнениях.
После чрескожной эхинококкэктомии осложнения в виде нагноения остаточной полости (ОП) отмечены в 1,7 % наблюдений. Все пациенты излечены дренированием под УЗ-наведением. Необходимо акцентировать внимание на том, что ОП после различных вариантов лечения не является эквивалентом рецидива. Отсутствие специфических УЗИ и МРТ признаков эхинококкоза, отрицательные серологические тесты свидетельствуют об эффективности лечения. В сомнительных случаях показана тонкоигольная пункция с цитологическим и иммунологическим исследованием содержимого. ОП определялись как после чрескожных - 125 (36,6%), так и после видеолапароскопических - 50 (37,5%) операций. Формирование ОП обусловлено пропотеванием плазмы из хорошо васкуляризированной фиброзной капсулы, что подтверждено при диагностической пункции под УЗ-наведением. К концу года, после операции ОП в 62-88% наблюдений редуцировались, в остальных отмечены ламинарные или неправильной формы полости, заполненные тканевым детритом. ОП в отдаленном периоде наблюдали только в 3,7 % наблюдений [29-31].
Из интраоперационных осложнений во время видеолапароскопической эхинококкэктомии можно упомянуть 5 (3,8%) наблюдений кровотечения при иссечении фиброзной капсулы и 2(1,5%) наблюдения разрыва эхинококковой кисты при введении первого троакара. Ни в одном наблюдении конверсии не потребовалось. Послеоперационных осложнений не отмечено.
У 92 (20%) пациентов имелись цистобилиарные свищи (ЦБС), которые у 13 (14.1%) пациентов во время видеолапароскопических операций были закрыты с помощью аргоно-плазменной коагуляции или ушивания. ЦБС начинали проявлять себя на 1-3 сутки после операции в виде желчеистечения по дренажу. Однако у 53 (57.9%) пациентов по дренажу отделялось не более 50 - 60 мл желчи в сутки, что свидетельствовало о небольшом размере свища. У данной подгруппы больных специального лечения не потребовалось, желчеистечение прекратилось на приеме одестона на 6 - 12 сутки. При большем объеме желчи (от 80-100 мл и более), в 28% наблюдений потребовалось комбинированное лечение, включавшее эндоскопические вмешательства (ЭПСТ и/или НБД) с последующей пломбировкой свища фибриновым клеем. Сроки стационарного лечения не превышали 2 недели[32,33].
Применение эффективных гермицидов, соблюдение правил абластики при операции, использование совершенного инструментария не исключают возможности рецидива заболевания. На результаты лечения заметно влияет последующая химиотерапия. Она необходима и для воздействия на маленькие отсевы эхинококка, недоступные современным методам диагностики. Наиболее эффективным препаратом, воздействующим на гидатидозный эхинококк, является альбендазол. В последние годы препарат находит все более широкое применение также как и самостоятельное лечение при кистах размерами до 30 мм. Противорецидивная терапия показана всем пациентам, оперированным по поводу эхинококкоза печени. Доза альбендазола составляет 10-15мг/кг/сут, продолжительность лечения - три курса по 1 месяцу, с перерывом между курсами 1-2 недели. В группе больных с высоким риском рецидива (множественный характер поражения, разрыв эхинококковой кисты, экзогенная пролиферация) более оправданы непрерывные курсы химиотерапии продолжительностью 2-3 и более месяцев[8,34-37].
На этапе освоения методики у одного пациента по ходу стояния дренажа возник рецидив эхинококковой кисты, что составило 0.3%. Сроки наблюдения за больными составили от полугода до 14 лет. Как известно, больные эхинококкозом после лечения подлежат динамическому наблюдению. До внедрения химиотерапии срок наблюдения составлял 5 лет. В последние годы в связи с использованием послеоперационной химиотерапии сроки учета могут быть сокращены. Критерием снятия больного с диспансерного наблюдения служит снижение титров серологических реакций до сомнительных цифр, либо отрицательный результат исследования. Обычно эти сроки не превышают 1-1,5 лет после хирургического лечения, при условии проведения полноценных курсов химиотерапии. В сроки наблюдения до 5-7 лет, рецидивов эхинококкоза после использования пункционного метода лечения не отмечено.
В рамках данной статьи мы не проанализировали данные по минимально инвазивным вмешательствам при рецидивном и резидуальном эхинококкозе, что является, несомненно, перспективным направлением.
Заключение.
Клиники обладают большим опытом проведения всех видов оперативного лечения гидатидного (цистного) эхинококкоза печени. Основываясь на результатах традиционного лечения, экспериментальных исследованиях и мировой практики была определена на текущий момент стратегия лечения эхинококкоза печени у взрослых и детей включающая в себя: противопаразитарную химиотерапию l минимально инвазивные вмешательства l традиционные операции l обязательную противорецидивную химиотерапию.
При интрапаренхиматозных кистах(СЕ, CE или I, CE3a или II, CE4 или IV типов) не выходящих за пределы 2-3 сегментов печени показаны операции под УЗ- и РТВ наведением.
При экстрапаренхиматозных кистах(СЕ или I,CE3a или II типов) кроме I, IVa и VII сегментов применимы видеолапароскопические вмешательства, с обязательной предварительной чрескожной или интраоперационной обработкой 85-87% раствором глицерина с экспозицией 7-10 минут.
Сберегающие операции (по строгим показаниям) с использованием современного оборудования, высокоэффективных гермицидов (85-87% раствор глицерина), проводимые в специализированных стационарах с последующей противорецидивной терапией (альбендазол 10-15мг/кг/сутки), не уступают по эффективности традиционным методам лечения эхинококкоза. К преимуществам метода относятся малая травматичность и быстрая реабилитация пациентов.
ЛИТЕРАТУРА
- Аскерханов Р.П. Некоторые общие вопросы патогенеза и клиники эхинококкоза // Диагностика и лечение эхинококковой болезни - Ставрополь - 1983 - С. 5-15.
- Петровский Б.В., Милонов О.Б., Дееничин П.Г. Хирургия эхинококкоза. - M.: Медицина, 1985; 216 с.
- Дейнека И.Я. Эхинококкоз человека.- M.: Медицина, 1986.-386 с.
- Милонов О.Б. Классификация операций, применяемых при эхинококкозе // Диагностика и лечение эхинококкоза - Баку - 1987 - С.135-136.
- Альперович Б.И. Хирургия печени и желчных путей. Томск: Красное знамя, 1997, 605 с.
- Руководство по хирургии печени и желчных путей. Под ред. Проф. А.Е. Борисова. Том I. Хирургия печени. - С-Пб.: Изд-во «Скифия», 2003; 261-273.
- Wang, X., Li, Y., Feng, S. Clinical treatment of hepatic and abdominal hydatid cyst by percutaneous puncture, drainage and curettage// Zhongguo Ji Sheng Chong Xue Yu Ji Sheng Chong Bing Za Zhi 1994.-No. 12.-P. 285-287.
- Brunetti E, Kern P, Vuitton D., Writing Panel for the WHO-IWGE. Expert consensus for the diagnosis and treatment of cystic and alveolar echinococcosis in humans.// Acta Trop. 2010. V. 114.p.1-16.
- Шкроб О.С., П.С.Ветшев, А.Н.Лотов с соавт. Использование ультразвука при хирургических заболеваниях гепатопанкреатодуоденальной зоны // Клин.мед. - 1986 - № 10, С. 76-83.
- Гаврилин А.В. Чрескожные лечебно-диагностические вмешательства под контролем УЗИ при хирургических заболеваниях органов гепатопанкреатобилиарной зоны. Автореф. докт. дис. М:1999. С. 48.
- Stoianov G., Grigorov N., Slavov V., Bogusheva E. Intraoperativen anafilactichen shok sled percutanna punktsiia na chernodrobna ekhinokokova kista// Khirurgiia Sofiia.-1995.-Vol.48, N4.-P.12-13.
- Гилевич М.Ю., Бодулин А.В. Зависимость способа эхинококкэктомии от стадии развития паразита // Хирургия.- 1986.-№°4.-С.94-97.
- Гилевич Ю.С.. Милонов О.Б. Диагностика и хирургическое лечение поддиафрагмального эхинококкоза печени и его осложнений. // Хирургия.-1988.-№12.-С.28-38.
- Григорьянц Р.Г. Диагностика и клинико-экспериментальное обоснование хирургического лечения эхинококкоза печени // Автореферат дисс. докт. мед. наук - 1991
- Кубышкин В.А., Кахаров М.А., Вишневский В.А., Икрамов Р.З., Гаврилин А. В. Эволюция методов хирургического лечения эхинококкоза// Анналы хирургической гепатологии.-2002.- том 7.- №1.- С.1822.
- Журавлев В.А., Русинов В.А., Щербакова Н.А. Гидатидозный эхинококкоз печени. Вопросы хирургического лечения. // Хирургия .-2004.-№4. С.51-54.
- Вишневский В.А., Икрамов Р.З., Кахаров М.А., Ефанов М.Г. Радикальное лечение эхинококкоза печени. Современное состояние проблемы.// Бюллетень сибирской медицины.- 2007.-№ 3.-С.22-26.
- Альперович Б.И., Сорокин Р.В., Толкаева М.В., Будков С.Р. Хирургическое лечение рецидивного эхинококкоза печени // Анналы хирург. гепатологии. 2006. Т. 11. № 1. С. 7—10.
- Коваленко Ф.П. «Экспериментальные модели эхинококкозов: оптимизация и применение в разработке методов диагностики, профилактики и лечения человека и животных». Дисс.. ..д.м.н. - М., 1998. - 69 с.
- Гальперин Э.И., Дедерер Ю.М. Нестандартные ситуации в хирургии желчных путей. М., 1987. С. 335.
- WHO. Informal Working Group. International classification of ultrasound images in cystic echinococcosis for application in clinical and field epidemiological settings// Acta.Trop.-2003. Feb.-Vol.85(2).-P.-253-261.
- Gharbi H.A., Hassin W., Braunner M.W. et.al.Ultrasound examination of the liver// Radiology.-1981.- Vol.139.-P.459-463
- Lotov A., Kuzin N., Kondrashin S.A. et al. Less-invasive method for treating liver echinococcosis // 37th World Congress of Surgery. - Acapulco, Mexico. - Aug. 24-30 1997. Abst.989.
- Дадвани С.А., Шкроб О.С., Лотов А.Н. Новое в лечении эхинококкоза печени. // Анналы хирургической гепатологии, 1998 -№3.-С.268-269.
- Дадвани С.А., Шкроб О.С., Лотов А.Н. Лечение гидатидозного эхинококкоза //Хирургия, 2000.-№8. - С.27-32.
- Sayek I, Onat D. Diagnosis and treatment of uncomplicated hydatid cyst of the liver. World J Surg. 2001.-No. 25.-P. 40-45
- Schipper H.G. et al. Diagnosis and treatment of hydatid cyst of the liver//Scand J. Gastroenterol. Suppl.-2004.- Vol.-241.-P.50-55.
- Белышева Е.С., Быченко В.Г., Лотов А.Н. с соавт. Магнитно-резонансная томография в комплексной диагностике гидатидозного эхинококкоза печени// Медицинская визуализация. 2003.№-2.-С. 6-12.
- Duta C., Lazar C., Bordos D. Percutaneous treatment of the liver Hydatid cysts//TMJ 2004.- Vol. 54.- No. 4.- P.342-345.
- Saglam A. Laparoscopic treatment of hydatid liver cysts// Surg. Laparosc. Endosc.-1996.Vol.6.-No.6.-P.16-21.
- Горемыкин И.В. Видеолапароскопия в лечении эхинококкоза печени. Автореф. дис. ... д-ра мед. наук. - Саратов., 1999.-34 с.
- Kayaalp C, Bostanci B, Yol S, Akoglu M. Distribution of hydatid cysts into the liver with reference to cystobiliary communications and cavity-related complications.//Am.J. Surg. 2003.-No. 185.-P. 175-179
- Джабраилов Д. А. Тактика ведения больных с цистобилиарными свищами при эхинококкозе печени. Автореф.канд.дис. :М. 2009.-21 с.
- Khuroo, M.S., Dar, M.Y., Yattoo еt al. Percutaneous drainage versus albendazole therapy in hepatic hydatidosis: a prospective, randomized study. //Gastroenterology 1993.-Vol.104.- P.1452-1459.
- Сергиев В.П. Легоньков Ю.А. Полетаева О.Г. и соавт. Эхинококкоз цистный (однокамерный).Клиника, диагностика, лечение, профилактика, Информационно-методическое пособие. М. 2008.-33 с.
- Arif S.H., Shams Ul, B., Wani N.A. et al. Albendazole as an adjuvant to the standard surgical management of hydatid cyst liver.// Int. J. Surg. 2008.-No.6.-P.448-451.
- Лотов А.Н., Чжао А.В., Черная H.P., Степанова Ю.А. Эхинококкоз: диагностика и органосохраняющая хирургия//Альманах Института хирургии имени А.В.Вишневского.2010.Т.5.№2. С.26-36.