Традиционными методами оздоровления посадочного материала сельскохозяйственных растений являются биотехнологические методы с использованием термотерапии, микроклонального размножения и тестирования на наличие вирусной инфекции. Они нашли широкое распространение в практическом растениеводстве.
Одной из главных причин вырождения яблонь сорта Апорт и других сортов являются вирусные и вироидные болезни. Наиболее вредоносными вирусами яблонь являются: Apple chlorotic leaf spot virus (ACLSV), Apple stem grooving virus (ASGV) и Apple stem pitting virus (ASPV). Вирусная инфекция приводит к задержке роста и развития растения, что приводит к снижению урожая до 70%, а в некоторых случаях до 100%. Проявление вирусной инфекции зависит от типа вируса. Болезнь может быть латентной, асимптоматичной, но часто может остро проявляться, вызывая серьезные повреждения или даже гибель яблони. Так, ASGV вызывает заболевание, носящее название стеблевая поровость яблони. При этом заболевании происходит повреждение проводящей системы растения – флоэмы, что впоследствии приводит к медленной гибели дерева. Нельзя не принимать во внимание и латентные инфекции, так как происходит перенос вирусов на более восприимчивые сорта, что приведет к значительному ущербу в плодоводстве.
Для предотвращения распространения болезней, вызываемых вирусами, необходим строгий контроль качества, как нового посадочного материала, выращенного в плодопитомниках, так и уже существующих плодовых садов. Иными словами, без детекции вирусов и вироидов фактически невозможно выращивать здоровые саженцы в плодопитомниках и поддерживать яблоневые сады в хорошем фитосанитарном состоянии. Однако это весьма сложная задача. Дело в том, что вирусные частицы можно увидеть только с помощью электронного микроскопа. Этот метод используется в научных целях. Для практического применения в полевых условиях не пригоден и стоит весьма дорого. О наличии вирусного заболевания можно судить и по визуальным признакам, проявляющимся на листьях, стеблях и плодах. Однако характерные признаки проявляются только через несколько лет, на более поздних стадиях заболевания. В настоящее время вирусный контроль осуществляется благодаря разработанным новейшим методам иммуноферментного анализа. Данный метод прост, высокочувствителен, экономически выгоден и пригоден для постоянного мониторинга фитосанитарного состояния плодовых насаждений.
Экспериментальная работа с водой доказала высокую вероятность повышения ее биологической активности происходящих за счет ее переструктуирования и устойчивого насыщения энергией при различных видах физического воздействия. В ряде опытов удалось достичь антиэнтропийного эффекта и прекращения развития патогенной микрофлоры. Контроль и диагностика энергетической активности жидких сред с помощью газовых разрядов. Газовый разряд поверхностного типа возникает в системе электродов «остриё-плоскость» при наложение импульсов высоковольтного напряжения. Разряд развивается вдоль поверхности тонкослойного диэлектрика. Структура разряда меняется от кваземерных фигур до сильно разветвлённых картин пробоя в зависимости отдиэлектрических характеристик материала, а также формы импульса и его полярности, конфигурации электродов, влажности и т. д.. Радиально разветвлённые структуры зафиксированные на фотоматериале являются результатом развития коронных искровых разрядов, известных под названием «фигуры Лихтенберга». При разряде вещество разделяется на области диэлектрической и проводящей фазы. Границы этих фаз являются динамическим объектом сложной стохастической формы. Нами установлено, что если «остриё» заменить капеляром с изучаемой жидкостью и ввести в неё электрод, то «фигуры Лихтенберга» будут менять свою конфигурацию в зависимости от физического состояния воды и степени её активности. Создан метод для мониторинга динамики фазовых состояний структурных модификаций в воде и других жидкостях.
Цель нашего исследования являлось апробирование, впервые в Казахстане, новой методики тестирования посадочного материала плодовых культур на наличие патогенной латентной вирусной инфекции и новой альтернативной методики его оздоровления с помощью фитогенной воды.
Программа и методика
Образцы использованные в настоящем исследовании собраны в питомниках Алматинской (Таблица1) и Жамбылской (Таблица2) областях. Листья сортов яблони М9 (клоны Nакobe и Pеijam1), ММ106 , Джонaголд, яблони Сиверса заморожены при -80оС или использовались свежими. Результаты иммуноферментного анализа представлены в таблицах 1 и 2 в виде значений оптической плотности при длине волны 415 нм
Для анализа вирусной инфекции в питомниках Казахстана отобраны наиболее распространенные вирусы, которые так же являются обязательными для диагностики питомников в европейских странах:
- вирус бороздчатости ствола яблони (ВБСЯ);
- вирус хлоротической пятнистости листьев яблони (ВХПЛЯ);
- вирус растрескивания ствола яблони (ВРСЯ);
- вирус мозаики яблони (ВМЯ)
- вирус кольцевой пятнистости томата (ВКПТ).
ВБСЯ – вирус нитевидной формы. Распространен повсеместно, поражает фруктовые деревья семейства Rosaceae. Переносчики вируса не известны. Вызывает бороздчатость на стволе, нарушения в месте прививки. ВХПЛЯ поражает яблони, груши, персики, сливы, абрикосы, вишню. Переносится во время прививок, механически. ВРСЯ латентный вирус, но при совместной инфекции с ВХПЛЯ, ВБСЯ и другими вирусами снижает урожайность. Пораженные деревья становятся хрупкими и чувствительными к дефициту питательных веществ. ВМЯ переносится прививкой и возможно пыльцой, вызывает мозаику на листьях яблони. ВКПТ вызывает нарушения в месте прививки, при чувствительном к вирусу привое или подвое происходит некроз в месте прививки.
В настоящей работе для анализа вирусной инфекции применен метод DAS-ELISA (double antibody sandwich enzyme-linked immunosorbent assay – двойной сэндвич твердофазный иммуносорбентный анализ).
Методы. Подготовка планшет.
Использованы первичные антитела специфичные к следующим вирусам, поражающим яблони:
Apple stem grooving virus (ASGV) – вирус бороздчатости ствола яблони (ВБСЯ);
Apple chlorotic leaf spot virus (ACLSV) - вирус хлоротической пятнистости листьев яблони (ВХПЛЯ); Apple stem pitting virus (ASPV) - вирус растрескивания ствола яблони (ВРСЯ); apple mosaic virus (ApMV) – вирус мозаики яблони и tomato ringspot virus (ToRSV) – вирус кольцевой пятнистости томата (ВКПТ).
Первичные антитела разбавлены 1:1000 в буфере состоящий из 1.59 г Na2CO3, 2.93 г NaHCO3 и 0.20 г NaN на 1 литр pH 9,6. 200 мкл разбавленных антител наносились в лунки и инкубировались в течении 12 часов при +4оС. После инкубации промывались буфером для промывки три раза по три минуты. Буфер для промывки состоит из 8.00 г NaCl, 0.20 г KH2PO4, 1.15 г Na2HPO4, 0.20 г KCl и 0.50 г Tween 20 на 1 литр буфера.
Подготовка экстракта.
100 мг листьев гомогонезировались в ступке в присутствии 2 мл буфера для экстракции:
20 мМ Tris HCl, 140 мМ хлорида натрия, 2 % поливинилпиролидона (молекулярный вес 25000), 0,05% Твин 20, 3 мМ хлорида калия, 0,02% азида натрия, pH буфера 7,4. 200 мкл экстракта нанесены на планшеты, содержащие первичные антитела и инкубировались при +4оС в течение 12 часов. По окончании инкубации плашки промывались буфером для промывки три раза по три минуты.
Детекция вирусов. В лунки наносились 200 мкл разбавленного 1:1000 соответствующее вторичное антитело конъюгированное с ферментом щелочной фосфатазы. Конъюгат разбавлялся в буфере содержащим 20 мМ Трис-HCl pH 7,4, 137 мМ хлорида натрия, 1 мМ хлорида магния, 2% поливинил пирролидона, 0,05% твеен 20, 0,2% БСА, 0,02% азида натрия. После инкубации при 30оС в течение 5 часов плашки промывались буфером для промывки. В каждую лунку наносился субстрат pNNP (p-nitro- phenyl-phosphate) в буфере для субстрата: 1М diethanolamine pH 9,8 и 0,02% азида натрия. Плашка инкубировалась в темноте при комнатной температуре в течение 30-60 минут. Оптическая плотность считывалась на фотометре 680 (Bio-Rad) при длине волны 415 нм.
Фитогенная вода подготавливалась по эксклюзивной методике В. М. Июшина и С. Н. Олейченко. Для исследования объектов в жидкой фазе разработано устройство, в котором дозированное количество воды набиралось металлическим поршнем шприца, снабженным диэлектрическим наконечником с калиброванным капиллярным отверстием радиусом Ro. Мениск жидкости на расстоянии 2мм размещался на фотоматериале, расположенном над слоем диэлектрика для блокировки электропробоя на плоский электрод. Контроль за качеством профиля капли осуществлялся выбором конструктивных элементов разрядного устройства. Параметры электрической схемы высоковольтного генератора обеспечивали режим работы устройства, при котором достигалось минимальное воздействие на объект. Мы использовали одиночные импульсы напряжения 3-5 кВ при длительности импульса порядка 1 мкс. Обеспечивалось постоянство амплитуды, формы электрического импульса, а также учет влажности, температуры, давления воздуха, что гарантировало воспроизводимость результатов эксперимента. Свечение газового разряда фиксировалось как с помощью спектральной аппаратуры, так и на фотоматериалах. Источником информации о состоянии воды служили параметры газового свечения (интенсивность, спектральный состав, формы двумерных газоразрядных структур). Наиболее сложной оказалась проблема адекватной оценки фигур Лихтенберга. Предложен набор геометрических параметров для определения нарушений формы контура и изменения топологии разрядных каналов.
Результаты. Образцы использованные в настоящем исследовании собраны в питомниках Алматинской (Таблица 1) и Жамбылской (Таблица 2) областях. Листья сортов яблони М9 (клоны Макабэ и Педжам), ММ106, Жана Голд, АРМ-18, яблони Сиверса заморожены при -80оС или использовались свежими. Результаты иммуноферментного анализа представлены в таблицах 1 и 2 в виде значений оптической плотности при длине волны 415 нм.
Таблица-1.
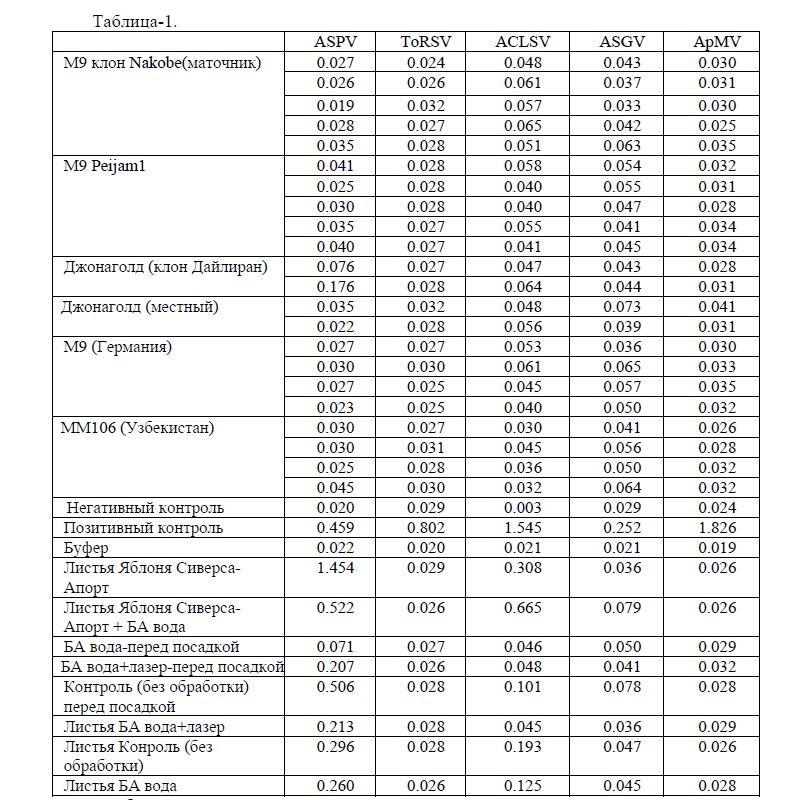
Таблица 2
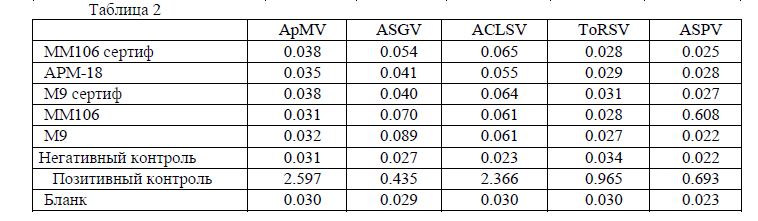
Как видно из результатов проведённых анализов растительных образцов из питомников ТОО «Торе Жайлау» и КХ «Айдарбаев» оба образца Джонаголд, Далиран поражены вирусом растрескивания ствола яблони (ASPV). Один из образцов культивируемого в местных условиях сорта Джонаголд поражен вирусом бороздчатости ствола яблони(ASGV). Вирус хлоротической пятнистости листьев яблони (ACLSV) найден только в яблоне сорта Апорт привитого на яблоню Сиверса, которое так же поражено ASGV и ASPV.
Ни в одном из исследованных образцов не найдены вирусы мозаики яблони (ApMV) и кольцевой пятнистости томата (ToRSV).
Серия опытов проведённых на подвоях яблони с биологически активной водой и лазерной активацией в начале, перед посадкой подвоев в первое поле, когда их погружали на сутки в БА воду, а затем в период вегетации, когда брались листья и на 15 минут погружались БА воду и в другом варианте активировались лазером. Установлена явная эффективность предпосадочной выдержки подвоев в БА воде. Латентная инфекция при данном методе обработки снизилась до минимума, что позволяет предложить для массового внедрения в производство данный альтернативный метод оздоровления растений. Два вида обработки листового аппарата в период активной вегетации растений существенного влияния на данные показатели не оказали. Следует так же отметить, что в рамках проекта было проведено пилотное тестирование подвойного материала в двух крупных питомниках Меркенского района Жамбылской области. Установлено сравнительная чистота нового подвоя яблони Арм 18 и оздоровленных подвоев завезённых из Голландии. Размножаемые длительный период в местных условиях подвой яблони ММ 106 и М 9 были завирусованы. Работа в данном направлении продолжается и в настоящее время охватывает питомники всех трех южных областей.
Выводы и заключения. Проведенный с использованием тест систем анализ на содержаний в подвоях и саженцах латентных вирусов показали, что местный исходный материал был в основном поражен одним или двумя вирусами. Особенно высокий их уровень отмечен к прививочной комбинаций Апорт\яблоня Сиверса. Это говорит о необходимости оздоровления стародавнего сорта и вероятно является одной из причин так называемого вырождения сорта. Примененные нами альтернативные методика показали определенную эффективность. Наибольшая чистота исходно зараженного посадочного материала была достигнута при суточном замачиваний подвоев биогенной воде перед посадкой. Применение этой воды в период вегетаций путем погружения надземной части с листьями в биогенную воду на 10 литров, а также ее применения совместно с лазером положительную результата не дали. Следовательно, можно рекомендовать применение данной воды только в предпосадочный период.
Этот агроприем будет иметь значительную перспективу. Для этого можно использовать различные емкости и полностью погружать в них оздоровительный посадочный материал.