Физико-химические исследования устойчивости растворов вольфрамата натрия при гидротермальном осаждении
Гидролитический способ выделения вольфрама из растворов в последние годы привлекает все большее внимание гидрометаллургов. Этот способ в ряде случаев позволяет достаточно полно и селективно отделить основной металл от многих ему сопутствующих. Достаточно эффективен способ гидролитического осаждения вольфрама из различных растворов, при котором возможно решение важных вопросов отделение вольфрама от фосфора, мышьяка и других примесей.
С целью снижения нагрузки на сорбционный предел, сокращения расхода ионообменной смолы и продолжительности процесса, был исследован вариант гидролитического осаждения вольфрама из растворов вольфрамата натрия, полученного после щелочного выщелачивания вольфрамового концентрата.
Известно, что дестабилизирующими факторами, влияющими на процесс выделения вольфрама в виде малорастворимых соединений, являются кислотность растворов, тип минеральной кислоты, температура процесса и присутствие комплексообразующих и затравочных компонентов.
При исследовании осаждения вольфрама из промышленных растворов вольфрамата натрия обнаружены некоторые различия в скорости, полноте осаждения и качестве осадков при подкислении исходных растворов той или иной минеральной кислотой. Названные параметры определяют рентабельность и эффективность этого способа выделения вольфрама из раствора, поэтому выявления причин, обуславливающих различия, очень важно при выборе условий осаждения и описания его механизма.
В работе методами ИК-спектроскопии и термогравиметрии изучались особенности поведения вольфрама в растворах вольфрамата натрия при подкислении соляной, азотной, хлорной, серной кислотами до рН 0,5-1,7 (предельное значение кислотности раствора при электрохимической обработке).
Процесс гидролиза вольфрамат-ионов в растворах вольфрамата натрия, подкисленных той или иной кислотой, реализуется по-разному. Так, подкисление раствора серной кислотой повышает его стабильность, в то время как в азотнокислых растворах гидролиз начинается раньше.
При регистрации спектров растворов в интервале 400-4000 см-1 на инфракрасном спектрофотометре UR-20 использован метод дифференциальной спектроскопии. При выдержке образцов водных растворов между крышками KRS-5 не менее 3-4 сут. образуются белые пленки, спектры которых также рассмотрены нами. Анализ спектров растворов и пленок позволяет проследить за изменением полос поглощения, связанных с колебаниями W=O и O-W-O-связей (область 500-1000 см-1) ОН-групп в таких оксигидрильных группировках, как OH-, H2O, H3O+ (области спектра 1100-1800 см-1 и 3000-3600 см-1), а также соответствующих групп и связей в
анионах NO- , SO- , HSO- , ClO- (область спектра 1000-1450 см-1).
3 4 4 4
В спектрах исследованных растворов в области 500-1100 см-1 присутствует широкая полоса поглощения с размытым максимумом, что свидетельствует о наличии цепей …WOWOWO… с мостиковыми кислородными атомами. В спектрах не обнаружено узких интенсивных полос поглощения в области 800-1100 см-1, которые можно было бы отнести к валентным колебаниям изолированных связей W=O. Однако, в соответствии с, высокое значение частоты (1100 см-1) говорит о том, что в цепях могут быть и двойные связи – W=O-W=O-W- . Узкие полосы поглощения в области 800-1100 см-1 можно отметить только в спектрах пленок, полученных из растворов, подкисленных серной, хлорной и соляной кислотами (рис. 1).
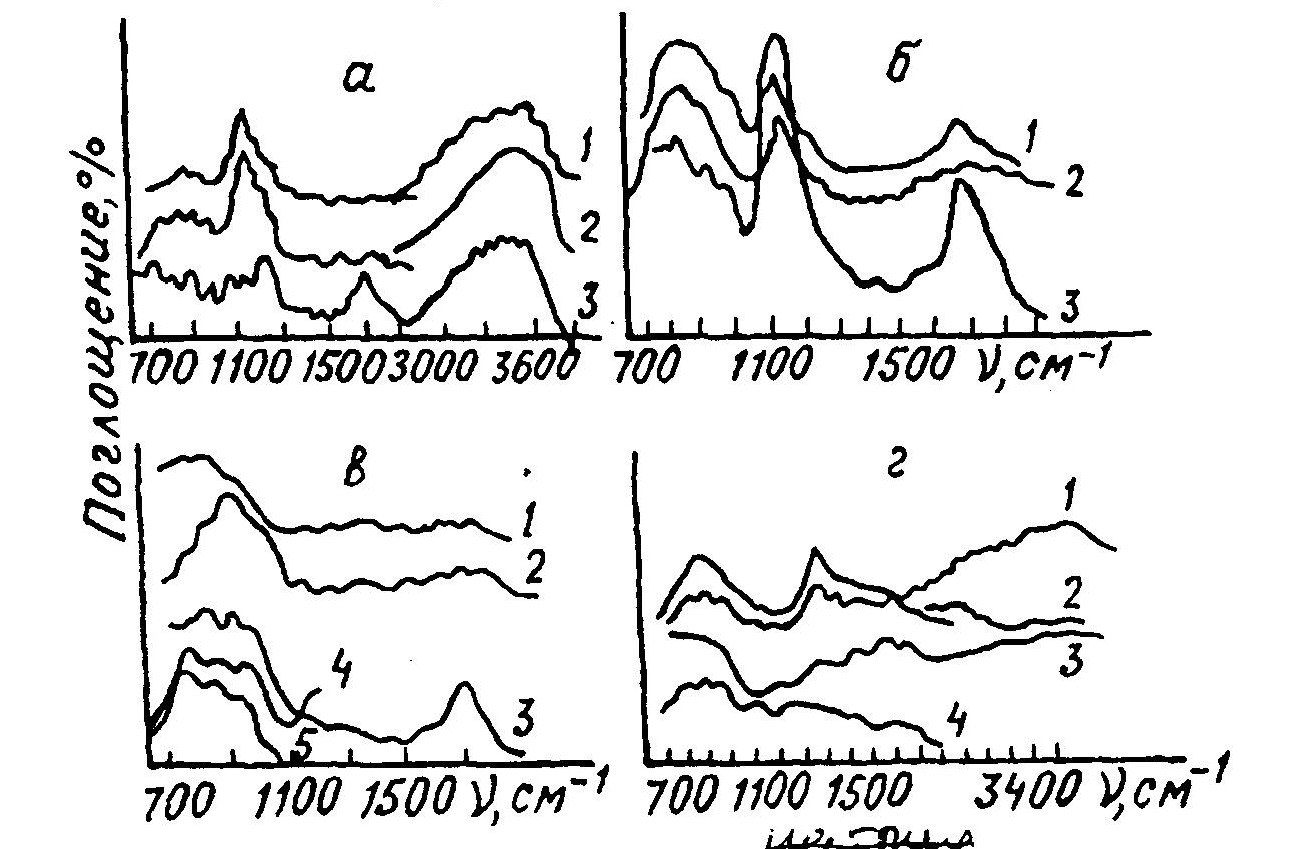 Рис. 1. ИК-спектры раствора вольфрамата натрия, подкисленного H2SO4 до рН 1,45 (а):
Рис. 1. ИК-спектры раствора вольфрамата натрия, подкисленного H2SO4 до рН 1,45 (а):
1 – свежеприготовленного; 2 – через 4 ч; 3 – пленка;
HClO4 до рН (б): 1 – 0,65; 2 – 1,67; 3 – пленка из
раствора 2; HCl до рН (в): 1 – 0,64; 2 – 1,65; 3 – пленка из раствора 2; 4 – реактивная соль паравольфрамата натрия; 5 – реактивный WO3; HNO3 до рН (г): 1 – 1,7; 2 – 0,65;
3 – пленка из раствора 2
При сравнении спектров пленок со спектрами реактивных триоксида вольфрама и паравольфрамата натрия видно, что из исследованных растворов в пленку переходит смесь этих соединений, так как спектры содержат полосы поглощенияобоих соединений (максимумы – 750, 820, 900, см-1). Выявленные закономерности отсутствуют в спектрах растворах и пленки, полученных при подкислении азотной кислотой, полоса поглощения в интервале 500-1100 см-1 практически не изменяется в спектрах раствора и пленки (рис. 1, 2).
Рис. 2. Термограммы осадков, полученных из растворов вольфрамата натрия при подкислении их до рН 0,8:
1 – азотной кислотой; 2 – хлорной кислотой
- Полоса поглощения, характерна дл колебаний ClO- -иона (1100-1200 см-1), не изменяется, за исключением того, что в спектре пленки по сравнению со спектрам раствора значительно возрастает ее интенсивность. Это можно объяснить повышением концентрации этих групп в объекте при испарении воды.
- В спектре раствора, подкисленного серной кислотой, полосу поглощения с максимумом 1130 см-1 и плечом 1220 см-1 можно отнести к колебаниям S=O-связей и ионах SO- и HSO-Вероятно, эти ионы входят в состав солей Na2SO4 и NaHSO4 или молекул свободной кислоты. В спектре пленки преимущественно присутствует HSO- -ион, о чем свидетельствует полоса поглощения с максимумом 1220 см-1, интенсивность которой возрастает за счет поглощения в области1130 см-1.
- Положение полосы поглощения, характерной для колебаний NO- -иона с максимумом при 1380 см-1, не изменяется в спектрах раствора и пленки, однако интенсивность заметно снижается в последнем спектре, а при выдержке пленки более недели эта полоса исчезает.
Описанные изменения можно объяснить следующим образом. При подкислении раствора вольфрамата аммония хлорной и серной кислотами в растворе образуются натриевые соли соответствующих кислот, различные формы поливольфраматов наряду с гидратированным триоксидом вольфрама, при выдержке раствора за счет свободного испарение воды образуется пленка, содержащая эти соединения. Снижение интенсивности полосы поглощения, связанной с колебанием NO-3-иона в спектре соответствующей пленки, по сравнению с таковой в спектре раствора, свидетельствует об уменьшении количества этих ионов в объекте.
В спектрах растворов и пленок, обработанных азотной кислотой, наблюдается поглощение, которое можно приписать колебаниям ОН-групп в соединениях типа WO(OH)n (область 1000–1500 см-1). Эта полоса огибает несколько полос, относящихся к колебаниям ОН-групп, испытывающих различные силовые воздействия со стороны центрального атома. Эти группировки в растворах говорят о том, что процесс гидролиза вольфрама должен начинаться раньше в тех растворах, где анион отсутствует или там, где влияние его невелико (азотнокислый раствор). На практике скорость осаждения из них выше, чем из остальных. Кроме гидроксильных группировок, в растворах присутствуют молекулы воды, деформационным колебаниям ОН-групп которых соответствует полоса поглощения с максимумом в интервале 1600-1700 см-1.
Полоса поглощения, связанная с валентными колебаниями ОН-групп, имеет максимумы около 3200 см-1 и 3400 см-1. В спектре пленки интенсивность первого снижается, а второго возрастает (рис. 1, 2). Эта также подтверждает вывод, что в объекте присутствуют различным образом координированные оксигидрильные группировки с неодинаковой силой водородных связей, которые при дегидратации видоизменяются, а возможно, частично разрушаются. Если первый из максимумов отнести к валентным колебаниям ОН-групп в соединениях типа WO(OH)n, а второй к колебаниям ОН-групп молекул воды, то можно сделать вывод о разрушении этих соединении при дегидратации растворов и формировании молекул гидратированного триоксида вольфрама.
В серно-, хлорно- и солянокислых растворах присутствуют оксигидрильные группирвоки различных типов: ионы ОН (поглощение, связанное с деформационными колебаниями ОН-групп в области 1700 см-1), гидроксид-ионы (полосы поглощения, обусловленные деформационными колебаниями ОН-групп в области 1500-1100 см-1) и молекул H2O (полосы поглощения деформационных колебаний ОН-групп в области 1680-1560 см-1). Однако интенсивность поглощения в интервале 1500-1100 см-1 вспектре этих растворов значительно ниже, чем в спектрах азотнокислого и электрохимически обработанного растворов.
В области валентных колебании ОН-групп присутствует широкая полоса поглощения при 3000-3700 см-1 с максимумом в области 3400-3600 см-1, характерная для молекул воды. Следовательно, гидратированных ионов типа WO(OH)n в этих растворах меньше. В спектрах пленок ясно указанные ионы, по-видимому, разрушаются, так как малоинтенсивные полосы поглощения в интервале 1100-1500 см-1 исчезают и появляется интенсивная полоса поглощения с максимумом при 1640 см-1, связанная с деформационными колебаниями ОН-групп молекул воды, в области валентных колебаний этих групп спектр остается прежним. Поскольку молекулы гидратированного триоксида вольфрама формируются через эти формы, то скорость осаждения из азотнокислых и электрохимически обработанных растворах будет выше, чем из других, что и наблюдается на практике.
Выявленные здесь различия в структуре растворов, подкисленных различными кислотами, могут явиться причиной различий в технологических показателях процесса осаждения вольфрама из этих растворов, что должно отразиться и на свойствах осадков. Для подтверждения этой концепции термически исследовано обезвоживание образцов осадков, полученных при подкислении растворов теми же кислотами, и электрохимической обработкой до рН 0,8 на дериватографе GD-102 с использованием приспособления, самогенерирующего атмосферу без доступа воздуха и непрерывного отвода паров. Диапазон температур 20-500 0С, чувствительность взвешивания 5 %. Осадки получены от образцов, подсушенных в течение 2 суток непосредственно после осаждения (рис. 2).
Анализ термограмм показывает, что влага теряется в температурном диапазоне 85-170 0С, что можно отнести к дегидратации образцов за счет удаления свободной и кристаллогидратной
влаги. Характер отщепления молекул воды идентичен для всех образцов и сопровождается эндоэффектом при температурах 110-170 0С. Наличие суммарного эндоэффекта свидетельствует о нескольких стадиях дегидратации. Для осадка, полученного осаждением хлорной кислотой, эндоэффект наблюдается при температурах 110, 130, 160 0С. После выдержки этого образца в течение 2 сут на воздухе эндоэффектам соответствуют температуры 160, 170 0С. В свежеприготовленных образцах присутствует некоторое количество свободной воды, которая удаляется при 110, 130 0С, подсушивание образцов на воздухе сопровождается удалением этой влаги (11-16 %) (см. табл.). с дальнейшим нагреванием удаляется связанная влага, входящая в состав соединений, в которых молекулы воды несколько меняют структуру, испытывая силовые воздействия со стороны центральных молекул. Такую влагу можно отнести к кристаллогидратной.
Количество влаги в осадках, полученных осаждением вольфрама из растворов вольфрамата аммония различными кислотами
|
Кислота |
Количество влаги, % |
|
|
свежеосажденный образец |
подсушенный на воздухе образец |
|
|
HNO |
81 |
65 |
|
H2SO4 |
83 |
61 |
|
HCl |
70 |
88 |
|
HClO4 |
85 |
64 |
Наименьшее и постоянное количество влаги содержит осадок, полученный при электрохимической обработке раствора и составляет 58 %. Вероятно, это явилось причиной кристаллизации аморфного триоксида вольфрама при температуре 270 С, о чем свидетельствует экзоэффект на термограмме (рис.2). На термограммах других образцов этот экзоэффект отсутствует.
Таким образом, различие в структуре соединений, образующихся в вольфрамсодержащих растворах при их подкислении минеральными кислотами может обуславливать не только различие в технологических параметрах процесса осаждения вольфрама, но и определить процесс структурирования осадка при дальнейшей термической обработке.
ЛИТЕРАТУРА
- Зеликман А.Н., Никитина Л.С. Вольфрам. М, Металлургия, 1978, 271 с.
- Харитонов Ю.Я., Буслаев Ю.А., Кузнецова А.А. и др. Инфракрасные спектры поглощения некоторых соединений вольфрама //Неорг. материалы. 1966, Т. 2, №2., С. 321-324.
- Холмогоров А.Г., Мохосоев М.В., Зонхоева З.Л. Модифицированные иониты в технологии молибдена и вольфрама. Новосибирск, 1985, 177 с.
- Юхневич Г.В. Инфракрасная спектроскопия воды. М., 1973, 207 с.
- Цундель Г. Гидратация и межмолекулярное взаимодействие. М., 1972, 404 с.
- Подшивалова А.К., Черняк А.С, Карпов П.К. О некоторых превращениях форм молибдена VI в кислых растворах //Журн. неорг. хим., 1984, Т. 29, №10, С. 2554-2557.
- Деркач Л.В., Полищук С.Я., Клоссе Г.А. и др. Изучение ванадо-вольфрамовых гетерополикислот теллура IV //Журн. неорг. хим., 1984, Т. 29,№6, С. 1473-1475.
- Юхневич Г.В. Состав продуктов термического разложения некоторых аква- и полисоединений //Журнал неорганической химии. 1960. №9. С. 123-134.
- Кiss А.В., Hild Е. Тungsram Technische Mitteilungen. 1975. N. 36. S. 1123-1138.
- Амелин А.Р. Технология серной кислоты. М., 1983. С. 13-25.