Исследования физико-химических свойств осадков, полученных из растворов вольфрамата натрия с помощью гидротермального осаждения триоксида вольфрама
Гидролитическое осаждение вольфрама из растворов – один из надежных и достаточно простых способов получения чистых солей этого металла. Для выбора оптимальных условий осаждения необходимы сведения о свойствах осадков, их структуре и составе. В ранее проведенной работе описаны результаты исследования растворов вольфрамата натрия, подкисленных разными кислотами, приведены некоторые сведения об осадках, полученных из этих растворов. В настоящей работе изложены результаты физико-химического исследования осадков, полученных при подкислении вольфрамсодержащих растворов соляной, серной и азотной кислотами. Сочетание методов рентгеноструктурного анализа, термогравиметрии и ИК- спектроскопии позволило провести исследования, на основании которых сделаны выводы о влиянии природы кислоты и ее количества, а также температуры раствора на состав и структуру соединений в фазе осадка.
Влияние соотношения вольфрам : кислота на молекулярный состав осадка исследовали, подкисляя раствор соляной кислотой. Солянокислые растворы отличие от серно- и азотнокислых готовили растворением вольфрамовой кислоты в растворе гидроксида натрия при соотношении NH4 : W = 4 : 1, T : Ж=1:10 – 1:5, t≤60 0C. Получали устойчивые в течение нескольких дней растворы, которые нейтрализовали соляной кислотой до рН 3,5 и осаждали вольфрам, вводя вновь концентрированную соляную кислоту; осадки промывали водой и просушивали на воздухе.
При осаждении вольфрама использовали раствор вольфрамата натрия, который подкисляли концентрированной азотной кислотой, выдерживая соотношение HNO3 : W = 12:1. Для выявления влияния температуры раствора на состав и структуру осадка исследовали осадки, полученные из азотнокислых растворов при температуре от 0 до 95 0С. При подкислении серной кислотой раствора вольфрамата аммония варьировали температуру и соотношение вольфрам : кислота.
Рентгеноструктурный анализ выполнен на дифрактометре ДРОН-3 на трубке с кобальтовым излучателем, термогравиметрические исследования – на дериватографе И. Паулик, Л.Паулик, И.Эрдеи. Термическое разложение осадков проведено в интервале температур 20-500 0С в условиях самогенерируемой атмосферы направленным отводом паров из зоны реакции. ИК- спектры регистрировали на спектрофотометре UR-20.
При осаждении вольфрама из растворов, подкисленных соляной кислотой варьировали ее содержание от 4-5 молей на моль вольфрама до 25 молей на моль, процесс вели при температуре 95 0С, первый осадок получен при комнатной температуре. Результаты рентгеноструктурного анализа свидетельствуют о наличии в составе осадков хлорида аммония (8-10 %), количество которого снижается до 1 % при увеличении кислотности раствора.
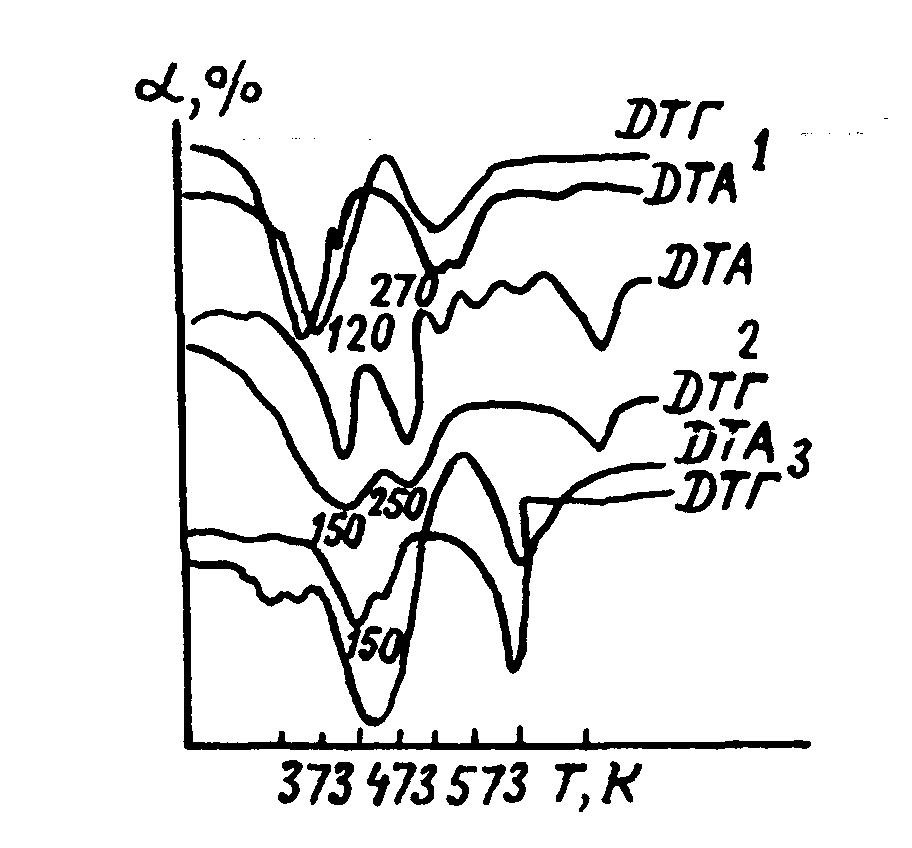
Результаты ТА-исследований показывают, что разложение осадков происходит в две стадии при непрерывном испарении воды, в зависимости от условий получения осадков глубина термического эффекта той или иной стадии превалирует. Для первой стадии температуры эндоэффекта 120 0С, вторая стадия характеризуется эндоэффектом при температуре 270 0С (рис. 1). В осадках 1-6 преимущественно присутствует первый эндоэффект, в остальных – глубина первого и второго эндоэффектов соизмерима. Кроме того, в осадках, полученных из менее кислых растворов (образцы 1, 3, 4), содержится больше влаги, чем в остальных (табл. 1). Все вышеизложенное позволяет предполагать, что объекты состоят из двух фаз, первая из которых формируется при соотношении W:HCl≤1:7, содержит до 20 % влаги, удаляющейся при температуре 120 0С. Для формирования второй фазы необходимо затратить большее количество кислоты, эти объекты характеризуются низким содержанием влаги, которая удаляется при температуре 250-270 0С. Сравнимая глубина эндоэффектов в образцах с высоким содержанием кислоты свидетельствует об одновременном и равнозначном присутствии обеих фаз в осадке.
Результаты рентгеноструктурного анализа также показывают присутствие двух фаз в объектах – одноводного гидроксида вольфрама с хорошо раскристаллизованными кристаллами и двуводного – с аморфизированной структурой. При соотношении HCl:W = 25:1 из раствора
выпадают кристаллы одноводного триоксида вольфрама, в остальных случаях смесь одно- и двуводного гидроксида вольфрама.
Рис. 1. Термограммы разложения осадков при нагревании в диапазоне температур 20-500 0С при подкислении вольфрамсодержащих растворов кислотами:
1 – соляной, 2 – азотной, 3 – серной
Таблица 1. Характеристика осадков, полученных при подкислении вольфрамсодержащих растворов соляной кислотой (CWO – 50 г/л)
|
№ п/п |
Соотношение HCl:W |
Т, 0С |
Степень осаждения, η, % |
Цвет осадка |
Масса воды, % |
Фазовый состав |
|
1 |
5:1 |
29 |
74 |
белый |
20,0 |
WO3·2H2O |
|
2 |
14:1 |
95 |
67 |
Желтый |
21,3 |
WO3·H2O |
|
3 |
4:1 |
95 |
54 |
белый |
11,3 |
WO3·2H2O |
|
4 |
7:1 |
95 |
77 |
кремовый |
20,0 |
WO3·2H2O |
|
5 |
12:1 |
95 |
96 |
желтый |
23,0 |
WO3·H2O |
|
6 |
19:1 |
95 |
100 |
желтый |
13,0 |
WO3·H2O |
|
7 |
25:1 |
95 |
100 |
желтый |
12,0 |
WO3·H2O |
ИК-спектры исследованных осадков подразделяются на две группы – от образцов 1, 3, 4 и 2, 5, 6, 7; первая группа спектров характеризуется широкой полосой поглощения с нечетками максимумами в интервале 700-1000 см-1, вторая – имеет дискретные полосы поглощения с максимумами при 760 и 960 см-1. По данным, спектры 1, 3, 4 коррелируются со спектром белой
вольфрамовой кислоты WO3·2H2O, а спектры 2, 5, 6, 7 ближе спектру желтой вольфрамовой кислоты WO3·H2O. Однако в последних, вероятно, имеется примесь белой вольфрамовой кислоты (рис. 2).
Отжиг всех осадков при температуре 500 0С приводит к переходу гидроксида в безводный
триоксид вольфрама, по результатам рентгеноструктурного анализа остается незначительное количество молекул WO3·H2O.
Рис. 2. ИК-спектры осадков, полученных при подкислении вольфрамсодержащих раствора соляной кислотой при температурах 20 0С (1) и 95 0С (2-7) и соотношении (моль):
(моль): 5:1 (1); 14:1 (2); 4:1 (3); 7:1 (4); 12:1 (5); 19:1 (6); 15:1 (7), отожженных при 500 0С (8)
При исследовании осадков полученных из азотнокислых сред пытались проследить за изменением фазового состава при варьирования температуры растворов объем осадков уменьшается, например осадок, полученный из раствора при температуре 15 0С, в 3,5 раза объемнее осажденного при температуре 95 0С.
Для определения фазового состава и структуры соединений, выделяющихся из растворов, целесообразно исследовать непромытые образцы, так как при контакте осадка с водой снижается кислотность в его фазе, что влияет на состав и структуру. При нагревании осадков в диапазоне температур 100-300 0С происходит термическое разложение двух структурных групп, первой – при температуре 100-150 0С и второй – при температуре 200-250 0С (см. рис. 1). При низких температурах превалирует эндоэффект при 120-150 0С, с повышением температуры глубина его уменьшается, в то время как эндоэффект при температуре 250 0С cтановится более заметным, а впоследствии сравнимым с первым.
Результаты рентгеноструктурного анализа показали присутствие незначительного количества (1,5-2,9 %) нитрата аммония в объектах. При температурах от 0 до 55 0С в осадках присутствуют две фазы – одно- и двуводный триоксид вольфрама, повышения температуры до 55 0С приводит к росту количества одноводного триоксида за счет снижения двуводного, при температуре 95 0С молекулы WO3·H2O доминируют.
Результаты ИК-спектроскопического исследования предполагают инойфазовый состав – до темпераутры 40-50 0С из растворов выпадает осадок, являющийсясмесью одно- и двуводного триоксида, а также поливольфраматов. Об этом свидетельствуют ИК-спектры соответствующих осадков (рис. 3). В ИК-спектрах осадков, полученных из растворов с температурой от 0 до 45 0С, присутствуют полосы поглощения с максимумами при 940-960 и 1010 см-1, которые авторы отмечают в спектрах поливольфраматов. Спектры осадков, полученных из растворов при температурах выше 55 0С, коррелируются со спектром одноводного триоксида вольфрама. ИК- спектры отожженных осадков содержат полосы поглощения в области 700-1000 см-1, характерные для вольфрамовой кислоты и триоксида вольфрама.
Осаждение вольфрама из растворов, подкисленных серной кислотой, приводит к получению аморфных сметанообразных продуктов ярких цветов.
 Увеличение соотношения W:H2SO4 от 1:4 до 1:25 сопровождается повышением степени осаждения и обеспечивает получение монофазы - WO3·H2O. Увеличение содержания кислоты в растворе более эффективно влияет на формирования однородного осадка – триокисда вольфрама, чем повышение температуры (см. табл. 3). Так, в осадке 6 даже при температуре 95 0С присутствуют и триоксид вольфрама и поливольфрамат.
Увеличение соотношения W:H2SO4 от 1:4 до 1:25 сопровождается повышением степени осаждения и обеспечивает получение монофазы - WO3·H2O. Увеличение содержания кислоты в растворе более эффективно влияет на формирования однородного осадка – триокисда вольфрама, чем повышение температуры (см. табл. 3). Так, в осадке 6 даже при температуре 95 0С присутствуют и триоксид вольфрама и поливольфрамат.
Рис.3. ИК-спектры осадков, полученных при подкислении вольфрамсодержащего раствора азотной кислотой (соотношение HNO3:W = 12:1) при температурах (0С) раствора: 0 (1); 25 (2);
45 (3); 55, 65, 75, 85,95 (4-8), отожженных при 500 0С (9)
Количество влаги в осадках порядка 20-30 %, причем определить это можно только при нагреве в условиях направленного отвода паров, так как в естественных условиях обжига на воздухе испаряющаяся влага вновь поглощается осадком. Это обстоятельство так же, как и эндоэффект при 350 0С, который обусловлен кипением серной кислоты, подтверждает факт ее присутствия в осадках.
ИК-спектры образца 1 (рис. 4) коррелируются со спектром гидратированного триоксида вольфрама, спектры осадков 2 и 3, вероятно, ближе к спектру поливольфраматов. В спектрах осадков из азотнокислых растворов при температурах от 0 до 45 0С присутствует высокочастотная компонента с максимумом выше 1000 см, в соответствующих спектрах осадков из сернокислых растворов – максимум полосы поглощения – при 980 см, общий вид спектра также различен (см. рис. 4). По интерпретации авторов можно сделать вывод о том, что осаждение из азотнокислых растворов способствует формированию более полимеризованных соединений, чем из сернокислых.
Таблица 2. Влияние температуры вольфрамсодержащих растворов, подкисленных азотной кислотой, на состав и структуру осадков (соотношение HNO3:W=12:1 )
|
№ п/п |
Т, 0С |
η, % |
Цвет осадка |
Масса воды, % |
Фазовый состав |
|
1 |
0 |
99,2 |
белый |
30,3 |
Смесь ПВ*, WO3·H2O, WO3·2H2O |
|
2 |
15 |
98,5 |
» |
20,8 |
» » » |
|
3 |
25 |
91,1 |
» |
20,0 |
» » » |
|
4 |
35 |
91,0 |
кремовый |
13,0 |
» » » |
|
5 |
45 |
89,7 |
» |
12,8 |
» » » |
|
6 |
55 |
88,7 |
желтый |
15,5 |
» |
|
7 |
65 |
87,7 |
» |
14,0 |
» |
|
8 |
75 |
92,2 |
Ярко-желтый |
10,0 |
» |
|
9 |
85 |
96,3 |
» |
11,2 |
» |
|
10 |
95 |
98,0 |
» |
14,7 |
» |
*ПВ – поливольфрамат.
Таблица 3. Влияние температуры и соотношения вольфрам : кислота в вольфрамсодержащих растворах при подкислении их серной кислотой на состав и структуру осадков (CW – 50 г/л)
|
№ п/п |
W:H2SO4, моль |
Т, 0С |
Масса воды, % |
Степень осаждения, η, % |
Цвет осадка |
Фазовый состав |
|
1 |
1:5 |
95 |
15,4 |
58 |
Ярко-желтый |
WO3·H2O |
|
2 |
1:5 |
50 |
34,0 |
48 |
Кремовый |
ПВ, WO3·H2O |
|
3 |
1:5 |
10 |
22,0 |
77 |
Белый |
ПВ |
|
4 |
1:25 |
95 |
20,0 |
90 |
Желтый |
WO3·H2O |
|
5 |
1:10 |
95 |
22,0 |
71 |
Желтый |
WO3·H2O |
|
6 |
1:4 |
95 |
20,0 |
55 |
Кремовый |
ПВ, WO3·H2O |
Сульфат-ион в осадках присутствует в составе кислоты (максимумы полос поглощения валентных колебаний S=O-связи 1060 и 1170 см-1), а также в составе соли (максимумы при 1150- 1170 см-1). В осадках 1 и 2 можно констатировать наличие молекул серной кислоты, в осадке 3 – смесь кислоты или сульфатной или бисульфатной соли. В осадке 6, полученном из раствора при соотношении вольфрам:кислота=1:4 полосы поглощения, соответствующие колебаниям S=O- связи в свободной кислоте отсутствуют, можно только отметить полосу поглощения с максимумом при 1170 см-1, относящуюся к колебаниям S=O-связи в ионах SO--4 в сульфатной соли.

Рис. 4. ИК-спектры осадков, полученных при подкислении вольфрамсодержащего раствора серной кислотой при соотношении W:H2SO4 =1:4 (6); 1:5; 1:10 (спектры совпадают (1)), при температуре раствора 95 0С (1), (6), 50 0С (2); 10 0С (3)
Серная кислота и ее кислая соль отличаются способностью поглощать пары воды, видимо, поэтому осадки, полученных из сернокислых растворов, содержат так много влаги. Процесс поликонденсации обеспечивается за счет отщепление молекул воды заторможено, следовательно, и поликонденсация ионов идет не столь активно. Вероятно, эти обстоятельства обуславливают невысокую степень полимеризации, а значит, и низкую степень осаждения.
ЛИТЕРАТУРА
- Юхневич Г.В. Состав продуктов термического разложения некоторых аква- и полисоединений //Журнал неорганической химии. 1960. №9. С. 123-134.
- Кiss А.В., Hild Е. Тungsram Technische Mitteilungen. 1975. N. 36. 8. 1123-1138.
- Амелин А.Р. Технология серной кислоты. М., 1983. С. 13-25.
- Деркач Л.В., Полищук С.Я., Клоссе Г.А. и др. Изучение ванадо-вольфрамовых гетерополикислот теллура IV //Журн. неорг. хим., 1984, Т. 29,№6, С. 1473-1475.
- Зеликман А.Н., Никитина Л.С. Вольфрам. М, Металлургия, 1978, 271 с.
- Харитонов Ю.Я., Буслаев Ю.А., Кузнецова А.А. и др. Инфракрасные спектры поглощения некоторых соединений вольфрама //Неорг. материалы. 1966, Т. 2, №2., С. 321-324.
- Холмогоров А.Г., Мохосоев М.В., Зонхоева З.Л. Модифицированные иониты в технологии молибдена и вольфрама. Новосибирск, 1985, 177 с.
- Юхневич Г.В. Инфракрасная спектроскопия воды. М., 1973, 207 с.
- Цундель Г. Гидратация и межмолекулярное взаимодействие. М., 1972, 404 с.