Учет неполноты исходной информации при разработке математических моделей технологических процессов
1. Анализ ситуаций неопределенности исходных данных при расчете химико- технологических процессов
Задача расчета потоков массы и тепла представляет собой чрезвычайно трудную проблему, поскольку промышленные процессы протекают в условиях, весьма далеких от границ устойчивости и осложнены влиянием различных физико-химических факторов. При неполной предварительной информации о кинетике процесса можно предложить следующую последовательность подготовки исходных данных для расчета и проектирования химических реакторов:
- получение корреляций коэффициентов переноса и эмпирических зависимостей от определяющих физико-химических параметров изучаемых систем;
- построение полуэмпирических моделей, описывающих основные наблюдаемые в экспериментах закономерности и содержащих минимальное число эмпирических параметров;
- математическое и компьютерное моделирование а также вычисление характеристик массо- и теплопереноса на примере модельных систем.
Эмпирические параметры, содержащиеся в полученных соотношениях должны определяться для каждой системы с известной структурой кинетических зон и гидродинамическими условиями. Необходимо обеспечить достаточную надежность математического моделирования хотя бы по ключевым характеристикам, определяющим режимные переходы в системе, т.к. ситуация неполноты информации о процессе весьма обычна при проектировании промышленных аппаратов.
Анализ известных литературных данных и результаты проведенных нами исследований [1- 4] позволяют предложить следующую классификацию процессов, для расчета которых необходимо учитывать неполноту исходной информации и использовать специальные подходы [5].
- Сложные многостадийные процессы с неизученной до конца кинетикой. Примеры: автокатализ; перекрестный катализ; ингибирование в проточных и периодических реакторах; системы, содержащие бромат и различные восстановители.
- Процессы, которые могут протекать по различным схемам в зависимости от ряда случайных факторов. Наличие сложных, разветвленных траекторий процесса. Примеры: прерывистая генерация волновых фронтов в проточных системах иодид-пероксидные системы; системы с зависимостью стехиометрии от изменяющихся в процессе параметров.
- Процессы, в которых не все управляющие параметры однозначно определены и сильно зависят от изменяющихся в процессе температуры, давления или концентрации. Примеры: термокинетические явления при гомогенном газофазном окислении в проточных реакторах: окисление ацетальдегидов в проточных реакторах; окисление углеводородов. Подобные реакционно-диффузионные процессы могут протекать по нескольким характерным механизмам (рис. 1).
Основные типы возможных систем:
- Самосопряженные реакции, в которых индуктор-конечный продукт.
- Цепные реакции, если в исходной смеси присутствует ингибитор. По мере его расходования скорость обрыва цепей уменьшается, возрастает концентрация активных центров, и реакция ускоряется.
- Цепные разветвленные реакции в условиях нестационарного режима. Самоускорение вызывается увеличением концентрации активных центров в ходе реакции из-за преобладания разветвления цепей над их обрывом.
- Окисление органических соединений вследствие образования промежуточных веществ (пероксидов, альдегидов), вызывающих вырожденное разветвление цепей.
- Радикальная полимеризация при глубоких степенях превращения, когда резко возрастает вязкость среды, замедляется рекомбинация макрорадикалов и вследствие этого увеличивается длина кинетической цепи.
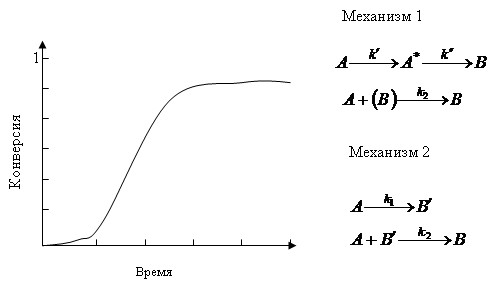
Рис. 1. Зависимость конверсии от времени по двум механизмам
- Реакции с участием твердых тел, которые локализуются на поверхности раздела твердых фаз реагента и продукта.
- Сильно экзотермические реакции, когда в условиях нескомпенсированного теплоотвода начинается саморазогрев системы или поверхности катализатора (для каталитических процессов).
Примеры реакционных систем:
- Окисление щавелевой кислоты перманганатом калия;
- Хлорит-иодитные системы;
- Бромат-иодитные системы;
- Хлорит-тиосульфатные системы.
2. Особенности расчета кинетики процесса при неполной информации на примере производства гуминовых веществ
О всех группах гуминовых веществ (ГВ) обычно говорят во множественном числе (например, гуминовые кислоты), поскольку их состав и свойства меняются в зависимости от источника ГВ, но даже в препаратах, полученных из одного источника (одного типа почв, торфа, угля), они неоднородны, полидисперсны и представлены большим набором сходных по строению, но неидентичных молекул [6, 7] .
Все ГВ образуются в результате постмортального (посмертного) превращения органических остатков. Превращение органических остатков в ГВ получило название процесса гумификации. Он идет вне живых организмов как с их участием, так и путем чисто химических реакций окисления, восстановления, гидролиза, конденсации и др.
В отличие от живой клетки, в которой синтез биополимеров осуществляется в соответствии с генетическим кодом, в процессе гумификации нет какой-либо установленной программы. Поэтому могут возникать любые соединения, как более простые, так и более сложные, чем исходные биомолекулы. Образующиеся продукты вновь подвергаются реакциям синтеза или разложения, и такой процесс идет практически беспрерывно. В результате многочисленных реакций в природных телах накапливаются только наиболее устойчивые соединения, существующие более длительное время, чем лабильные вещества.
Содержание различных химических элементов в веществах хорошо изучено [6]. В зависимости от происхождения и источника ГВ содержание углерода в массовых долях колеблется от 40 до 60 %. Азот есть всегда, но его мало - 3-5 %. Водорода обычно содержится 3-6
%, а кислорода - 33-37%. Обязательно входят сера - до 0,7-1,2 % и фосфор - до 0,5 %. Всегда есть разные металлы, хотя пока трудно сказать, обязательны ли они для ГВ или просто являются примесью, поскольку очистить ГВ нелегко.
Найдены мелкокристаллический кварц SiO2, мелкокристаллический гетит FeOOH в препаратах ГВ, что приходится признать явными примесями. Кислород обычно находят по разности, поэтому сумма четырех элементов в таблице равна 100%. Фульвокислоты отличаются резко пониженным содержанием углерода (до 40 мас. %) и соответственно более высоким содержанием кислорода, они более окислены, чем другие ГВ.
Гуминовые вещества разнообразны в природе, о чем можно судить не только по элементному составу, но и по набору функциональных групп и другим свойствам. Любые ГВ содержат большой набор функциональных групп, они полифункциональны. Их молекулы содержат карбоксильные группы -СООН, фенольные -ОН, хинонные =С=О, аминогруппы -NH2 и др. Их количество велико и они распределены неравномерно по молекулам различного размера. Молекулы одного размера могут различаться по содержанию функциональных групп.
Состав гуминовых веществ различаются по количеству входящих в их состав остатков аминокислот (всего их 17-20), по количеству углеводных остатков и характеру их расположения. Большую роль играют группы -NН2. Разнообразие кислых функциональных групп столь велико, что Л.И. Глебко предложила их не идентифицировать, а лишь разделить в соответствии с кажущимися константами диссоциации, pK = - lg K, где K - константа диссоциации.
Существует два способа дробления больших молекул на составные части: 1) относительно мягкий - гидролиз растворами кислот или щелочей, 2) жесткий - окисление ГВ растворами марганцевокислого калия или окисью меди. При гидролизе в раствор переходят, отделившись от молекулы ГВ, низкомолекулярные фрагменты, аминосахара и моносахариды. Аминокислот бывает от 17 до 22, все они альфа-аминокислоты, те же, что есть в растениях, бактериальной плазме, причем примерно в тех же соотношениях.
Гуминовые вещества в своем составе содержат моносахариды: глюкоза, галактоза, манноза, ксилоза, арабиноза, рибоза, рамноза, фукоза, фруктоза и др. Всего они могут составлять до 25% массы ГВ, а в составе моносахаридов на долю глюкозы приходится до 20%. Продуктами окисления ГВ главным образом являются бензолполикарбоновые кислоты. В их составе преобладают 1,2,4-бензолтрикарбоновая (тримеллитовая) - С6Н3(СООН)3, 1,2,4,5- бензолтетракарбоновая (пиромеллитовая) С6Н2(СООН)4 и пентакарбоновая кислота С6Н(СООН)5. Можно сделать следующие выводы:
- В гуминовых веществах белки и углеводы растительных тканей могут стать источниками аминокислот и моносахаридов, тогда обнаружение шестичленных бензоидных циклов указывает на лигнин и флавоноиды как исходные продукты. Все вещества гидролизатов ГВ почти полностью установлены, но их сочетание и расположение в молекулах ГВ пока остаются неизвестными.
- Все полученные данные позволяют говорить о нерегулярности структур молекул ГВ и возможном разнообразии в них взаимного расположения и сочетания известных фрагментов.
- Гуминовые вещества считают высокомолекулярными соединениями, однако дискуссии о размерах молекулярных масс (ММ) продолжаются до последнего времени.
Вывод. Получение гуминовых веществ производится в условиях неполноты информации о постадийном механизме процесса.
Физико-химический процесс в реакторе (рис. 2) протекает в условиях неполноты информации о постадийной кинетике по механизму 1:
A k A k B
A Bk2 B
(1)
Здесь A – уголь, переходящий в реакции с аммиаком и щелочью в экстрагированную форму A .
Затем происходит образование гумата B .
 dB
dB
dt
f1 A, (2)
С учетом автокатализа и частичной обратимости процесса превращения в реакторе представим кинетическое уравнение для скорости превращения вещества A в общем виде [5]:
 dA f dt 2
dA f dt 2
A, B. (3)
 1
1
2
3
Рис. 2. Схема производства гумата аммония 1 – мельница–активатор, 2 – реактор– смеситель, 3 – центрифуга
Определяем стационарные точки:
 где
где
0
A, B 0, B , (4)
f 0, B 0 . (5)
2
- В соответствии с предлагаемой методикой записываем кинетическое уравнение для продукта
B :
Процесс протекает при конкуренции двух факторов. Во-первых, присутствие вещества B в
системе может катализировать процесс превращения вещества A . Во-вторых, при достаточной скорости обратного превращения конверсия может уменьшаться. Если первый фактор превалирует, то скорость превращения вещества A является возрастающей функцией, как концентрации A , так и концентрации вещества B . Якобиан данной динамической системы:
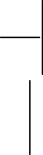
 f2 f2
f2 f2
J
A 0
f1
A 0
B 0 . (6)
0
В соответствии с механизмом реакции смысл элементов якобиана:
 f 2
f 2
A
k2 ;
f2
 B
B
k
; f1 k . (7)
 A
A
- При массовом соотношении угля и раствора NaOH менее, чем 1 : 3 и в присутствии более, чем 10 % аммиака от массы сухого угля стадия перехода A A протекает необратимо
при константе k 2 102 1/с. В то же время при таких условиях стадия перехода A B
по мере возрастания концентрации гумата B переходит в полностью обратимую реакцию. Поэтому обратное превращение протекает достаточно интенсивно, и справедливо
мере возрастания концентрации гумата B переходит в полностью обратимую реакцию. Поэтому обратное превращение протекает достаточно интенсивно, и справедливо
 f1
f1
f2
0 . (8)
A 0 B 0
Для этого условия стационарная точка является седловой. Это означает, что процесс превращения в системе носит нестационарный, переходный характер. Поскольку стационарное состояние не устойчиво, то и не выполняются также условия существования периодического режима. Такой режим проведения процесса не рекомендуется.
Если при массовом соотношении угля и раствора NaOH 1 : 3 и более и в присутствии менее, чем 10 % аммиака от массы сухого угля, то стадия перехода
A A
по-прежнему
протекает необратимо при константе k 1.8 102 1/с. Теперь стадия перехода A B при
 возрастании концентрации гумата B протекает с преобладанием необратимой реакции. Таким образом, в этом случае выполняется условие:
возрастании концентрации гумата B протекает с преобладанием необратимой реакции. Таким образом, в этом случае выполняется условие:
 f1
f1
f2
0 , (9)
A 0 B 0
В этом случае тип стационарной точки является центром, и в подобной системе может возникать периодическое изменение концентрационного поля. На основании проведенного анализа были предложены следующие рекомендации по организации технологического процесса.
Для повышения технологичности способа и увеличения выхода гуматов аммония выделение гуматов рекомендуется проводить процесс в три стадии, на первой из которых обработку угля раствором аммиака ведут в мельнице-активаторе непрерывного действия - 1 при массовом соотношении твердой и жидкой фаз т : ж = 1 : 3 и в присутствии 8 % аммиака от массы сухого угля. После этого необходимо экстрагировать полученный продукт. Для этого к полученной суспензии необходимо добавить воду до достижения соотношения т : ж = 1 : 8 (по данным [7]) и проводить далее процесс экстракции в реакторе-смесителе -2 с интенсификацией физико- химических процессов в течение как минимум 15 мин.
Далее жидкую фазу предлагается отделять центрифугированием на центрифуге-3 непрерывного действия, а оставшуюся твердую фазу - остаточный уголь - дополнительно подвергать обработке на второй и третьей стадиях, на каждой из которых его измельчают в мельнице-активаторе, затем добавляют воду до достижения соотношения т : ж = 1 : 8 и проводят процессы экстракции и отделения жидкой фазы при тех же условиях, что и на первой стадии.
Для реализации данных методов нами разработаны алгоритмы, которые реализованы в программной оболочке Borland Delphi7.0.
Выводы
Разработана классификация процессов, для расчета которых целесообразно использование подходов, учитывающих неполноту исходной информации. Рассмотрен пример расчета химического реактора в технологической схеме получения низкобалластных и безбалластных гуматов аммония из бурого угля и рекомендации по использованию и внедрению результатов исследований. Применение этой методики позволит согласно нашим расчетам сократить расходы реагентов и уменьшить энергопотребление.
ЛИТЕРАТУРА
- Aronson D.G. Density-Dependent Interaction-Diffusion Systems, in Dynamics and Modelling of Reactrive Systems//Publ. Math. Res. Cent. Univ. Wis.Madison. – 1980. – Vol. 44. – P. 161.
- Эпштейн И., Орбан М. Галогенсодержащие колебательные системы в проточном реакторе //В сб. "Колебания и бегущие волны в химических системах", М.: Мир, 1988, С. 285-318.
- Мусабекова Л.М., Абдураимова Б.К., Оспанова А.О. Ефремов Г.И. Особенности моделирования режимов работы реакторов при неполной информации о процессе //Труды международной научно- практической конференции «Наука и образование на современном этапе.». Южно-Казахстанский Гуманитарный институт им. М. Сапарбаева. Шымкент. 2005.-Т1, с.119-124.
- Абдураимова Б.К., Мусабекова Л.М., Мырзахметова Б.Ш. Особенности расчета неравновесных процессов в хим. аппаратах с фазовыми превращениями// Доклады НАН РК.-2005.-№4.-С.81-85.
- Мусабекова Л.М., Юнусова А.А. Автоволновые режимы тепло – массопереноса в неизотермических трубчатых реакторах //Труды 6-го Минского международного форума по тепло- и массообмену - ММФ-2008.-Минск.-Т1.-С.350-351.
- Орлов Д.С. Гумусовые кислоты почв и общая теория гумификации. М.: Изд-во МГУ, 1990. 325 с.
- Горовая А.И., Орлов Д.С., Щербенко О.В. Гуминовые вещества. Киев: Наук. думка, 1995. 304 с.