Металлические черни металлов платиновой группы являются одним из традиционных типов нанодисперсных систем, которые функционируют как катализаторы и используются в форме активного компонента анодов и катодов электрохимических генераторов тока, а также являются основой металлизационных паст, используемых в производстве резисторов и конденсаторов. Задачей настоящей работы являлось изучение фазового состава, динамики межфазных взаимодействий, локализации и морфологии фазовых составляющих в Pt-чернях по Адамсу- Фрамптону на стадии окислительной плавки [1,2]. Окислительную плавку проводили в кварцевых ампулах диаметром 20 мм. Перемешивание расплава и контроль температуры проводились кварцевой трубочкой диаметром 4 мм с запаянной в ней Pt-Pt/Rh – термопарой. Отклонения от заданных температур реакции /250, 350, 400, 450, 500, 600, 700, 800, и 10000С/ не превышало ±100. Навески NaNO3 и H2PtCl6 марки х.ч. для получения слитков весом 5 г брались из расчета их полного взаимодействия. Продолжительность отжига сплавов при отмеченных температурах составляла 30 мин, после чего ампула с расплавом закаливалась в воде при 2000С. Слитки выкалывались из ампул и из них готовились металлографические шлифы и порошки дисперсностью 10 мкм для термо-, рентгено- и электронографического анализов, а также электонномикроскопических исследований на просвет. Термичские исследования взаимодействия NaNO3 и H2PtCl6 выполнены на дериватографе Q-1500D в атмосфере воздуха с записью ДТА, ДТГ и ТГ- кривых на образцах, приготовленных в виде механической смеси исходных порошков. Масса навески для ТГ составляла 500 мг, а для ДТА и ДТГ – 250 мг. Скорость линейного нагрева – 10 град/мин. Рентгеновские дифрактограммы полного спектра отражений получены на аппарате ДРОН-2,0 с использованием CoKα – излучения.
Данные дифференциально-термического и рентгенофазового анализов показывают, что взаимодействие NaNОз и H2PtCl6. 6H2O носит многостадийный характер. По литературным данным [1,2], исходные компоненты начинают претерпевать изменения при температурах 240— 300°С: H2PtCl6.6H2O разлагается на PtCl4, Н2О и НС1 при 2400С, а NaNОз расплавляется при 280 °С. На кривой ДТА в этом интервале температур наблюдается интенсивный экзоэффект,сопровождающийся потерей веса образца.
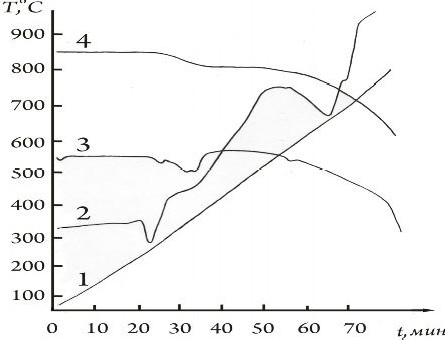
Исходные компоненты реагируют между собой с образованием Na2PtCl4 (ASTM 1-0083) и выделением HCl, что подтверждается данными рентгенофазового анализа образца, закаленного с температуры 250°С. При этой температуре также идентифицирована фаза исходного нитрата натрия (АSТМ7-271). Дальнейшее повышение температуры сопровождается уменьшением веса образца на фоне не ярко выраженного эндоэффекта в интервале 300—400°С. По данным работы [2], при 340° начинается выделение атомов хлора из PtCl4 с образованием PtCl2 (АSТМ 10-902), что и фиксируется на рентгенограмме образца, закаленного с температуры 350°С. При 4000 (закалка от этой температуры) состав фаз тот же, что и при 360°, но уменьшается интенсивность рефлексов Na2PtCl4 и PtCl2 и появляются слабые рефлексы NaCl (АSТМ 5-0628). При этом количество NaCl нарастает симбатно температуре.
Рис. 1. Термограмма NaNO3 + H2PtCl6 .
6H2O кривая нагревания, 2 – ДТА, 3 – ДТГ, 4 – ТГ
В интервале температур 400—500°С не происходит изменений фазового состава образца при постоянстве его веса. В согласии с литературными данными [2] при 5500С идет кристаллизация платины, сопровождающаяся интенсивным эндоэффектом и на рентгенограмме образца, закаленного с температуры 600°, появляются слабые рефлексы наиболее сильных отражений Pt (А5ТМ 4-0802) на фоне практически полных спектров NaNO3 и NaCl. Вслед за эндоэффектом наблюдается резкий экзоэффект с монотонным понижением веса образца (630 °С), обусловленный как выделением атомарного кислорода из нитрата натрия [1], так и окислением этим кислородом атомов платины с образованием недоокиси платины Рt304 .
На рентгенограмме образца, закаленного с температуры 650°, интенсивность пиков макси- мальна, но с повышением температуры она ослабевает, а при 800° появляются высокие четкие пики, сдвинутые в сторону малых углов, проиндицированные как NaPt3O4 (АSТМ 6-0534) — натриево-платиновая бронза. В результате дальнейшего нагревания рефлексы натриево- платиновой бронзы становятся очень слабыми (900°), а при 10000С - исчезают полностью и оста- ются только рефлексы, принадлежащие ГЦК решетке платины.

Рис. 2. Рентгенограммы плавов NaNO3 + H2PtCl6 . 6H2O, закаленных с температур: 1 - 250, 2 - 350,
3 - 400, 4 - 450, 5 - 500, 6 - 550, 7 - 600, 8 - 650,
9 - 700, 10 - 800, 11 - 900, 12 - 10000С
На рентгенограммах отсутствуют отражения PtO2 и ее полиморфных модификаций (АSТМ 2-613, 21-1283), как это ожидалось из [1, 2]. Одной из причин этого, возможно, является высокая дисперсность PtO2 в плавах (рентгеноаморфность). Неожиданный результат—появление отражений Рt3O4 в области 600— 700°С и NaPt3O4 при 800°С.
В свете работ Л.К.Шубочкина, результатов термического анализа и рентгенографических данных о фазовом составе не трудно идентифицировать фазовую принадлежность отдельных участков на металлографических шлифах. Следовательно, на основе полученных
экспериментальных результатов можно сделать заключение о том, что при взаимодействии NaNO3 и H2PtCl6 . 6H2O в интервале температур 350-5000С идет последовательная диссоциация PtCl6 до PtCl2 и металлической платины. В области 500-8150С в плаве накапливается NaxPt3O4 (0 ≤ х ≤ 1). Выше 8150С натрий-платиновая бронза разлагается с выделением Pt в форме нанодисперсных частиц с размерами от 2 до 50 нм. Диоксид платины во всех его структурных модификациях в продуктах окислительной плавки рентгенографически не обнаружен.
Обобщение результатов фазового анализа приведено в табл.1.
Таблица 1. Фазовый состав закаленных продуктов окислительной плавки NaNO3 + H2PtCl6 . 6H2O
|
№ |
Температура окислительной плавки, 0С |
Фазовый состав плавов |
|
1 |
250 |
Na2PtCl6, NaNO3 |
|
2 |
350 |
PtCl4, PtCl2, NaNO3, NaNO2 |
|
3 |
400 |
PtCl2 (следы), NaNO2 NaCl, Pt (следы) |
|
4 |
450 |
PtCl2 (следы) , NaNO3, NaCl, Pt (следы) |
|
5 |
500 |
NaNO3, NaCl, Pt (следы) |
|
6 |
550 |
NaNO3, NaCl, Pt (следы) |
|
7 |
600 |
NaCl, Pt3O4, Pt (количество растет) |
|
8 |
650 |
NaCl, Pt3O4, Pt |
|
9 |
700 |
NaCl, NaxPt3O4 (размытые рефлексы), Pt |
|
10 |
800 |
NaCl, NaxPt3O4 (интенсивные отражения), Pt |
|
11 |
900 |
NaCl, NaPt3O4 (очень слабые отражения), |
|
12 |
1000 |
NaCl, Pt (яркие рефлексы) |
ЛИТЕРАТУРА
- Андерсон Дж. Структура металлических катализаторов,— М.: Мир, 1979.— 402 с. 2. Miller O., Roy R.//J. Less – Common Metals. -1968 – V. 16, # 2. – P.129-146.
- Шубочкин Л.К., Гущин В.И. Варфоломеев М.Б., Шубочкина Е.Ф. //Ж. неорг. химии, 1973, т. 18, в. 6, с. 1613-1616.
- Шубочкин Л.К., Гущин В.И. Варфоломеев М.Б., Барановский И.Б. // Ж. неорг. химии, 1974, т. 19, в. 1, с. 139-145.