Разработка и внедрение новых технологий переработки золотосодержащего полиметаллического сырья продиктована современными требованиями к охране окружающей среды, а также тем, что разработка эффективной технологии позволит увеличить объемы добычи благородных металлов.
Во многих месторождениях золотосодержащих руд сосредоточено значительное количество мышьяка, являющегося вреднойпримесью.
Вскрытие золота, субдиспергированного в сульфидах, окислительным обжигом при переработке богатых мышьяком сульфидных концентратов влечет за собой загрязнение окружающей среды вредными оксидами мышьяка и потери ценногометалла.Главнымиколлекторамизолотавсульфидныхконцентратахявляютсяпиритиарсенопирит.
Золотосодержащие сульфидные концентраты вскрываются пиро- и гидрометаллургическими методами. Существенным недостатком первых является сложность обеспечения охраны окружающей среды от загрязнения токсичными соединения мышьяка и серы. Для их улавливания используются сложные и громоздкие системы. Перспективными представляются гидрометаллургические методы, позволяющие вывести из процесса токсичные соединения мышьяка в виде малорастворимых арсенатов железа и кальция.
Наиболее эффективным реагентом для окисления сульфидов металлов до сульфатов и вскрытия золота следует считать азотную кислоту. Благодаря высокому тепловому эффекту реакции окисления сульфидов азотной кислотой создаются условия для нагревания пульп до желаемых температур без дополнительного расхода тепла. Процесс окисления сульфидов с образованием в водных растворах в присутствии азотной кислоты идет значительно быстрее и полнее, чем при использовании других реагентов; кроме того, не выделяется арсин - наиболее ядовитое соединение мышьяка. Азотная кислота может регенерироваться из отходящих нитрозных газов и возвращается для повторного использования в процесс. Использование же дополнительно в качестве сильнейшего окислителя - озона позволяет резко интенсифицировать процесс извлечения золота в товарный золотосодержащий раствор и при этом на 20-25% снизить расход азотной кислоты идущей на вскрытие золота из полиметаллического сырья.
В настоящее время ведутся разработки по применению хлорных методов переработки материалов, содержащих благородные металлы. Характерной особенностью хлоридных процессов является их экологичность, а также возможность селективно выделить металл без высоких капитальных затрат. Важнейшим условием в достижении высокого извлечения золота в раствор и сохранения его в растворенном состоянии в процессе гидрохлорирования является отсутствие в исходном сырье восстановителей золота. К их числу в золотосодержащих концентратах относятся соединения двухвалентного железа, восстанавливающее действие которого можно устранить путем окисления хлором в процессе гидрохлорирования. Однако в этом случае расход хлора составляет значительную величину. При выщелачивании концентрата азотной кислотой железо полностью переходит в раствор и
кек таким образом, пригоден для осуществления процесса гидрохлорирования 1,2.
Нами создана специальная установка для азотнокислотного разложения сульфидных концентратов, обеспечивающая интенсификацию процесса выщелачивания и предотвращения выброса нитрозных газов в атмосферу.
Это достигается ионизацией газовой фазы в специальной ионизационной камере.
На рис. 1 схематически изображена разработанная нами установка и разрез по А − А (рис.
1).
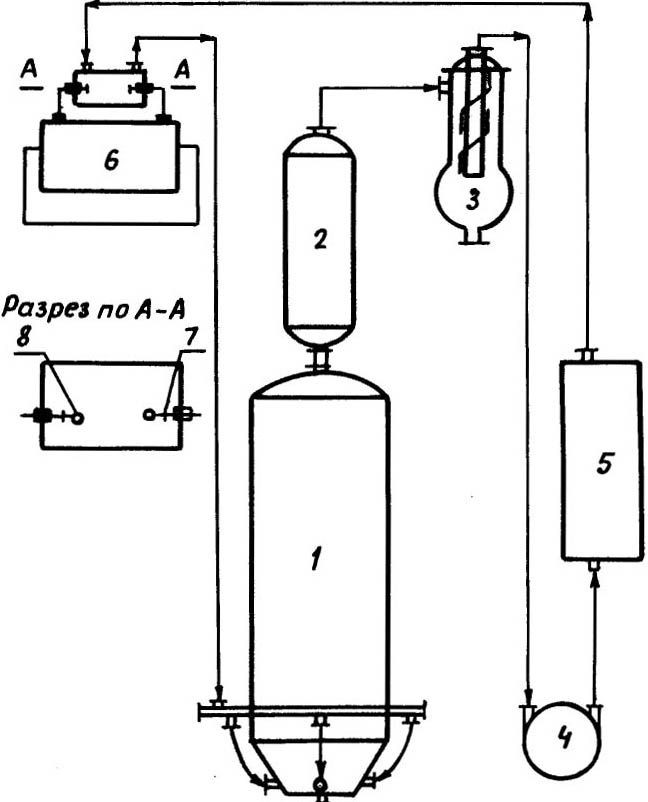
Рис. 1. Установка для азотнокислотного выщелачивания 1 − реактор; 2 − холодильник; 3 − каплеотбойник; 4 − газодувка; 5 − ресивер; 6 − ионизирующее устройство;
7 − разрядные электроды; 8 − патрубки.
Работа установки заключается в следующем: замкнутая система сначала заполняется кислородом (воздухом) до заданного давления, а затем при работающей газодувке в реактор заканчивается пульпа с заданными плотностью и температурой. Выделяющиеся в процессе выщелачивания нитрозные газы в смеси с кислородом циркулируют по замкнутому циклу. Циркулирующий газ охлаждается в холодильнике, осушается в каплеотбойнике, а затем с помощью газодувки сжимается в ресивере и после этого поступает в камеру ионизации. Здесь он, проходя между разрядными электродами, под действием разряда подвергается ионизации, в результате которой оксиды азота окисляются до диоксида, которые при последующем контакте с пульпой в реакторе образуют азотную кислоту, которая интенсивно взаимодействует с сульфидным концентратом.
Разработанная установка способствует интенсификации выщелачивания и позволяет более полно использовать азотную кислоту; процесс осуществляется при атмосферном давлении.
Окисленные кислород, оксиды азота (II) до NO2 вместе с конденсированными водяными парами образуют азотную кислоту, которая вновь вступает во взаимодействие с сульфидами концентрата.
Опыты проводили следующим образом. В первую ячейку загружали навеску концентрата, заливали выщелачивающий раствор, продували ячейки кислородом, тщательно герметизировали, включали нагрев нижней части ячеек и охлаждение верхней части и перемешивание. Нагрев осуществляли термостатированием с точностью 0,5оС, перемешивание вели при помощи магнитной мешалки. Процесс вели в течение 4-х ч, изменяя отношение Ж:Т, количество азотной кислоты и температуру. Во всех опытах в ячейку загружали 20 г концентрата. Кислород поступал из газометра автоматически, расход которого измеряли по градуировочной шкале.
Показано, что при всех условиях проведения опытов с использованием кислорода, окисление азота (II) до (IV) протекает с высокой скоростью, при этом все газообразные продукты реакции растворяются в жидкой фазе и наблюдается только расход кислорода. По окончании опытов отключали подачу кислорода, измеряли его расход, ячейки разгерметизировывали, пульпу отфильтровывали и определяли содержание металлов в жидкой и твердой фазах, концентрацию азотной и серной кислот, а также степень вскрытия концентрата.
Основная масса кека представлена пустой породой, содержание золота составляет 50 г/т. Кек указанного состава подвергался гидрохлорированию в лабораторном термостатированном реакторе емкостью 0,25 л изготовленного из стекла. Реактор снабжен механической мешалкой. Контакт кека с газообразным хлором осуществлялся в реакторе путем продувки хлора через водную пульпу при одновременном механическом ее перемешивании. Количество хлора, подаваемого в реактор, контролировалось реометром. Хлор подавался из ресивера через осушительную систему, состоящую из склянок с хлористым кальцием и серной кислотой. Для выбора оптимального технологического режима гидрохлорирования было изучено влияние на извлечение золота в раствор основных технологических параметров процесса в широком
интервале: плотности пульпы от Ж:Т=4:1 до 1:1, количестве вводимого в пульпу хлора от 0,1 до 5 г на 10 г материала, при длительности контакта хлора с пульпой от 0,5 до 3,0 ч (табл. 1).
В результате исследования установлена возможность осуществления процесса гидрохлорирования с извлечением золота в раствор 90-93% от исходного содержания в концентрате при остаточной концентрации золота в кеке 5,0-4,6 г/т. Эти результаты были достигнуты при гидрохлорировании в следующих оптимальных условиях: плотность пульпы Ж:Т=3:1, длительность контакта пульпы с хлором − 2 ч, в течение которого в пульпу было введено на 10 г материала 2,5 г хлора при расходе хлора 4 л/ч в раствор 0,1-0,5 н соляной кислоты при температуре 70-90 °С.
Таблица 1. Влияние основных параметров на результат извлечения золота в раствор при гидрохлорировании
|
№ п/п |
Кол-во введенного в пульпу хлора г/кг концентрата |
Длительность контакта хлора с пульпой, ч |
Плотность пульпы, Ж:Т |
Содержание золота в кеках, г/т |
Извлечение золота в раствор, % |
|
1 |
500 |
0,5 |
3:1 |
3,5 |
90 |
|
2,0 |
2,2 |
96,2 |
|||
|
3,0 |
3,0 |
94,0 |
|||
|
2 |
250 |
2,0 |
3:1 |
2,0 |
97,0 |
|
2:1 |
2,2 |
96,0 |
|||
|
3 |
150 |
2,0 |
3:1 |
8,0 |
83,0 |
|
4 |
100 |
2,0 |
3:1 |
8,2 |
83,0 |
|
5 |
50 |
2,0 |
3:1 |
20,0 |
50,0 |
Также был исследован способ хлоридовозгонки. Кек гранулировали с добавлением углерода 10% от веса концентрата. Гранулы сушили и коксовали при температуре 800 °С.
Исследования проводили в интервале температур 600-1000 °С, продолжительности 30-90 мин и расхода хлоре 15 л/ч. Лучший результат по извлечению золота в хлоридовозгоны получается при температуре 650-900°С, повышение температуры до 1000 °С снижает извлечение золота за счет спекания гранул.
Извлечение золота в возгоны составило 92-95%, что несколько выше, чем при гидрохлорировании. Содержание золота в огарке составило 4,5 г/т. Парогазовая смесь выводилась из реактора через штуцер, проходила через обогреваемый газоход и улавливалась в системе конденсации, состоящей из емкости, заполненной 1% соляной кислотой. Золотосодержащие растворы могут быть поданы либо на экстракционное, либо на сорбционное выделение золота.
Сорбционное извлечение золота из растворов гидрохлорирования осуществлялось на полистиролдисульфидной смоле (ПДС). Для определения емкости смолы в статистических условиях был использован раствор золотохлористоводородной кислоты, содержащий 0,8-1,0 г-экв. НС1 и 1,8 г/дм3 золота. Навеска смолы – З г, объем раствора − 0,1 дм3. Смолу поместили в коническую колбу и заливали золотосодержащим раствором указанной концентрации. Время контакта 8 ч при перемешивании. Раствор отделяли от смолы и анализировали на остаточное содержание золота. В колбу со смолой заливали новую порцию раствора. После 4-х ступеней сорбции емкость смолы составила 210 мг/т смолы.
Полидисульфидная смола является селективной по отношению к золоту и если в растворе присутствуют примеси, такие как медь, железо, свинец, мышьяк, цинк, сурьма, селен, теллур и др., то они не сорбируются. Емкость ПДС на порядок выше, чем емкость традиционной смолы АМ-2Б. При дальнейшем насыщении смолы начинает выделяться элементарное золото, что связано с присутствием в смоле серы, которая всплывает на поверхность раствора в виде светложелтых чешуек. Из этого факта следует вывод, что полистиролсульфидную смолу при эксплуатации не следует насыщать выше 200 мг/г.
Десорбцию насыщенной смолы вели сернокислотным тиомочевинным раствором, содержащим 30 г/дм3 тиомочевины и 90 г/дм3 серной кислоты. Получен десорбат, пригодный для электролитического осаждения катодного золота.
ЛИТЕРАТУРА
- Лодейщиков В.В. Технология извлечения золота и серебра из упорных руд. – Иркутск: Иргиридемет, 1999. – Т. I. – 342 с. – Т. II. – 786 с.
- Мартынов В.И., Страцева Г.Ф. Опыт складирования отвальных кеков, содержащих мышьяк //Известия ВУЗов. Цветная металлургия. – 1983. − №13. – С. 28-30.