Введение
В рудах Бозшакольского месторождения медь представлена в основном атакамитом CuCl2·3Cu(OH)2, в меньших количествах присутствует малахит – CuCO3·Cu(OH)2. В сульфидной форме медь в руде не представлена. Содержание меди в руде колеблется в пределах 0,68-0,75%. Переработка руды такого типа пирометаллургической технологией, включающей флотационной обогащение с последующей плавкой концентрата невозможна [1].
Кучное выщелачивание медных руд сернокислыми растворами с рН от 1 до 3,5 успешно применяется на многих предприятиях Южной Америки, США, Африки. Исследования [2] по выщелачиванию руд Бозшакольского месторождения показали, что скорость процесса лимитируется диффузией. Однако, в работе не рассмотрена кинетика растворения отдельных составляющих исходной руды. Целью работы являлось изучение кинетических закономерностей выщелачивания основного медного минерала Бозшакольской руды – атакамита растворами серной кислоты.
Для кинетических исследований зерна атакамита, вкрапленные в основную породу Бозшакольской руды, выбирались вручную, дробились и измельчались до фракции крупностью - 0,104+0,074 мм. Удельная поверхность измельченного атакамита - 2,58 м2/г. Исходный атакамит (СuСl2(ОН)з) имел состав в %: Сu 57,72; Сl2 - 16,02; Н2О - 12,7; прочие примеси 2,51 (СаО - 1,69; Fе2О3 - 0,52). Спектральным анализом Мg, Рb, Zn не обнаружены.
Удельная поверхность атакамита определялась методом адсорбции.
Все рабочие растворы готовили на дистилляте из реактивов марки "х.ч." или особой чистоты. Состав минерала атакамита контролировали химическим, спектральным и рентгенофазовым методами анализов, а также сравнивали с физико-химическими характеристиками искусственно приготовленного атакамита.
Изучалось влияние концентрации серной кислоты, температуры и продолжительности процесса, а также интенсивности перемешивания на скорость растворения.
Результаты
Исследованиями [2] установлено, что при увеличении концентрации серной кислоты в выщелачивающем растворе с 5 до 10 г/дм3 скорость растворения атакамита увеличивается в 2 раза. Максимальная скорость процесса растворения отмечается при концентрации кислоты 100 г/дм3. Дальнейшее увеличение концентрации кислоты приводит к снижению скорости растворения. Нами принята к исследованию кислота концентрацией 0,05, 0,005 и 0,0005 М, что соответствует 4,9, 0,49 и 0,049 г/дм3.
 Навеску исследуемого минерала (20 мг) помещали в термостатированную колбу емкостью 150 мл, доливали 50 мл раствора серной кислоты заданной концентрации. Герметично закрывали колбу и включали мешалку. Скорость вращения мешалки - 140-150 оборотов в минуту. После окончания опыта раствор отфильтровывали, промывали фильтр водой, из фильтрата отбирали аликвотную часть 25 мл, затем определяли содержание меди атомно-адсорбционным методом. Температура поддерживалась с точностью ±0,1 °С. Значения константы скорости (К) изучаемой реакции рассчитывали по уравнению Щукарева-Доливо-Добровольского.
Навеску исследуемого минерала (20 мг) помещали в термостатированную колбу емкостью 150 мл, доливали 50 мл раствора серной кислоты заданной концентрации. Герметично закрывали колбу и включали мешалку. Скорость вращения мешалки - 140-150 оборотов в минуту. После окончания опыта раствор отфильтровывали, промывали фильтр водой, из фильтрата отбирали аликвотную часть 25 мл, затем определяли содержание меди атомно-адсорбционным методом. Температура поддерживалась с точностью ±0,1 °С. Значения константы скорости (К) изучаемой реакции рассчитывали по уравнению Щукарева-Доливо-Добровольского.
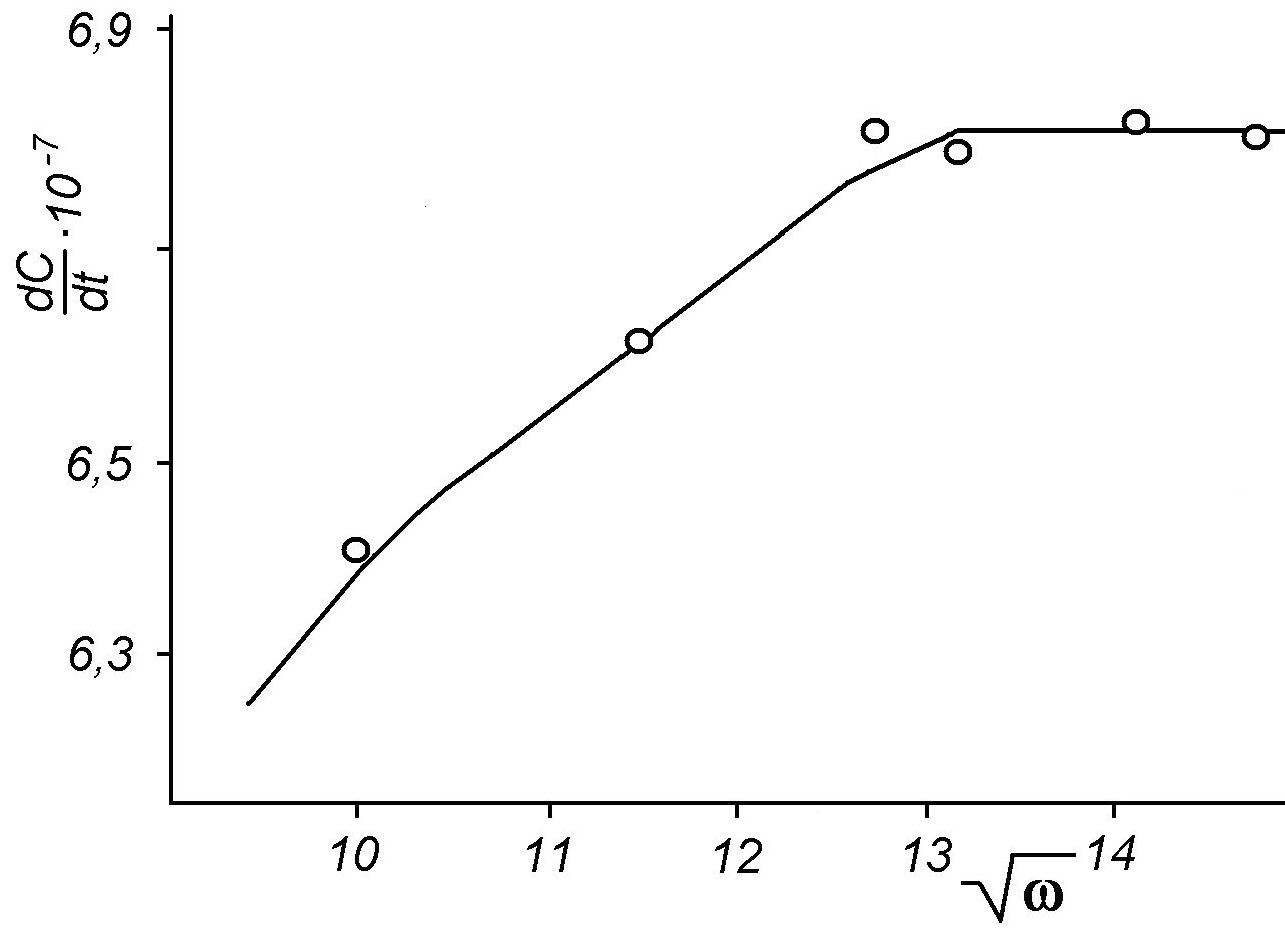
Рис. 1. Зависимость скорости растворения атакамита от скорости вращения мешалки
Для определения роли внешней диффузии, как составляющей скорости процесса выщелачивания, в первую очередь было изучено влияние скорости перемешивания на скорость процесса. Скорость мешалки изменялась от 50 до 200 об/мин. На рис. 1 представлена зависимость скорости перехода меди в раствор от числа оборотов мешалки.
 Как видно, скорость растворения возрастает при увеличении числа оборотов мешалки и достигает максимального значения - 6,8 г·см-2·сек-1 при =13. Дальнейшее повышение скорости вращения мешалки на скорость перехода меди в раствор влияния не оказывает. Это говорит о том, что при этой скорости вращения мешалки скорость растворения не зависит от внешних
Как видно, скорость растворения возрастает при увеличении числа оборотов мешалки и достигает максимального значения - 6,8 г·см-2·сек-1 при =13. Дальнейшее повышение скорости вращения мешалки на скорость перехода меди в раствор влияния не оказывает. Это говорит о том, что при этой скорости вращения мешалки скорость растворения не зависит от внешних
диффузионных факторов. Дальнейшие исследования проводились при скорости вращения мешалки, исключающей влияние внешних диффузионных факторов.
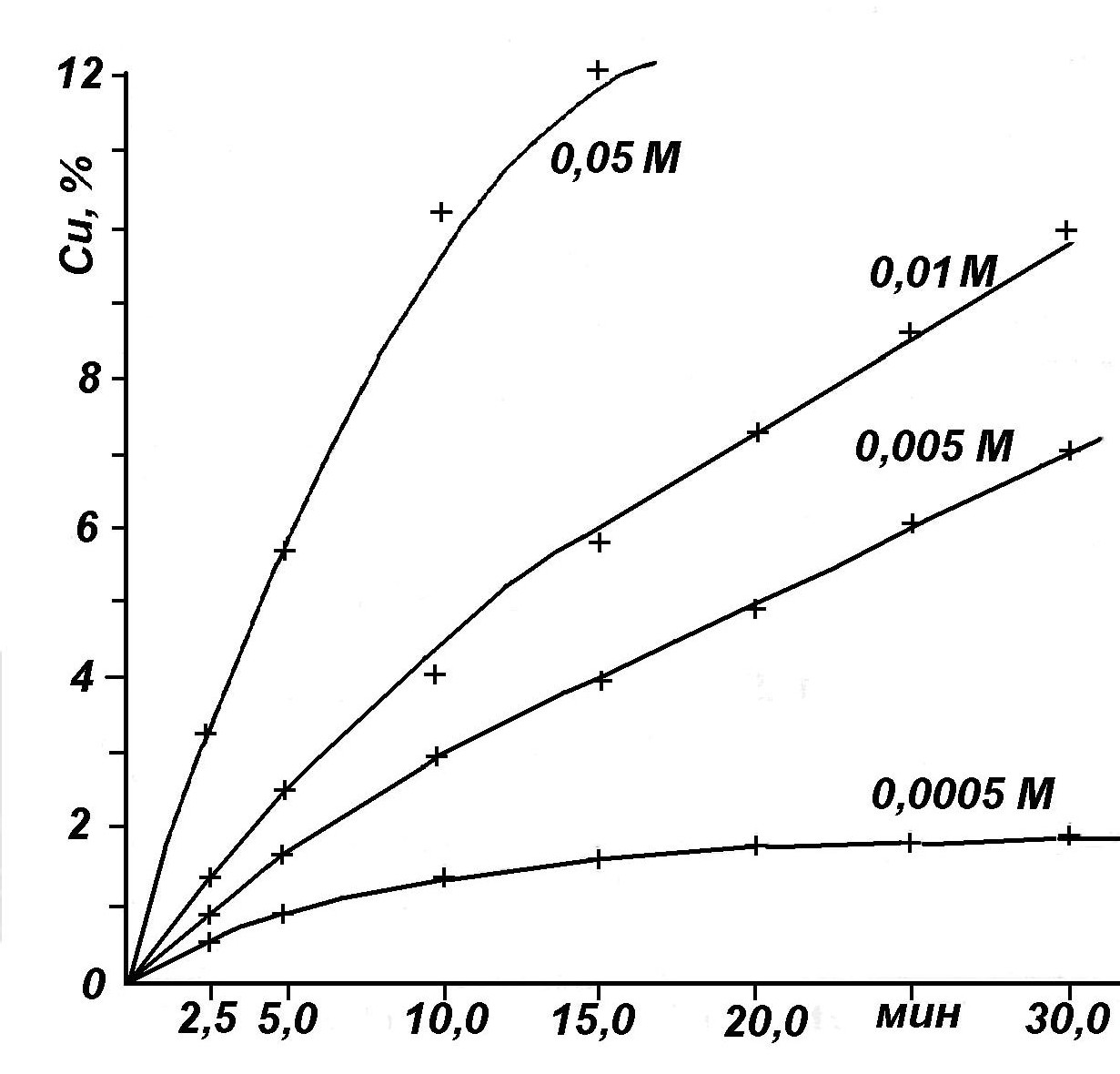
На рис. 2 представлены кинетические кривые взаимодействия атакамита с растворами серной кислоты различной концентрации в зависимости от продолжительности перемешивания. Концентрация растворов серной кислоты взята заниженной по сравнению с технологической (200 г/л или 2 моль/л) для более точных кинетических измерений. Ход кинетических кривых взаимодействия атакамита при всех концентрациях серной кислоты при продолжительности перемешивания до 15 мин носит линейный характер. Это указывает на то, что поверхность атакамита на данном участке остается свободной от продуктов реакции. При дальнейшем перемешивании выше 20 мин взаимодействие постепенно затухает. Химизм взаимодействия атакамита с серной кислотой можно представить следующим уравнением:
 СuСl2·ЗСu(ОН)2 + 4Н2SO4 = 4СuSO4 + 2НСl + 6Н2O
СuСl2·ЗСu(ОН)2 + 4Н2SO4 = 4СuSO4 + 2НСl + 6Н2O
Рис.2. Кинетические кривые взаимодействия атакамита в зависимости от концентрации Н2SО4 (моль)
Как видно, увеличение концентрации кислоты приводит к возрастанию количества меди, перешедшей в раствор. Данные для расчета константы скорости, порядка реакции и удельной скорости представлены в табл.1.
Таблица 1. Результаты выщелачивания атакамита в зависимости от концентрации серной кислоты и продолжительности перемешивания
|
Концентрация H2SO4, М |
Время перемешивания, с |
Извлечение меди, Сτ % |
Концентрация меди в растворе, C·10 -5моль/л |
|
0,0005 |
150 |
0,42 |
3,8 |
|
300 |
0,83 |
7,5 |
|
|
600 |
1,25 |
11,3 |
|
|
0,005 |
150 |
0,62 |
5,6 |
|
300 |
1,45 |
13,1 |
|
|
600 |
2,9 |
26,2 |
|
|
0,05 |
150 |
3,3 |
30,0 |
|
300 |
5,8 |
52,5 |
|
|
600 |
9,2 |
82,5 |
Порядок реакции определялся графически по дифференциальному методу Вант-Гоффа. В соответствии с этим методом скорость реакции в изотермических условиях связана с концентрацией реагентов уравнением:
V=kСn,
где n – порядок реакции. Прологарифмируя уравнение, получим:
lgV=lgk + nlgC0
В координатах lgV-lgC0 график зависимости будет представлен прямой линией, и угол наклона линии даст величину порядка реакции по отношению к веществу, концентрация которого меняется.
В табл. 2. приведены данные для построения этого графика.
Таблица. 2. Расчетные данные, отражающие зависимость lgC -1- lg C0.
|
C·10-5 |
|
V=C -1·10-6 |
lg(C -1) |
C0 |
lg C0 |
|
7,5 |
300 |
0,25 |
-6,602 |
0,0005 |
-3,301 |
|
13,1 |
300 |
0,44 |
-6,357 |
0,005 |
-2,301 |
|
52,5 |
300 |
1,75 |
-5,76 |
0,05 |
-1,301 |
На рис. 3 приведен график зависимости lgC -1- lg C0. По графику определяем, что тангенс угла наклона равен 0,7; т.е. порядок данной реакции на границе раздела фаз равен 0,7.
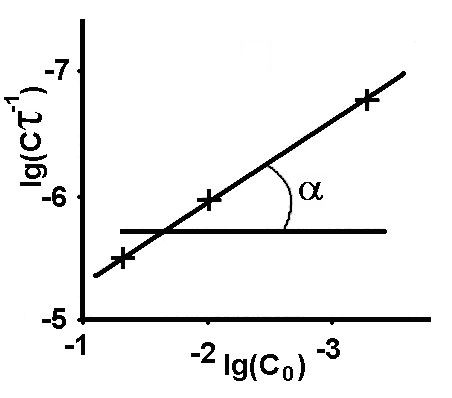 Рис. 3. График зависимости lgC -1- lg C0
Рис. 3. График зависимости lgC -1- lg C0
Константа скорости реакции рассчитывалась по уравнению Доливо-Добровольского В.В.:
 K C ,
K C ,
C0 A0
где К - константа скорости реакции;
С - количество металла, перешедшего из твердой фазы в раствор, моль/л;
А0 - удельная площадь реагирующей поверхности твердого вещества в момент времени ;
- порядок химической реакции на границе раздела фаз, в нашем случае =0,7;
- - стехиометрический коэффициент, указывающий число молей реагента, необходимое для растворения одного моля твердого вещества, σ = 4;
С0 - концентрация растворяющего реагента;
- время контакта твердой фазы с растворителем.
Удельная поверхность исходной пробы атакамита А0 2,58 м2/г;
Удельная поверхность навески весом 20 мг А0 = 516 (см2). Поскольку при расчете константы скорости необходимо использовать удельную поверхность нерастворившейся части навески, то
A (100- C )516 ,

где C в % взято из таблицы 3,
0 100
4 ,
С01 = 0,005М Н2SО4; С02 = 0,05М Н2SО4;
= 150; 300; 600 с;
= 0,7.
Тогда для 0,005 М раствора серной кислоты значения константы скорости будут равны:
K1 = 1,16 10-7с-1; К2 = 1,37 10-7с-1; К3 = 1,39 10-7с-1.
Для раствора 0,05 М серной кислоты:
К1 = 1,3 10-7с-1; К2 = 1,17 10-7с-1; К3 =1,0 10-7с-1.
Из полученных значений видно, что константа скорости с достаточной точностью остается постоянной и не зависит от концентрации реагента.
К = (1,19±0,19)10-7с-1.
Удельная скорость растворения определялась по уравнению:
(моль/см2с)
 C M A 0
C M A 0
Рассчитанные значения удельной скорости растворения при разных концентрациях серной кислоты приведены в табл. 3.
Таблица 3. Удельные скорости растворения атакамита
|
0,0005 М Н2SО4 |
0,005 М Н2SО4 |
0,05 М Н2SО4 |
|
W1=1,3 ·10-12 |
W1=2,72 ·10-12 |
W1=8,65 ·10-12 |
|
W1=0,7 ·10-12 |
W2=2,42 ·10-12 |
W2=6,0 · 10-12 |
Таким образом, с увеличением концентрации кислоты скорость растворения возрастает, а с увеличением продолжительности перемешивания уменьшается.
Значения кажущейся энергии активации Е процесса взаимодействия атакамита с серной кислотой найдены на основе экспериментальных данных по изучению влияния температуры на скорость процесса при 25, 35, 45, 55, 65, 75, 95°С. Для каждой температуры определяли количество меди, перешедшее из твердой фазы минерала в раствор за определенный промежуток времени и рассчитывали константы скорости растворения. Затем строился график зависимости логарифма константы скорости растворения от обратной температуры.
Величина кажущайся энергии активации процесса определялась графическим и расчетным способом по уравнению Аррениуса.
Результаты изучения влияния температуры на скорость процесса приведены в табл. 4 и на рис. 4. При изучении влияния температуры концентрация серной кислоты составляла 0,01 М; продолжительность перемешивания 10 мин (600 с).
Таблица. 4. Влияние температуры процесса на извлечение меди
|
T, °C |
T, К |
Извлечение меди, % |
Концентрация меди в растворе, моль/л 10-5 |
Константа скорости, 10-7с-1 |
|
25 |
298 |
4,2 |
37,5 |
1,26 |
|
35 |
308 |
6,6 |
60,0 |
2,07 |
|
45 |
318 |
8,8 |
78,75 |
2,78 |
|
55 |
328 |
10,8 |
97,5 |
3,53 |
|
65 |
338 |
12,5 |
112,5 |
4,15 |
|
75 |
348 |
15,0 |
135,0 |
5,12 |
|
85 |
358 |
17,5 |
157,5 |
6,16 |
|
95 |
368 |
20,0 |
180,0 |
7,26 |
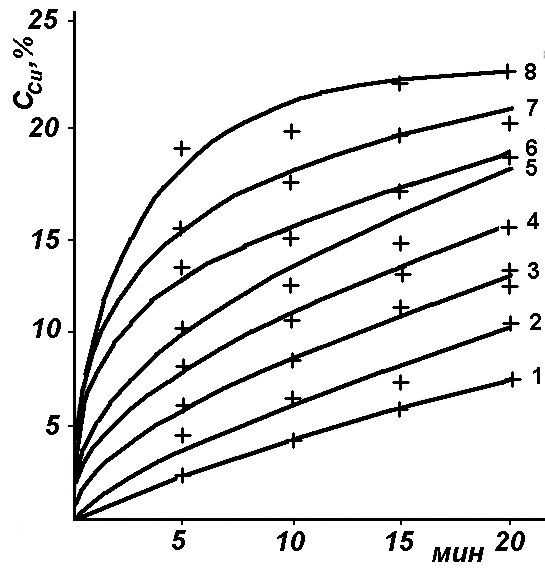
Рис. 4. Кинетические кривые взаимодействия атакамита С 0,01 М Н2SO4, (навеска 20 мг)
1 – 25 °С, 2 – 35 °С, 3 – 45 °С, 4 – 55 °С, 5 -65 °С,
6 – 75 °С, 7 – 85 °С, 8 - 95 °С
По данным табл. 4 построен график зависимости lgk – 1/T, по которому определена энергии активации (рис. 5).
Коэффициент наклона кривой tg = 1,125.
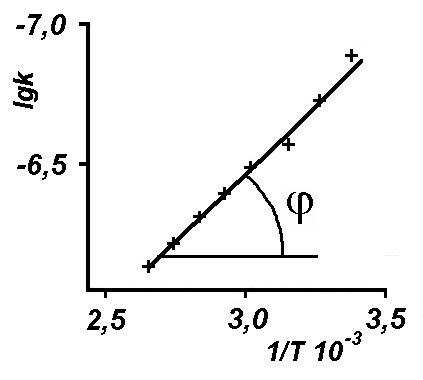
Рассчитанная графоаналитически энергия активации оказалась равной: Eакт = 2,3 R tg = 21,5 (21,5 кДж/моль);
Рис. 5. Зависимость lg k от 1/T
Расчетная по уравнению Аррениуса кажущаяся энергия активации также оказалась равной 21,5 кДж/моль.
Таким образом, величина кажущейся энергии активации процесса растворения атакамита в серной кислоте равна 21,5 кДж/моль, что указывает на протекание реакции в диффузионной области. Ранее нами было установлено, что внешнедиффузионные факторы не влияют на скорость процесса, т.е. можно заключить, что процесс растворения лимитируется скоростью внутренней диффузии.
ЛИТЕРАТУРА
- Медведев А.С. Выщелачивание и способы его интенсификации. М.: МИСиС, 2005 г, 240 с.
- Павличенко Г.А., Рогов Б.М., Пирмагомедов Д.А. Возможности геотехнологии в переработке медьсодержащих окисленных руд.//Цветные металлы. –№ 4. – 1992. – С. 17–20.