Салициловую кислоту получают в основном под давлением по методу Кольбе-Шмидта. Одним из больших недостатков данного способа является необходимость предварительного синтеза фенолята натрия, что связано со значительными технологическими трудностями: отгонка воды в вакууме и чрезвычайная гигроскопичность сухого фенолята натрия. Поэтому представляет интерес поиск более удобных альтернативных путей синтеза салициловой кислоты, исключающих использование фенолята натрия и этот недостаток устранен с помощью применения в качестве карбоксилирующего агента натриевой и калиевой солей этилугольной кислоты.
Следовательно, по более удобному методу нами получена кислота салициловая. В медицине применяется 1% раствор салициловой кислоты в 70% спирте под названием салициловый спирт как антисептическое средство. Нами исследованы антимикробная активность 1% раствора кислоты салициловой в различных концентрациях этилового спирта (40%, 50%, 60%, 70%, 80% и 90%) в целях определения влияние разных концентрации этилового спирта на антимикробную активность кислоты салициловой. В результате эксперимента доказано, что 1% раствор кислоты салициловой в различных концентрациях этилового спирта (40-90%) на соответствующие штаммы бактерии действует с одинаковой активностью независимо от концентрации этилового спирта (40%, 50%, 60%, 70%, 80% и 90%).
Такое действие кислоты связано с его растворимостью в спиртах различной концентрации и полным распадом молекулы кислоты салициловой на ионы. Таким образом, на основании проведения антимикробных исследований, доказана необходимость приготовления 1% спиртового раствора кислоты салициловой в 40% спирте так, как данный препарат дешевле и экономический выгодней для производства. Разработана технология получения нового композиционного препарата «Азисал», состоящий из азитромицина 0,25 г и кислоты салициловой 1,0 г в 60% этиловом спирте, аналогичным способом приготовлен в 60% этиловом спирте раствор азитромицина в различных концентрациях 0,25; 0,5; 0,75; 1,0% и установлены их антимикробные активности.
Сравнение их антимикробной активности показывает эффективность композиционного препарата под названием «Азисал». Органический синтез является наиболее важной и сложной частью современной фармацевтической науки. Продукция, выпускаемая химико-фармацевтическими предприятиями широко используется в самых различных областях медицины. Это синтетические химиотерапевтические лекарственные средства, витамины, гормоны, пищевые добавки и др. /1,2/. В последнее время синтез биологических активных веществ является чрезвычайно востребованным и имеет хорошие перспективы. В современной медицине остается актуальной проблема борьбы с гноеродной инфекцией, несмотря на большой арсенал антибактериальных средств. В структуре инфекционной патологии населения важное место занимают местные процессы различной локализации, вызываемые, преимущественно, условно патогенными микроорганизмами. Приоритет в лечении местных инфекционных процессов отдается антисептикам, противовоспалительным средствам и антибиотикам. Однако, большинство из них, не обладает одновременно рядом необходимых свойств как, например, широким спектром антимикробной активности избирательно подавлять синтез простагландинов и гистаминов в воспаленных клетках, нормализовать обменные процессы в тканях раны. Следовательно, создание композиционных лекарственных форм дает возможность обеспечить практическую медицину активными терапевтическими средствами, позволит производить одновременную терапию нескольких заболеваний,расширить спектр их применения и уменьшить дозировки лекарственных средств /3-5/. Перспективным направлением является создание комбинированных лекарственных средств на основе сочетания антисептиков, противовоспалительных средств и антибиотиков с препаратами различных фармакологических групп. Оптимальная комбинация антисептиков и препаратов различных фармакологических групп обеспечит синергизм и много направленность фармакологического действия и снижает побочные реакции последних. Существуют разнообразные методы и способы лечения ран, но ни один из них полностью не отвечает требованиям современной хирургии /6,7/. Практически самую важную группу лечебных средств составляют антисептические химиотерапевтические, противовоспалительные средства.
Учитывая, вышеизложенные, мы обратили внимание на препарат, так называемый салициловый спирт или 1% раствор кислоты салициловый в 70% спирте. Так как данный препарат широко используется как антисептик во многих странах и содержит в своем составе 1% кислоту салициловую. Это соединение содержится в коре ивы и его целебные свойства были известны с древности. Отвар коры ивы как жаропонижающее, обезболивающее противовоспалительное средство рекомендовал применять еще Гиппократ. Немецкий химик Бюхнер из коры ивы выделил вещество, которое назвал салицин (от латинского названия ивы - Salix). Чуть позже из салицина была получена чистая салициловая кислота и доказано, что она обладает лечебными свойствами. Кстати, кислота салициловая нашла свое место в медицине, ее раствор - салициловый спирт применяется при кожных воспалительных процессах и входит в состав многих косметических лосьонов.
Кислота салициловая впервые При синтезе кислоты салициловой по методу Кольбе- Шмидта реакция проходит при присутствии очень гигроскопического реактива фенолята натрия. Следовательно, присутствие воды в реакционной среде приводит к различным осложнениям, что уменьшает выход кислоты салициловой. Поэтому представляет интерес поиск более удобных альтернативных путей синтеза салициловой кислоты, исключающих использования фенолята натрия.
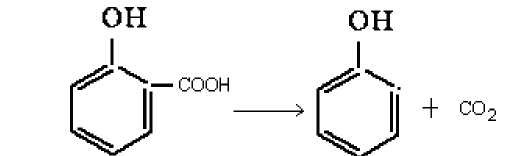
Ранее в литературе имелась только одна работа, содержащая лишь отрывочные сведения о применении в качестве карбоксилирующего агента натриевой и калиевой солей этилугольной кислоты в реакции карбоксилирования фенола. При медленном нагревании до 1750С смеси фенола с суспензией натрийэтилкарбоната в этаноле с одновременной отгонкой растворителя (до 1000С, 1атм) и части непрореагировавшего фенола (до 1700С, пониженное давление) и последующей обычной обработкой реакционной смеси (обработка водой, экстрагирование эфиром, подкисление водной фазы кислотой) получена получена Пирием в 1838 г. при окислении салицилового альдегида. Строение кислоты салициловой, как о- оксибензойной кислоты, установлено Кольбе в 1853году, наблюдавшего разложение ее при нагревании на фенол и двуокись углерода.
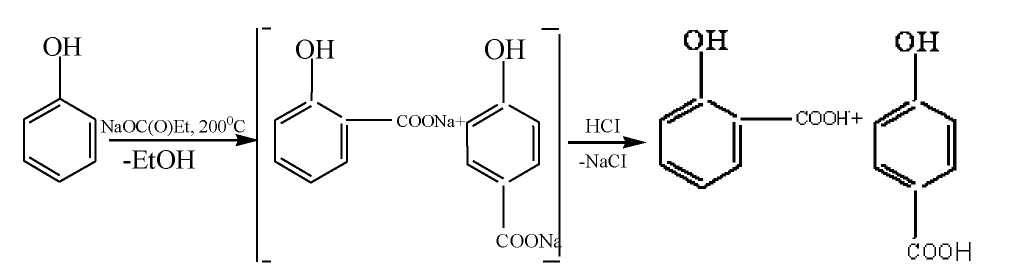
При проведении карбоксилирования фенола натрийэтилкарбонатом в условиях работы /7,8/ нам не удалось получить салициловую кислоту вследствие сильного осмоления (обугливания) реакционной смеси из-за окислительных процессов конденсации и уплотнения. Нами были исследованы некоторые закономерности протекания реакции карбоксилирования фенола натрийэтилкарбонатом и найдены оптимальные условия проведения процесса, исключающие вышеотмеченные нежелательные окислительные процессы. Установлено, что натриевая соль этилугольной кислоты может быть успешно применена в реакции карбоксилирования фенола и что карбоксилирование идет в основном в о- положение с образованием салициловой кислоты. Найдено, что реакцию необходимо проводить в инертной газовой среде (аргон, диоксид углерода), т.к. в воздушной среде из-за окислительных процессов конденсации выход салициловой кислоты не превышает 23-26%. Определено вляние на ход реакции температуры, давления и продолжительности реакции.
Оптимальными условиями проведения реакции карбоксилирования фенола натрийэтилкарбонатом оказались: Pai-Co2 = 1.0 MПа, T=2000C, t=6ч., при которых суммарный вход о- и п- изомеров оксибензойной кислоты составляет 87,5% (70,0% салициловой кислоты и 17,5% п-оксибензойной кислоты). Побочный продукт данного процесса – п-оксибензойная кислота, находит применение в качестве пищевого консерванта и для получения полимерных материалов и жидкокристаллических полиэфиров, обладающих высокой термостойкостью. Отработан лабораторнотехнологический регламент получения салициловой кислоты по разработанному новому способу получения в соответствии с требованиями действующей нормативнотехнической документации. Проработаны вопросы,связанные с определением наиболее оптимальной технологической схемы производства, требований к качеству исходного сырья, методикой разделения о- и п- изомеров оксибензойной кислоты, очисткой товарного продукта (салициловая кислота) и регенерацией непрореагировавшего фенола. На кафедре фармацевтической химии Казахского национального медицинского университета им. С. Д .Асфендиярова проведен полный фармакопейный анализ салициловой кислоты, полученной по новому способу. Испытания данного препарата на соответствие требованиям действующей нормативно-технической документации на кислоту салициловую включали следующие показатели качества: описание, растворимость, подлинность, температура плавления, прозрачность и цветность
раствора, хлориды, сульфаты, органические примеси, красящие вещества и фенол, оксидифенил, сульфатная зола и тяжелые металлы, потеря в массе при высушивании и количественные определения. Все испытания проводились по методикам ГФ XI издания. В результате проведенных испытаний установлено полное соответствие качественных показателей салициловой кислоты, полученной по новому способу, требованиям действующей ВФС на данный препарат. Высокие качественные показатели салициловой кислоты, полученной по новому способу, подтверждены также методами ИК-, ЯМР. Таким образом, разработан простой и удобный способ получения салициловой кислоты - карбоксилированием фенола натрийэтилкарбонатом. Найдены оптимальные условия проведения процесса (Р^сœ) = 1.0 MПа, Т=2000С, t=6ч.), при которых выход салициловой кислоты достигает 70,0% (88,0% в расчете на вступивший в реакцию фенол). Установлено полное соответствие качественных показателей салициловой кислоты, полученной по новому способу, требованиям действующей ВФС на данный препарат. Имеется в виду, что этот способ получения салициловой кислоты может быть использован на Павлодарском химико -фармацевтическом заводе. Структуру полученного продукта подтвердили ИК-, ПМР-спектрами, а также элементным анализом. ИК-спектры записаны на спектрофотометре ÙŔ-20(ГДР) в таблетках KBr, ПМР- спектры в 10%-ном растворе в ,M∞-d6 на приборе «Tesla»-BS 487 (60Мгц), сдвиги даны относительно ТМС. В ИК-спектре кислоты салициловой имеются полосы, соответствующие ароматическим связям (Ar) в области 700, 1610, 3020 см-1, С=0 связям (карбонильным) в области 1670 см-1, ОН-группе, в области 3240 см-1. Таблица. №1.
В карбоксильной группе кислоты салициловой водород находится в виде гидрида иона, поэтому не улавливается прибором «Tesla» BS467 (60Мгц). Сдвиги даны относительно ТМС. При снятии ПМР-спектра кислоты салициловой ароматические протоны проявляются в виде мультиплета (за счет не эквивалентности протонов из ароматического углерода) и находится в области 7,66 м.д. с площадью, соответствующей 4-м протонам. Гидроксильный протон ароматического углерода проявляются в виде синглета в области 11,7 м.д. с площадью соответствующей 1 м.д. протону. Таб.№1.
Таблица 1 - ИК-, ПМР-спектры салициловой кислоты .
|
№ соед. |
Частота валентных колебаний (γ), см-1 |
Величины хим. Сдвигов (σ), м.д. |
|||||
|
Ar |
Alk (CH3) |
C=O |
OH спирт. |
Ar |
Alk (CH3) |
OH спирт. |
|
|
¯¯ī |
700,1610, 3020 |
1670 |
3240 |
7,56 (м) |
11,7 (с) |
||
Кислоту салициловую применяют в медицинской практике как антисептическое, отвлекающее, раздражающее и кератолитическое средство в присыпках (2-5%) и (1-10%) мазях, пастах, спиртовых растворах (1-2%), при этом как растворитель во всех случаях берется 70% этиловый спирт и этот препарат называется салициловым спиртом.
Кислота салициловая по фармакологическим действиям относится к нестероидным противовоспалительным средствам, кроме того, к этой группе относятся следующие группы веществ:
- Кислота ацетилсалициловая.
- Производные антраниловой (орто-аминобензойной) кислоты - мефенамовая, кислота флуфенамовая.
- Производные пиразолона - бутадион, амидопирин.
- Производные индолуксусной кислоты -индометацин.
- Производные фенилуксусной кислоты - ортофен.
- Производные фенилпропионовой кислоты ибупрофен.
- Производные нефтилпропионовой кислоты напроксен. Нестероидные противовоспалительные средства оказывают противовоспалительное, анальгетическое, жаропонижающее действие.
Механизм противовоспалительного действия этих препаратов связывают их ингибирующим влиянием на фермент циклооксигеназы, необходимой для синтеза циклических эндопероксидов. В результате уменьшается продукция простогландинов. Это приводит к снижению таких проявлений воспаления, как гиперемия, отек, боль. Нестероидные воспалительные средства проявляют также анальгетическое и жаропонижающее действие. Анальгетический эффект, большинства рассматриваемых препаратов объясняется тем, что уменьшает сенсибилизирующие влияния простогландинов на чувствительные окончания, уменьшая эффект действия на них «медиаторов воспаления» (брадикинин) и других типов раздражителей. Кроме того, снижение под влиянием нестероидных средств интенсивности воспалительной реакции, также сопровождается уменьшением болевых ощущений. Жаропонижающее действие рассматриваемых препаратов также связывают с угнетением биосинтеза простогландинов Е1 и уменьшением их пирогенного влияния на центр теплорегуляции гипоталамуса.
Среди различных направлений современной клинической хирургии вопросы местного лечения гнойных ран занимают особое место. За рубежом и в нашей стране интенсивно ведется исследование и разработка новых лекарственных препаратов. Многие антимикробные препараты позволяют вылечивать различные заболевания, вызываемые бактериями /11/. В связи с этим, авторами /12,13/ для определения влияния различных концентрации спирта на антимикробную активность действующего вещества приготовлен 1% раствор кислоты салициловой в 6 образцах в этиловом спирте различных концентрации (40%, 50%, 60%, 70%, 80%, 90%). Технологический процесс производства 1% раствора кислоты салициловой в различных концентрациях спирта состоит из 2 технологических процессов, 3 вспомогательных работ и 3 УМО.
Лабораторные испытания на антимикробную активность препаратов кислоты салициловой проводились в соответствии с существующими методами по изучению обеззараживающей активности дезинфектантов (Методы испытания дезинфекционных средств для оценки их безопасности и эффективности. Москва, 1998г.; Методы бактериологического контроля антимикробной активности дезинфицирующих и антисептических средств. Астана, 2006г.) в качестве тест-штаммов использовались микроорганизмы, рекомендуемые для таких исследований: штаммы грамположительных бактерий Bacillus Subtilis, Staphilococcus aureus, штаммы граммы грамотрицательных Escherichia coli и дрожжевые грибы Candida albicans методом диффузии в агар (лунок). Результаты исследований антимикробной активности образцов раствора кислоты салициловой (1-6) показаны в таблице №2. и графике №1.
Таблица 2 - Результаты исследований антимикробной активности образцов раствора кислоты салициловой
|
№ п/п |
Штаммы |
1% раствор кислоты салициловой |
|||||
|
1-обр. |
2-обр. |
3-обр. |
4-обр. |
5-обр. |
6-обр. |
||
|
40%- ∞ирт |
50%- ∞ирт |
60%- ∞ирт |
70%- ∞ирт |
80%- ∞ирт |
90%- ∞ирт |
||
|
1 |
S.aureus |
13 ± 0,2 |
13 ± 0,2 |
13 ± 0,2 |
13 ± 0,2 |
13 ± 0,3 |
13 ± 0,2 ¯¯ |
|
2 |
Bacillus Subtilis |
13 ± 0,3 |
13 ± 0,3 |
13 ± 0,3 |
13 ± 0,3 |
13 ± 0,3 |
13 ± 0,3 |
|
3 |
Escherichia coli |
13 ± 0,2 |
13 ± 0,2 |
13 ± 0,2 |
13 ± 0,2 |
13 ± 0,2 |
13 ± 0,2 |
|
4 |
Candida albicans |
13 ± 0,2 |
13 ± 0,2 |
13 ± 0,2 |
13 ± 0,2 |
13 ± 0,2 |
13 ± 0,2 |
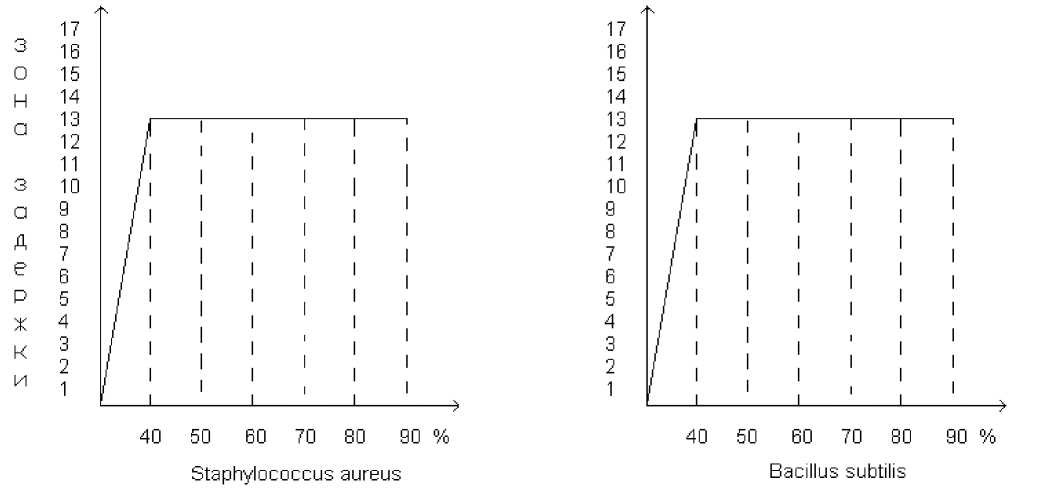
Таким образом, на основании биологических исследований спиртовых растворов кислоты салициловой и сравнивая данные таблицы №2 и графика №1 мы установили, что 1% раствор кислоты салициловой влияет на соответствующие штаммы бактерий с одинаковой активностью независимо от концентрации этилового спирта (40%, 50%, 60%, 70%, 80%, 90%). Это показано в таблице №2 и графике №1. Такое действие кислоты связано с его растворимостью в разбавленных спиртах и полным распадом молекулы кислоты салициловой на ионы. Кроме того, спирт и кислота салициловая обладают раздражающим, противовоспалительным действием, т.е. синергетическим действием. Таким образом, на основании проведения антимикробных исследований, доказана необходимость приготовления 1% раствора кислоты салициловой в 40% спирте в целях получения более дешевых препаратов, чем существующие, т.е., получение 1% раствора кислоты салициловой в 40% спирте был бы более экономичным.
В последнее время, когда фармацевтический рынок активно заполняется новыми лекарственными средствами, которые позволяются разными, в том числе ранее неизвестными производителями и поставщиками, качество поступающих лекарственных форм остаются сомнительными. Поэтому ориентация отечественных фармацевтических предприятий на позиции GMP обеспечивает разработку и производство эффективных, конкурентоспособных лекарственных форм и будут удовлетворять потребности охраны здоровья населения. Использование лекарственных средств в медицинской практике предусматривает применение эффективных лекарственных форм. Рационально подобранная ЛФ позволяет максимально оказывать лечебное действие препарата при минимальных побочных эффектах, значительно менять действия субстанции, т.е. ускорять или пролонгировать фармацевтический эффект, регулировать всасывание и выведение, аллергизирующие действие, улучшать органолептические свойства ЛФ. В связи с этим, к лекарственным формам предъявляются следующие требования: по лечебному назначению, высокая биодоступность лекарственной субстанции в данной лекарственной форме и соответствующая фармакокинетика, равномерность распределения лекарственной субстанции в массе вспомогательных веществ, а отсюда - точность дозирования их в процессе хранения, соответствие нормам микробной контаминации, удобство приема и простота приготовления лекарственной формы.
Учитывая вышеизложенное, мы обратили внимание на медицинские растворы, так как они широко используются в медицинской практике как наружные и внутренние средства и их в стерильном виде часто применяют парентерально, кроме того, растворы готовятся без особого труда. В состав раствора можно вводить различные лекарственные вещества, в основном, это антисептики, местные анестетики, противомикозные, антибактериальные, противовоспалительные и болеутоляющие средства. Широкое применение спиртовых растворов обусловлено простотой их изготовления, разнообразием способов назначения и более высокой, чем у водных растворов, стабильностью /14-15/.
Ранее под руководством профессора Кияшева Д.К. были получены на основе 40%, 50%, 60%, 70%, 80%, 90% этиловых спиртов композиционный препарат «Брисал», состоящий из бриллиантового зеленого и кислоты салициловой в различных соотношениях ингредиентов. Продолжая исследования в указанной области в целях повышения лечебной эффективности лекарственной формы, нами разработан новый композиционный
препарат, содержащий азитромицетин и кислоты салициловой в 60% этиловом спирте в целях определения противомикробной активности комбинированного спиртового раствора под условным названием «Азисал».
Азитромицин кислотоустойчивый антибиотик группы макролидов, является представителем азолидов, широкого спектра действия: механизм антимикробного действия связан с нарушением синтеза белков микроорганизмов. Действует в малых дозах бактериостатически а в больших бактерицидно. Активен в отношении грамположительных (стафилококки и стрептококки) и грамотрицательных кокков (гонококки, менингококки). Показания: инфекционно воспалительные заболевания, в т.ч., бронхит, пневмония, инфекции кожи и мягких тканей, средний отит, синусит,фарингит, тонзиллит, гонорейный и негонорейный уретриты, цервицит, болезнь Лайма (боррелиоз) и т.д., а кислота салициловая проявляет противовоспалительное действие и применяют наружно как антисептическое, отвлекающее, раздражающее и кератолитическое средство в присыпках (2-5 %) и 1-10% мазях, пастах, спиртовых растворах (1% и 2%). При сочетании азитромицина и кислоты салициловой в одном композиционном препарате «Азисал» должны проявить синергетическое действие. При выборе дозы ингредиентов в растворе за основу взяты литературные данные.
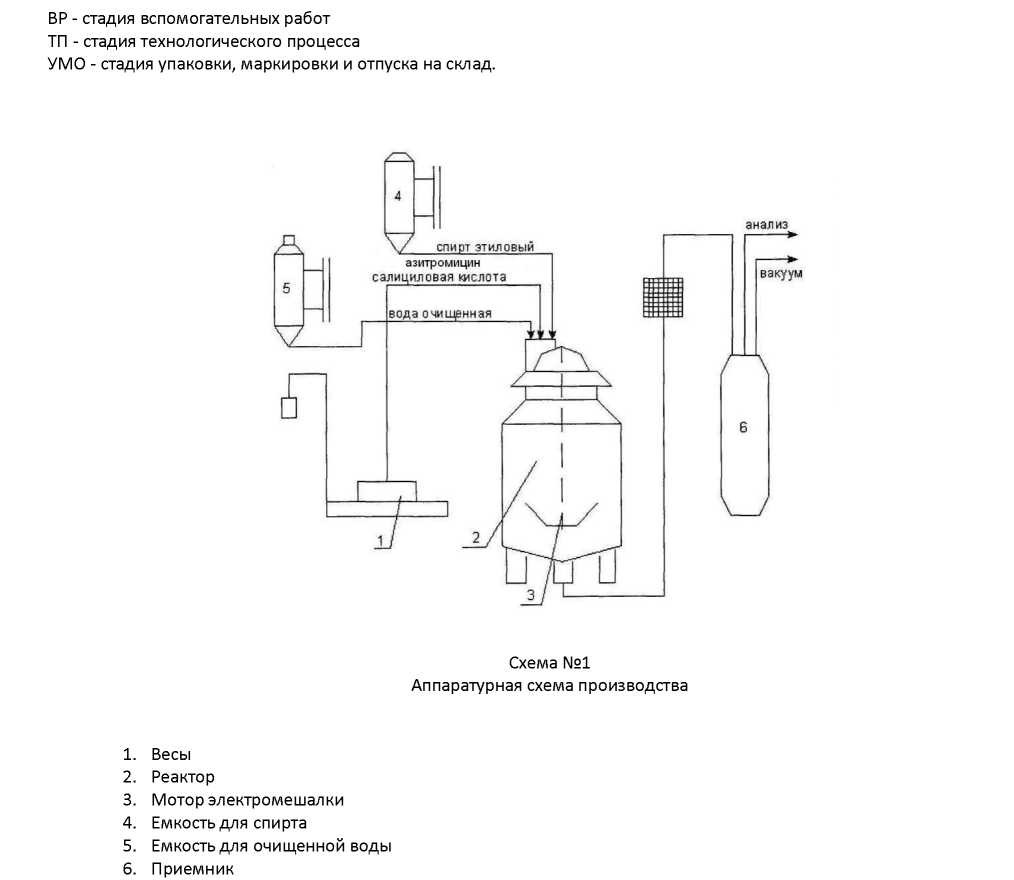
Состав композиционного спиртового раствора «Азисал» приведен в таблице №3, технологический процесс производства в таблице №4, а аппаратурная схема производства в схема №1
Таблица 3 - Образец композиционного препарата «Азисал»
|
№ серий |
Наименование компонентов |
№ образцов |
|
"ĩ |
Ингредиенты |
|
|
Азитромицин |
0,75г |
|
|
Кислота салициловая |
1 г |
|
|
Спирт этиловый 60% до |
100мл |
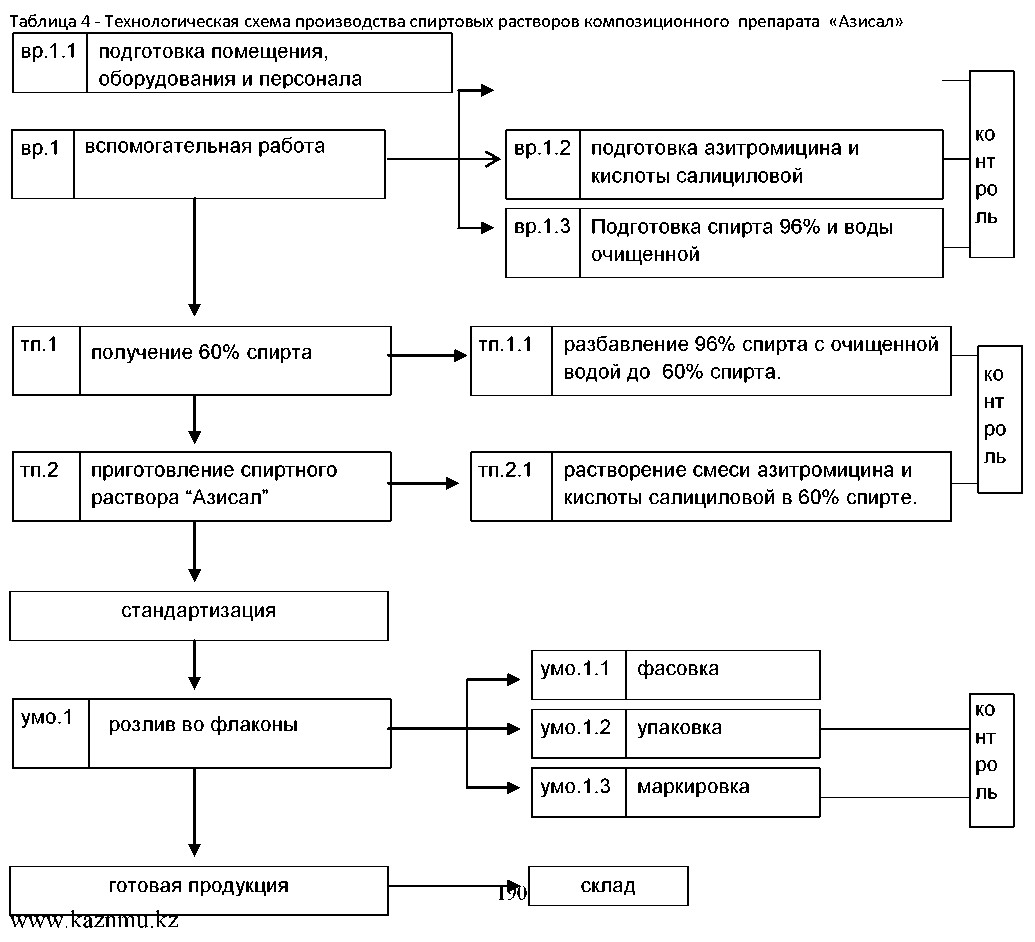
В соответствии с аппаратурной схемой производства (схема №1) для получения 60% этилового спирта в реактор (2) из емкости (4) наливаем рассчитанное количество 96% этилового спирта и рассчитанное количество воды очищенной из емкости (5). Расвор перемешивают несколько раз электромеханической мешалкой (3).
На весах (1) отвешивают предварительно мелко измельченный порошок 0,75кг азитромицина и 1кг салициловой кислоты и загружают все в реактор (2). После этого включают электромеханическую мешалку (3) и перемешивают их до полного растворения. Затем раствор фильтруют. Получается раствор - прозрачная жидкость с запахом спирта. Затем их переливают во флаконы. Далее определяют биологическую активность нового композиционного спиртового препарата «Азисал».
Состав комбинированного препарата «Азисал»: Азитромицина 0,75 Кислоты салициловой 1,0 Спирта этилового 60 % до 100мл
Далее приготовлены 4 образца азитромицина в различных концентрациях 0,25; 0,5; 0,75; 1,0; в 60% спирте по анологичной методике получения композиционного спиртового раствора «Азисал» для сравнения антимикробной активности с активностью комбинированного препарата «Азисал» и все образцы были испытаны на антимикробную активность.
Состав спиртовых растворов азитроимцина Азитромицин 0,25 -1,0 Спирт 60% до 100 мл
Краткое описание антимикробного метода исследования препарата «Азисал»:
Изучение антимикробной актиности препарата «Азисал» проводилось по отношению к штаммам бактерий Staphilococcus aureus, Escherichia coli, Pseudomonas aeruginosa и дрожжевому грибу Candida albicans методом диффузии в агар (лунок). Исследуемые образцы растворяли в 96% этиловом спирте в концентрации 1мг/мл. культутру выращивали при температуре 370С в течение 18-24 часов. Культуру разводили в 0,9% растворе хлорида натрия, бактерии вносили по 1 мл в чашки с мясопептонным агаром, а кандиду – в среду Сабуро и засевали по методу получения «сплошного газона». Формировали лунки диаметром 6 мм куда вносили препараты и 96% этиловый спирт в качестве контроля.
Результаты исследований антимикробной активности препарата «Азисал» приведены в таблице 5.
Таблица 5 - Антимикробная активность препарата «Азисал»
|
№ |
шифр |
Staphilococcus aureus |
Escherichia coli |
Pseudomonas aeruginosa |
Candida albicans |
|
«Азисал» |
ДКК-4 |
29 ¯ |
7 |
27 |
10 |
Краткое описание антимикробного метода исследования спиртовых растворов азитромицина в различных концентрациях:
Изучение антимикробной актиности вышеуказанных образцов проводилось по отношению к штаммам бактерий Staphilococcus aureus, Escherichia coli, Pseudomonas aeruginosa и дрожжевому грибу Candida albicans методом диффузии в агар (лунок). Исследуемые образцы растворяли в 96% этиловом спирте в концентрации 1мг/мл. культутру выращивали при температуре 37:С в течение 18-24 часов. Культуру разводили в 0,9% растворе хлорида натрия, бактерии вносили по 1 мл в чашки с мясопептонным агаром, а кандиду – в среду Сабуро и засевали по методу получения «сплошного газона». Формировали лунки диаметром 6 мм куда вносили препараты и 96% этиловый спирт в качестве контроля.
Результаты исследований. Результаты исследований антимикробной активности образцов приведены в таблице 6.
Таблица 6 - Антимикробная активность спиртовых растворов азитромицина в различных концентрациях:
|
№ |
шифр |
Процентное содержание азитромицина в 60% спирте |
Staphilococcus aureus |
Escherichia coli |
Pseudomonas aeruginosa |
Candida albicans |
|
1 |
ДК-5 |
0,25 |
25 |
12 |
14 |
0 |
|
2 |
ДК-6 |
0,5 |
29 |
7 |
27 |
0 |
|
3 |
ДК-7 |
0,75 |
26 |
0 |
16 |
0 |
|
4 |
ДК-8 |
1,0 |
26 |
0 |
25 |
0 |
Таким образом, на основании антимикробного исследования спиртовых растворов азитромицина в различных концентрациях (0,25-1,0) и комбинированного препарата «Азисал», сравнивая данные таблицы 5 и 6 установили, что комбинированный препарат «Азисал» проявляет максимальную эффективность, а по отношению к дрожжевым грибам дополнительно проявляет кандидомикозное действие, что обусловлено синергизмом двух препаратов: азитромицина и кислоты салициловой.
СПИСОК ЛИТЕРАТУРЫ
- Солдатенко А.Т., Колядина Н.М., Шендрик И.В. Основы органической химии лекарственных веществ. - М.: Мир. Бином. Лаборатория знаний, 2009. - 190 c.
- Душенков И., Раскин И., новая стратегия поиска природных биологически активных веществ // Физиология растений. - 2008 - Т.55. - №4. - C.624-628.
- Кияшев А.К. исследование антимикробной активности 1% раствора в зависимости от концентрации спирта (40-90%) // Фармацевтический бюллетень. - 2010. - №9-10. - C. 17-18.
- Жансарина Г.Х., Рахметова А.А. Нестероидные противовоспалительные средства на казахстанском фармацевтическом рынке.// Фармация Казахстана. - 2009. - №11. - C. 27-31.
- Кияшев А.К., Шакиев С.Ш., Бисенбаев Э.М., Кияшев Д.К. Противомикробная активность и количественное определение ингредиентов препарата «Левисал» // Фармация Казахстана.- 2009. - вып. №12. - C. 32-36
- Смагулов М.К., Кияшев Д.К., Ахметова С,Б., Сейдахметова Р.Б. Антимикробная активность композиционных препаратов «Брисал» и «Левисал».//Инновационные технологии в медицине и фармации. – Караганда: 2008. - C. 255-258.
- Кияшев Д.К. Синтез салициловой, ацетилсалициловой кислоты, бриллиантового зеленого и на их основе приготовление лекарственных форм. // Караганда: 2008 . – 128 c.
- Кияшев Д.К. Синтез новых цис-2,6-дифенилтетрагидротиопирановых производных и определение их биологической активности // Караганда: 2008. - 128 c. Отпечатано в типографии ТОО «Алтын гуль»
- Бейсенбеков А.С., Нокербек Ш., Буленова К.Ж., Битаева Д.Е. // Ацетилсалицил қышқылын дамыған елдердің аналитикалық нормативтік құжаттарында ұсынылған көрсеткіштермен салыстырып бақылау. // Материалы международной научно-практической конференции «Фармация: современное состояние, достижения и перспективы», посвященной 80-летию КазНМУ им.С.Д.асфендиярова. – Алматы: 2011. - C. 56-59
- Азембаев А.А. Перспективы развития отечественного производства в странах СНГ. // Материалы международной научно-практической конференции «Фармация: современное состояние, достижения и перспективы», посвященной 80- летию КазНМУ им.С.Д.Асфендиярова. - Алматы: 2011. - C. 49-52.
- Тлеулинова А.Н. Азитромицин: современные аспекты клинического применения вчера, сегодня, завтра.//Фармация Казахстана. - 2011.- №3. - C.26-28.
- Ахметова С.Б., Батыралиева А.К., Кияшев М.Д., Смагулов М.К., Кияшев Д.К. Определение биологической активности образцов (1-10) в 6-ти сериях спиртового раствора «Брисал». //Материалы научно-практической конференции «Фармация Казахстана»: интеграция науки, образования и производства. - Том № 2. – Шымкент: 2009. - C. 7274-276.
- Кияшев М.Д. Определение биологической активности образцов 1% спиртового раствора бриллиантового зеленого и 1% спиртового раствора кислоты салициловой в спиртах различной концентрации.//Материалы международной научнопрактической конференции «Фармация Казахстана»: интеграция науки, обраования и производства. Шымкент: 2009. - с. 331-333.
- Кияшев М.Д., Батыралиева А.К., Ахметова С.Б., Кияшев Д.К. Приготовление раствора бриллиантового зеленого и раствора кислоты салициловой в спиртах различной концентрации и определение их биологической активности.//Вестник Киргизской гос. мед. академии им. А. К. Ахунбаева. - Бишкек: 2009. - №1. - C.182-186.
- Разработка состава и технологии композиционного препарата «Брисал» на 70% этиловом спирте.//Вестник АлИУВ. Материалы 1 центрально-Азиатского научного форума «Клиническая фармакология»: опыт, современное состояние, перспектива». - 17 октября 2008. - Алматы. - №4 (спец.выпуск). – 99 c.