В данном обзоре представлены современные иммунологические маркеры, используемые для диагностики туберкулеза и предикции прогрессирования латентного туберкулеза. Проведен анализ диагностической значимости различных тестов, их преимущества и недостатки. Также рассмотрены перспективные маркеры, значимость которых находится на стадии изучения.
Туберкулез (ТБ) - это инфекционное заболевание, которое является одной из главных причин смертности и заболеваемости во всем мире. По данным ВОЗ, ежегодно регистрируется 10,4 миллиона новых случаев туберкулеза [1]. В то же время, инфицирование может проявляться в латентной форме – латентная туберкулезная инфекция (LTBI), то есть протекать со стертой клиникой и бессимптомно. Такая скрытая туберкулезная инфекция может длиться годами. С патогенетической точки зрения, латентная форма туберкулеза отражает состояние стойкого иммунного ответа на микобактерии туберкулеза, обнаруженные либо туберкулиновым кожным тестом (ТSТ), либо исследованием продукции интерферона (IGRA- InterferonGammaReleaseAssay) при отсутствии клинических проявлений.
При этом, как было отмечено выше, в большинстве случаев латентная формане трансформируется в активный, клинически выраженный туберкулез. Возможно, это связано с эффективным контролем иммунной системынад процессом размножения микобатерий, или же с отсутствием живыхмикобактерий в организме. Эта гипотеза подтверждается фактом увеличения риска реактивации и последующего заболевания у лиц, инфицированных микобактериями туберкулеза с иммунодефицитным состоянием, в результате ВИЧ-инфекции, или применения в лечении ингибиторов фактора некроза пухоли (TNF) -α [2-4], а также терапия другими иммуносупрессивными препаратами, которые используются при воспалительных заболеваниях и трансплантации [5]. Повлиять на иммунную регуляцию, повысив риск активации туберкулеза, так же могут неинфекционные заболевания, такие как сахарный диабет 2 типа [6,7].
Постановка правильного диагноза, эффективное лечение и профилактика заболевания играют решающую роль в снижении передачиинфекции, заболеваемости и смертности от туберкулеза. До недавнего времени LTBI считался однородным состоянием [8]. Однако, на сегодняшний день стало ясно, что LTBI представлен широким спектром инфекционных состояний, которые различаются по степени репликации возбудителя, устойчивости к организму хозяина и к воспалению [8-11]. Также разноообразны и клинические проявления ТБ. Эта гетерогенность включает в себя как тип патологии, (легочный и внелегочный ТБ), так и распространенность поражения, характеристики иммунной системы и воспаления, активность репликациимикобактерий и бактериальную нагрузку. Также, на сегодняшний день увеличивается число доказательств, подтверждающих гипотезу о том, что генетический фон хозяина влияет на риск развития заболевания и характер его проявления. [12-15].
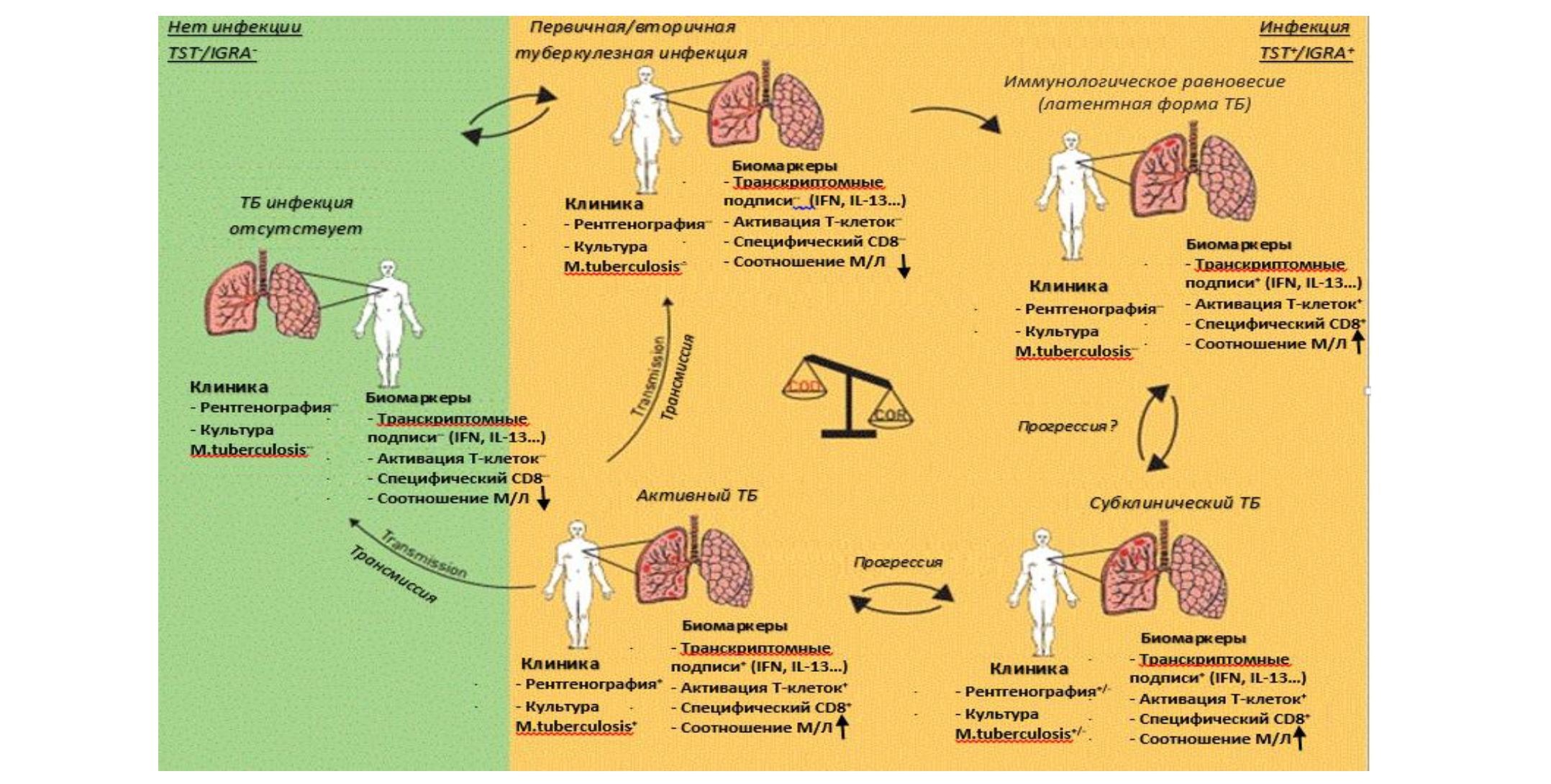
Взаимодействие организма хозяина и микобактерий, а также клинические и доклиинические маркеры различных форм туберкулеза представлены на рисунке.http://erj.ersjournals.com.
Описание рисунка: Результатом заражения M. tuberculosis является не только LTBI или активный ТБ, а непрерывный спектр состояний, которые различаются по степени репликации возбудителя, устойчивости хозяина и маркерам воспаления. Идентификация инфекции M. tuberculosis сложна из-за отсутствия клинических признаков поражений легких, обнаруживающихся рентгенограммой грудной клетки или M. tuberculosis в культуре мокроты. Латентное состояние характеризуется иммунологическим равновесием и предполагаемым контролем репликации бактерий. По мере развития инфекции этот баланс теряется, что приводит к росту бактериальной нагрузки и / или развитию патологии. Это состояние можно определить как субклиническое или зарождающееся заболевание ТБ, при котором идентификация заболевания все еще затруднена. На этой фазе биомаркеры риска туберкулеза могут помочь в идентификации лиц, подвергающихся риску для их профилактического лечения. Например,, усиление экспрессии генов интерлейкина (IL) -13 и интерферона (IFN) типа I и II, повышение маркеров активации на Т-клетках (например, экспрессия D-родственного человеческого лейкоцитарного антигена и снижение экспрессии CD27), как увеличение соотношения моноцитов / лимфоцитов (M / L), являются прогностическим фактором развития туберкулеза. Прогрессирование субклинического ТБ до клинической формы, вероятно, связано с дальнейшим повышением бактериальной нагрузки. Поэтому диагностика активного туберкулеза основана на результатах рентгенографии грудной клетки, обнаружении M. tuberculosis в мокроте. Передача M. Tuberculosis от больных активным туберкулезом может привести к первичной или вторичной инфекции M. tuberculosis. Первичная инфекция M. tuberculosis определяется методом анализа IFN-γ (IGRA) / туберкулинового кожного теста (TST) и отсутствием рентгенологических повреждений легких и отрицательной мокроты на МТ.
Серьезным препятствием при изучении туберкулеза является то, что бактерии не могут быть обнаружены invivo во время скрытой, бессимптомной формы заболевания. Тест, который сможет количественно определять бактерии или уровни их репликации во время LTBI, повысит нашу способность определения этапов инфекции, что позволит более детально изучить патогенез и иммунитет при бессимптомной туберкулезной инфекции.
 Таким образом, результатом заражения M. tuberculosis является не только LTBI или активный ТБ, а непрерывный спектр состояний, отличающихся друг от друга по патогенезу развития и реактивности хозяина. В результате этого требуется разработка различных диагностических и лечебных стратегий.
Таким образом, результатом заражения M. tuberculosis является не только LTBI или активный ТБ, а непрерывный спектр состояний, отличающихся друг от друга по патогенезу развития и реактивности хозяина. В результате этого требуется разработка различных диагностических и лечебных стратегий.
Биомаркеры, используемые на современном этапе
Результатом заражения M. tuberculosis (MBT) является не только LTBI или активный ТБ, а непрерывный спектр состояний, которые различаются по степени репликации возбудителя, устойчивости хозяина и характером воспаления. Латентное состояние характеризуется иммунологическим равновесием и предполагает иммунный контроль репликации бактерий.По мере развития инфекции этот баланс теряется, что приводит к росту бактериальной нагрузки и вероятности развития клинических признаков патологии.Это состояние можно определить как субклиническое или зарождающееся заболевание ТБ, при котором маркеры заболевания могут быть все еще недостаточно информативными. С другой стороны, имеющиеся маркеры риска (МР) могут потенциально допускать идентификацию лиц, подвергающихся риску развития заболевания, для профилактического лечения. Так, например, усиление экспрессии генов интерлейкина (IL) -13 и интерферона (IFN) типа I и II, повышение маркеров активации на Т-клетках (например, экспрессия D- родственного человеческого лейкоцитарного антигена и снижение экспрессии CD27), как и увеличение соотношения моноцитов/лимфоцитов (M / L), являются прогностическим фактором развития туберкулеза. Прогрессирование субклинического ТБ до клинической формы, вероятно, связано с дальнейшим повышением бактериальной нагрузки.Таким образом, диагностика активного туберкулеза основана на корреляции результатов рентгенографии грудной клетки, обнаруженииMBTв мокроте и положительные тесты на МР. Передача MBTот больных активным туберкулезом может привести к первичной или вторичной инфекции M. tuberculosis. Первичная инфекция MBTопределяется методом анализа IFN-γ (IGRA)/туберкулинового кожного теста (TST), отсутствием рентгенологических изменений в легких и отрицательным результатом мокроты для MBT.
Как с клинической, так и с исследовательской точки зрения очень важно правильно идентифицировать индивидуумы, инфицированные MBT, которые наиболее подвержены риску перехода LTBI в активную форму туберкулеза, с целью проведения целевого профилактического лечения [16, 17]. Поэтому, профилактика заболевания, вызванного скрытой инфекцией, является ключевым решением в достижении целевых показателей ВОЗ по ликвидации ТБ [16, 18, 19]. Однако массовая профилактическая терапия в эндемичных по туберкулезу странах, основанная на скрининге IGRA / TST, по большей части неоправдана, так как, в этом случае необходимо будет лечить 50-80% населения, притом, что у 85-95% латентно инфицированных людей не произойдет активизации LTBI в течение всей жизни [20-22]. Положительное прогностическое значение теста IGRA / TST слишком низкое, поэтому необходимы более информативные прогнозные тесты.
Тесты TST и IGRA основаны на иммунологической чувствительности к антигенам микобактерий. В случае TST, это количественно определяется поперечным диаметром уплотнения кожи, возникающим в результате внутрикожной инъекции производного очищенного белка, сырой смеси антигенов, многие из которых разделены на MBT, M. bovis, bacilleCalmette-Guérin (BCG) и несколько видов экологических микобактерий. IGRA проводитсяна основе исследования крови и включает в себя квантифероновый тест (QFT-GIT, Qiagen, Hilden, Германия) и T-SPOT.TB (OxfordImmunotec, Abingdon, UK). При проведении исследованийinvitro измеряют продукцию IFN-γ при стимуляции антигеном цельной крови с использованием ELISA или мононуклеарные клетки периферической крови (РВМС) путем иммуноферментного анализа (ELISPOT), соответственно [23]. В этих анализах специфичность M. tuberculosisобусловлена стимуляцией пептидами, включающими антигены MBTESAT-6, CFP-10 (и TB7.7 для QFT-GIT), которые ограничены областью генома MBT, свободны от M. bovis BCG и отсутствуют у большинства экологических микобактерий [24-27].
Практическое преимущество тестов IGRA заключается в том, что они требуют только одного лабораторного теста с отрицательным и положительным контролем и только одной проверки. Более того, тесты invitro могут отличать истинные отрицательные ответы от анергии [23].
На сегодняшний день существует обновленная версия QFT- GIT - QuantiFERON TB Plus [23, 28] . Этот тест включает дополнительную пробирку антигена в QFT-GIT, которая содержит пептиды, предназначенные специально для индукции ответа со стороны CD8+Т-клеток в дополнение к CD4+Т-клеточному ответу [29], обнаруженному с помощью оригинального анализа QFT-GIT [30]. Включение новых CD8- специфических пептидов базируется на данных о том, что MBT - специфичные CD8 + Т-клетки чаще обнаруживаются у субъектов с активным заболеванием туберкулеза по сравнению с LTBI [31-34]. Первые данные о производительности QuantiFERON TB Plus в многоцентровом европейском исследовании были опубликованы [35, 36].
Перспективные модели, их преимущества и задачи
На сегодняшний день новые прогностические тесты, предупреждающие прогрессирование туберкулеза от латентной до активной форм, привлекают все больше внимания. В 2015 году была созвана группа экспертов ВОЗ для обсуждения целевого продукта, а именно теста на основе доступной базы данных. Такой тест должен быть полезным в условиях высокой ТБ нагрузки, и более доступным, чем мокрота. Разработка теста с высокой положительной прогностической ценностью (PPV,> 95%) для прогрессирования LTBI в активный ТБ в краткосрочной перспективе невозможна. Поэтому, для достижения приемлемых положительных и отрицательных прогностических значений подобрали значения для чувствительности и специфичности выше 90%, с минимальным значением равным 75% в двух случаях.
Необходимо отметить дополнительные многообещающие тесты для обнаружения LTBI. Это кожный тест (C-Tb) [37], который измеряет гиперчувствительность к рекомбинантным белкам ESAT-6 и CFP-10 после внутрикожного введения. Авторы утверждают, что тест сочетает в себе преимущества технологий TST и IGRA и характеризуется низкой стоимостью, простотой в использования (как TST), и высокой специфичностью, (как IGRA).
В то же время, следует отметить, что возможности TST и IGRA ограничены, так как точность этих тестов низкая по отношению к пациентам с ослабленным иммунитетом. Более того, они не могут различать LTBI и активный ТБ [23]. Этот факт является серьезной проблемой в эндемичных по туберкулезу областях и приводит к недостаточной прогностической значимости, определяющей развитие ТБ у лиц с LTBI [23, 39, 40]. Эти ограничения являются веской причиной, по которой простое измерение ответа IFN-γ не позволяет правильно оценить риск прогрессирования от латентности к активному заболеванию.
Вследствие этого, открытие биомаркеров, способных различать активную и покоящуюся бактериальные репликации у лиц с LTBI, а такжемаркеров организма хозяина, определяющих лица, наиболее подверженных риску развития активного заболевания [9, 41, 42], имеет большое значение.
Кроме того, крайне важно, чтобы вновь выявленные маркеры подтверждались в разных географических условиях, поскольку человеческое население имеет различный генетический фон и подвержено различным влияниям окружающей среды также как и МВТ различного происхождения. Это ведет к разнообразию скоростей прогрессирования заболевания ТБ [43].
Другим перспективным биомаркером можно считать экспрессию генов IL-13 / AIRE (аутоиммунный регулятор). Исследования проводились на архивных образцах ВИЧ- инфицированных больных [44,45]. Оценка экспрессии генов проводилась методом мультиплексной ПЦР с использованием двухцветной обратной транскриптазы (dcRT-MLPA- dual-colorreverse-transcriptasemultiplexligation- dependentprobeamplification). Экспрессия интерлейкина (IL) -13 в отсутствие AIRE была прогностическим критерием риска развития туберкулеза у ВИЧ-инфицированных больных. Интересно отметить, что при анализе людей из группы IL-13 / AIRE, у которых туберкулез прогрессировал в течение следующих нескольких месяцев, было также много экспрессии генов IFN типа I, что указывает на выявление ранних маркеров заболевания у этих людей. Однако, данные исследования необходимо повторить в более крупных, продольных и независимых когортах, а также в ВИЧ- неинфицированных группах.
Интересны также биомаркеры, выявленные при оценке эффективности иммунизации. Так, например, при изучении эффективности вакцины MVA85A (векторная вакцина - "ModifiedVacciniaAnkara", экспрессирующая антиген 85А туберкулезной микобактерии)[63] было выявлено, что у младенцев, у которых развился туберкулез, отмечались высокие уровни активированных CD4 + Т-клеток, чем у младенцев, оставшихся здоровыми [46, 47]. Аналогичный результат был получен у подростков, инфицированных MВТ [47]. Обращает внимание тот факт, что при исследовании младенцев ответТ-клеток на цитомегаловирус был значительно выше у тех младенцев, у которыхразвился ТБ [47]. Исходя из этих данных, можно предположить, что коинфекции могут стимулировать иммунную систему, что может быть связано с риском развития туберкулеза.
Другой биомаркер был выявлен на второй фазе испытания MVA85A [46]. Более высокие уровни антител к Ag85A- связывающему Ig G наблюдались в контроле, чем у младенцев заболевших ТБ. Ag85A-специфический IgG, таким образом, был связан с уменьшением риска развития заболевания ТБ. Кроме того, увеличение количества БЦЖ- специфических IFN-γ секретирующих Т-клеток, измеренные с помощью анализа ELISPOT, также были связаны с уменьшением риска развития заболевания ТБ. Однако, другие исследования такой зависимости не выявили [48]. Несколько других исследований показали, что фенотипические маркеры активации и дифференцировки Т- клеток могут характеризовать различные клинические проявления туберкулеза. Так, например, было выявлено, что CD27 Т-клетками может служить биомаркерами. В нескольких исследованиях было показано, что значительное числоспецифичных к МБ CD4 + Т-клеток, продуцирующих IFN-y,н℮ экспрессируют CD27 (CD27- IFN-γ+ CD4+) у лиц с активным туберкулезом по сравнению со здоровым контролем [49]. Кроме того, было показано, что частоты CD27-IFN-γ + CD4 + клеток сильно коррелируют со степенью поражения легких [49] и успешностью лечения туберкулеза [50].
Также активно изучается возможности определения IFN-γ- индуцибельного белка-10 (IP-10) в качестве биомаркера.IP- 10представляет собой хемокин, секретируемый различными типами клеток, включая моноциты, эндотелиальные клетки и фибробласты, в ответ на IFN-γ. Он действует как хемоаттрактант для моноцитов / макрофагов, Т-клеток, естественных киллерных клеток и дендритных клеток и способствует адгезии Т-клеток [51,52]. Показано, что концентрации IP-10, измеренные после воздействия антигена M. tuberculosis, повышаются у пациентов с ТБ как с ВИЧ коинфекциейтак и без нее и в крови [53], и в моче [54].
Выводы
Точная и быстрая диагностика играет ключевую роль в контроле над туберкулезом.Применяемые в настоящее время тесты для диагностики латентной туберкулезной инфекции (LTBI) имеют свои ограничения, связанные с трудоёмкостью, длительностью, а также сневозможностью дифференциации активного туберкулеза от латентного. Перспективным направлением для совершенствования методов диагностики туберкулезной инфекции является идентификация биомаркеров данного заболевания. В этих случаях большое значение приобретают иммунологические методы исследования. Преимуществом их использования является сокращение времени для получения окончательного результата, большая безопасность для больного по сравнению с радиологическими методами, снижение инфекционной опасности для персонала, работающего с биологическим материалом.
Дальнейшие интенсивные исследования в данном направлении необходимы для текущего обнаружения, оценки и разработки биомаркеров. Кроме того, очень важно, чтобы различные маркеры были проверены в разных географических условиях (и, следовательно, на разных генетических фонах-хозяевах и линиях циркулирующих патогенов).
СПИСОК ЛИТЕРАТУРЫ
- World Health Organization (WHO). Global Tuberculosis Report 2016.
- Cantini F, Lubrano E, Marchesoni A, et al. Latent tuberculosis infection detection and active tuberculosisprevention in patients receiving anti-TNF therapy: an Italian nationwide survey // Int J Rheum Dis. – 2016. - №19. – Р. 799–805.
- Cantini F, Niccoli L, Goletti D. Tuberculosis risk in patients treated with non-anti-tumor necrosis factor-α(TNF-α) targeted biologics and recently licensed TNF-α inhibitors: data from clinical trials and nationalregistries // J RheumatolSuppl. – 2014. - №91. – Р. 56–64.
- Solovic I, Sester M, Gomez-Reino JJ, et al. The risk of tuberculosis related to tumour necrosis factor antagonisttherapies: a TBNET consensus statement // EurRespir J. – 2010. - №36. – Р. 1185–1206.
- Bumbacea D, Arend SM, Eyuboglu F, et al. The risk of tuberculosis in transplant candidates and recipients:a TBNET consensus statement // EurRespir J. – 2012. - №40. – Р. 990–1013.
- Harries AD, Kumar AM, Satyanarayana S, et al. Addressing diabetes mellitus as part of the strategy for endingTB // Trans R Soc Trop Med Hyg. – 2016. - №110. – Р. 173–179.
- Ronacher K, Joosten SA, van Crevel R, et al. Acquired immunodeficiencies and tuberculosis: focus on HIV/AIDSand diabetes mellitus // Immunol Rev. – 2015. - №264. – Р. 121–137.
- Barry CE 3rd, Boshoff HI, Dartois V, et al. The spectrum of latent tuberculosis: rethinking the biology andintervention strategies // Nat Rev Microbiol. – 2009. - №7. – Р. 845–855.
- Esmail H, Barry CE 3rd, Young DB, et al. The ongoing challenge of latent tuberculosis // Philos Trans R SocLondB BiolSci. – 2014. - №369. – Р. 201-210.
- Delogu G, Goletti D. The spectrum of tuberculosis infection: new perspectives in the era of biologics // J RheumatolSuppl. – 2014. - №91. – Р. 11–16.
- Dorhoi A, Kaufmann SH. Pathology and immune reactivity: understanding multidimensionality in pulmonarytuberculosis. // SeminImmunopathol. – 2016. - №38. – Р. 153–166.
- Homolka S, Niemann S, Russell DG, et al. Functional genetic diversity among Mycobacterium tuberculosiscomplex clinical isolates: delineation of conserved core and lineage-specific transcriptomes during intracellularsurvival // PLoSPathog. – 2010. - №6. – Р. 88-96.
- Marquina-Castillo B, García-García L, Ponce-de-León A, et al. Virulence, immunopathology and transmissibilityof selected strains of Mycobacterium tuberculosis in a murine model // Immunology. – 2009. - №128. – Р. 123–133.
- Palanisamy GS, DuTeau N, Eisenach KD, et al. Clinical strains of Mycobacterium tuberculosis display a widerange of virulence in guinea pigs // Tuberculosis. – 2009. - №89. – Р. 203–209.
- Coscolla M, Gagneux S. Consequences of genomic diversity in Mycobacterium tuberculosis // SeminImmunol. – 2014. - №26. – Р. 431– 444.
- Lönnroth K, Migliori GB, Abubakar I, et al. Towards tuberculosis elimination: an action framework forlow-incidence countries // EurRespir J. – 2015. - №45. – Р. 928–952.
- Getahun H, Matteelli A, Abubakar I, et al. Management of latent Mycobacterium tuberculosis infection:WHO guidelines for low tuberculosis burden countries // EurRespir J. – 2015. - №46. – Р. 1563–1576.
- D'Ambrosio L, Dara M, Tadolini M, et al. Tuberculosis elimination: theory and practice in Europe // EurRespir J. – 2014. - №43. – Р. 1410– 1420.
- Tiberi S, D'Ambrosio L, De Lorenzo S, et al. Tuberculosis elimination, patients' lives and rational use of newdrugs: revisited // EurRespir J. – 2016. - №47. – Р. 664–667.
- Sester M, Sotgiu G, Lange C, et al. Interferon-γ release assays for the diagnosis of active tuberculosis: a systematicreview and metaanalysis // EurRespir J. – 2011. - №37. – Р. 100–111.
- Sester M, van Leth F, Bruchfeld J, et al. Risk assessment of tuberculosis in immunocompromised patients. A TBNET study // Am J RespirCrit Care Med. – 2014. - №190. – Р. 1168–1176.
- Sester M, van Crevel R, Leth F, et al. Numbers needed to treat to prevent tuberculosis // EurRespir J. – 2015. - №46. – Р. 1836–1838.
- Goletti D, Sanduzzi A, Delogu G. Performance of the tuberculin skin test and interferon-γ release assays: anupdate on the accuracy, cutoff stratification, and new potential immune-based approaches // J Rheumatol Suppl. – 2014. - №91. – Р. 24–31.
- Mahairas GG, Sabo PJ, Hickey MJ, et al. Molecular analysis of genetic differences between Mycobacterium bovisBCG and virulent M. bovis. // J Bacteriol. – 1996. - №178. – Р. 1274–1282.
- Gey van Pittius NC, Sampson SL, Lee H, et al. Evolution and expansion of the Mycobacterium tuberculosis PEand PPE multigene families and their association with the duplication of the ESAT-6 (esx) gene cluster regions // BMC EvolBiol. – 2006. - №6. – Р. 95-100.
- Whitworth HS, Scott M, Connell DW, et al. IGRAs – the gateway to T cell based TB diagnosis // Methods. – 2013. - №61. – Р. 52–62.
- Andersen P, Munk ME, Pollock JM, et al. Specific immune-based diagnosis of tuberculosis // Lancet. – 2000. - №356. – Р. 1099–1104.
- QuantiFERON®-TB Gold Plus (QFT®-Plus) ELISA Package Insert. PLUS/2PK-Elisa/UK.pdf Date last accessed: February 2015. Date last updated: February 2015.
- Petruccioli E, Chiacchio T, Pepponi I, et al. First characterization of the CD4 and CD8 T-cell responses toQuantiFERON-TB Plus // J Infect. - 2016. – Р. 88-96.
- Mori T, Sakatani M, Yamagishi F, et al. Specific detection of tuberculosis infection: an interferon-γ-based assayusing new antigens // Am J RespirCrit Care Med. – 2004. - №170. – Р. 59–64.
- Chiacchio T, Petruccioli E, Vanini V, et al. Polyfunctional T-cells and effector memory phenotype are associatedwith active TB in HIV- infected patients // J Infect. – 2014. - №69. – Р. 533–545.
- Day CL, Abrahams DA, Lerumo L, et al. Functional capacity of Mycobacterium tuberculosis-specific T cellresponses in humans is associated with mycobacterial load // J Immunol. – 2011. - №187. – Р. 2222–2232.
- Rozot V, Patrizia A, Vigano S, et al. Combined use of Mycobacterium tuberculosis-specific CD4 and CD8 T-cellresponses is a powerful diagnostic tool of active tuberculosis // Clin Infect Dis. – 2015. - №60. – Р. 432–437.
- Rozot V, Vigano S, Mazza-Stalder J, et al. Mycobacterium tuberculosis-specific CD8+ T cells are functionally andphenotypically different between latent infection and active disease // Eur J Immunol. – 2013. - №43. – Р. 1568–1577.
- Barcellini L, Borroni E, Brown J, et al. First independent evaluation of QuantiFERON-TB Plus performance // EurRespir J. – 2016. - №47. – Р. 1587–1590.
- Barcellini L, Borroni E, Brown J, et al. First evaluation of QuantiFERON-TB Gold Plus performance in contactscreening // EurRespir J. – 2016. – Р. 23-31.
- Aggerbeck H, Giemza R, Joshi P, et al. Randomised clinical trial investigating the specificity of a novel skin test(C-Tb) for diagnosis of M. tuberculosis infection // PLoS One. – 2013. - №8. – Р. 41-46.
- Millington KA, Fortune SM, Low J, et al. Rv3615c is a highly immunodominant RD1 (Region of Difference 1)-dependent secreted antigen specific for Mycobacterium tuberculosis infection // ProcNatlAcadSci. – 2011. - №108. – Р. 5730–5735.
- Zellweger JP, Sotgiu G, Block M, et al. Risk assessment of tuberculosis in contacts by IFN-γ release assays.A Tuberculosis Network European Trials Group study // Am J RespirCrit Care Med. – 2015. - №191. - Р. 1176–1184.
- Rangaka MX, Wilkinson KA, Glynn JR, et al. Predictive value of interferon-γ release assays for incident activetuberculosis: a systematic review and meta-analysis // Lancet Infect Dis. – 2012. - №12. – Р. 45–55.
- Ottenhoff TH, Ellner JJ, Kaufmann SH. Ten challenges for TB biomarkers // Tuberculosis. – 2012. - №92, Suppl. 1. – Р. 17–20.
- Wallis RS, Peppard T. Early biomarkers and regulatory innovation in multidrug-resistant tuberculosis // Clin InfectDis. – 2015. - №61, Suppl. 3. – Р. 160–163.
- Jong BC, Hill PC, Aiken A, et al. Progression to active tuberculosis, but not transmission, varies byMycobacterium tuberculosis lineage in the Gambia // J Infect Dis. – 2008. - №198. – Р. 1037–1043.
- Sloot R, Schim van der Loeff MF, van Zwet EW, et al. Biomarkers can identify pulmonary tuberculosis in HIV-infected drug users months prior to clinical diagnosis // EBioMedicine. – 2014. - №2. – Р. 172–179.
- Sloot R, Schim van der Loeff MF, Kouw PM, et al. Risk of tuberculosis after recent exposure. A 10-year follow-up study of contacts in Amsterdam // Am J RespirCrit Care Med. – 2014. - №190. – Р. 1044–1052.
- Tameris MD, Hatherill M, Landry BS, et al. Safety and efficacy of MVA85A, a new tuberculosis vaccine, in infants previously vaccinated with BCG: a randomised, placebo-controlled phase 2b trial // Lancet. – 2013. - №381. – Р. 1021–1028.
- Fletcher HA, Snowden MA, Landry B, et al. T-cell activation is an immune correlate of risk in BCG vaccinated infants // Nat Commun. – 2016. - №7. – Р. 112-119.
- Kagina BM, Abel B, Scriba TJ, et al. Specific T cell frequency and cytokine expression profile do not correlate with protection against tuberculosis after bacillus Calmette-Guérin vaccination of newborns // Am J RespirCritCare Med. – 2010. - №182. – Р. 1073–1079.
- Lyadova IV, Oberdorf S, Kapina MA, et al. CD4 T cells producing IFN-γ in the lungs of mice challenged with mycobacteria express a CD27negative phenotype // ClinExpImmunol. – 2004. - №138. – Р. 21–29.
- Petruccioli E, Petrone L, Vanini V, et al. Assessment of CD27 expression as a tool for active and latent tuberculosis diagnosis // J Infect. – 2015. - №71. – Р. 526–533.
- Dufour JH, Dziejman M, Liu MT, et al. IFN-γ-inducible protein 10 (IP-10; CXCL10)-deficient mice reveal a rolefor IP-10 in effector T cell generation and trafficking // J Immunol. – 2002. - №168. – Р. 3195–3204.
- Ferrero E, Biswas P, Vettoretto K, et al. Macrophages exposed to Mycobacterium tuberculosis release chemokinesable to recruit selected leucocyte subpopulations: focus on γδ cells // Immunology. – 2003. - №108. – Р. 365–374.
- Vanini V, Petruccioli E, Gioia C, et al. IP-10 is an additional marker for tuberculosis (TB) detection inHIV-infected persons in a low-TB endemic country // J Infect. – 2012. - №65. – Р. 49–59.
- Cannas A, Calvo L, Chiacchio T, et al. IP-10 detection in urine is associated with lung diseases // BMC InfectDis. – 2010. - №10. – Р. 333339.