Цель исследования – оценить результаты торакоскопичекой коррекции дефекта межжелудочковой перегородки. За период с июня 2015 по декабрь 2016 года изучены 8 пациентов, всем проведена полная торакоскопическая коррекция. Все операций были выполнены успешно. Послеоперационных осложнений не наблюдалось, конверсий в стандартный метод не было, без признаков остаточного шунта. Все пациенты были удовлетворены косметическим эффектом. Наш первый опыт торакоскопического закрытия дефекта межжелудочковой перегородки является осуществимым и безопасным. Данный метод может быть применен в клинической практике.
Введение.
В последние годы минимально инвазивная кардиохирургия применяется при коррекции дефекта межпредсердной перегородки (ДМПП) и дефекта межжелудочковой перегородки (ДМЖП) [1-3]. Однако эти оперативные вмешательства сложно выполнить при выполнении хирургических манипуляций на сердце через небольшие разрезы, но с развитием компьютерных эндоскопических технологий, позволило оценить структуры сердца на большой глубине через камеру стало возможным с помощью роботизированной хирургической системы [4].
В последние годы, полностью эндоскопические процедуры, как сообщалось рядом авторами, является безопасным и эффективным характеризуется быстрым восстановлением после операции и улучшению качества жизни и снижение боли по сравнению со стернотомией и миниторакотомией [5-8].
Проведение полностью эндоскопических процедур остаются весьма сложным и требует помощи компьютера и робототехники. Эти процедуры были использованы для коррекции простых врожденных дефектов, таких ДМПП [5-10]. Тем не менее, эффективность и безопасность полностью эндоскопической коррекции ДМЖП не были изучены. Цель нашего исследования оценить результаты полностью торакоскопичекой коррекции ДМЖП, описать возможности, показания, ограничения и проблемы.
Материалы и методы исследования.
Данное исследование было одобрено локальной этической комиссией, Казахского национального медицинского университета им С.Д. Асфендиярова (протокол №5) от 27.05.2015г. Письменное информированное согласие было получено от всех пациентов и родителей детей.
Клиническое наблюдение по дизайну исследования.
Для торакоскопической коррекции ДМЖП, критериями включения были: наличие перимембранозного ДМЖП любого размера, возраст более 5 лет с массой тела более 20 кг. Критерии исключения являются: надгребешковый (supra crista ventricularis) ДМЖП, давление в легочной артерии более 60 мм рт. ст; отсутствие в анамнезе операций на правой стороне грудной клетки, отсутствие заболеваний сосудов нижних конечностей, отсутствие получение согласие на торакоскопическую операцию. Наличие сопутствующих врожденных пороков сердца, также были исключены из исследования.
За период с июня 2015 по декабрь 2016 года были оперированы 8 пациентов. Средний возраст составил 11 Ã 9,3 лет. Средний вес пациентов составил 34 Ã 20кг. Все пациенты были обследованы стандартно. По обзорной рентгенографии органов грудной клетки в прямой проекции определялись точки для установки портов.
Для оценки эффективности и безопасности проводилась хронометрия общей продолжительности операции, времени искусственного кровообращения, кровопотери, нахождение в отделение интенсивной терапии, время искусственной вентиляции легких, койко дни после операции, применение анальгетиков с целью обезболивания.
Хирургическая техника.
После индукции общей анестезии, под интубационным наркозом, частота дыхания была в диапазоне от 18 до 30 вдохов минуту, насыщения кислорода артериальной крови более 97¿. После индукции общей анестезии, был установлен чрезпищеводный датчик для эхокардиографии.
Положение пациента с подъемом правой половины грудной клетки на 15-20 градусов. После общей гепаринизаций, была выполнена катетеризация правой яремной вены и правой бедренной артерии и вены, разрез вдоль паховой складки [7]. Три небольших разреза выполнены на правой стороне груди (Рисунок 1): порт 1 (1-1,5 см) расположен в третьем межреберье по задней подмышечной линии, порт 2 расположен во 2 межреберье по парастернальной линии, порт 3 в пятом межреберье по среднеключичной линии.
Порт 1 использовался для размещения эндоскопической камеры фирмы Karl Storz (Германия). Порт 2 и 3 использовались инструменты для торакоскопической хирургии сердца, такие как пинцет или ножницы, иглодержатель фирмы Aesculap (Германия)
После того, как три порта были установлены, выполнялось перикардиотомия на 3см выше диафрагмального нерва, которое фиксировалось на держалки, далее проводился обход полых вен до восходящей аорты. После начала искусственного кровообращения, проводилось охлаждение всего организма до 34 С. Зажим для пережатия аорты располагался на восходящей аорте через порт 1 (рисунок 2). Кардиоплегическая канюля была проведена через порт 1 в корень аорты для кровяной кардиопелегии (рисунок 2).
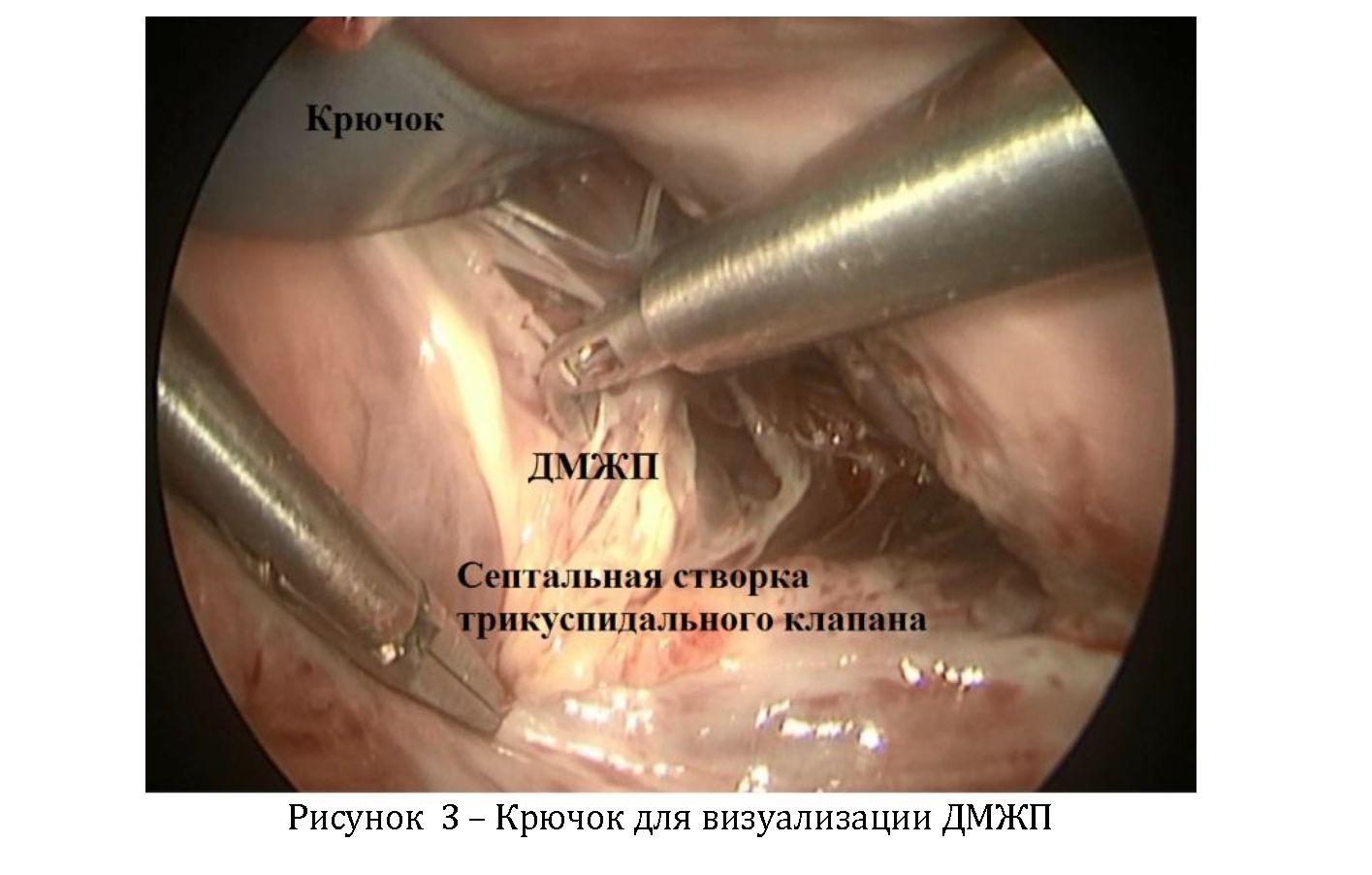
Затем после остановки сердца выполнялся разрез правого предсердия параллельно атриовентрикулярной борозде, которые также взяты на держалки. В области овальной ямки выполнялся 3 мм разрез для разгрузки левых отделов сердца. Передняя створка трехстворчатого клапана отведена крючком, чтобы визуализировать ДМЖП (рисунок 3).


Далее были выполнены пластики аутоперикардом обработанная глютаральдегидом или при дефекте менее 4 мм ушивание. Пластика трикуспидального клапана выполнена двоим пациентам после рассечения септальной створки для визуализации истинного ДМЖП. После закрытия ДМЖП, герметизация разреза в области овальной ямки и правого предсердия. Профилактика воздушной эмболии осуществляли через катетер расположенный на восходящей аорте с помощью отрицательного давления, дополнительно инсуфляция углекислым газом. После снятие зажима с восходящей аорты, согревание пациента до нормотермии. После стабилизации гемодинамики конец искусственного кровообращения.
Чреспищеводная эхокардиография проводилась для контроля герметичности заплаты, после расчетной дозы протамина сульфата выполняли гемостаз, в порт 3 устанавливалась дренажная трубка. Провели деканюляцию правой бедренной вены и артерии, правой яремной вены. Послойные швы на рану.
Результаты.
Среди проведенных коррекции ДМЖП пластика проводилась 6 пациентам, и 2 пациентам ушивание. Продолжительность операции 206Ã26 минут, время искусственного кровообращения составило 81Ã26 минут. После снятие зажима на восходящей аорте сердечная деятельность восстановилась самостоятельно у 6 пациентов, у 1 пациента восстановлен синусовый ритм после однократной наружной дефибриляции. Среднее время нахождение в отделении реанимации составило 16,5Ã2,2 часов, время нахождение на искусственной вентиляции легких составило 102Ã24минут, койко дни после операции 5Ã0,7 дней, интраоперационная кровопотеря 109Ã55мл. Также отмечается снижение боли в области послеоперационных ран, только в течение 3-х дней после операции применялись обезболивающие препараты. Восстановление целостности трикуспидального клапана выполнена 2 пациентам после коррекции ДМЖП. При контрольной эхокардиографии не выявило ни одного случая недостаточности трикуспидального клапана.
Все 8 операций с использованием полной торакоскопической коррекции ДМЖП были выполнены успешно. Послеоперационных осложнений не наблюдалось, конверсий в стандартный метод не было. У 1 пациента отмечается нарушение чувствительности в паховой области на стороне канюляции, которая через 1 месяц полностью восстановилась. У 1 пациента отмечался ателектаз легкого справа, которое так же после дыхательных упражнений легкое расправилось в течении первых суток.
Всем пациентам перед выпиской выполнена трансторакольная эхокардиография без признаков остаточного шунта, также проводили ультразвуковое исследование сосудов нижних конечностей с доплерографией, проходимость сохранены, признаков стеноза не отмечено.
После перенесенной торакоскопической коррекции ДМЖП все пациенты были удовлетворены косметическим эффектом.
Обсуждение.
Компьютеризированная телемикроманипуляция или роботизированная система является новым устройством для минимально инвазивной хирургия сердца. С помощью этого устройства, хирурги могут манипулировать небольшим инструментом через небольшие надрезы грудной клетки, чтобы выполнить процедуры, которые были ранее возможны только при открытой экспозиции [2]. Полностью эндоскопический метод был использован для коррекции ДМПП [6-10], лечение фибрилляции предсердий [11] и аортокоронарного шунтирования [12]. Хотя эффективность и безопасность полностью эндоскопической техники все еще на стадии оценки, недавние клинические результаты по коррекции ДМПП были весьма обнадеживающими, поскольку операция может быть выполнена безопасно, без перехода на конверсию на срединную продольную стернотомию или миниторакотомию во всех случаях [5-10]. Возможный недостаток, который может помешать широкому использованию полностью эндоскопической техники, является опора на роботизированную хирургическую систему. Сложность и стоимость этих компьютеризированных систем может быть проблемой для Казахстана.
На сегодняшний день существуют единичные опубликованные данные про полностью торакоскопическое закрытие ДМПП. Исследователи сообщают, что при эндоскопической коррекции ДМПП время ИК было от 122 до 135 минут и пережатие аорты от 32 до 70 минут [5-10]. Поэтому наши интраоперативные данные по сравнению с ними выгодно отличаются, хотя коррекция ДМЖП является технически более сложным, чем закрытия ДМПП. Эти результаты свидетельствуют о том, что после некоторых пациентов, оператор может достичь компетентности для полностью торакоскопической коррекции ДМЖП, даже без помощи роботизированной системы. Одним из потенциальных ограничений в этом одноцентровом исследовании является то, что лишь небольшая группа пациентов была вовлечена. Эффективность и безопасность отдаленных результатов торакоскопической техники еще предстоит определить на большом количестве пациентов.
Заключение.
В данном исследовании с применением полной торакоскопической эндоскопической техники коррекции ДМЖП получили хорошие результаты, и эти данные свидетельствуют о том, что полностью торакоскопическое закрытие перимембранозного ДМЖП без помощи роботизированной системы это практически осуществимо и безопасно. Данный метод может быть применен в клинической практике в будущем.
СПИСОК ЛИТЕРАТУРЫ
- 1 Xing Q., Pan S., An Q., Zhang Z., Li J., Li F., et al. Minimally invasive perventricular device closure of perimembranous ventricular septal defect without cardiopulmonary bypass: multicenter experience and mid-term follow-up // J. Thorac. Cardiovasc. Surg. - 2010. -Vol. 139. -Р. 1409-1415.
- Vistarini N., Aiello M., Mattiucci G., Alloni A., Cattadori B., Tinelli C., et al. Port access minimally invasive surgery for atrial septal defects: a 10-year single center experience in 166 patients // J. Thorac. Cardiovasc. Surg. - 2010. -Vol. 139.-Р. 139145.
- Doll N., Walther T., Falk V., Binner C., Bucerius J., Borger M.A., et al. Secundum ASD closure using a right lateral minithoracotomy five-year experience in 122 patients // Ann. Thorac. Surg. -2003.-Vol. 75.-Р. 1527-1531.
- Falk V., Walther T., Autschbach R., Diegeler A., Battellini R., Mohr F.W. Robot-assisted minimally invasive solo mitral valve operation // J. Thorac. Cardiovasc. Surg. -1998. -Vol.115. -Р. 470-471.
- Wimmer-Greinecker G., Dogan S., Aybek T., Khan M.F., Mierdl S., Byhahn C., et al. Totally endoscopic atrial septal repair in adults with computer-enhanced telemanipulation // J. Thorac. Cardiovasc. Surg. - 2003. -Vol.126. -Р.465-468.
- Argenziano M., Oz M.C., Kohmoto T., Morgan J., Dimitui J., Mongero L., et al. Totally endoscopic atrial septal defect repair with robotic assistance // Circulation. - 2003. -Vol. 108 (suppl 2). -Р. 191-194.
- Bonaros N., Schachner T., Oehlinger A., Ruetzler E., Kolbitsch C., Dichtl W. et al. Robotically assisted totally endoscopic atrial septal defect repair: insights from operative times, learning curves, and clinical outcome // Ann. Thorac. Surg. -
- -Vol.82. -Р. 687-693.
- Morgan J.A., Peacock J.C., Kohmoto T., Garrido M.J., Schanzer B.M., Kherani A.R., et al. Robotic techniques improve quality of life in patients undergoing atrial septal defect repair // Ann. Thorac. Surg. - 2004. -Vol. 77. -Р. 1328-1333.
- Torracca L., Ismeno G., Alfieri O. Totally endoscopic computer - enhanced atrial septal defect closure in six patients // Ann. Thorac. Surg. - 2001. -Vol. 72. -Р. 1354-1357.
- Ma Z.S., Dong M.F., Yin Q.Y., Feng Z.Y., Wang L.X. Totally thoracoscopic repair of atrial septal defect without robotic assistance: a single-center experience // The Journal of Thoracic and Cardiovascular Surgery.- 2011. Vol.-141. P.-13801383.
- Loulmet D.F., Patel N.C., Patel N.U., Frumkin W.I., Santoni - Rugiu F., Langan M.N., et al. First robotic endoscopic epicardial isolation of the pulmonary veins with microwave energy in a patient in chronic atrial fibrillation // Ann. Thorac. Surg. - 2004. -Vol.78. -Р. 24-25.
- Canniere D., Wimmer - Greinecker G., Cichon R., Van Praet F., Seshadri Kreaden U., Falk V. Feasibility, safety, and efficacy of totally endoscopic coronary artery bypass grafting: multicenter European experience // J. Thorac. Cardiovasc. Surg. -
- -Vol.134. -Р. 710-716.