Цель исследования - оценить безопасность и эффективность минимально инвазивной торакоскопической технологии коррекции ДМПП. Проанализированы 98 пациентов, которые разделены на 2 группы: 1 группа–33(34%) пациента оперированные торакоскопический, 2 группа–65(66%) больных оперированные миниторакотомией. В результате у больных отмечается уменьшение болевого синдрома, снижение кровопотери во время операции, короче нахождение в отделение реанимации, более ранняя выписка из стационара, более значимый косметический эффект.
Введение.
Минимально инвазивная хирургия сердца в последнее десятилетие завладевает большую популярность. Коррекция врожденных пороков сердца наряду с хирургическим лечением ишемической болезни и приобретенных пороков сердца стала областью интенсивного развития применения миниинвазивных торакоскопичеких технологий [1-4].
Открытая коррекция ДМПП двигалась в сторону минимально инвазивной хирургии сердца, особенно с помощью эндоскопических инструментов с периферической канюляцией искусственного кровообращения (ИК) [5-11]. Так называемая, полностью эндоскопическая коррекция ДМПП, стала возможным с помощью роботизированных систем, во многих исследованиях они показали отличный успех и низкий уровень осложнений [12-17]. Лишь в двух отдельных исследованиях имелись сообщения об успешных устранении ДМПП проводимых полностью эндоскопическим методом без робот - асситированной хирургической системы «Dа Vinchi» [18,19]. Для Республики Казахстан применения робот - ассистированной хирургической системы «da Vinci» не выгодна и не рентабельна для стационара, вполне эффективно и безопасно выполнимо хирургом без робот - ассистированной технологии. [11,18,19]. В Республике Казахстан имеются сообщения о сравнительном анализе клинических результатов пациентов при коррекции ДМПП оперированных из передней миниторакотомии и традиционной стернотомией [20]. Эти исследования основаны на опыте одного центра и на небольшом количестве пациентов, от которого было трудно сделать окончательный вывод о безопасности и эффективности минимально инвазивной техники с применением эндоскопического оборудования, однако анализ литературных данных показывает об отсутствии аналогичных исследований в Республике Казахстан.
Поэтому нами было решено оценить безопасность и эффективность минимально инвазивной торакоскопической технологии коррекции ДМПП без робот - ассистированной хирургической системы «Dа Vinchi», при помощи сравнительного анализа результатов хирургического лечения ДМПП из торакоскопического и миниторакотомического доступа.
Материалы и методы исследования.
Данное исследование было одобрено локальной этической комиссией, Казахского национального медицинского университета им С.Д. Асфендиярова (протокол №5) от 27.05.2015г. Письменное информированное согласие было получено от всех пациентов и родителей детей.
За период с июня 2015 по октябрь 2016 года анализированы 98 пациентов, которые разделены на 2 группы: 1 группа больных, которым была проведена операция торакоскопическим методом - 33 случая (34%), 2 группа больных, которым выполнена коррекция миниторакотомическим доступом - 65 случаев (66%).
По дизайну исследование ретроспективное. Критериями включения были следующие: возраст более 5 лет, масса тела более 20 кг, давление в легочной артерии более 60 мм рт.ст., отсутствие в анамнезе операций или заболевания легких на правой стороне грудной клетки, отсутствие заболеваний сосудов нижних конечностей. В данное исследование вошли только пациенты с изолированными дефектами межпредсердной перегородки сердца, тогда как пациенты в сочетании с другими врожденными пороками сердца, такие как стеноз легочной артерии и дефект межжелудочковой перегородки исключались из исследования. Также пациенты, которые не в состоянии дать информированное согласие на торакоскопическое хирургическое лечение, были исключены из исследования.
Все пациенты были обследованы по алгоритму, принятому в Центре: рентгенография органов грудной клетки в прямой проекции, ЭКГ, ЭХО-КГ. Основную роль в определении выбора тактики оперативного лечения основывались на ЭХОКГ. По данным рентгенографии органов грудной клетки определялись подходящие точки для установки мягких портов. Проводилась хронометрия общей продолжительности операции, времени искусственного кровообращения, кровопотери, нахождение в отделение интенсивной терапии, время искусственной вентиляции легких, койко дни после операции, применение анальгетиков с целью обезболивания.
|
Параметры |
Группа 1- Торакоскопический метод |
Группа 2- миниторакотомический доступ |
Р-оценка |
|
Общее количество пациентов |
33 (34%), |
65(66%) |
|
|
Средний возраст, лет |
27,5 ã14,8 |
26,2 ã16,6 |
0,705 |
|
Вес, кг |
52,2 ã18,5 |
46 ±22,1 |
0,170 |
|
Рост, см |
145,9 ±23,8 |
150,7±24,6 |
0,358 |
|
Пол: мужчины женщины |
5 (16%) 28 (84%) |
13(20%) 52(80%) |
|
|
Функциональный класс сердечной недостаточности (NYHA): |
|||
|
I |
7(21%) |
11(17%) |
|
|
II |
24(73%) |
49(75%) |
|
|
III |
2(6%) |
5(8%) |
|
Таблица 1- основные характеристики пациентов
|
Параметры |
Группа 1- Торакоскопический метод |
Группа 2- миниторакотомический доступ |
Р-оценка |
|
ЭХОКГ |
|||
|
ПЖ, мм |
2,59 ±0,5 |
3,1±1,0 |
0,007 |
|
ФВ ЛЖ ¿ |
65±2 |
63±5 |
0,030 |
|
Qp / Qs |
2,1±0,2 |
2,2± 0,3 |
0,087 |
|
Диметр ДМПП, мм |
26±5 |
28±6 |
0,103 |
|
Давление в легочной артерии |
31±12 |
31±7 |
1,000 |
|
По локализации |
|||
|
Центральный |
4(12%) |
7(11%) |
|
|
Верхний |
6(18%) |
15(23%) |
|
|
Нижний |
22(67%) |
41 (63%) |
|
|
Синус венозус дефект |
1(3%) |
2(3%) |
|
|
Кардио - торакальный индекс, ¿ |
55±5 |
52±6 |
0,015 |
Таблица 2- Дооперационные инструментальные данные.
Хирургическая техника.
Операция проводят под общим инкубационным наркозом с применением двухпросветной эндотрахеальной трубки для обеспечения однолегочной вентиляции левого легкого во время работы хирурга, также снижают объем вентиляции и увеличение частоты дыхания, не влияющие на физиологические показатели кислотно-щелочного состояния. Затем анестезиологом проводилась канюляция правой яремной вены по Сельдингеру.
Положение больного на спине, под правой лопаткой плоский валик с подъемом правой половины грудной клетки на 20 градусов. После подготовки операционного поля, первым этапом проводится кожный разрез длиной 1,5-2,0 см походу 4 межреберья справа по передней подмышечной линии, после гемостаза устанавливают первый силиконовый порт - порт 1. Через этот порт вводят оптику диаметром 5 мм с углом обзора 30º фиксированный вспомогательной механической «рукой» (рисунок 1), который прикреплен к операционному столу.
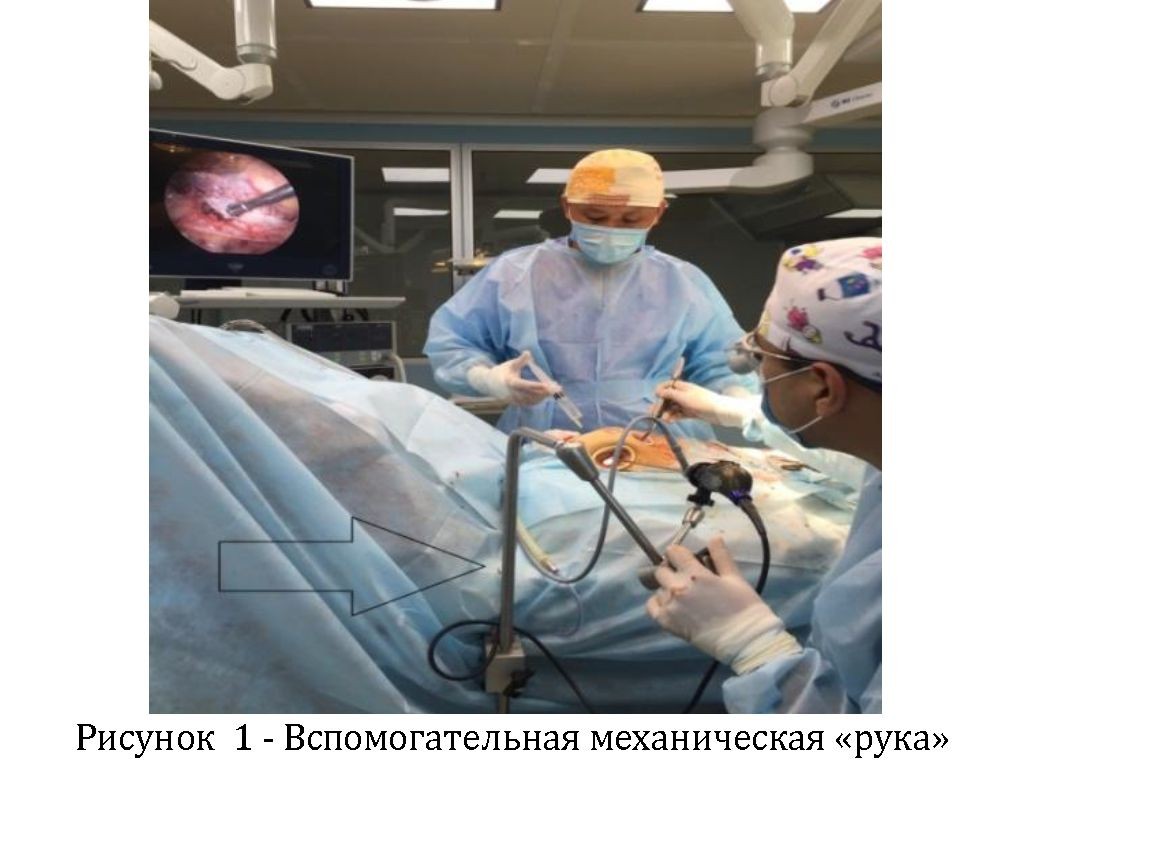
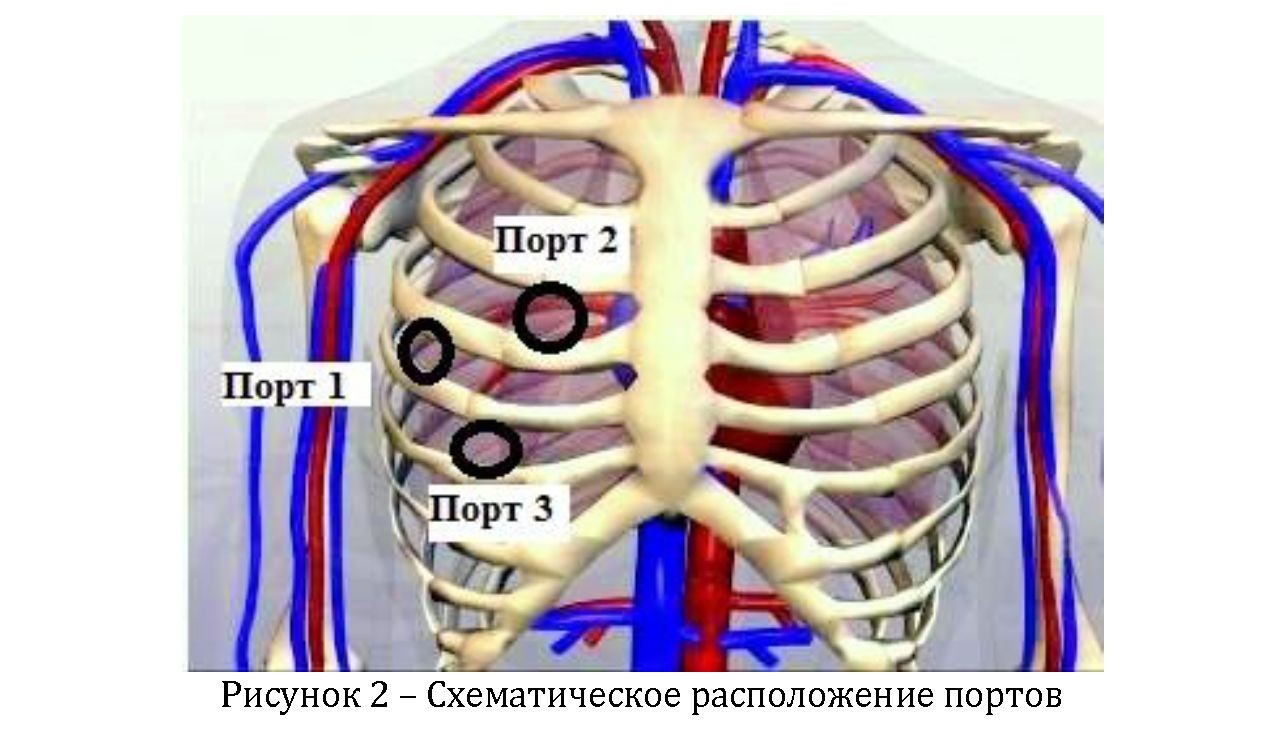
Затем во 2 - м межреберье справа по 2. Далее в 4-м межреберье справа по парастернальной линии латеральнее от правой среднеключичной линии устанавливают порт 3.
внутренней грудной артерии устанавливается порт -
|
Показатели |
Группа 1- Торакоскопический метод |
Группа 2- миниторакотомический доступ |
Р-оценка |
|---|---|---|---|
|
Длительность операции, мин |
260ã64 |
191ã42 |
0,0001 |
|
Длительность ИК, мин |
64ã22 |
38ã16 |
0,0001 |
|
Кровопотеря |
|||
|
Во время операций, мл |
85ã37 |
129ã92 |
0,010 |
|
Время нахождение в ОРИТ, часы |
16ã5 |
21ã6 |
0,0001 |
|
Время нахождения на ИВЛ, мин |
202ã133 |
211ã175 |
0,796 |
|
Сроки пребывания в стационаре после операции, дни |
6,4 ã 0,8 |
10,5ã4,8 |
0,0001 |
|
Применение анальгетиков |
|||
|
1 сутки, мг |
227ã58 |
266ã46 |
0,0001 |
Результаты.
Таблица 3- клиническая оценка эффективности
После установки всех портов (рисунок 2), выполняют доступ к бедренным артериям и венам для подключения аппарата искусственного кровообращения. Параллельно паховой связки поэтапно выделяют общую правую бедренную артерию и бедренную вену. После введения расчетной дозы гепарина, проводят канюляцию бедренной артерии расчетной канюлей, затем выполняют канюляцию общей бедренной вены расчетным диаметром. Обеспечение искусственного кровообращения осуществлялось путем канюляция бедренной артерии и вены Á правой яремной вены.
После чего, подключают систему искусственного кровообращения и начало перфузии с выключением искусственной вентиляции легких (ИВЛ). Рассекают продольно перикард по верхнему краю параллельно диафрагмальному нерву с отступом 3см выше с выкраиванием заплаты у нижнего края до устья нижней полой вены, причем верхний край до восходящей аорты. Для улучшения визуализации правого предсердия берут лоскут перикарда на две нити-держалки, и у верхнего и у нижнего края держалки выводятся через порт 1. Затем выделяют устье верхней и нижней полых вен, пережимают их турникетами. Выполняют продольную атриотомию правого предсердия до ушка правого предсердия, накладываются держалки на правое предсердие. Закрытие дефекта межпредсердной перегородки проводят заплатой из аутоперикарда путем наложения непрерывного обивного шва на работающем сердце. Дренирование крови осуществляют ассистентом кардиотомным отсосом с устья коронарного синуса. Для профилактики воздушной эмболии поддается постоянная инсуфляция СО2.
Чреспищеводная эхокардиография проводится во время всей операции, которая подтверждает адекватность проведенных манипуляций. Далее герметизация правого предсердия, последовательно отпускают турникеты полых вен и включают ИВЛ. После стабилизации гемодинамики заканчивают искусственное кровообращение. Проводят деканюляцию бедренной вены и бедренной артерии. Для нейтрализации гепарина вводят протамин сульфат в расчетной дозе. Выполняют тщательный хирургический гемостаз. Устанавливают дренаж в правую плевральную полость через - порт3 и заканчивают послойным швом на грудной клетки и паховой области.
Торакоскопическая коррекция проводилась с помощью эндоскопических инструментов Aesculap (Германия) и видеоэндоскопической стойки Karl Storz (Германия).
|
2 сутки, мг |
163ã47 |
244ã46 |
0,0001 |
|
3 сутки, мг |
93ã55 |
202ã47 |
0,0001 |
Как видно из таблицы 3, при использовании торакоскопической технологии хирургические манипуляции в операционной не были ограничены, поэтому среднее время пережатия аорты и длительность искусственного кровообращения существенно не отличались, тогда как общая продолжительность операции у больных, которым провели миниторакотомию, была меньше, чем у больных после торакоскопичской технологии. Мы это связываем с особенностью эндоскопической технологии, позволяющей безопасно работать и полностью оценить структуры сердца и магистральных сосудов применяя 16 кратное увеличение, эндоскопическими инструментами на большой глубине при минимальных кожных разрезах при закрытой грудной клетки, также с затратой времени на подключение искусственного кровообращения путем канюляции периферийных сосудов. Однако, у больных после торакоскопической технологии отмечается уменьшение болевого синдрома, снижение кровопотери во время операции, короче нахождение в отделение реанимации и интенсивной терапии, более ранняя выписка из стационара, время искусственной вентиляции легких меньше, но статистически не значима.
Все случаи закрытия ДМПП сердца были успешные. Не отмечались осложнений: конверсий, неврологического дефицита, послеоперационной смертности, повторной операции по поводу кровотечения.
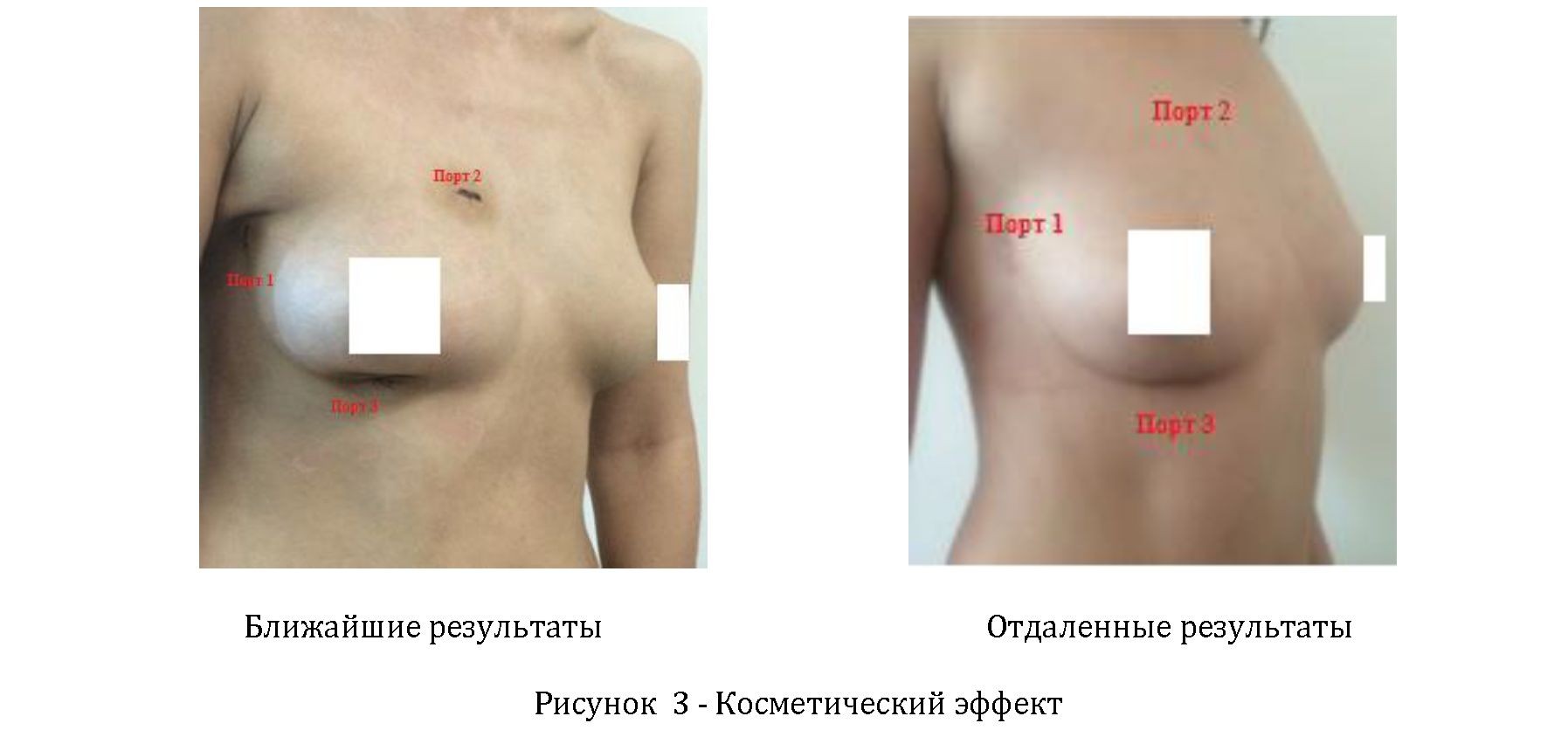
Из особенностей выполнения операции следует отметить, что у 84% пациентов женского пола после операции были отмечены удовольствие от косметического эффекта, как в ближайшие, так и в отдаленные сроки после операции (рисунок 3).
Обсуждение.
С момента введения роботизированная сердечной хирургии в 1997 году, [1-4] было проведено несколько исследований по эндоскопической коррекции врожденных пороков сердца, в частности ДМПП. В начале роботизированная эндоскопическая технология использовалась для улучшения визуализации внутрисердечных структур путем эндоскопического управления камерой и для облегчения манипуляций хирургическими инструментами через ограниченные порты. Позже, некоторые авторы сообщали полную торакоскопическую коррекцию ДМПП через три надреза, с высокой вероятностью успеха и очень мало осложнений и без перехода на стернотомный и торакотомный доступ [5,12-15].
Полная эндоскопическая коррекция ДМПП приводит к минимальной травматичности, к ускорению послеоперационного восстановления и улучшению качества жизни, однако продолжительность нахождения в стационаре особо не изменилась [15].
Хирургическое устранение ДМПП эндоваскулярным путем с применением катетерной технологии являются одним из методов миниинвазивного закрытия ДМПП со всеми краями [2,14,17]. Тем не менее, которым противопоказаны катетерное закрытие, направляются на открытые хирургические методы с использованием эндоскопии [11-13]. В связи с развитием роботизированной технологии и периферической канюляции, полное эндоскопическое закрытие ДМПП успешно проводятся в ряде центров развитых стран [9,10]. Так как Казахстан все еще развивающая страна роботизированная технология не выгодна (слишком дорого). По этой причине полностью эндоскопическая минимально инвазивная хирургия сердца внедряется в повседневную практику без роботизированной помощи.
Torracca et al. [16] сообщили о сложностях роботизированных хирургических методов и высокой финансовых затрат, связанных с обслуживанием техники, они выявили, что его трудно использовать широко, в частности, в развивающихся странах.
Ма et al. [11,18,21] сообщили об усовершенствовании методики полной эндоскопической коррекции ДМПП без роботизированной помощи, они полагают, что с точки зрения технических деталей и результатов роботизированной и не роботизированная полностью эндоскопическое закрытие ДМПП имеют схожие показатели успеха и частоту осложнений.
Позже Ма выявил, что полная эндоскопическая коррекция ДМПП приводит к более быстрому восстановлению физической функции и улучшению качества жизни по сравнению со стандартной стернотомией.
В то же время Bonaros N. et al. [14] выявили ряд преимуществ полной эндоскопической коррекции ДМПП по сравнению со стернотомным доступом, что: общая продолжительность операции, время искусственной вентиляция легких, продолжительность пребывания в отделении интенсивной терапии и нахождения в стационаре короче; меньшая послеоперационная боль; быстрое восстановление трудоспособности и продолжение обучение. Таким образом, полностью эндоскопическая технология закрытия ДМПП, улучшает качество жизни, чем обычные стернотомия. Xu et al. [22] сообщили, что в последнее время один из минимально инвазивных часто используемых доступов – является правостороння миниторакотомия. Они показали отличные результаты коррекции ДМПП миниторокотомии справа относительно стернотомных разрезов, кроме того, при сравнении торакотомных и торакоскопических разрезов у женщин, они выявили, что при торакотомии длина разреза больше, расположен ближе к грудине, что вызывает асимметрию молочных желез и неудовлетворительность рубцом.
В нашем исследовании определены те же преимущества торакоскопической технологии по сравнению с правосторонней миниторакотомией. На наш взгляд дынный метод является безопасным, эффективным и выполнимо без роботизированной помощи.
Выводы
Таким образом, выполнение операций торакоскопическим способом позволяет открыть новые возможности для мининвазивной хирургии сердца, как альтернатива для миниторакотомии. Основным преимуществом торакаскопического доступа является максимальное снижение травматичности, позволяющий сохранить грудино- реберный каркас грудной клетки, уменьшить интенсивность болевого синдрома и общую кровопотерю, что позволит уменьшить сроки пребывания в стационаре и достигнуть косметический эффект.
Данные операции являются перспективными и могут выполняться с высокой долей эффективности и надежности.
СПИСОК ЛИТЕРАТУРЫ
- 1 Chitwood W.R., Wixon C.L. Video-assisted minimally invasive mitral valve surgery // J. Thorac. Cardiovasc. Surg. -1997. –Vol.114.-Р. 773-779.
- Бокерия Л.А., Алекян Б.Г., Подзолков В.П. Эндоваскулярная и минимально инвазивная хирургия сердца и сосудов у детей. - М.: Изд-во Медицина, 1999. – 321 с.
- Mishra Y.K. Minimaly invasive mitral valve surgery through right anterolateral minithoracotomy // Ann. Thorac. Surg. - 1999. -Vol. 68. - Р. 1520-1524.
- Falk V., Walther T., Autschbach R., Diegeler A., Battellini R., Mohr F.W. Robot assisted minimally invasive solo mitral valve operation //J. Thorac. Cardiovasc. Surg. -1998.-№115.-Р.470-471.
- Vistarini N., Aiello M., Mattiucci G., Alloni A., Cattadori B., Tinelli C. Port-access minimally invasive surgery for atrial septal defects: a 10-year single-center experience in 166 patients // Journal of Thoracic and Cardiovascular Surgery. - 2010. - № 139. – Р. 139–145.
- Doll N., Walther T, Falk V, Binner C, Bucerius J, Borger MA, et al. Secundum asd closure using a right lateral minithoracotomy: Five-year experience in 122 patients // Ann. Thorac. Surg. -2003. -№ 75. –Р.1527–1530.
- Black MD., Freedom RM. Minimally invasive repair of atrial septal defects // Ann. Thorac. Surg. -1998.-№ 65. -Р. 765–767.
- Izzat MB., Yim AP., Chang CH., Lin PJ., Mavroudis C., Shetty DP, et al. Minimally invasive direct atrial septal defect closure // Ann. Thorac. Surg. -1997. -№ 63. -Р. 1831–1834.
- Zhang Z.W., Zhang X.J., Li C.Y., Ma L.L., Wang L.X. Technical aspects of anesthesia and cardiopulmonary bypass in patients undergoing totally thoracoscopic cardiac surgery // J. Cardiothorac. Vasc. Anesth. -2012. -№ 26. –Р. 270–273.
- Dong M.F., Ma Z.S., Wang J.T., Chai S.D., Tang P.Z., Wang L.X. Effect of preoperational mechanical ventilation on short- term postoperative outcomes in patients with severe tetralogy of fallot // Heart. Lung Circ. -2012;-№21. –Р. 679–683.
- Ma Z.S., Wang J.T., Dong M.F., Chai S.D., Wang L.X. Thoracoscopic closure of ventricular septal defect in young children: technical challenges and solutions // Eur. J. Cardiothorac. Surg. –2012. -№ 42. –Р.976–979.
- Wimmer-Greinecker G., Dogan S., Aybek T., Khan M.F., Mierdl S., Byhahn C. Totally endoscopic atrial septal repair in adults with computer-enhanced telemanipulation // J. Thorac. Cardiovasc. Surg.- 2003. -№ 126. –Р. 465–468.
- Argenziano M., Oz M.C., Kohmoto T., Morgan J., Dimitui J., Mongero L. Totally endoscopic atrial septal defect repair with robotic assistance // Circulation.-2003-.№108. –Р. 191–194.
- Bonaros N., Schachner T., Oehlinger A., Ruetzler E., Kolbitsch C., Dichtl W. Robotically assisted totally endoscopic atrial septal defect repair: insights from operative times, learning curves, and clinical outcome // Ann. Thorac. Surg. -2006. –№ 82. –Р. 687–693.
- Morgan J.A., Peacock J.C., Kohmoto T., Garrido M.J., Schanzer B.M., Kherani A.R. Robotic techniques improve quality of life in patients undergoing atrial septal defect repair// Ann. Thorac. Surg.- 2004. -№ 77.-Р.1328–1333.
- Torracca L., Ismeno G., Alfieri O. Totally endoscopic computer-enhanced atrial septal defect closure in six patients // Ann. Thorac. Surg.- 2001.-№72. -Р.1354–1357.
- Ak K., Aybek T.,Wimmer-Greinecker G., Ozaslan F., Bakhtiary F., Moritz A. Evolution of surgical techniques for atrial septal defect repair in adults: a 10-year single-institution experience // J. Thorac. Cardiovasc. Surg.- 2007.-№ 134.-Р.757–764.
- Ma Z.S., Dong M.F., Yin Q.Y., Feng Z.Y., Wang L.X. Totally thoracoscopic repair of atrial septal defect without robotic assistance: a single-center experience // The Journal of Thoracic and Cardiovascular Surgery.- 2011. Vol.-141. P.-13801383.
- 19. Л.К. Кошербаева, К.К. Куракбаев, А.Б. Кумар, А.Д., Дуйсекевеев, К.Т. Надырова, Ж.А. Оценка экономической эффективности внедрения робот- асситированной хирургической системы «Dа Vinchi» // Вестник КазНМУ.- 2014.- №4. -С.434-438.
- Джошибаев С.‚ Шейшенов Ж.О., Нарбаев Д.А., Сравнительный анализ клинических результатов пациентов, оперированных из передней миниторакотомии и традиционной стернотомии // Центрально-азиатский Медицинский Журнал. - 2010. - №3. - С. 180-184.
- Ma Z.S, Yin Q.Y, Dong M.F., Feng Z.Y.,Wang L.X. Quality of life in patients undergoing totally thoracoscopic closure for atrial septal defect // Ann.Thorac. Surg.- 2011.-№ 92. -Р. 2230-2234.
- Ming Xu., Shaoping Zhu., Xianguo Wang., Hua Huang and Jinping Zhao. Two Different Minimally Invasive Techniques for Female Patients with Atrial Septal Defects: Totally Thoracoscopic Technique and Right Anterolateral Thoracotomy Technique // Ann. Thorac. Cardiovasc. Surg. -2015.-№ 21.-Р. 459-465