На полученной модели экспериментального пародонтита у кроликов изучены клинико-рентгенологические результаты операции остеогингивопластики с пластикой послеоперационной костной полости композитным материалом на основе костного коллагена, гидроксилапатита и аутологичных мультипотентных мезенхимальных стромальных клеток жировой ткани.
Воспалительно-деструктивные заболевания тканей пародонта представляют собой весьма важную и актуальную проблему современной стоматологии в связи с многофакторной этиологией, сложностью патогенеза, сравниельно кратковременной ремиссией большинства лечебных мероприятий [1,2]. При лечении генерализованного пародонтита важнейшими задачамиявляются купирование процессов воспаления и обеспечение оптимальных процессов репаративной регенерации костной ткани альвеолярного отростка челюсти, утраченных в результате воспалительной резорбции [3,4] .
Вопросы репаративной регенерации тканей пародонта до настоящего времени продолжают оставаться актуальными, поскольку до настоящего времени еще не решена проблема полноценного восстановления опорного аппарата зуба, разрушенного в результате постоянно прогрессирующего воспалительно - деструктивного процесса. Учитывая, что восстановление тканей пародонта предусматривает восполнение утраченных структур, включая кость альвеолярного отростка, внимание большинства исследователей было направлено на замещении утраченной костной ткани различными трансплантационными и имплантационными материалами [5,6]. Однако, многочиленные исследования показали, что использование биологических пластических материалов, способно лишь временно улучшить клиническое состояние тканей пародонта и рентгенологическую картину кости альвеолы [7,8,9].
Параллельно с ранее предложенными методами комплексного лечения воспалительно-деструктивных процессов в тканях пародонта, развивался и принципиально иной подход к восстановлению кости, основанный на принципе направленной тканевой регенерации с использованием мембранной техники. Клиникогистологические исследования показали, что регенерат, сформированный в подмембранном пространстве, является органотипичным, подвергаясь последующему созреванию в хорошо дифференцированные ткани опорного аппарата зуба [6].
Последующие исследования показали, что для привлечения клеток в зону регенерации и высокого уровня их пролиферативной активности необходимо наличие достаточного объёма сохраненных витальных структур, ограничивающих дефект, и оптимальное кровоснабжение зоны поврежденных тканей, что в клинике встречается не так уж сравнительно часто. В результате, развившегося воспалительно-деструктивного процесса в пародонте, потеря опорных тканей составляет 50% и более, наблюдается значительный дефицит клеточных форм, способных регенерировать новые ткани взамен утраченных [2, 10].
В последние десятилетия многие исследователи сосредоточили свое внимание на стимуляции резидентных клеток-предшественников полипептидными факторами роста [2, 7,11]. Известна уникальная способность костного морфогенетического белка (КМБ) индуцировать костное образование в эктопических зонах. В эксперименте на животных было изучено действие этого белка на регенерацию периодонтальной связки, цемента корня зуба и кости альвеолы. Было отмечено, что при имплантации в область пародонтального дефекта рекомбинантного КМБ-2 наблюдался анкилоз корней зубов и их резорбция в проксимальном отделе. Недавно эти данные были подтверждены: обнаруживалось формирование новой периодонтальной связки лишь в нескольких случаях и только на отдельных участках корневой поверхности [12]. Дальнейшие исследования показали, что потенциальными митогенными и хемотаксическими белками для фибробластов периодонтальной связки и клеток кости зубной альвеолы, а также улучшающими ангиогенез, является тромбоцитарный фактор роста и инсулиноподобный фактор роста -1. В стоматологическую практику уже внедрена простая методика использования возможностей тромбоцитарного геля, полученного из периферической крови пациента, при замещении дефектов пародонта и альвеолярной кости[2,7].
В современной регенеративной медицине на лидирующие позиции выходят исследования в области клеточной биологии, направленные на изучение стволовых клеток, в которых заложены колоссальные терапевтические возможности. Термин «стволовая клетка» определяет популяцию тканевых или циркулирующих в крови низкодифференцированных клеток-предшественников, обладающих способностью к самообновлению путем асимметричного деления и дифференцировке в клеточные компоненты различных тканей [13,14].
Неограниченным пролиферативным потенциалом и возможностью дифференцировки invivo и invitro более чем в 200 различных клеточных типов (производные трёх зародышевых листков) обладают эмбриональные СК [15,16]. Трансплантируемые клетки, обеспечивающие непосредственное восстановление костной ткани denovo, представляют собой культуру остеогенных клеток- предшественников, которые могут быть получены путем направленной дифференцировки мультипотентных мезенхимальных стромальных клеток (ММСК) костного мозга, жировой ткани или других источников, таких, как надкостница, селезенка, тимус, плацента и др. [17]. Однним из перспективных источников ММСК является жировая ткань (ЖТ). Исследования иммуннофенотипа ММСК из жировой ткани и красного костного мозга показали, что они практически идентичны друг другу. Однако при этом они обладают значительными преимуществами, важными из которых являются сравнительная доступность, простота и безопасность их получения в сравнении с методиками забора стволовых клеток из других [18,19,20,21].
В настоящее время в пластической хирургии широко используется костный коллаген и имплантационный материал – гидроксиапатит (ГА). К основным достоинствам костного коллагена, как пластического материала, следует отнести его свойство оптимизировать репаративный остеогенез, низкую токсичность и антигенность, устойчивость к тканевым протеазам [22]. На экспериментальной модели локального пародонтита у кроликов изучить особенности заживления краевых дефектов альвеолярного отростка при пластике их разработанным нами трансплантатом [23,24].
Целью работы явилось получение модели экспериментального локального пародонтита, выделение стволовых клеток из жировой ткани кролика с последующим изучением клинико-рентгенологических особенностей заживления краевых дефектов альвеолярного отростка при пластике их разработанным нами трансплантатом.
Материалы и методы исследования. Экспериментальное исследование произведено на 18 кроликах породы «Шиншилла» весом 3500 – 4500 грамм, которым на первом этапе эксперимента воспроизводился локальный пародонтит. Животные разделены на две равные группы - контрольная и подопыная.У подопытных животных сразу после наложения проволочных лигатур забирался жир из брюшной полости и отправлялся в лабораторию для приготовления ММСК. Спустя две недели после наложения лигатур в области развившегося локального пародонтита формирорвался костный дефект в межкорневой перегородке центральных резцов нижней челюсти диаметром 2 мм и проводилась операция – остеогингивопластика при этом в контрольной группе животных послеоперационная костная полость заполнялась композитным трансплантационным материалом на основе костного коллагена и гидроксилапатита в равных весовых пропорциях, а в опытной группе кроликов костный дефект замещался композитным материалом,отличающегося от биокомпозита, применяемого в контрольной группе тем, что в него дополнительно вводилась взвесь культуры аутологичных мультипотентных мезенхимальных стромальных клеток жировой ткани, выращенных в лаборатории ТОО «Научно-производственное предприятие «Антиген».
Результаты и обсуждения. Первым этапом нашего исследования заключалось в получении экспериментального пародонтита. Для этой цели кроликам под внутривенным наркозом 2% раствором Рометара и инфильтрационной анестезией 2% раствора лидокаина вокруг шеек центральных резцов нижней челюсти фиксировались лигатуры из танталовой проволоки диаметром 0,2 мм (Рисунок 1).
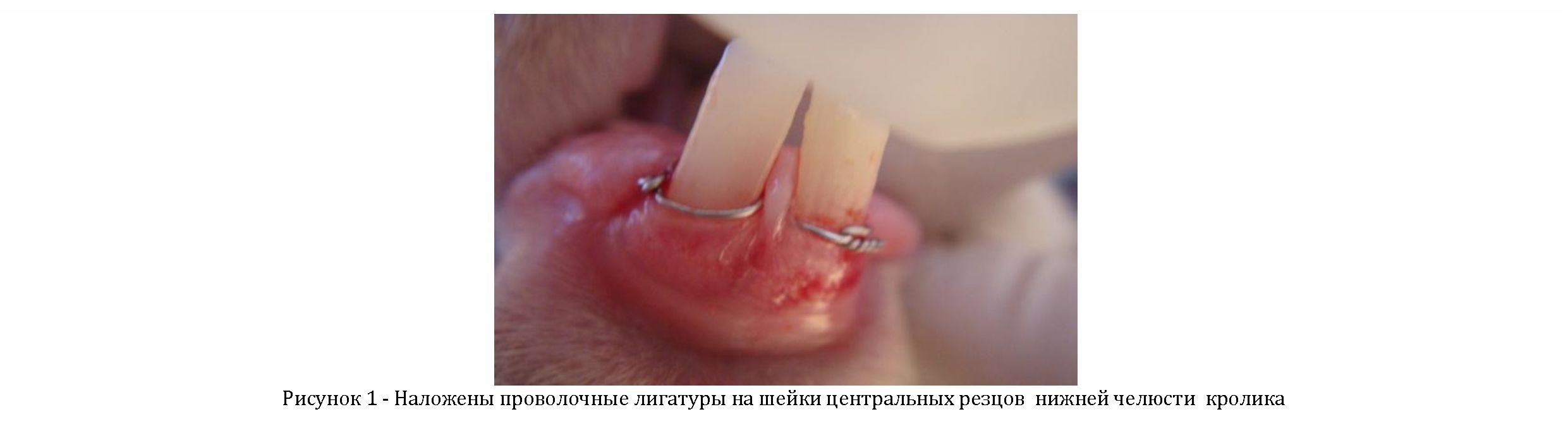 Кролики разделены на две группы по 9 животных (контрольная и подопытная).
Кролики разделены на две группы по 9 животных (контрольная и подопытная).
У подопытных кроликов сразу после наложения проволочных лигатур проводился забор жировой ткани из брюшной полости. Для этой цели с соблюдением асептики производился разрез по средней линии живота с последующим послойным вскрытием стенок брюшной полости (Рисунок 2).
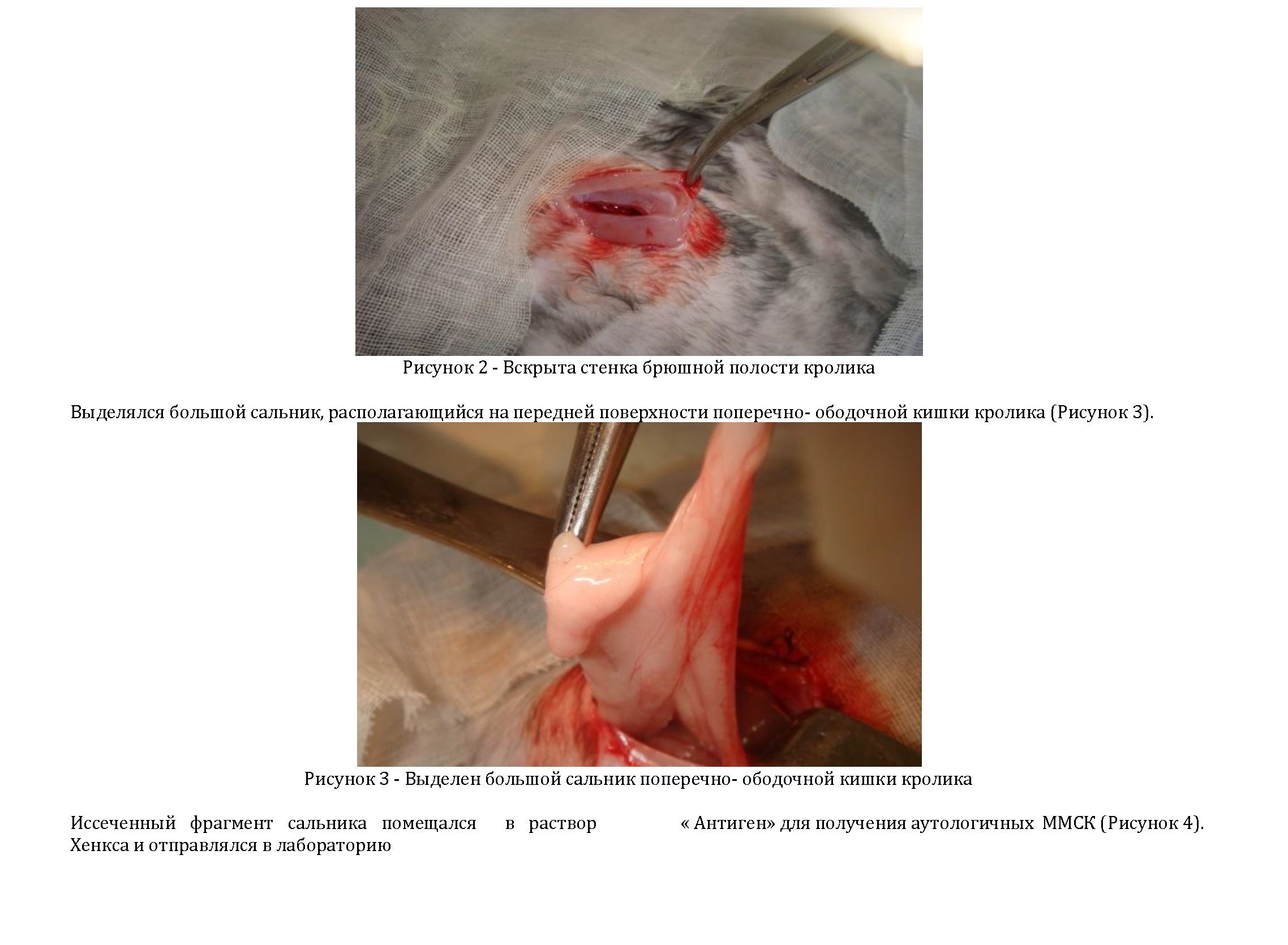
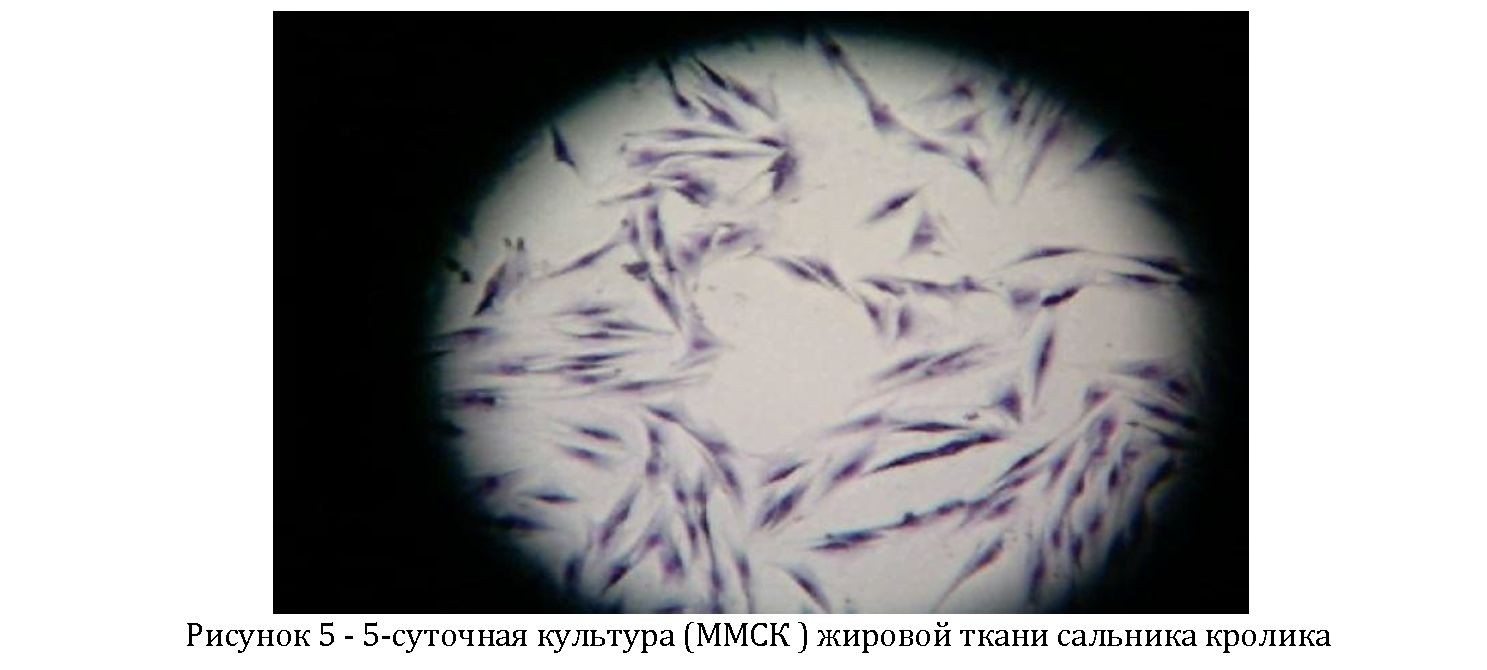
Для выделения стромально-васкулярной фракции жировой ткавни кролика, гомогенизированная жировая ткань промывалась стерильным раствором Хенкса и инкубировалась в течение 45 минут с 0,075% раствором коллагеназы I типа (Sigma) в фосфатно-солевом буфере (ФСБ) при 370С. Нейтрализация фермента проводилась равным объемом ФСБ, содержащего 10% эмбриональную телячью сыворотку. Суспензия клеток обрабатывалась лизирующим раствором для удаления эритроцитов в соотношении 1:10. Клетки отмывались центрифугированием, клеточный осадок ресуспендировался в 5 см3 среды DMEМ. Затем подсчитывали концентрацию клеток в см3. Полученную суспензию клеток отмывали раствором Хенкса центрифугированием при 1200 об/мин в течение 10 минут. Для выделения стромально-васкулярной фракции жировой ткавни кролика, гомогенизированная жировая ткань промывалась стерильным раствором Хенкса и инкубировалась в течение 45 минут с 0,075% раствором коллагеназы I типа (Sigma) в фосфатно-солевом буфере (ФСБ) при 370С. Нейтрализация фермента проводилась равным объемом ФСБ, содержащего 10% эмбриональную телячью сыворотку. Суспензия клеток обрабатывалась лизирующим раствором для удаления эритроцитов в соотношении 1:10. Клетки отмывались центрифугированием, клеточный осадок ресуспендировался в 5 см3 среды DMEМ. Затем подсчитывали концентрацию клеток в см3. Полученную суспензию клеток отмывали раствором Хенкса центрифугированием при 1200 об/мин в течение 10 минут. Полученную суспензию клеток разводили раствором Хенкса до концентрации 1000 000 клеток/см3 (Рисунок 5).
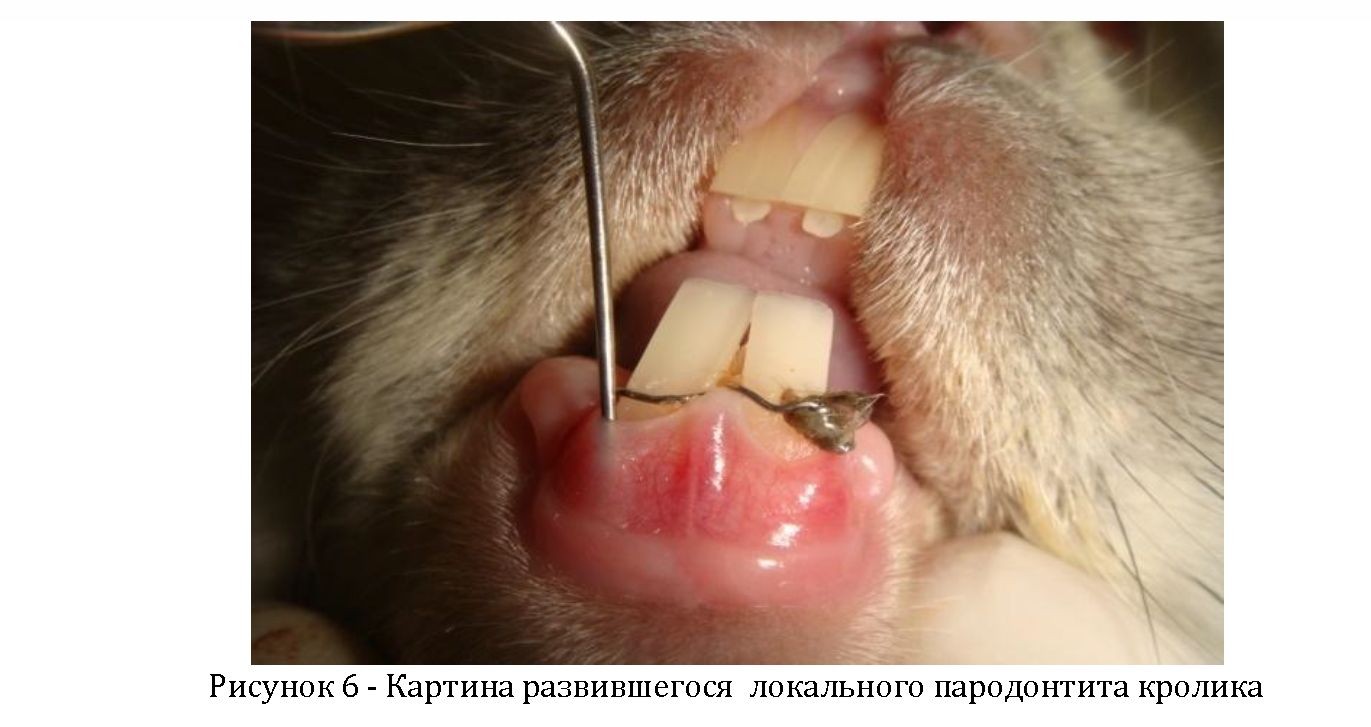
Через две недели после наложения проволочных лигатур на шейки центральных резцов у всех кроликов отмечалась картина локального пародонтита, выражающаяся наличием над и поддесневого зубного налета. Слизистая оболочка десны в области нижних резцов была отечной и гиперемированной. При пальпации в области маргинального края наблюдалась выраженная кровоточивость десны и незначительное выделение гноя из пародонтальных карманов. Средняя глубина карманов в области резцов составляла 3-4 мм. Подвижность центральных резцов в зоне полученного экспериментального пародонтита I степени (Рисунок 6).

Под внутривенным наркозом 2% раствором Рометара и инфильтрационной анестезией 2% раствора лидокаина удалялись проволочные лигатуры. С помощью пародонтологического набора инструментов LM 6840 XSi проводился тщательный кюретаж пародонтальных карманов с вестибулярной и язычной поверхностей алвеолярных отростков нижней челюсти, а затем
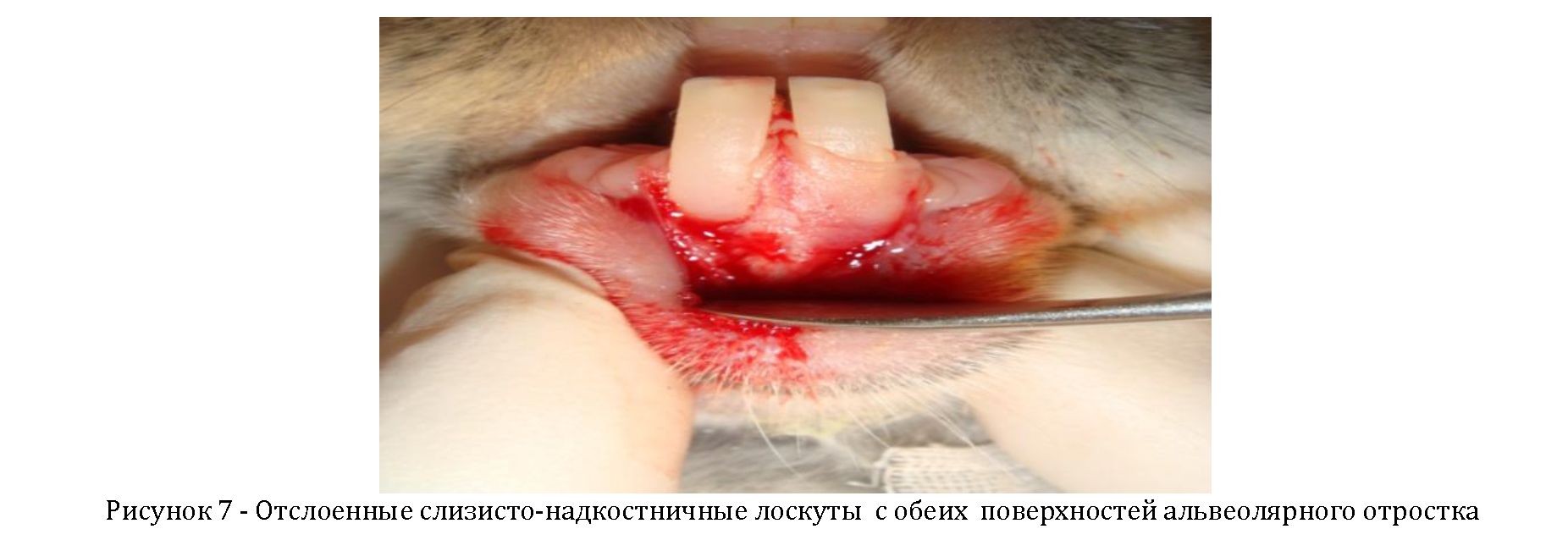
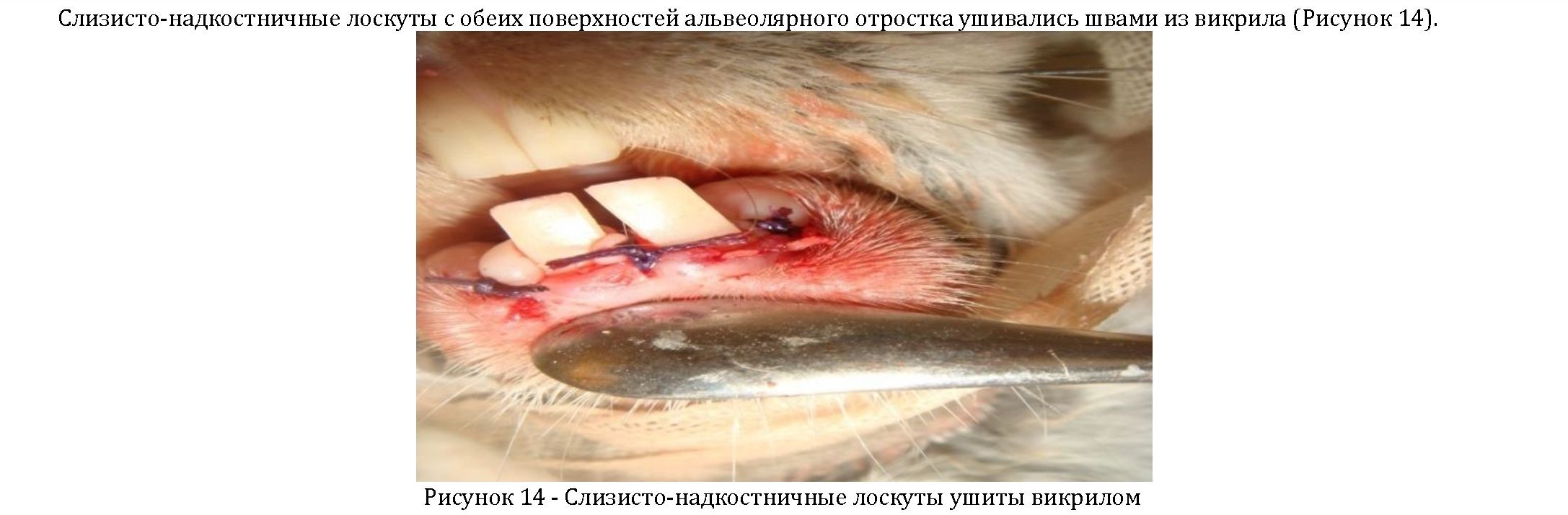
осуществлялся разрез по десневым сосочкам центральных резцов в области воспроизведенного пародонтита. С вестибулярной и язычной поверхностей альвеолярного отростка отслаивались слизисто-надкостничные лоскуты на максимальную глубину пародонтальных карманов (Рисунок 7).
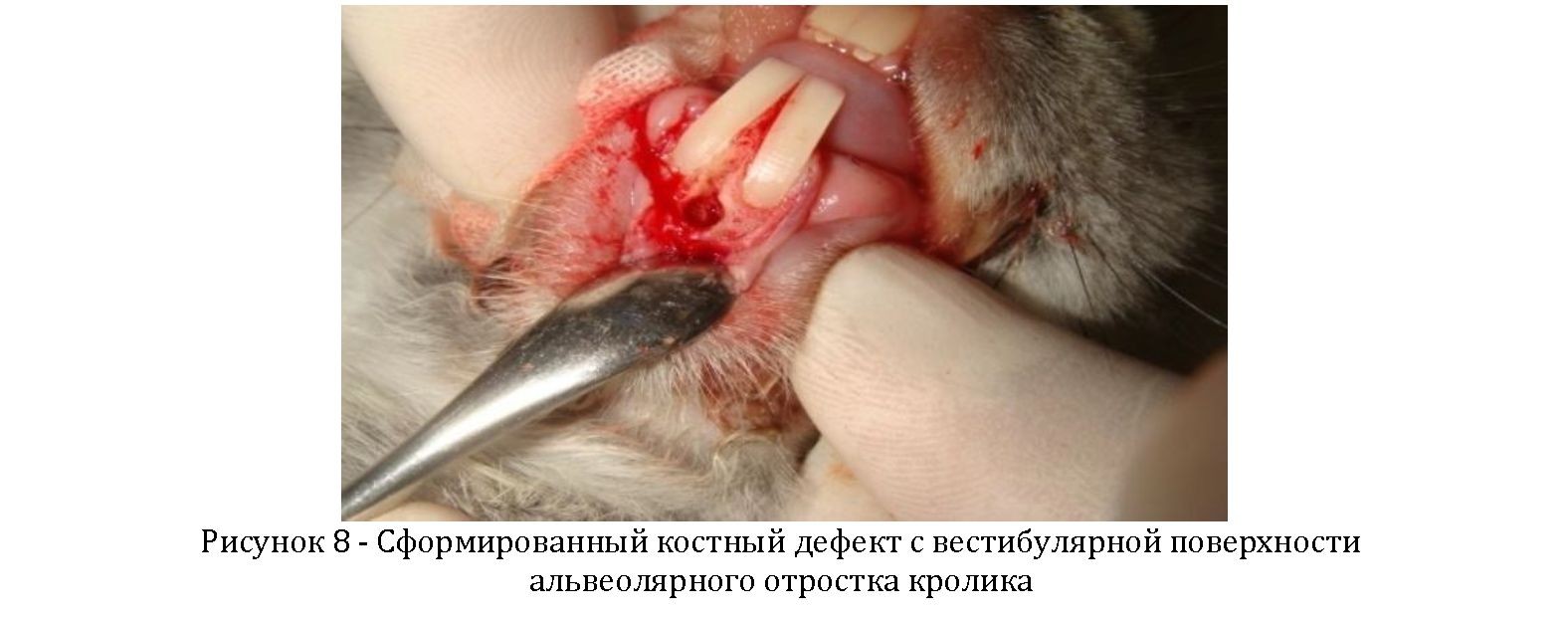
С помощью окончатой фрезы диаметром 2мм формировался костный дефект в межкорневой перегороке центральных резцов нижней челюсти кролика (Рисунок 8).
После промывания раны антисептиками костный дефект в коллагена ТОО «Н.П.П. «Антиген» и отечественного контрольной группы животных заполнялся гидроксилапатита ТОО «ЮКОК» (Рисунок 9, 10, 11, 12, 13).
биотрансплантатом, на основе отечественного костного
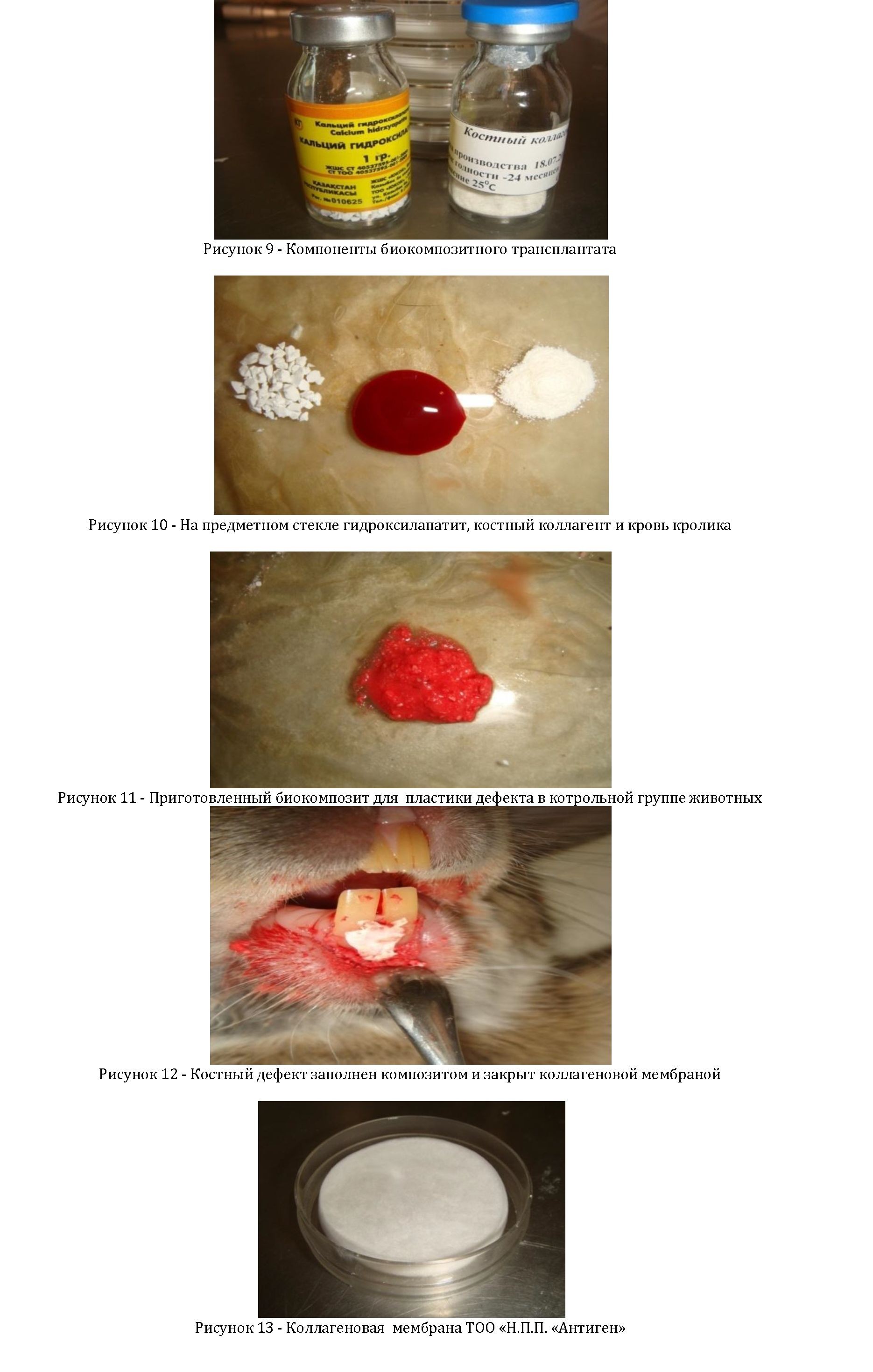
В подопытной группе кроликов все основные этапы операции соответствовали таковым контрольной группы животных, за исключением использования композитного материала, отличающегося от биокомпозита, применяемого в контрольной группе тем, что в него дополнительно вводилась взвесь культуры аутологичных стромальных клеток жировой ткани, выращенных в лаборатории фирмы «Антиген».
Клинические наблюдения послеоперационного периода в обеих группах животных показали, что спустя сутки после оперативного вмешательства в области травмы определялся умеренный отек мягких тканей, который постепенно увеличивался и достигал максимальных размеров к третьим суткам. Затем послеоперационный отек мягких тканей постепенно уменьшался и полностью исчезал в контрольной группе к 9 суткам, в подопытной же группе к 6 суткам. Послеоперационные раны в контрольной группе животных зажили первичным натяжением на 11 сутки, а в подопытной группе на 8 сутки после операции.
Под внутривенным введением 2% раствора Рометара в количестве 6 мл выведены из опыта 9 кроликов контрольной и 9 кроликов подопытной групп (по 3 животных на каждый срок наблюдения). С помощью скальпеля и бормашины вычленены фрагменты нижней челюсти кролика в ее фронтальном отделе. Все 18 фрагментов помещены в 10% раствор формалина. С помощью цифрового рентгенаппарата -Titan 2000-V производства Южной Кореи в центре ветеринарной медицины, ТОО »Акита Ину» проведены рентгеновские снимки и записаны на диске.
Рентгенологические исследования, проведенные нами в различные сроки после операции, позволили в динамике проследить регенерационные процессы в области образованного дефекта в зоне экспериментально воспроизведенного пародонтита.
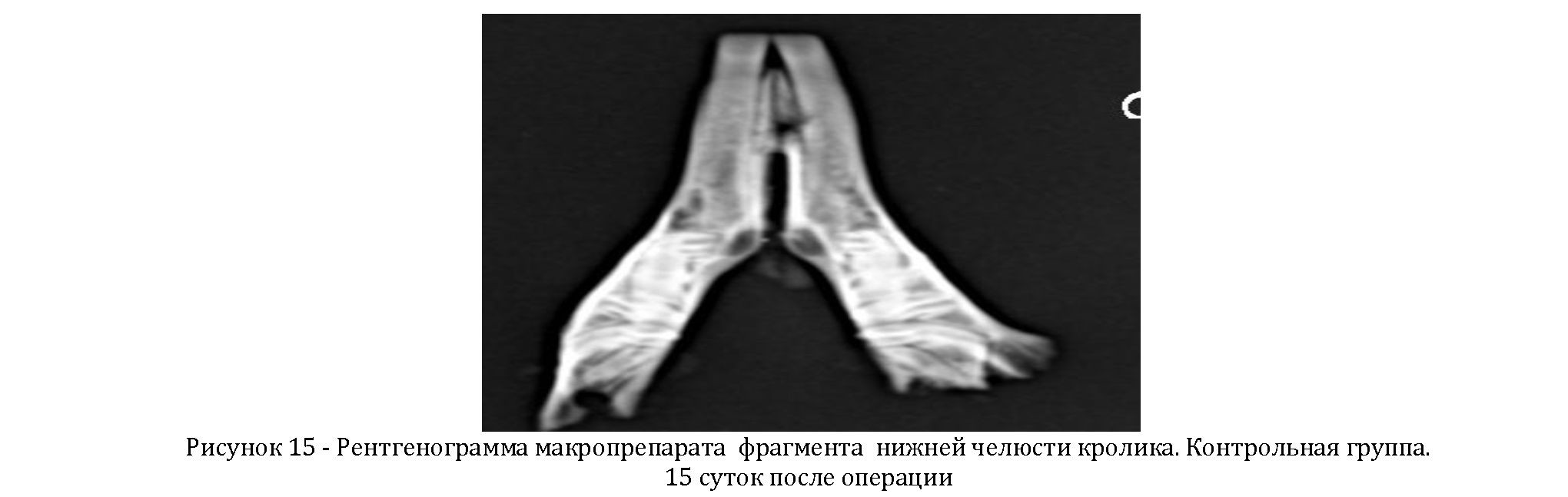
Через 15 суток после операции в контрольной группе животных определяются сравнительно четкие контуры посттравматического дефекта округлой формы диаметром 2 мм (Рисунок 15).
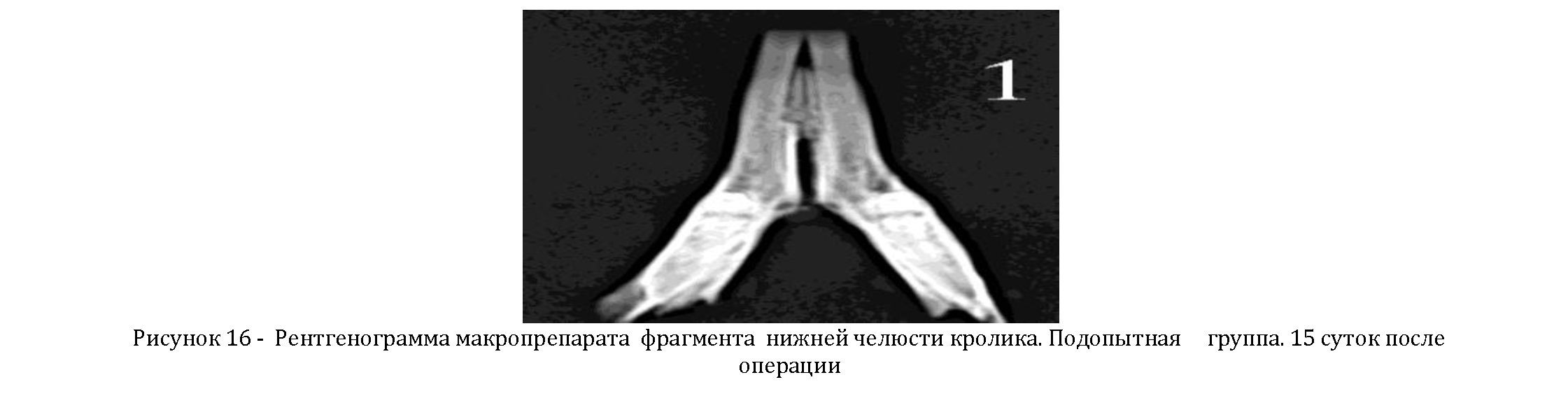
Через 15 суток после операции в подопытной группе кроликов отмечалась нечеткость контуров дефекта за счет остеопороза материнской кости в виде узкой полоски, а в дефекте кости определяются хорошо выраженные тени не правильной формы, характерные для новообразованного регенерата (Рисунок 16).
№1-2016 · KaзH МУ • kaznm∪.kz
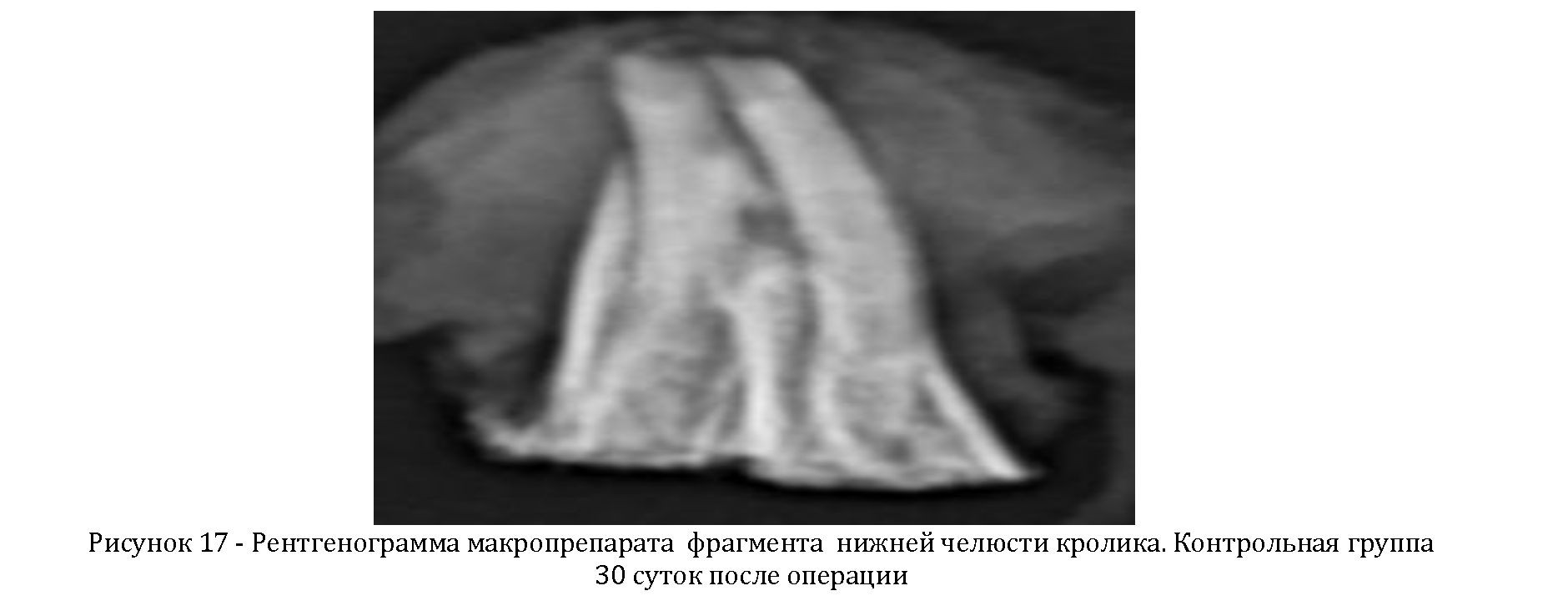
Через 30 суток после операции в контрольной группе животных костный дефект прослеживается еще сравнительно четко на всем протяжении и только в
периферической зоне послеоперационной костной полости определяется тень новообразованного костного регенерата с низкой плотностью и структурированностью (Рисунок 17).
У подопытных же животных к 30 суткам послеоперационный костный дефект значительно уменьшился в размере. Контуры костной полости были нечеткими за счет полосы новообразованного регенерата, проростающего со стороны материнской кости. Плотность тени постепенно снижалась в направлении от периферии к центру (Рисунок 18).
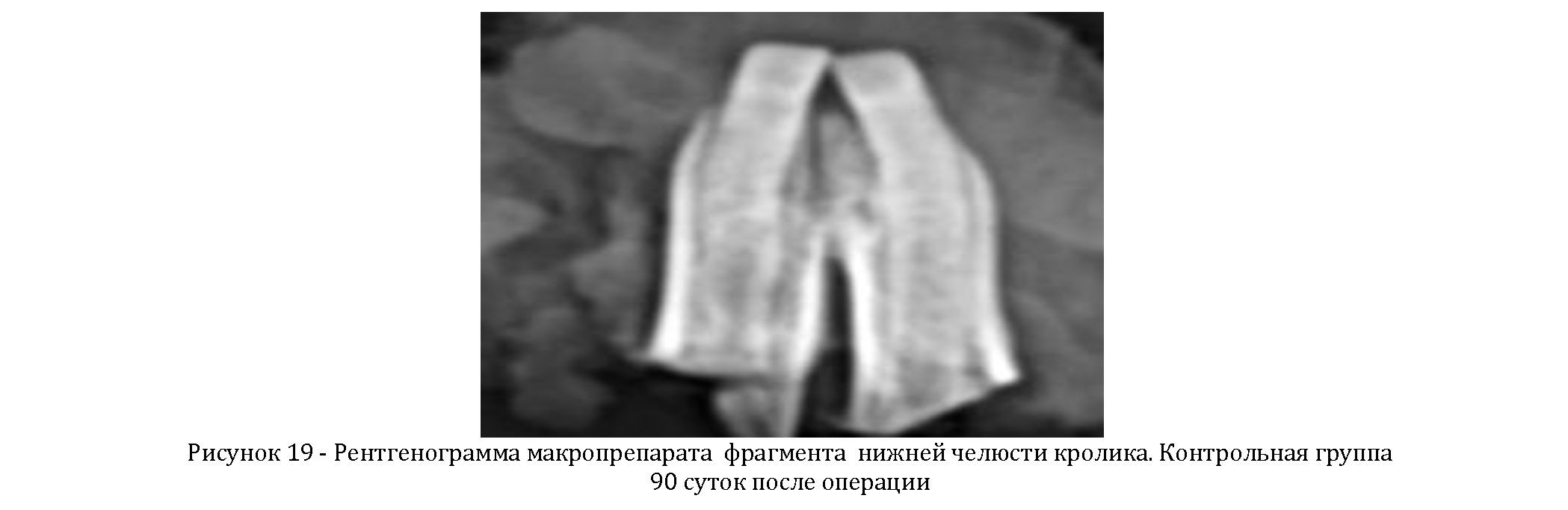
Через 3 месяца в контрольной группе кроликов дефект сократился в размере за счет интенсивной тени новообразованной костной ткани в периферических ее
отделах. В остальной части бывшей костной полости тень регенерата еще сравнительно низкой плотности. (Рисунок 19).
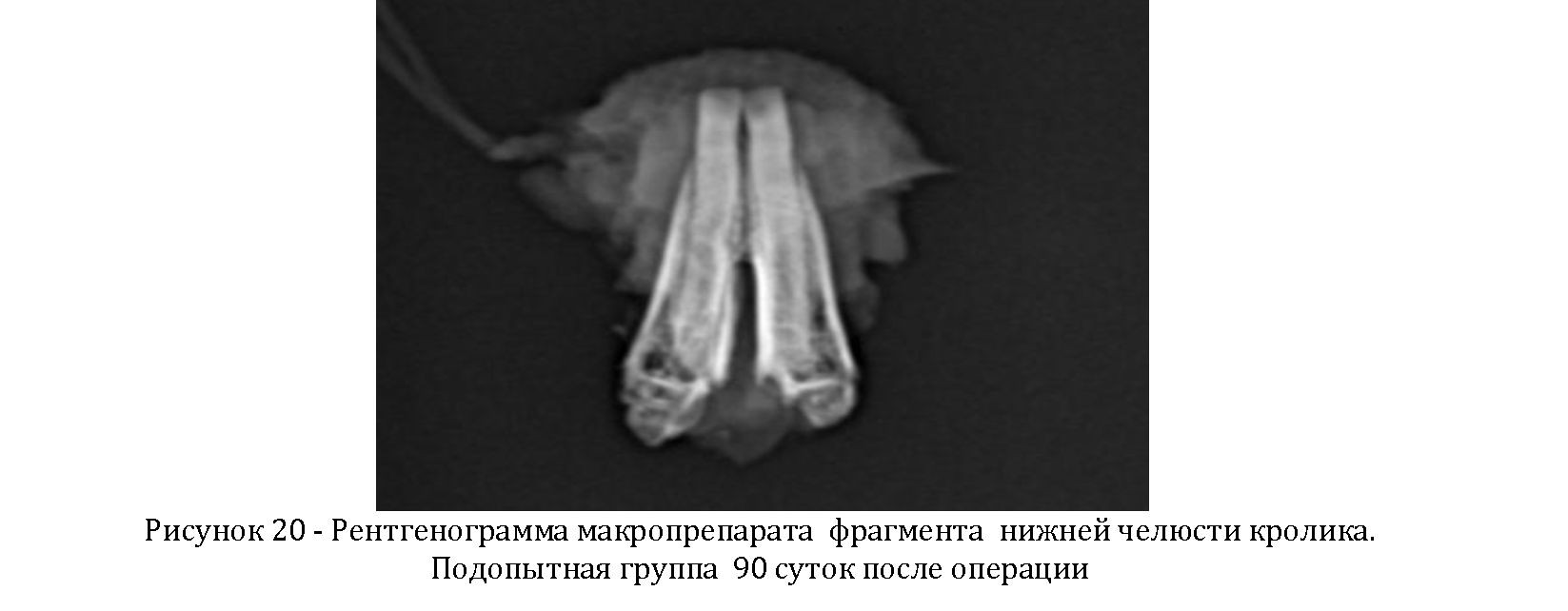
У подопытных же животных к 90 суткам определить место протяжении предсуществующего дефекта определялась бывшего дефекта не представлялось возможным. На зрелая костная ткань

Таким образом, клинические наблюдения послеоперационного периода в обеих группах животных показали, что послеоперационные раны в контрольной группе животных зажили первичным натяжением на 11 сутки, а в подопытной группе на 8 сутки после операции. Результаты рентгенологического исследования показали, что более интенсивная репаративная регенерация в послеоперационной костной полости наблюдалась в подопытной группе животных, где костный дефект заполнялся композитом на основе аутологичных мультипотентных мезинхимальнх стромальных клеток жировой ткани , костного коллагена и гидроксилапатита. В этом случае зрелая костная ткань была сформирована к 90 суткам от начала эксперимента.
В контрольной же группе кроликов, спустя 90 суток после создания костной полости и пластики ее биокомпозитом на основе костного коллагена и гидроксилапатита, регенераторный процесс к этому сроку еще далек от завершенности.
СПИСОК ЛИТЕРАТУРЫ
- Грудянов А.И. Средства и методы профилактики воспалительных заболеваний пародонта. - М.:000 Медицинское информационное агенство, 2012. – 367 с.
- Мусиенко А.И., Мусиенко С. И.,Кушнир.Д.В., Мусиенко .А. А. Комплексный подход к планированию лечения заболеваний пародонта фактором роста // Стоматология Казахстана. - 2014. - № 3-4. - С.67-68.
- Сорокина, М. А. Разработка и оценка эффективности показаний к хирургическим методам лечения заболеваний пародонта: Дисс. … канд. мед. Наук - Воронеж, 2012 .- 170 с.
- Модина Т.Н., Вольвач Ю.Ю., Кащеев Б.В., Петрук А.В., Бабусенко Л.В. Комплексное лечение пациентов с генерализованным пародонтитом // Клиническая стоматология. - 2015. - №2 .- С.14-17.
- Бисултанов Х. У. Сравнительная эффективность применения отечественных костнопластических материалов при лечении пародонтита: Автореф. дисс. ... канд. мед. Наук – Саратов, 2013. – 24 с.
- Грудянов А.И., Чупахин П.В.Методика направленной регенерации тканей. Подсадочные материалы // Медицинское информационное агенство. - 2007. - С.9-11.
- Ефимов Ю.В., Стоматов А.В., Иванов П.В. и др. Использование аутогенного тромбоцитарного геля при хирургическом лечении хронического пародонтита // Медицинский алфавит. Стоматология. - 2010. - №1. -С. 26-27.
- GimbleM.,Katz A.,Bunnell B. Adipose-derived stem cells for regenerative medicine // Circ. Res.-2007. - №100.- P.1249-1260.
- JurgensW.Oedayrajsilgh-Varma M., Helder M.et al. Effekt of tissue-harvesting site on yield of stem cells derived from adipose tissue : implications for cell-based therapies // Сell Tissue Res.-2008.-332.-№ 3.-P.415-426.
- Перова М.Д. [и др.] Оценка эффективности новой нерезорбируемой ПТФЭ–мембраны при направленной регенерации тканей пародонта // Новое в стоматологии. – 2002. - №6 (105). – С.47-57.
- Lee R.H [et al] Characterization and expression analysis of mesenchymal stem cells from human bone marrow and adipose tissue // Cell PhysiolBiochem. – 2004. - v. 14. - P. 311-324
- Jones A.A. [et al] The effect of rhBMP-2 around endosseous implants with and without membranes in the canine model // J Periodontol . – 2002 .- v. 77.- P. 1184-1194.
- Пальцев М.А. [и др.] Стволовые клетки в современной медицине: настоящее и будущее // Молекулярная медицина. – 2006. - №2. - С. 5-9.
- Алексеева И.С., Волков А.В., Кулаков А.А., Гольдшейн Д.В. Клинико-экспериментальное обоснование использования комбинированного клеточного трансплантата на основе мультипотентных мезенхимныхстромальных клеток жировой ткани у пациентов с выраженным дефицитом костной ткани челюстей //Клеточная трансплантология и тканевая инженерия. -2012.- №1. – С. 97-105.
- Киселев С.Л [и др.] Молекулярная и клеточная биология линий эмбриональных стволовых клеток человека // Молекулярная медицина. – 2006. - №2. – С. 29-37.
- Rasmussen, T.P. Embryonic stem cell differentiation: a chromatin perspective // Reprod Biol Endocrinol. – 2003. - v. 1. - P. 100-110.
- Francis J. Hughes Mesenchymal Stem Cells and Periodontal Regeneration// Hughes Curr Oral Health Rep .- 2014.-№.-1.- P. 1–8
- Черняев С.Е.,Киселева Е.В.,Григорьян А.С.,Воложин А.И. Влияние аллогенных и аутологичных мультипотентных стромальных клеток жировой ткани на регенерацию костной ткани дефекта угла нижней челюсти кролика // Стоматология. - 2010. - №1. – С. 23-29.
- Бухарова Т.Б., Арутюнян И.В., Шустров С.А., Алексеева И.С., Федюнина И.А., Логовская Л.В., Волков А.В., Ржанинова А.А., Григорьян А.С., Кулаков А.А., Гольдштейн Д.В. Тканеинженерная конструкция на основе мультипотетных стромальных клеток жировой ткани и материала «Остеоматрикс» для регенерации костной ткани // Клеточные технологии в биологии и медицине. - 2011. - №3. - С.167-170.
- 20. Алексеева И.С., Волков А.В., Кулаков А.А., Гольдшейн Д.В. Жировая ткань как перспективный источник получения мультипотентных стромальных клеток взрослого организма // Пародонтология. - 2012 .- №2(63) .- С. 21-25.
- Алексеева И. С.Применение комбинированного клеточного трансплантата на основе мультипотентных мезенхимальныхстромальных клеток жировой ткани у пациентов с дефицитом костной ткани (клинико-экспериментальное исследование): Автореф. Дисс. … д-р. мед. Наук - М., 2012. - З7с.
- Мартиросян А.К. Использование остеопластических биорезорбируемых материалов на основе минерального сырья и костного коллагена при хирургических вмешательствах в челюстнео-лицевой области: Автореф дисс. ... канд.мед. наук. - Тверь, 2013. - 23 с.
- Русанов В.П. Совершенствование хирургических методов лечения воспалительно-деструктивных процессов в альвеолярном отростке челюстей: Автореф. Дисс. . д-р. мед. Наук - Алматы, 1993. - 46 с.
- Бисултанов Х.У, Лепилин А.В, Ерокина Н.Л.и др. Сравнительный анализ применения отечественных гидроксиапатит содержащих костнопластических материалов при лечении пародонтита // Российский стоматологический журнал.—2012.- №3.—С.31-34