В статье представлены результаты комплексного лечения пациентов с деструктивной формой острого панкреатита с применением методов эфферентной терапии гемодиафильтрации (ГДФ), плазмафереза (ПФ), внутрисосудистого лазерного облучения крови (ВЛОК), ультрафиолетового облучения крови (УФО). Раннее включение гемодиафильтрации в комплексную интенсивную терапию сепсиса и септического шока при панкреонекрозах позволяет быстрее стабилизировать гемодинамику, дыхательные расстройства и отказаться от применения адреномиметиков, а также значительно уменьшить клинические проявления тяжелой интоксикации, гипоксии и эндотоксикоза.
Актуальность: Одной из причин, приводящих к развитию абдоминального сепсиса, является острый деструктивный панкреатит (панкреонекроз). Смертность при сепсисе составляет 28,6%, увеличиваясь с возрастом до 38,4% [1,2].
Средняя длительность нахождения пациентов в отделении реанимации и интенсивной терапии составляет 7,5±1,5 суток, а в стационаре - 35±9 суток [3,4].
Септический шок – самая частая причина гибели больных в отделении интенсивной терапии. Только в США примерное число смертей от септического шока составляет 100 000 в год [5].
Наиболее опасным периодом в отношении летальности является период гемодинамических расстройств и панкреатогенного шока. Столь высокая летальность (90100%) в этом периоде обусловлена патогенетическими особенностями течения панкреонекроза, а именно усилением проявлении интоксикации, выбросом в кровь большого количества медиаторов воспаления (TLR2, TLR4, ИЛ-6, ИЛ-8, ИЛ-10, ФНОα), транслокацией в кровь низко- и среднемолекулярных токсических веществ из желудочнокишечного тракта, что приводит к развитию «медиаторного хаоса» и мультиорганной дисфункции в ответ на действие микроорганизмов. При сепсисе происходит не просто повышенная продукция про и противовоспалительных медиаторов, а возникает дисрегуляция этого процесса – своеобразное «злокачественное внутрисосудистое воспаление», которое приводит к повреждению эндотелия, развитию септического шока и синдрома мультиорганной дисфункции.
Применение экстракорпоральных методов детоксикации в комплексном лечении пациентов с тяжёлыми формами деструктивного панкреонекроза, осложнённого сепсисом и септическим шоком, позволяет устранить гистотоксическую гипоксию и является средством предупреждения развития мультиорганной дисфункции [6,7,8].
Цель исследования – изучить эффективность методов эфферентной терапии в комплексном лечении деструктивного панкреатита.
Задачи исследования:
- Определение степени тяжести эндотоксикоза при деструктивном панкреатите.
- Оценка гемодинамических показателей у больных деструктивным панкреатитом.
- Оценка эффективности эфферентных методов терапии. Материалы и методы исследования
В исследование включено 23 пациента с деструктивным панкреатитом, находившихся на стационарном лечении в отделении реанимации и интенсивной терапии ГКБ №4 г. Алматы, в возрасте от 18 до 87 лет. Среди обследованных больных было 21 мужчин (91,3%) и 2 женщины (8,7%). По характеру некротического поражения – с геморрагическим панкреонекрозом было 8 больных (34,7%), с жировым панкреонекрозом 1 (4,3%), и смешанная форма встречалась в 14 (61%) случаях. Основными причинами деструктивного панкреатита были: алиментарный фактор – 47,8%, злоупотребление алкоголем – 34,8%, причина не установлена в 17,4%. По длительности заболевания – 78,2% больных поступило через 12-24 часа от начала заболевания. Тяжесть состояния пациентов оценивалась по шкале APACHE-II. Степень выраженности мультиорганной дисфункции по шкале SOFA.
Всем больным проводилось комплексное клиниколабораторное и инструментальное обследование, включающее сбор анамнестических данных, физикальное обследование, оценку клинических и биохимических показателей, морфологическое исследования при выполнении хирургического вмешательства, а также ежедневное проведение УЗИ при поступлении и в динамике. Ультрасонографию проводили на аппаратах SonoAcePico (Корея), Vivid-7 (Generalelectrics, США), Toshiba Xario. Определяли форму, контуры, размеры поджелудочной железы в целом и каждого из ее отделов, эхогенность, и состояние панкреатического протока, наличие и отсутствие парапанкреатических инфильтратов, абсцессов, кист, а также состояние начального отдела тонкой кишки (парез, наличие жидкости в просвете кишки с хаотическим движением или вялая антиперистальтика), гидроторакс, расширение ретрогастрального пространства и др. Оценка частоты встречаемости ультразвуковых признаков проводилась 3 раза в следующие сроки с момента заболевания: до 12 часов, от 12 до 24 ч и более 1 суток.
В зависимости от характера проводимой интенсивной терапии больные были разделены на 2 группы.
- группа (основная) – с деструктивными формами панкреатита (n=11, все мужчины, женщин не было), получавшие стандартную интенсивную терапию (блокада секреции поджелудочной железы, обеспечение системной и регионарной микроциркуляции, ИВЛ, цитокиновая блокада, антибактериальная терапия, возмещение водноэлектролитных и метаболических потерь, хирургическая детоксикация, дренирование), дополненную методами эфферентной терапии: гемодиафильтрация (ГДФ) – на аппарате Multifiltrate (фирмы Fresenius, Германия), внутрисосудистое лазерное облучение крови (ВЛОК) и ультрафиолетовое облучение крови (УФО) – на аппарате лазерной терапии «Матрикс-ВЛОК» (Adamant Group, Казахстан) с излучающей головкой МС-ВЛОК-365. Инфузионная терапия дополнялась препаратами Сорбилакт и Реосорбилакт (Юлия Фарм, Украина).
- группа (сравнения) – больные с деструктивными формами панкреатита, получавшие стандартную терапию – 12 человек (10 мужчин и 2 женщины) и традиционную инфузионную терапию (препараты ГЭК, гелофузин, кристаллоиды). Проводилась эфферентная терапия – плазмаферез – на аппарате Haemonetics (США), внутрисосудистое лазерное облучение крови (ВЛОК) и ультрафиолетовое облучение крови (УФО), форсированный диурез.
Тяжесть по шкале APACHE II составила в 1 группе 23,2±1,2 балла, во 2 группе 23,4±2,3 балла. Тяжесть по шкале SOFA составила в 1 группе 12,3±0,1 балла, во 2 группе 12,1±0,1 балла. Различий между группами по тяжести состояния при поступлении в стационар не было.
Программа экстракорпоральной детоксикации у больных в 1 группе (исследуемая) состояла в следующем:
- Хирургическая коррекция
- ГДФ – подключали через 8-12 часов после операции
- Через 12-24 часа после хирургической коррекции ВЛОК и УФО крови
Программа экстракорпоральной детоксикации у больных с некротической формой панкреатита во 2 группе (контрольная) включала:
- Хирургическую коррекцию
- Через 12-24 часа после хирургической коррекции ВЛОК и УФО крови
- Плазмаферез начинали проводить через 12-24 часа после операции
- Форсированный диурез
Проведение ГДФ осуществляли в период между оперативными вмешательствами и на 7 день лечения в ОРИТ, 1 раз в сутки, продолжительностью 12-24 часа, 1-2 сеанса ГДФ. Основными показаниями являлось ухудшение клинического состояния, рост эндогенной интоксикации с усугублением мультиорганной дисфункции, отражающей тяжесть сепсиса.
Первые сеансы ГДФ начинали, как минимум, через 8-12 ч после завершения оперативного вмешательства. Сосудистый доступ – двухпросветный венозный катетер Certofix DuoHF. Скорость потока крови через гемодиафильтр для гемодинамический стабильных больных устанавливали 150-200 мл/мин. У больных, которые нуждались в инфузии симпатомиметиков — 80-100 мл/мин с постепенным наращиванием скорости и пролонгацией сеанса детоксикации до 24 ч.
ГДФ выполняли на аппарате «Multifiltrate» с применением стандартных пакетированных стерильных растворов на основе бикарбонатного буфера. Замещение в объеме 20004000 мл/час проводили методом постдилюции на гемодиафильтрах AV600S. Поток диализирующего раствора составил 2000-4000 мл/час.
Лечение было дополнено проведением непрерывно поточного плазмафереза на аппарате «Haemonetics PCS-2», с целью удаления антигенов, антител, биогенных аминов, иммунных комплексов, продуктов распада тканей гнойновоспалительного происхождения.
Непрерывно поточный плазмаферез проводили с первых суток после хирургической санации очага инфекции и антибактериальной терапии. Перед плазмаферезом проводили коррекцию гипопротеинемии, гипогликемии, анемии, водно-электролитных нарушений. При неустойчивой гемодинамике использовали вазопрессоры (дофамин, мезатон и т.д.). Однократный объем эксфузии плазмы составлял 600-1200 мл. Объем эксфузированной плазмы у больных 2 группы восполняли донорской свежезамороженной плазмой (40%), 10-20%-раствором альбумина (20%), коллоидно-криссталлоидными растворами (40%). В зависимости от исходной тяжести состояния, эффективности и переносимости процедуры проводили 3-6 сеансов плазмафереза каждые 24-48 часов. Методы квантовой терапии применяли в обеих группах по следующей методике:
- Внутрисосудистое лазерное облучение крови (ВЛОК) длина волны излучения 635 нм, мощность излучения на конце световода 1,5-2 мВт, время воздействия составляло 20 мин, в течение 7-10 дней, с противовоспалительной целью и для улучшения микроциркуляции.
- Ультрафиолетовое облучение крови (УФО) – длина волны 365 нм, мощность излучения на конце световода 1,0 мВт, время воздействия 5-7 мин в течение 10 дней, с целью стимуляции клеточного и гуморального иммунитета.
Инфузионную поддержку осуществляли препаратами Сорбилакт и Реосорбилакт (Украина, Юлия Фарм), которые относятся к малообъёмным инфузионным средствам, вводились внутривенно капельно 30-40 кап./мин. При шоке объём инфузии составил 600-1000 мл (10-15 мл/кг массы тела), сначала струйно, потом капельно. Основными составляющими препаратов являются сорбитол и натрия лактат. Оба препарата содержат электролиты (натрий, калий, кальций, магний) в сбалансированном соотношении, натрия лактат имеет нейтральную реакцию, но при введении в сосудистое русло диссоциирует на ионы натрия и молочную кислоту, которая метаболизируется в печени до натрия бикарбоната, что повышает резервную и титруемую щёлочность крови. Коррекция метаболического ацидоза при этом осуществляется постепенно и не вызывает резких колебаний рН, в отличие от воздействия натрия бикарбоната.
Сорбитол (С6Н14О6) – шестиатомный спирт, который быстро включается в общий метаболизм, используется для срочных энергетических потребностей, повышает энергетический баланс, усиливает процессы регенерации гепатоцитов, обладает антикетогенным действием. Гипертонический (20%) раствор сорбитола имеет высокую осмолярность и оказывает диуретический эффект, а 6% изотонический обладает дезагрегантными свойствами.
Для оценки гемодинамических показателей проводили измерение АД (систолическое, диастолическое, среднее), центрального венозного давления, частоты сердечных сокращений, пульса. Оценку транспорта кислорода осуществляли по газовому и кислотно-основному составу крови, пульсоксиметрии и капнографии.
Забор крови для исследования осуществляли поэтапно в течение всего периода нахождения больного в ОРИТ: на 1, 3, 5, 7 сутки до и после сеансов эфферентной терапии.
Лабораторные обследования больных включали общий анализ крови и мочи, биохимический анализ крови (общий белок, альбумины, мочевина, креатинин, билирубин общий, прямой, непрямой, АЛТ, АСТ, глюкоза, электролиты, амилаза, лактат), состояние системы гемостаза (ПТИ, фибриноген).
Результаты и их обсуждение.
Больные поступали в тяжелом и крайне тяжелом состоянии с клинической картиной острого панкреатита и интоксикации, при УЗИ органов брюшной полости подтвержден деструктивный панкреатит – увеличение размеров железы, снижение эхогенности паренхимы, формирование очагов деструкции, появление жидкости в сальниковой сумке, формирование кист.
Гемодинамический профиль в обеих группах соответствовал гиподинамическому типу кровообращения, что было обусловлено сепсисом и гиповолемией, связанной не только с перераспределением жидкости, но и с повышенными ее потерями (перспирация, секреция в желудочно-кишечный тракт и т.д.). Увеличение ЧСС, в ряде случаев до 140 ударов в мин, рассматривали как важное звено компенсаторного механизма, направленного на поддержание достаточного кровоснабжения органов и тканей. Для стабилизации гемодинамики требовалось введение больших доз симпатомиметиков (дофамин 6-12 мкг/кг/мин, мезатона 200-2000 мг/кг/мин, адреналина 200-2000 мг/кг/мин).
У больных 1 группы, в течение первых 2 ч после начала сеанса эфферентной терапии, улучшения показателей гемодинамики не отмечалось. К 3 ч ГДФ отмечено увеличение САД на 14,5%, на фоне урежения ЧСС на 10%. К началу 7 ч стабилизация системной гемодинамики позволила в 15% случаев прекратить введение катехоламинов, у 45% больных удалось снизить исходные дозы дофамина и/или адреналина в четыре и более раз, или полностью от них отказаться. В среднем дозировка дофамина составила 1-5 мкг/кг/ч к концу первых суток. В 1 группе инотропная поддержка у всех больных полностью прекращалась к 7 суткам, тогда как во 2 группе только к 15 суткам (Таблица 1).
Т аблица 1 - Количество больных,
|
Группы больных |
1 сут |
3 сут |
5 сут |
7 сут |
9 сут |
12 сут |
|---|---|---|---|---|---|---|
|
1 группа |
11 |
5 |
1 |
0 |
0 |
0 |
|
2 группа |
12 |
12 |
8 |
6 |
4 |
3 |
Незначительно повышенное ЦВД в результате эфферентной терапии нормализовалось к началу 3 суток. Таким образом, проведение эфферентных методов терапии приводило к стабилизации гемодинамики в более ранние сроки, это связано с быстрой элиминацией цитокинов, коррекцией осмотического равновесия и протезированием гомеостатической функции почек. По показателям «красной крови» за счёт гемоконцентрации и гиповолемии на момент поступления в обеих группах отмечалось повышение уровня Hb и эритроцитов. Но за счёт гемодилюции и интоксикации эти показатели достоверно были снижены. Достоверно снижался уровень лейкоцитов, ЛИИ, лимфоцитов, палочкоядерных и юных форм нейтрофилов.
На момент поступления в ОРИТ уровень лейкоцитов в обеих группах превышал нормальные показатели (от 9 до 15,7 x 109/л). Снижение лейкоцитоза в 1 группе до нормальных цифр (среднее значение 9,53+1,71) отмечено к 7 суткам. Во 2 группе количество лейкоцитов сохранялось повышенным в течение всего анализируемого срока (диаграмма 1).
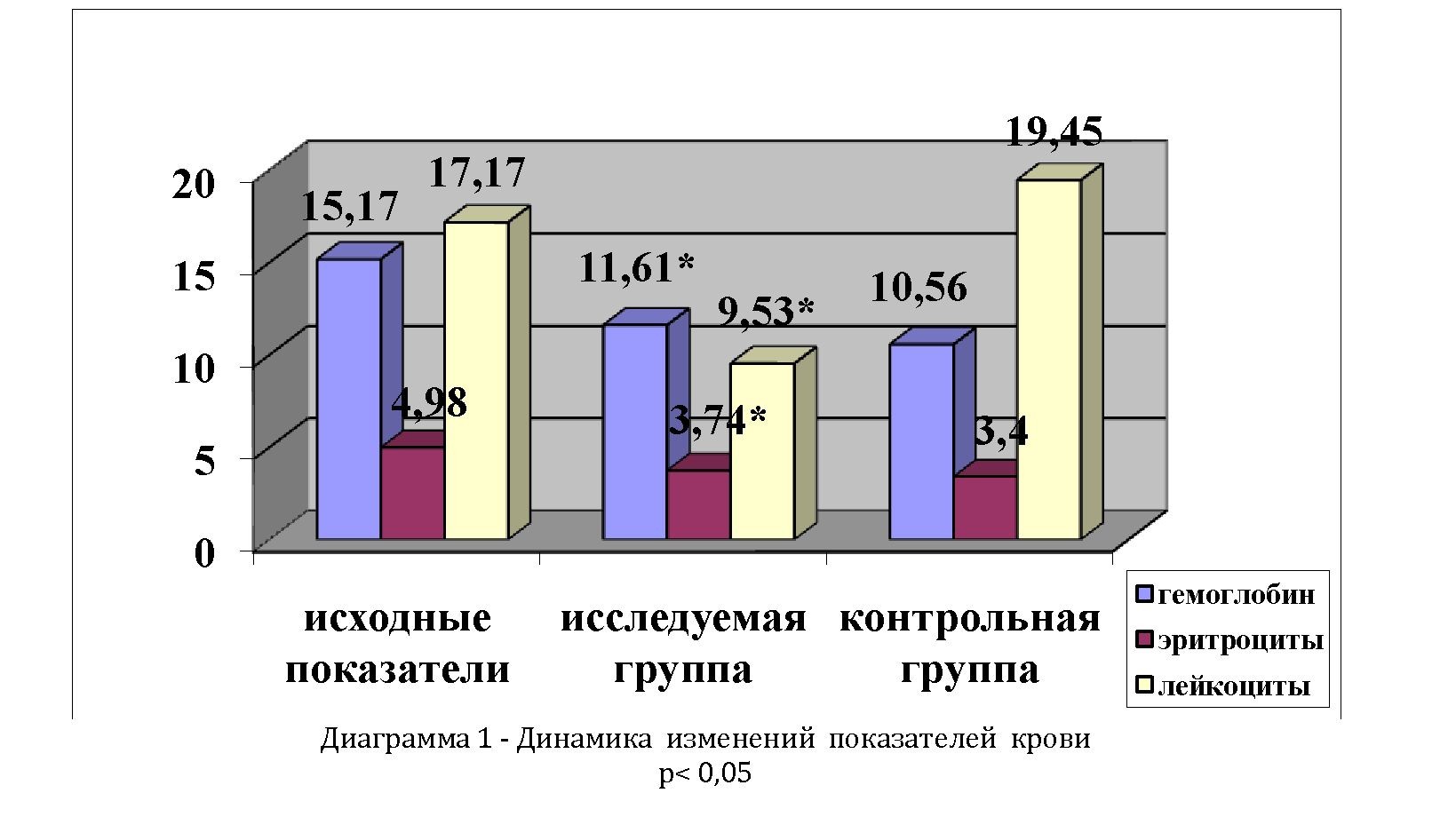
В биохимическом анализе крови статистически достоверно отмечались изменения уровня белка, мочевины, креатинина, билирубина, АЛТ, АСТ, амилазы. В течение 7 суток количество общего белка крови у больных всех групп оставалось ниже нормальных значений. На 3-5 сутки отмечено, что количество общего белка у больных 1 группы выше на 10,3% по сравнению со 2 группой.
На момент поступления в ОРИТ уровень мочевины и креатинина в обеих группах превышали нормальные показатели. Снижение мочевины и креатинина в 1 группе до нормальных цифр (среднее значение 8,9+4,15 для мочевины и 99,47+70,61 для креатинина) отмечено к 3 суткам. Во 2 группе количество этих показателей сохранялось повышенным в течение всего анализируемого срока (диаграмма 2).
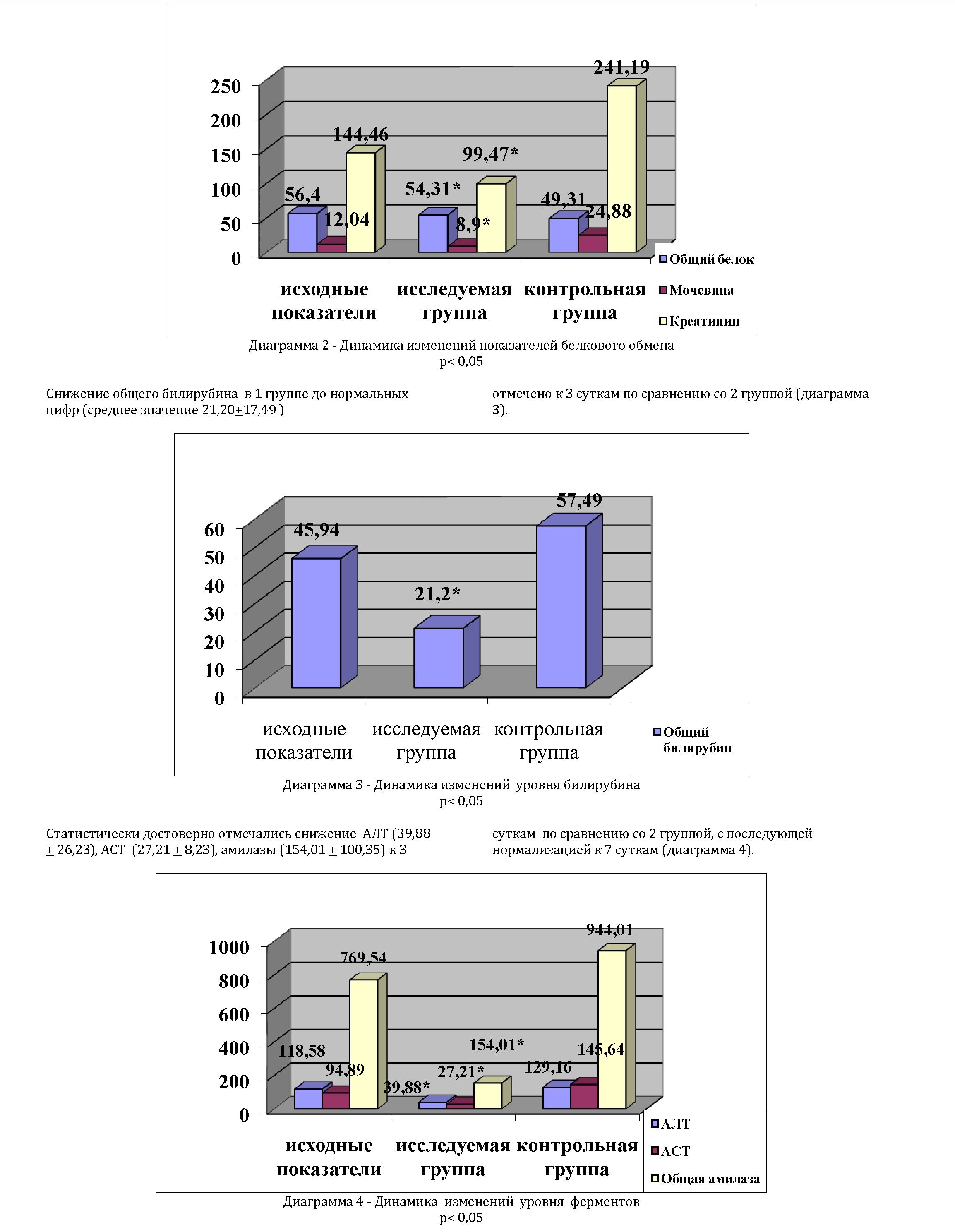
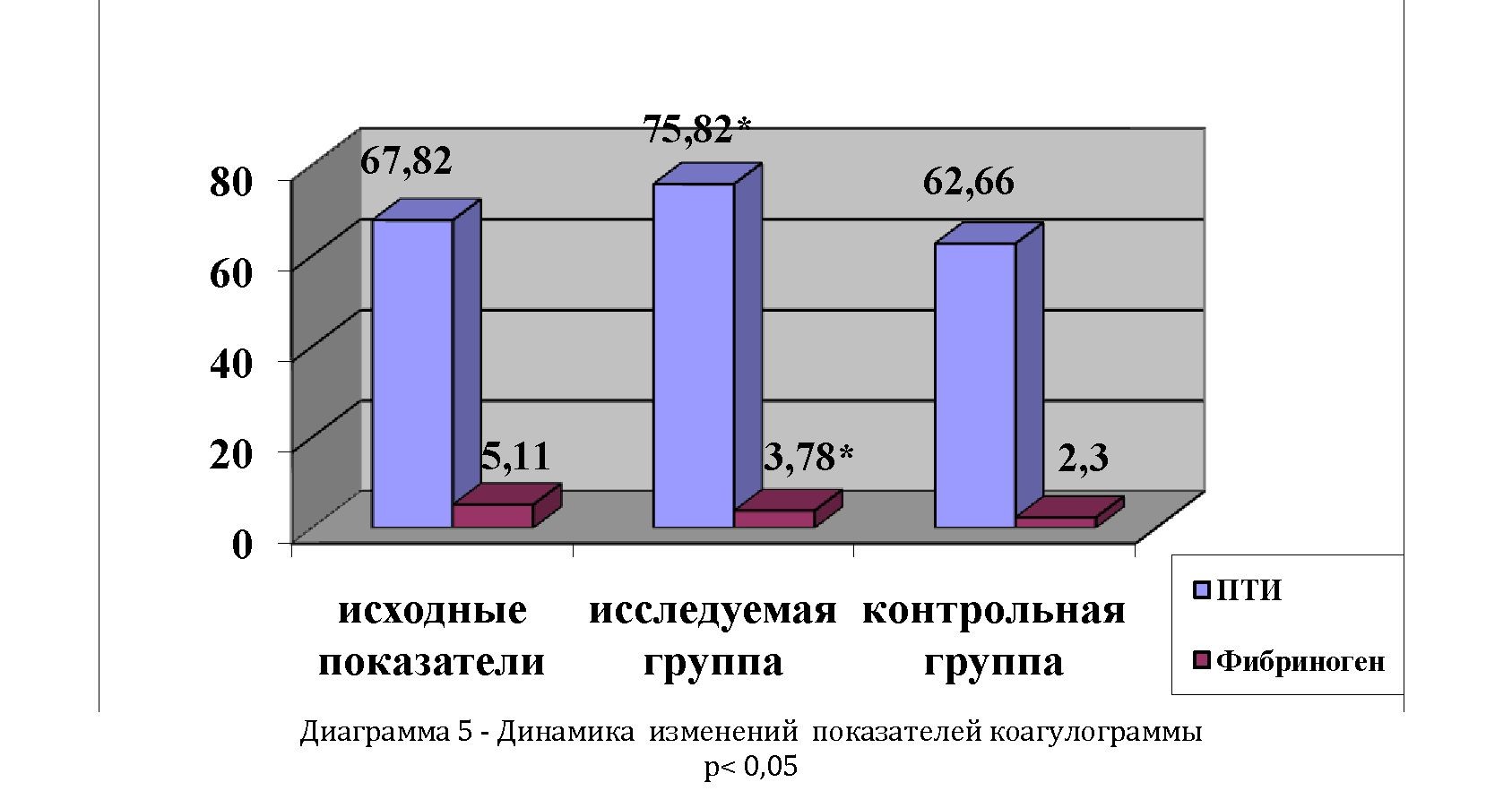
На 3-5 сутки в обеих группах отмечено снижение уровня фибриногена до нормальных значений. Показатели ПТИ были исходно снижены в обеих группах, но к 3 суткам в 1 группе эти показатели были стабилизированы (75,82 + 5,34) по сравнению со 2 группой (диаграмма 5).
ЛИИ превышал норму в 5 раз уже с 1 суток заболевания, что, по данным литературы, свидетельствует о недостаточности иммунитета и выраженной эндогенной интоксикации. Высокие значения ЛИИ свидетельствуют о необходимости более активной дезинтоксикационной терапии, с другой стороны, подтверждают наличие патологических изменений иммунной системы.
К 3 суткам в 1 группе отмечено уменьшение ЛИИ на 40,8% по сравнению со 2 группой. Выявлено, что раннее включение методов эфферентной терапии в комплексном лечении панкреонекроза снижает тяжесть эндотоксикоза на 2-3 сутки послеоперационного периода, во 2 группе - только на 15 сутки (Таблица 2).
р< 0,05
Таблица 2 -
|
Группы больных |
1 сутки |
3 сутки |
5 сутки |
7 сутки |
9 сутки |
12 сутки |
15 сутки |
|
1 группа |
5,7 +1,05 |
3,37+ 0,4* |
2,7 +0,3* |
1,6 + 0,5* |
0 |
0 |
0 |
|
2 группа |
5,7 +1,07 |
5,2 + 0,4 |
5,7 + 0,5 |
5,5+ 0,4 |
5,7 + 0,4 |
5,8 +0,6 |
3,9 + 0,2 |
индекса интоксикации
Анализ полученных данных показал, что в 1 группе уровень лактата приходил к норме к 7 суткам (среднее значение 1,8+0,5 ммоль/л), во 2 группе - к 15 суткам (среднее значение 1,7+0,2 ммоль/л).
Выявлено, что раннее проведение эфферентных методов терапии в комплексном лечении панкреонекроза обеспечивает снижение клинических проявлений эндотоксикоза в 1 группе на 30-50% по сравнению со 2 группой. Таким образом, у больных 1 группы отмечено двукратное снижение среднего балла по шкале APACHE II и уменьшение тяжести эндотоксикоза уже на 2-3 сутки послеоперационного периода, во 2 группе - только на 15 сутки (Таблица 3).
|
Показатель |
Группы |
На момент поступления |
3 сутки |
7 сутки |
9 сутки |
12 сутки |
15 сутки |
|
Тяжесть состояния по шкале APACHEII (баллы) |
1 |
24,2±1,2 |
13,1±1,3* |
10,7±1,2* |
|||
|
2 |
23,4±2,3 |
22,2±1,3 |
21,6±1,4 |
19,6±1,4 |
17,6±1,3 |
11,6±1,4 |
Таблица 3 - Динамика тяжести состояния некротической формы панкреатита (по шкале APACHE II)
р< 0,05
По шкале SOFA больные 2 группы долгое время оставались в тяжелом состоянии, что отразилось на летальности (50%),
тогда как в 1 группе летальных случаев было - 9% (Таблица 4).
Таким образом, нарушения витальных функций, развивающиеся при деструктивном панкреатите, являются отражением нарушений органной перфузии. При анализе полученных результатов исследования в динамике удалось выявить, что раннее включение эфферентных методов терапии в комплексное лечение деструктивного панкреатита обеспечивает уменьшение клинических признаков эндотоксикоза в 1 группе на 30-50% по сравнению со 2 контрольной группой. У больных 1 группы отмечено двукратное снижение среднего балла по шкале APACHE II и уменьшение тяжести эндотоксикоза уже на 2-3 сутки послеоперационного периода, во 2 группе – только на 15 сутки. Стабилизация гемодинамики, возможность уменьшения доз адреномиметиков и восстановление функции почек свидетельствуют о возможной нормализации всего висцерального кровотока, что в 63% случаев позволило предупредить развитие анурической формы острой почечной недостаточности, а в 31% случаев – избежать развития мультиорганной дисфункции. Проведение эфферентных методов терапии позволило достоверно снизить летальность.
Выводы.
- При деструктивном панкреатите отмечается выраженный эндотоксикоз с повышением лейкоцитарного индекса интоксикации. Показано, что раннее включение эфферентных методов терапии в комплекс лечения деструктивного панкреатита обеспечивает снижение клинических признаков эндотоксикоза на 30-50%.
- Тактика лечения больных абдоминальным сепсисом должна быть направлена на устранение патогенетических основ развития патологического процесса – ранняя респираторная и адекватная гемодинамическая поддержка.
Антимедиаторная терапия и антибактериальная терапия в лечении абдоминального сепсиса патогенетический обоснована и приводит к уменьшению частоты развития системных осложнении и летальности.
Гемодиафильтрация является наиболее эффективным методом элиминации медиаторов воспаления и цитокининов, стабилизирует гемодинамику,препятств ует развитию синдрома мультиорганной дисфункции и снижает летальность больных при абдоминальном сепсисе.
Таблица 4 - Оценка полиорганной недостаточности по шкале SOFA
|
Группы больных |
Баллы |
|||||||
|
1 сутки |
3 сутки |
5 сутки |
7 сутки |
9 сутки |
12 сутки |
15 сутки |
18 сутки |
|
|
1 группа |
12-14 |
6-7 |
3-4 |
1-2 |
0 |
0 |
0 |
Летальность 9% |
|
2 группа |
12-14 |
13-14 |
15-16 |
17-18 |
18-19 |
18-19 |
20-21 |
Летальность 50% |
СПИСОК ЛИТЕРАТУРЫ
- Iskander K.N., Osuchowski M.F., Stearns-Rurosawa D.J., Kurosawa S., Stepien D., Valentine C., Remick D.G. Sepsis: multiple abnormalities, heterogeneous responses, and evolving understanding. - Phisiol. Reu. – 2013. - 93 (3). –Р. 1247-1288. http: // dx.doi. org/ 10.1152 / physrev. 00037. 2012. PMID: 23899564
- Мороз В.В., Лукач В.Н., Шифман Е.М.,Долгих В.Т., Яковлева И.И. Сепсис. Клинико – патофизиологические аспекты интенсивной терапии. - Петрозаводск: Интел Тек, 2004. – 217 с.
- Руднов В.А. Сепсис: современный взгляд на проблему // Клиническая антимикробная химиотерапия. - 2000. - Т.2. - №1. - С. 2-7.
- Salvo J., de Cian W., Musicco M. et al. The Italian sepsis studi; preliminary results on the incidence and evolution of SIRS, sepsis, severe sepsis and septic shock // Intensive Care Med. - 1995. - V.21. - P.244-249
- Parrillo J.E. Pathogenetic mechanisms of septic shock // N. Engl. J. Med. - 1993. -V.328. - P.1471-1477
- Исмаилов Е.Л., Ералина С.Н., Абдрасулов Р.Б., Текесбаев Б.Б. Методы экстракорпоральной детоксикации в лечении деструктивного панкреатита. // Общая реаниматология. - М.: 2015. - Том 11. - №3. - С. 65-74.
- Протас В.В. Применение гемодиафильтрации в комплексном лечении острого респираторного дистресс-синдрома взрослых в критических больных с некротическим панкреатитом / В. Протас / / Украинский журнал экстремальной медицины имени Можаева. - 2006. - № 3. - С. 31-34.
- Хорошилов С.Е., Павлов Р.Е., Смирнова С.Г. и др. Высокообъемная гемофильтрация в лечении» сепсиса и септического шока // Альманах анестезиологии и реаниматологии. — 2007. — № 3. — С. 631