Гастроэзофагеальная рефлюксная болезнь широко распространена в мире. Вопрос об оперативном лечении ГЭРБ возникает, когда консервативная терапия не дает ожидаемого эффекта, несмотря на неоднократные курсы медикаментозной терапии и соблюдение всех рекомендаций по нормализации образа жизни. Консервативное лечение позволяет снизить остроту симптомов и не дать развиться осложнениям и не устраняет причину заболевания. Целью исследования является выбор хирургической тактики видеоэндохирургической лапароскопической фундопликации при рефлюкс- эзофагите, так как она дает хорошие результаты (94,4%).
Актуальность. Гастроэзофагеальная рефлюксная болезнь (ГЭРБ) широко распространена в мире. Количество людей, страдающих рефлюкс-зофагитом (Рисунок 1), значительно (3-4 % всей популяции). Это обусловлено ростом гастродуоденальных язв, грыж пищеводного отверстия диафрагмы, хронического холецистита. В настоящее время общепризнанно, что гастроэзофагеальная рефлюксная болезнь (ГЭРБ) обусловлена повреждением пищевода и смежных органов вследствие первичного нарушения двигательной функции пищевода, ослабления антирефлюксного барьера нижнего пищеводного сфинктера (НПС), снижения пищеводного клиренса и опорожнения желудка. Достигнут консенсус в том, что в результате действия множества ослабляющих факторов определяющим дефектом при ГЭРБ является патологический нейромышечный контроль НПС, приводящий к частым длительным периодам преходящего расслабления НПС, ‘'вялому'', ‘'некомпетентному'' сфинктеру. Недостаточность замыкательной функции НПС наблюдается при многих заболеваниях желудочно-кишечного тракта — грыже пищеводного отверстия диафрагмы (ГПОД),гастродуоденальной язве, желчнокаменной болезни, хроническом толстокишечном стазе. Хирургическая коррекция недостаточности замыкательной функции НПС при ГПОД составляет основу лечения этого заболевания. Согласно данным Института Gallop (США), 44% американцев по крайней мере один раз в месяц жалуются на изжогу, 7% испытывают ее ежедневно и 18% вынуждены прибегать к самолечению. Среди этих пациентов 20% страдают тяжелым рефлюксом, вызывающим такие осложнения, как синдром Barrett (10-15%), изъязвление (27%), стриктура (4-20%), кровотечение (2%). Вопрос об оперативном лечении рефлюкс-эзофагита (ГЭРБ) возникает, когда консервативная терапия не дает ожидаемого эффекта, несмотря на неоднократные курсы медикаментозной терапии и соблюдение всех рекомендаций по нормализации образа жизни. Консервативное лечение позволяет снизить остроту симптомов и не дать развиться осложнениям и не устраняет причину заболевания. Целью работы явился выбор наиболее рационального хирургического метода лечения при различных видах фундопликаций.

Современным методом выбора хирургического лечения ГЭРБ является лапароскопическая антирефлюксная операция. До настоящего времени наиболее распространенной остается операция Ниссена, но она имеет ряд недостатков: гиперфункция манжетки, гипофункция манжетки, “соскальзывающая” манжетка, “тянущая” манжетка, приводящая к латеральному изгибу абдоминального отдела пищевода, деформация желудка, феномен “песочных часов” при низком наложении манжетки, аксиальная ротация абдоминального отдела пищевода. Наиболее серьезным недостатком этой операции остается дисфагия, частота которой колеблется от 6 до 42%, что у ряда больных требует повторной операции. Некоторые авторы отдают предпочтение неполной фундопликации, при которой фундопликационная манжетка окутывает пищевод на 180—240°. Однако по данным других наблюдений, при этом типе операции достичь стойкого антирефлюксного эффекта не удается. В связи с этим остается актуальной проблема совершенствования методик антирефлюксных операций с восстановлением замыкательной функции НПС.
Хирургическое лечение.
Показания к оперативному лечению:
- Неэффективность консервативного лечения в течение 6 месяцев независимо от наличия или отсутствия диафрагмальной грыжи.
- Быстрый рецидив ГЭРБ после прекращения медикаментозного лечения.
- Явления рефлюкс-эзофагита.
- Осложнения ГЭРБ (пищеводные кровотечения, язва пищевода, пептические стриктуры пищевода, развитие пищевода Баррета, сочетание ГЭРБ с грыжей пищеводного отверстия диафрагмы).
Открытая фундопликация по Nissen. Основным методом хирургического лечения гастроэзофагеальной рефлюксной болезни является операция – фундопликация. Основной целью оперативного лечения является восстановление нормальной функции нижнего пищеводного сфинктера, неправильная работа которого как раз и позволяет желудочному содержимому попадать в пищевод, вызывая, тем самым, рефлюкс-эзофагит.
Суть способа заключается в следующем. Выполняли селективную проксимальную ваготомию (СПВ), при этом десерозированную малую кривизну желудка укрывали путем наложения швов на переднюю и заднюю стенки малой кривизны с мобилизацией не менее 5—6 см пищевода, дна желудка. С помощью турникета пищевод максимально низводили в брюшную полость.
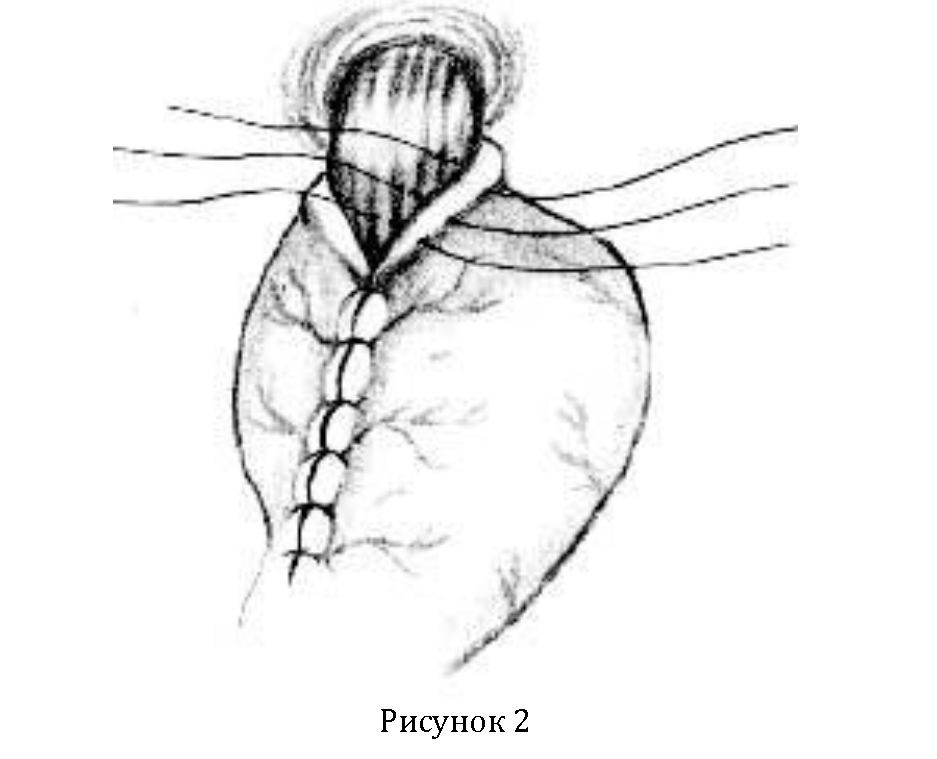
Накладывали шов-держалку на переднюю поверхность мобилизованного дна желудка и на левую стенку пищевода, отступив 3—4 см от эзофагокардиального перехода. Дно желудка заводили за пищевод и аналогичный шов-держалку накладывали на правую стенку пищевода. При этом из дна желудка создается треугольник, острый угол которого направлен к малой кривизне. Накладывали швы по сторонам этого треугольника, в результате создается определенное сдавление абдоминального отдела пищевода (Рисунок 2).
Описанный способ эзофагофундопликации применяют и в настоящее время при открытых операциях, если ГПОД сочетается с язвенной болезнью и требуется ее коррекция тем или иным методом. В клинике не используются дренирующие желудок операции, разработаны методики пилороподобных антирефлюксных гастродуоденоанастомозов с сохранением в большинстве наблюдений пассажа по двенадцатиперстной кишке.
Видеоэндохирургическая антирефлюксная лапароскопическая фундопликация. Очередной этап развития антирефлюксной хирургии пищеводножелудочного перехода наступил в связи с внедрением в практическую медицину эндоскопических технологий. Лапароскопическая фундопликация получила широкое распространение, так как она менее агрессивна и пациенты имеют более короткий период восстановления по сравнению с лапаротомией. Внедрен в клинику способ (Жерлов Г.К., Гюнтер В.Э., Кошель А.П., Козлов С.В., Рудая Н.С., Соколов С.А., Слугин Д.Г. Видеоэндохирургическая антирефлюксная лапароскопическая
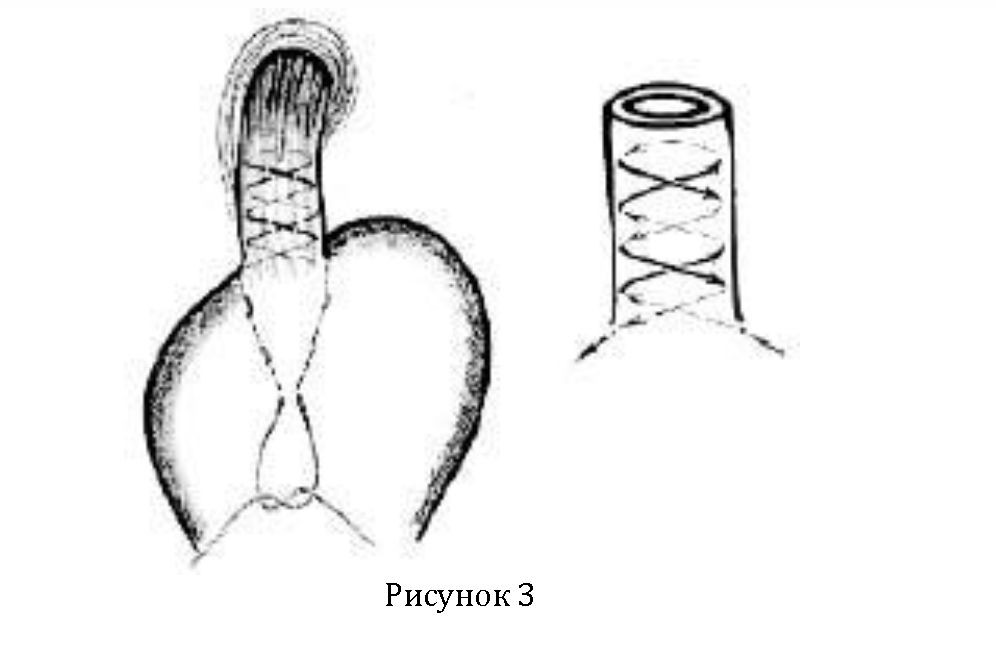
фундопликация.//2001.) осуществляется следующим образом. После введения в брюшную полость 5 троакаров производят мобилизацию проксимальной части малой кривизны желудка (по типу СПВ), 4—5 см дистальной части пищевода, дна желудка. Далее формируют искусственный НПС путем наложения непрерывного шва эластичной сверхтонкой нитью. Начинают шов в субкардиальном отделе на малой кривизне желудка, продолжают на правую стенку пищеводно-желудочного перехода и далее на заднюю стенку пищевода накладывают 2—3 спиралевидных витка по ходу циркулярных мышечных волокон пищевода в восходящем направлении. В общей сложности формируют 2—3 спирали общей высотой витков до 3 см. Затем шов продолжают в обратном (нисходящем) направлении — спиралевидно до левой стенки пищеводно-желудочного перехода и на малую кривизну желудка к началу шва, где узел завязывают интракорпорально (Рисунок 3).
При наложении непрерывного шва дозированно натягивают нить до создания в области формируемого НПС давления, равного 22—25 мм рт.ст. Интраоперационное измерение давления в области искусственного НПС производят по методу В.И. Оскреткова и В.А. Ганкова [5]. На конце толстого желудочного зонда укрепляют баллон, давление в котором передается на регистрирующее устройство. После
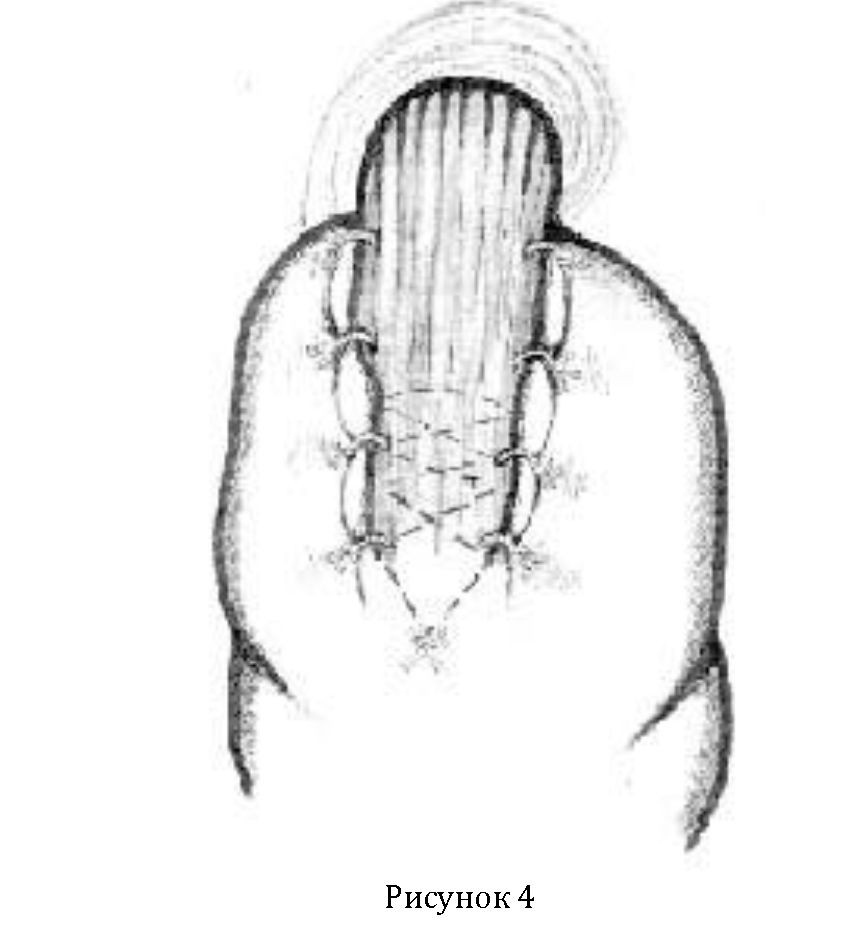
заполнения баллона воздухом формируют искусственный НПС. Способ завершают эзофагофундорафией путем наложения 3—4 швов по правой и левой стенке пищевода с целью формирования угла Гиса и клапана в области кардиальной вырезки (Рисунок 4). Давление в области искусственного НПС должно превышать давление в желудке в 2—2,5 раза.
Характеристики используемой нити из сплава никелид- титана:
- Напряжение деформации (прочность) нити толщиной 95 мкм до 1,5 кг.
- Гистерезисное напряжение тканей (величина деформации) 8%.
- Обратимая возвратная деформация (эластичность) 10%.
За период с 2001 г. по 2003 г. в клинике (Жерлов Г.К., Гюнтер В.Э., Кошель А.П., Козлов С.В., Рудая Н.С., Соколов С.А., Слугин Д.Г.) выполнены 26 лапароскопических антирефлюксных операций с формированием искусственного НПС. Давление в области НПС у пациентов после операции возросло в среднем на 70%. После операции с формированием искусственного НПС у 1 (3,8%) пациента отмечалась легкая дисфагия, купировавшаяся в течение 2 мес. В отдаленном послеоперационном периоде (от 1 года до 2,5 лет) после операций с формированием искусственного НПС обследованы 18 (69,2%) пациентов. Согласно результатам опроса и анкетирования, 17 (94,4%) пациентов оценивали свое состояние как отличное и хорошее, 1 — как удовлетворительное. При рентгенологическом исследовании, ЭГДС признаков недостаточности кардии не обнаружено ни у одного пациента.
Таким образом, разработанный способ видеоэндохирургической антирефлюксной лапароскопической операции с моделированием искусственного НПС является выбором хирургической тактики при рефлюкс-эзофагите и обеспечивает создание зоны повышенного давления в абдоминальном отделе пищевода, что является основой профилактики рецидива симптомов заболевания. Сформированный искусственный НПС за счет свойств нити не подвергается рубцеванию, остается эластичным и позволяет сохранить проходимость кардии, что отвечает основным требованиям, предъявляемым к антирефлюксным операциям.
Видеоэндохирургическая антирефлюксная лапароскопическая фундопликация менее агрессивна и пациенты имеют более короткий период восстановления по сравнению с лапаротомией, дает хорошие отдаленные результаты (94,4%) до 3 лет.
СПИСОК ЛИТЕРАТУРЫ
- Билхарц Л.И. Осложнения гастроэзофагеальной рефлюксной болезни. //Рос. Журн. Гастроэнтерол. гепатол. – 1998. - №5. – С. 69—76.
- Кубышкин В.А., Корняк Б.С. Гастроэзофагеальная рефлюксная болезнь. Диагностика, консервативное и оперативное лечение. - М.: 1999. – 208 с.
- Оскретков В.И., Ганков В.А. Результаты хирургической коррекции недостаточности замыкательной функции кардии. //Хирургия. - 1997. - №8. –С. 43—46.
- Ривкин В.Л. Лапароскопическая фундопликация. //Международный конгресс по эндоскопической хирургии, 5-й: Тезисы. Эндоскоп хир. - 1998. - №1. – С. 34—36.
- Сигал Е.И., Бурмистров М.В., Петрунин В.М. Преимущества лапароскопической фундопликации при грыжах пищеводного отверстия диафрагмы перед традиционной открытой. //Эндоскоп хир. – 1998. - №1. – С. 49.
- Федоров В.Д., Кубышкин В.А., Корняк Б.С. Гастроэзофагеальная рефлюксная болезнь и миниинвазивная хирургия. //Эндоскоп хир. – 1999. - №2. – С. 67.
- Черноусов А.Ф., Шестаков А.Л. Хирургическое лечение рефлюкс-эзофагита и пептической стриктуры пищевода. // Хирургия. – 1998. - №5. - С. 4—8.
- Черноусов А.Ф., Богопольский П.М., Курбанов Ф.С. Хирургия пищевода: Руководство для врачей. - М.: Медицина. - 2000. – 320 с.
- Черноусов Ф.А. и соавт. Оценка эффективности фундопликации по методике РНЦХ // Вестник хирургической гастроэнтерологии. - 2010. - № 3. - С. 126-127.
- Черноусов Ф.А. и соавт. Качество жизни у пациентов в отдаленном послеоперационном периоде после фундопликации в модификации РНЦХ // Вестник хирургической гастроэнтерологии. - 2010. - № 3. - С. 126.
- 5. Черноусов Ф.А., Шестаков А.Л. и соавт. Первые результаты лапароскопической фундопликации, селективной проксимальной ваготомии в модификации РНЦХ//Альманах института Хирургии им. А.В. Вишнев-ского. - 2010. - № 1 (1). – С. 34.
- Anvari M., Allen С. Incidence of dysphagia following laparoscopic Nissen fundoplication without division of short gastric vesels. //Surg Endosc. – 1996. - №10. – Р. 199.
- Champault G., Volter F., Rizc N. et al. Gastroesophageal reflux: Conventional Surgical Treatment Versus Laparosc. //Eur J Coelio-Surg. – 1997. - №2 – Р. 32—38.