Проанализированы результаты лечения 40 пациентов, с очаговыми заболеваниями печени на фоне цирроза. Очаговые заболевания печени на фоне цирроза значительно суживает показания к оперативному лечению, утяжеляет течение основного заболевания и послеоперационного периода. Применяемый алгоритм ведения больных в предоперационном, интраоперационном и послеоперационном периоде позволяет увеличить процент радикально оперированных больных, уменьшить осложнения и летальность. Ограниченная возможность радикального лечения и высокий риск летального исхода после резекции печени – две основные грани этой проблемы. Определение показаний к операции, объема резекции, с активной предоперационной подготовкой, и последующего послеоперационного ведения, является основополагающим в решении этой проблемы.
Введение:
Последние годы отмечается тенденция к росту заболеваемости населения различными очаговыми поражениями печени, что связано как с ростом количества больных, так и с улучшением диагностики [1,3,5]. Сопутствующее поражение хроническим вирусным гепатитом и циррозом значительно утяжеляет течение болезни, иногда являясь ее первопричиной [7]. Резекция печени остается единственным способом радикального лечения пациентов с различными очаговыми поражениями печени [1,2,3,5]. Количество таких операций последние годы увеличивается. В то же время резекция печени является операцией высокого риска развития в послеоперационном периоде тяжелой печеночно - почечной недостаточности, часто приводящей к летальному исходу [1,2,4,5].
При наличии сопутствующего диффузного процесса (гепатит, цирроз) риск печеночно-почечной недостаточности значительно увеличивается. Определение показаний и противопоказаний к операции, использование оригинальных способов введения современных лекарственных препаратов в послеоперационном периоде, позволит повысить процент радикально оперированных больных с очаговыми поражениями печени на фоне хронического вирусного гепатита и цирроза и снизить вероятность развития некурабельной печеночно- почечной недостаточности после резекции печени.
Цель работы. Улучшение результатов хирургического лечения больных с очаговыми поражениями печени на фоне сопутствующего хронического вирусного гепатита, эхинококкоза, альвеококкоза и цирроза.
Материалы и методы. В отделении плановой хирургии с центром гепатопанкреатобилиарной хирургии и трансплантации печени городской клинической больницы №7 г. Алматы с 2012 по 2014г. находились на лечении 40 больных с очаговыми поражениями печени с сопутствующим хроническим вирусным гепатитом и эхинококкозом, альвеококкозом и циррозом в возрасте от 16 до 70 лет, женщин-16(35,1%), мужчин-24(64,9%).
Первичный рак печени выявлен у 10(25%) больного, метастатическое поражение у 6(15%), альвеококкоз у 7(17,5%), эхинококкоз у 11(27,5%), ГЦР у 6(15%).
Сопутствующее диффузное поражение: хронический вирусный гепатит В-10(25%), хронический вирусный гепатит С -2(5%), хронический вирусный гепатит В + С - 3(7,5%), цирроз печени вирусной В этиологии -1(4%), цирроз печени вирусной С этиологии - 7(17,5%), цирроз печени вирусной В + D -1(4%), цирроз печени вирусной В + С - 1(4%), паразитарные заболевание - 15(37,5%)
Функциональная активность по Child-Pugh: класс А - 5(50%), В - 4(40%), С - 1(10%).
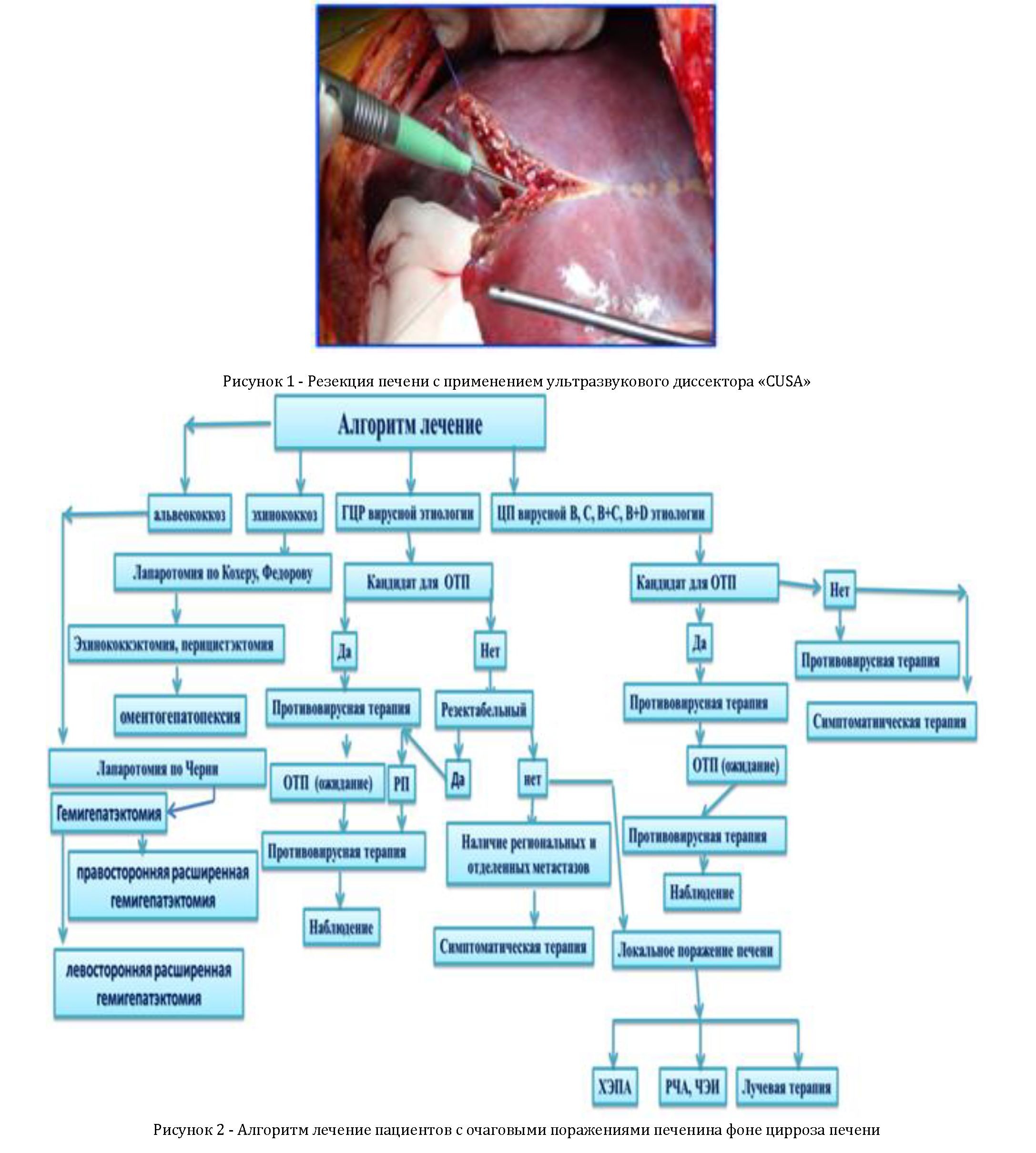
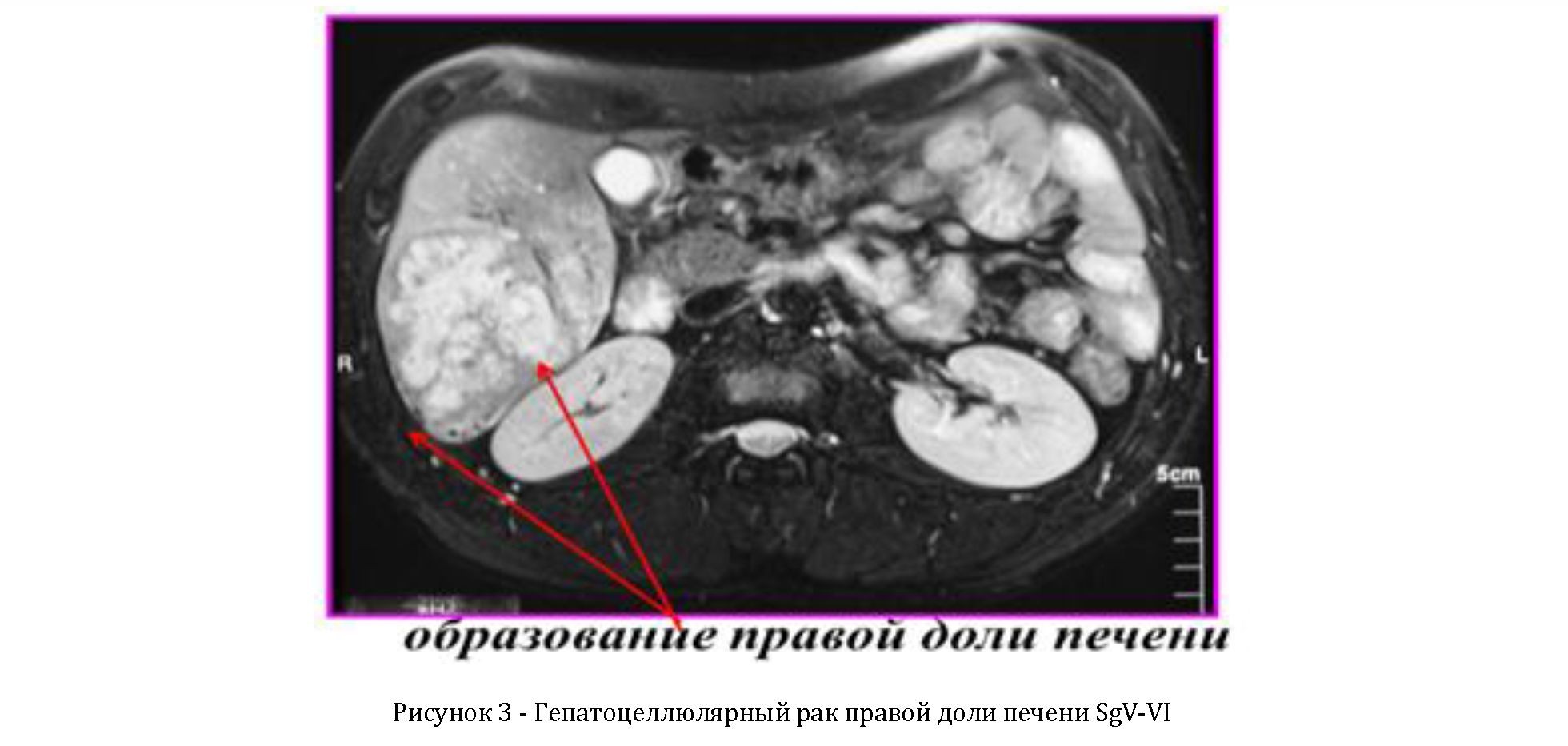
Предложен алгоритм диагностики и предоперационного отбора пациентов, предоперационной подготовки, алгоритм технических приёмов, используемых во время операции, с применением физических методов (ультразвуковой деструктор - CUSA, аргоноплазменный коагулятор), схема послеоперационного ведения больных (рисунок 1, 2, 3).
Резекция печени в различном объеме выполнена 24(60%) пациентам, 16(40%) пациентам оперативное лечение не производилось из-за распространенности процесса, из них 2- вследствие декомпенсации диффузного поражения печени. Все больные оперированы под интубационным многокомпонентным наркозом. Хирургический доступ определялся локализацией, размерами патологического образования, конституциональными особенностями пациента: верхнесрединная лапаротомия - у 6 -ти, лапаротомия по Черни - у 13-х, Кохера-Федорова - у 5-х. При локализации патологического процесса в I-V сегментах применяли верхнесрединную лапаротомию, в области VIVIII сегментов - абдоминальную часть по Черни или Кохера. Ни в одном случае не приходилось дополнять разрез торако- или френотомией.
Резекционные вмешательства выполнены по поводу следующих заболеваний: первичный рак печени - 11 (45,8%), аденома печени - 2 (8,3%),альвеоккокоз - 5 (20,8%), эхинококкоз - 2 (8,3%), мтс поражение - 1 (4,1%), гемангиома - 2 (8,3%), гамартома - 1 (4,1%). Резекции печени выполнены в следующем объеме: сегментэктомии - 1 (4,1%), бисегментэктомии - 1 (4,1%), трисегментэктомии - 1 (4,1%), правосторонняя гемигепатэктомии -3 (12,5%), правосторонняя расширенная гемигепатэктомия - 3 (12,5%). Левосторонняягемигепатэктомия выполнена в 1 случай (4,1%), в расширенном варианте в 3 (12,5%) случаях, эхинококкэктомия 11(45,8%) случаях.
Учитывая изначально пораженной диффузным процессом печеночной ткани и, следовательно, ее низкий функциональный статус, с целью профилактики послеоперационной печеночно- почечной недостаточности предложен алгоритм предоперационного отбора пациентов и схема послеоперационного ведения. Профилактика послеоперационной печеночно-почечной недостаточности начинается с этапа определения показаний и противопоказаний к операции с расчетом объема остающейся паренхимы после резекции печени. Абсолютным противопоказанием к резекции печени считаем цирроз класса С по Child-Pugh. Относительное противопоказание - высокая активность хронического гепатита. При выполнении резекции печени на фоне цирроза в отношении объема остающейся паренхимы печени придерживаемся следующих принципов - объем остающейся паренхимы, рассчитанной по КТ, при циррозе класса В по Child-Pugh должен быть не менее 60%, класса А не менее 50%. На фоне хронического гепатита сегмент - и бисегментэктомии выполнены в 2(8,3%) случаях, гемигепатэктомии в 4 (16,6%)случаях, расширенные вмешательства в 6 (25%) случаев. На фоне цирроза класса А и В по Child - Pugh операции в объеме би - и трисегментэктомии выполнены в 5 (20,8%) случаях, гемигепатэктомии в 4 (16,6%) случаях, в расширенном варианте в 1 (4,1%) случае.
Результаты и обсуждение.
Явления печеночно-почечной недостаточности легкой и средней степени зафиксированы у всех пациентов с хроническим гепатитом, которым были выполнены резекции печени в объеме геми- и расширенной гемигепатэктомии (n=10). Одной больной, которой была выполнена правосторонняя гемигепатэктомия, в послеоперационном периоде проводилось внутрипортальное введение гепатопротекторов. Явлений печеночно-почечной недостаточности у данной пациентки зафиксировано не было. У больных с сопутствующим циррозом после резекции печени также наблюдали явления печеночно - почечной недостаточности различной степени тяжести. Повышение уровня ферментов (маркеров цитолиза) составило: АСТ - 556,8+130u/l, АЛТ -
351,3+110u/l, маркеры холестаза - ЩФ - 560,3+90,4ЕД\л, ГГТП - 190+2ед\л., протромбин - 53%+11%. Асцитическое отделяемое по дренажам увеличивалось со 2-3 суток и продолжалось вплоть до выписки пациента из стационара. В послеоперационном периоде умерло 2 (57,1%) больных на фоне цирроза с «плотной» тканью печени после трисегментэктомии, правосторонней гемигепатэктомии и расширенной правосторонней гемигепатэктомии. Биопсия печени показала наличие репаративной регенерации поражённой диффузным процессом печёночной ткани.
В раннем послеоперационном периоде у 8(57,1%) радикально оперированных больных без использования алгоритма вне зависимости от объёма операции и характера сопутствующего диффузного поражения наблюдали острую печёночную недостаточность средней и тяжёлой степени.
При анализе течения послеоперационного периода критическим и переломным моментом являются 7-8 сутки (максимум уровня маркеров цитолиза и холестаза), когда происходит резкое снижение энергетического потенциала печеночной ткани и декомпенсация всех функций печени. Морфологически печень в данный период представлена паренхимой каменистой плотности с выдавливанием узлов регенератов, что нами выявлено у больных при релапаротомии и результатах вскрытия умерших больных.
При определении показаний к резекции печени на фоне цирроза, выполнение операций и ведения пациента в послеоперационном периоде следует также ориентироваться на морфологическую интраоперационную картину и разделять цирроз на мягкий (крупноузловой) и плотный (мелкоузловой), как один из факторов прогноза послеоперационной печеночно-почечной недостаточности и т. к. не цирроза являются
При наличии плотного вмешательства летального исхода. расширенные нецелесообразными, продолжительность летальному исходу.
целесообразны сегментарные и периопухолевые резекции с максимальным сохранением печеночной паренхимы. Перспективным методом, вероятно, будет радиочастотная увеличивают приводят к больных более жизни и зачастую В этой группе деструкция очагов при наличии соответствующего оборудования.
Выводы:
Хирургическое лечение пациентов с очаговыми поражениями печени ассоциированных с диффузными заболеваниями является сложнейшей проблемой хирургической гепатологии.
Ограниченная возможность радикального лечения и высокий риск летального исхода после резекции печени - две основные грани этой проблемы.
Определение показаний к операции, объема резекции, с активной предоперационной подготовкой, и последующего
послеоперационного ведения, является основополагающим в решении этой проблемы.
Прогнозирование объема остающейся паренхимы и разработанный алгоритм послеоперационного ведения пациентов с внутрипортальнойинфузиейгепато протекторов уменьшает тяжесть печеночной недостаточности - главной причины летального исхода в послеоперационном периоде.
Заключение: Очаговые заболевания печени на фоне циррозазначительно суживает показания к оперативному лечению, утяжеляет течение основного заболевания и послеоперационного периода. Применяемый алгоритм ведения больных в предоперационном, интраоперационном и послеоперационном периоде позволяет увеличить процент радикально оперированных больных, уменьшить осложнения и летальность.
Ограниченная возможность радикального лечения и высокий риск летального исхода после резекции печени - две основные грани этой проблемы.
Определение показаний к операции, объема резекции, с активной предоперационной подготовкой, и последующего послеоперационного ведения, является основополагающим в решении этой проблемы.
СПИСОК ЛИТЕРАТУРЫ
- Вишневский В.А., Кахаров М.А., Камолов М.М. Радикальные операции при эхинококкозе печени // Актуальные вопросы хирургической гепатологии: Сб. тезисов XII Международного конгресса хирургов-гепатологов стран СНГ. — Ташкент, 2005. — С-106.
- Гарин А.М., Базин И.С. Первичный рак печени / Десять наиболее распространенных злокачественных опухолей. -2006. - C.197- 220.
- Новзурбеков М. С.,Донова Л. В., Ходарева Е. Н., Андросова М. В.,Чжао А.В., Невмержицкий В.И. Прогностические критерии печеночной недостаточности после резекции печени при ее очаговом поражении // Анналы хирургической гепатологии, 2009 т.14, No 1. - 41 - 48.
- Пасечник И.Н., Кутепов Д.Е. Печеночная недостаточность - современные методы лечения / / МИА. 2009. - 12 - 135.
- Рахманова А. Г. Хронические вирусные гепатиты и цирроз печени // М.: Медицина - 2006, - 210 с.
- Краснов О.А., Павленко В.В., Краснов К.А., Краснов А.О., Пельц В.А., Старцев А.Б., Аминов И.Х., Сохарев А.С., Керопян С.Е. Современные методы оценки функционального резерва печени в резекционной хирургии // Медицина и образование в Сибири. 2014 г.- № 6.
- Garcia M. et al. American Cancer Society, 2007. www.cancer.org. Accessed March 20, 2008. 6. http://www.who.int/mediacentre/factsheets/fs297/en/index.html. Accessed June, 2008.
- Мurata S. Однократное введение тромбопоэтина предотвращает прогрессирование фиброза печени и стимулирует регенерацию печени после ее резекции у крыс с циррозом //Аnn. Surg.2008, V. 248(5).Р. 821 - 828 - Анналы хирургической гепатологии, 2009, т. 14. No 1. 112 - 113 с
- Kazaryan A.M. et al. Comparative evaluation of laparoscopic liver resection for posterosuperior and anterolateral segments. Surg.Endosc. 2011; 25: 12: 3881—3889.
- Kitisin K. et al. A current update on the evolution of robotic liver surgery. Minerva.Chir. 2011; 66: 4: 281—93.
- Nadalin S., Li J., Lang H. et al. The White test: a new dye test for intraoperativedetection of bile leakage during major liver resection. Arch.Surg. 2008; 143: 402-404.
- Rahbari N.N., Koch M., Schmidt T. et al. Metaanalysis of the clampcrushing technique for transection of the parenchyma in elective hepatic resection: back to where we started? Ann. Surg.Oncol. 2009; 16: 630—639.
- Schnelldorfer T., Ware A.L., Smoot R. et al. Management of giant hemangioma of the liver: resection versus observation. J. Am. Coll.Surg. 2010; 211: 6: 724—730.
- Aloia T.A., Fahy B.N., Fischer C.P. et al. Predicting poor outcome following hepatectomy: analysis of 2313 hepatectomies in the NSQIP database. HPB (Oxford). 2009; 11: 510-515.
- Erdogan D., Busch O.R.C., van Delden O.M. et al. Incidence and management of bile leakage after partial liver resection. Dig.Surg. 2008; 25: 60-66.
- Schnitzbauer A.A. et al. Right portal vein ligation combined with in sity splitting induces rapid left lateral liver lobe hypertrophy enabling 2-staged extended right hepatic resection in small-for-size settings. Annals of surgery. 2012; 255: 3: 405-414.
- Wong S., Mangu P., Choti M., Crocenzi T., Dodd G., Dorfman G., Eng., Fong Y., Giusti A., Lu D., Marsland T., Michelson R., Poston G.,Schrag D., Seidenfeld J., Benson A. American Society of ClinicalOncology 2009 Clinical Evidence Review on Radiofrequency Ablationof Hepatic Metastases From Colorectal Cancer. J.Clin.Oncol. 2009;28: 493-508.
- 52. Yao F.Y. et al. Liver transplantation for hepatocellular carcinoma:validation of the UCSF-Expanded criteria based on preoperativeimaging. AmJ.Transpl. 2007; 7: 11: 2587-2596.