На основе анализа 11 случаев расслоения аорты были представлены основные диагностические и лечебные мероприятия при данной патологии в условиях ургентной хирургии. Индекс клинической настороженности при расслоении аорты остается низким. Незамедлительное проведение УЗИ в области локализации болей позволяет сократить время диагностики. Антигипертензивное лечение даже при незначительном повышении артериального давления позволяет остановить дальнейшее распространение расслоения тканей по аорте.
Введение. Расслоение аорты относится к редким заболевание встречается относительно редко, часто её заболеваниям, уровень заболеваемости колеблется от 5 до исход является смертельным, и многие пациенты с 30 случаев на миллион человек в год [1-3]. Хотя данное расслоением аорты умирают до госпитализации в больницу или до постановки диагноза.
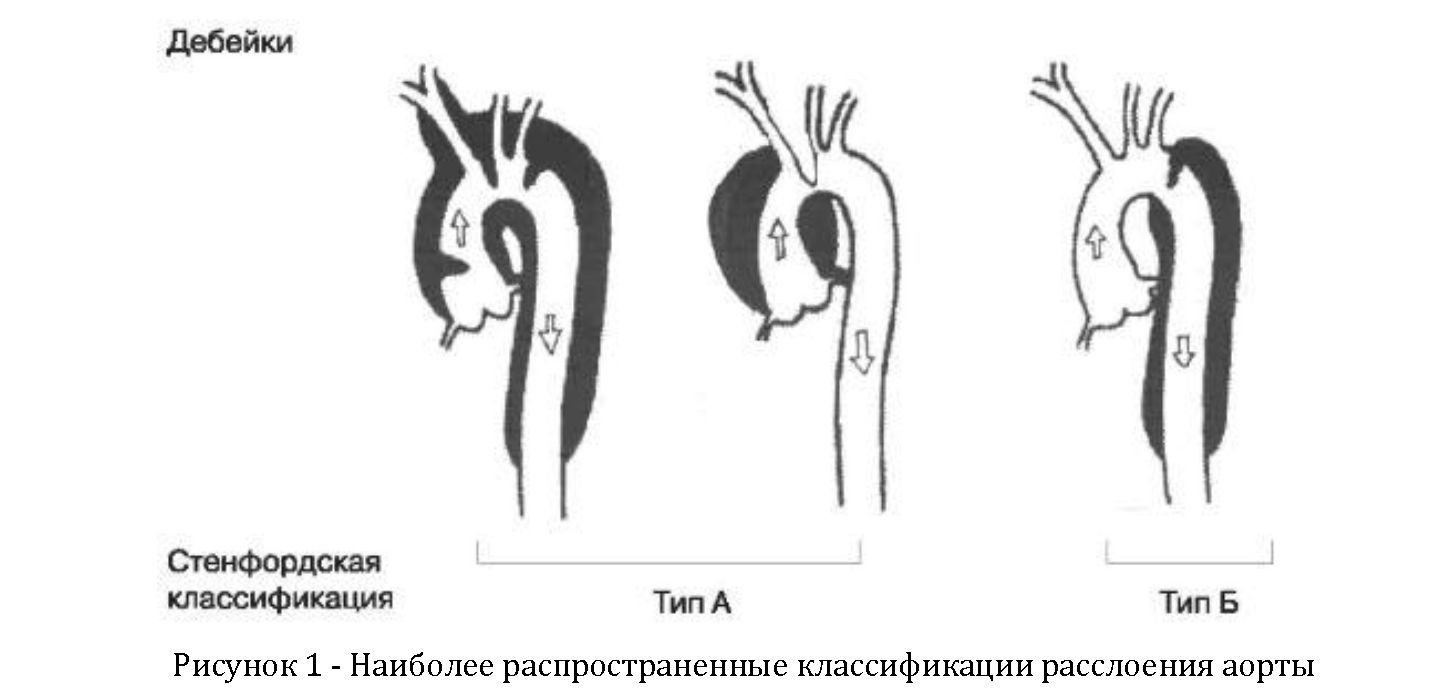
Существует три классификации РА по локализации: Дебейки, Стенфордская и описательная (Рисунок 1). Классификация Дебейки включает в себя следующие 3 типа: тип I - поражение восходящей и нисходящей аорты; тип II - изолированное поражение восходящей аорты; тип III - поражение нисходящей аорты.[4] Стенфордская классификация состоит из 2 типов: тип А - расслоение восходящей аорты (включает тип I и тип II по классификации Дебейки); тип В - расслоение нисходящей аорты без вовлечения восходящей.[5] Следовательно описательной классификации проксимальный тип включает тип А, дистальный включает тип В. Расслоение восходящей аорты (Тип А) встречается в 2-4 раза чаще, характеризуется высокой догоспитальной летальностью, высокой частотой ранних фатальных осложнений и требует неотложного хирургического вмешательства; расслоение нисходящей аорты (тип Б) лечится обычно консервативно.[5] По течению заболевания расслоение аорты делится на острый и хронический типы. При остром расслоении аорты диагноз ставится в течении 2 недель после первоначального проявления симптомов. Диагноз хроническое расслоение аорты имеет место при давности симптомов свыше 2 недель. Хроническое расслоение аорты встречается у каждого третьего пациента. [2]
Расслоение аорты развивается у мужчин чаще, и соотношение мужчин/женщин по разным источникам варьирует от 2:1 до 5:1. [1,3,6] Проксимальное расслоение аорты наиболее часто приходиться на возраст от 60 до 70 лет. Хроническая артериальная гипертензия является самым распространенным предрасполагающим фактором и выявлена у 62-78¿ пациентов с расслоение аорты. [1-2,7] Первичное проявление заболевания более свойственно пациентам с проксимальным нежели с дистальным расслоением аорты (70¿ vs 35¿). Такие заболевания аорты, как аортальная дилатация, аневризма аорты, аннулоаортальная эктазия, хромосомальные абберации (например, синдром Шерешевского-Тёрнера, синдром Нунан), гипоплазия дуги аорты, коарктация аорты, аортальный артериит, бикуспидальный аортальный клапан и наследственные заболевания соединительной ткани (например, синдром Марфана, синдром Элерса-Данлоса) являются предрасполагающими факторами к развитию расслоения аорты. [3] Большинство пациентов с расслоением аорты младше 40 лет страдают синдромом Марфана.
Риск развития расслоения аорты повышается при беременности. У женщин старше 40 лет в 50¿ случаев расслоение аорты развивается во время беременности. Гипертензия выявлена в 25-50¿ случаев расслоения аорты при беременности. Самым распространенным расположением расслоения при беременности является проксимальная часть аорты, и 75¿ случаев разрыв интимы происходит в пределах 2 см от аортального клапана. Разрыв аорты часто происходит во время третьего триместра или во время первого периода родов.
Боль является самым распространенным симптомом при расслоении аорты. Боль появляется в разных местах грудной клетки, в зависимости от расположения расслоения. Боли достигают наивысшего уровня в первые минуты. Характер боли может быть острым, рвущим, режущим, но внезапность боли - это самая специфическая характеристика при расслоении аорты. Боль иррадиирует в шею, плечо или руку, также как и при инфаркте миокарда. По данным Международного Реестра Острого Расслоения
Аорты [1] по 464 пациентам, в 95¿ случаях проявлялись боли, в 85¿ случаев боль начиналась резко. Острая боль была у 64¿ пациентов, тогда как классическая рвущая боль была отмечена у 51 ¿ пациентов. Боль чаще локализовалась спереди (73¿). Боль в спине появлялась у 53¿ пациентов, и абдоминальная боль была отмечена у 30¿ пациентов.
Расслоение аорты также было диагностировано при случайных обследованиях, таких как черезпищеводная электрокардиография (ЧПЭКГ), КТ или МРТ, которые проводились по иным причинам [8-9]. Возможно, что боль у этих пациентов была незначительной, и расслоение аорты прошло незамеченным.
Более трети пациентов с расслоением аорты имели вторичные признаки и симптомы вовлечения других систем. [10] Самый распространенный механизм - это ишемия, вызванная обструкцией веток аорты.
Хотя большинство пациентов с расслоением аорты страдают гипертензией, начальное АД ниже 100 мм рт.ст. наблюдалось у 25¿ пациентов. Гипотензия и шок у пациентов с расслоением аорты вызваны острой тяжелой аортальной регургитацией, разрывом аорты, тампонадой сердца или левожелудочковой систолической дисфунцией. Распространение расслоения в перикардиальную полость может привести к гемоперикарду или к смерти. [10] Аритмии, наблюдаемые у 10-15¿ пациентов, вызваны недостаточным коронарным кровообращением.
Недостаточное коронарное кровообращение также может быть вызвано сдавлением коронарных сосудов расширенной за счет ложного просвета аорты, распространением расслоения на стенки коронарных сосудов, гипотензией, либо комбинацией вышеназванных патологический состояний. [3] Вовлечение правой коронарной артерии происходит чаще, чем левой артерии.
Ишемия миокарда с систолической дисфункцией левого желудочка способствуют развитию гипотензии и шока у пациентов с расслоением аорты.
Неврологическая патология развивалась в 18-30¿ случаев.
Наиболее частым проявлением, связанным с расслоением аорты является церебральная ишемия (5-10%). [12] При проксимальной форме расслоения аорты до 12
случаев наблюдается синкопе. [13] Вовлечение в процесс спинного мозга наблюдалось в 10% случаев. [12] Поражение спинного мозга при расслоении аорты приводит к различным спинномозговым синдромам, как трансверсальный миелит, прогрессивная миелопатия, передний спинномозговой синдром, параплегия и квадриплегия. [14]
Поражение периферического нерва при данной патологии встречается редко, это может привести к парестезии в бедрах, осиплости голоса, ишемической люмбо-сакральной плексопатии. [13-15]
Легочные проявления при расслоении аорты встречаются редко. При расслоении нисходящей аорты, местом скопления крови является левая плевральная полость. [16] Безболевая форма расслоения аорты может быть расценена как нетравматичный левосторонний гемоторакс. Описаны редкие случаи, когда расслоение переходило на легочную артерию или сдавливало ее или паренхиму легких, что приводило к тяжелым гемодинамическим рассройствам, одностороннему отеку легких или гемоптизису. [17]
Острое желудочно-кишечное кровотечение упоминается в литературе очень редко. [18]
von Kodolitsch Y. et al [19] разработали модель предугадывания расслоения аорты на основании анамнеза и лабораторно-инструментальных исследований. Было исследовано 250 пациентов с острой болью в груди, спине. Следующие симптомы были признаны, как предвестники расслоения аорты: острая боль в груди или спине, разрывающего характера; разница пульса и/или разница АД; расширение средостения и/или расширение аорты. Оценка этих 3 переменных позволила выявить 96% случаев расслоение аорты. Вероятность расслоения была высока (т.е., ≥ 83%) с изолированным различием пульса или АД или любой комбинацией этих трех переменных, средняя с изолированной аортальной болью (31%) или расширением средостения (39%), и вероятность была низкой (7%) с отсутствием всех трех переменных. Эта простая клиническая модель могла быть полезна для быстрой оценки начальных признаков расслоения аорты.
Диагностика расслоения аорты начинается с клинической настороженности, которая является самым решающим шагом в диагностировании этой катастрофической болезни. Следующие два важных шага в оценке пациентов с подозрением на расслоение аорты должны подтвердить наличие расслоения и дифференцировать проксимальное и дистальное расслоение. Разграничение этих особенностей должны быть важной частью диагностической тактики для пациентов с подозрением на расслоение аорты. [20]
Выбор ранней диагностики расслоение аорты зависит главным образом от наличия соответствующей диагностической аппаратуры в лечебном учреждении. Диагностическими методами расслоения аорты являются КТ, МРТ, ТТЭ и ангиография. По данным различных исследований, каждый из этих методов визуализации, обладает высокой чувствительностью, специфичностью и диагностической точностью. Тем не менее, они могут значительно различаться в зависимости от распространенности расслоения аорты.
По данным Jagannath A.S., Sos T.A., Lockhart S.H. et al. (1986) рентгенография грудной клетки не является специфичной для диагностики расслоения аорты, однако расширение тени средостения, изменение конфигурации аорты, локализованной на горб дуге аорты, расширение дистального отдела аорты после левой подключичной артерии, утолщение стенки аорты, обозначенной шириной тени аорты за кальцификацией интимы, смещение кальцификации в аортальной дуге, двойная аортальная тень, разница в размерах восходящих и нисходящих отделах аорты, и наличие гемоторакса, чаще слева в 50% случаев наводили на мысли о расслоении аорты. [21]
КТ является наиболее распространенным методом исследования при начальной диагностике, который был проведен в пациентов, включенных в Международный регистр острого расслоения аорты.[1,22] Чувствительность КТ при диагностике расслоения аорты составляет от 83 до 94%, а специфичность от 87 до 100%, за исключением случаев расслоения восходящей аорты, при котором его чувствительность <80%. [23-24] Основные недостатки использования КТ, кроме проблем с использованием контрастного вещества, являются следующие: трудности в определении места разрыва интимы; трудность в оценке вовлечения веток аорты; и неспособность предоставить информацию о регургитации аортального клапана. [20]
МРТ может обнаружить расслоение аорты, точно оценить масштабы расслоения, продемонстрировать место начала разрыва, определить вовлеченные сосуды дуги, и оценить участие почечной артерии. [25] В исследованиях, которые сравнивали МРТ с ТПЭ или КТ [26] чувствительность и специфичность МРТ была выше среди пациентов с предшествующими заболеваниями аорты. Кроме того, МРТ дает возможность выполнить трехмерную реконструкцию изображений в любой плоскости.
К недостаткам МРТ относятся длительность обследования, ограниченность доступа к пациенту и контроля жизненно важных органов, особенно у больных с нестабильной гемодинамикой. [27]
Чувствительность и специфика TTЭ при диагностике расслоения аорты колеблются от 35 до 80% и 39 - 96%, соответственно, в зависимости от анатомического местоположения расслоения. [28] С введением двумерной эхокардиографии и возможностью обзора супрастернальной, субкостальной и субстернальной проекций стало возможным обследование восходящей аорты и дуги аорты на наличие отслойки и разрыва интимы, ложных просветов. Однако, несмотря на это, исследование аорты методом ТТЭ остается трудным из-за технических ограничений, узких межреберных мест, ожирения и легочной эмфиземы. Поэтому ТТЭ не является окончательным методом диагностики расслоения аорты.
ЧПЭКГ широко доступна, безопасна и может быть выполнена быстро и легко у кровати пациента. Чувствительность ЧПЭКГ составляла целых 98%, и диапазоны специфики от 63 до 96%. [29-31] ЧПЭКГ определяет место начала расслоения, присутствие тромба в ложном просвете, аномальные характеристики потока, участие коронарных сосудов и веточек арки, наличие, степень и гемодинамическое значение гемоперикарда, и присутствие и тяжесть аортальной регургитации.
Главный недостаток ЧПЭКГ - ее сильная зависимость от опыта врача-диагноста и трудности в объективном документировании патологических результатов для сравнения с последующими исследованиями. Поле зрения ограничено грудной и проксимальной брюшной аортой, таким образом периферическое расширение расслоения ниже чревного ствола при ЧПЭКГ визуализироваться не может. Кроме того, ЧПЭКГ не может быть выполнена у пациентов с варикозным расширением вен или стенозом пищевода. [32]
При диагностике расслоения аорты чувствительность аортографии составляет 86-88%, а специфичность 75-94%. [33-34] ранее аортография была методом выбора, но сейчас из-за инвазивности и длительности этот метод исследования используется редко.
Некоторые исследования [35-36] выявили биохимический маркер расслоения аорты. При расслоении аорты повреждается мышечный слой сосудов, что приводит к высвобождению структурных белков из клеток гладких мышц, в том числе к высвобождению тяжелой цепи миозина. Для выявления тяжелой цепи миозина гладкой мускулатуры был разработан специальный иммунологический анализ. Он рассматривается как потенциальный метод ранней диагностики расслоения аорты. [35-36] Сывороточный уровень тяжелой цепи миозина увеличивается в первые 6 часов после начала расслоения аорты. [36]
Медикаментозное лечение является эффективным методом лечения на начальном этапе. Антигипертензивная терапия должна быть проведена в экстренном порядке у всех пациентов, исключая пациентов с гипотонией, как только возникает подозрение на расслоение аорты. Цель данной терапии – снизить нагрузку на левый желудочек, снизить пульсовую волну аорты, и снизить артериальное давление настолько, насколько это возможно, без снижения перфузии жизненно важных органов. Снижение роста аортального пульса путем уменьшения нагрузки на левый желудочек может замедлить расспространение расслоения аорты и снизить риск разрыва аорты. [37]
Потенциальными трудностями, возникающими в ходе лечения могут быть распространение расслоения, расширение аневризмы и компрессия соседних структур, в результате чего снижается кровоснабжение органа.
Хирургическое лечение показано всем больным с проксимальным расслоением, за исключением пациентов с серьезными сопутствующими заболеваниями, которые являются противопоказаниями к операции. [38] Инсульт часто является противопоказанием к операции, поскольку существует реальная угроза того, что антикоагулянтная терапия и реперфузии может привести к дальнейшему ухудшению неврологического статуса путем преобразования ишемического инсульта в геморрагический инсульт. Тщательное исследование на наличие гемоперикарда и гемоторакса, распространения расслоения на крупные ветви аорты, локализация начала расслоения, и наличие тромбоза в ложном просвете дает информацию, которая может быть полезна при планировании тактики и степени оперативного вмешательства. [39] Показаниями для проведения ранней операции у пациентов с дистальным расслоением являются быстрое расшиерение аневризмы, кровоизлияние, угроза разрыва, постоянная и некупируемая боль и/или нарушение кровотока в органах или конечностях. [40-41]
До сих пор нет единого мнения о наилучшей хирургической тактике при расслоении аорты. Самые известные хирургические техники – это операция Бенталла-ДеБоно, операция Каброля, эндопротезирование «elephant trunk».
[41] Целью хирургического вмешательства является ремоделирование места начала расслоения, но не замена всего поврежденного участка. У половины оперирорваннных пациентов часть расслоенной аорты сохраняется.
Применения клея для соединения разделенных слоев аорты значительно снизило частоту замены аортального клапана, а также частоту интра- и послеоперационного кровотечений и осложнений. Интерес заслуживают новые подходы эндопротезирования с применением гибридных протезов, получившие название «замороженный хобот слона» (frozen elephant trunk). [41]
Цель: улучшение алгоритма диагностики расслоения аорты при оказании помощи в общехирургических стационарах в условиях ургентной хирургии.
Задачи:
- Изучить патогномичные симптомы расслоения аорты.
- Изучить основные методы диагностики расслоения аорты и их достоверность.
- Определить алгоритм диагностики расслоения аорты.
- Определить тактику лечения в условиях стационара общего профиля.
Материалы и методы. Проведен ретроспективный анализ 11 историй болезни пациентов с расслоением аорты на базе ГКБ №7 г. Алматы в 2009-2015гг. На основании жалоб изучены наиболее частые начальные признаки расслоения аорты. Также был рассмотрен перечень диагностических мероприятий, которые проводились данным пациентам.
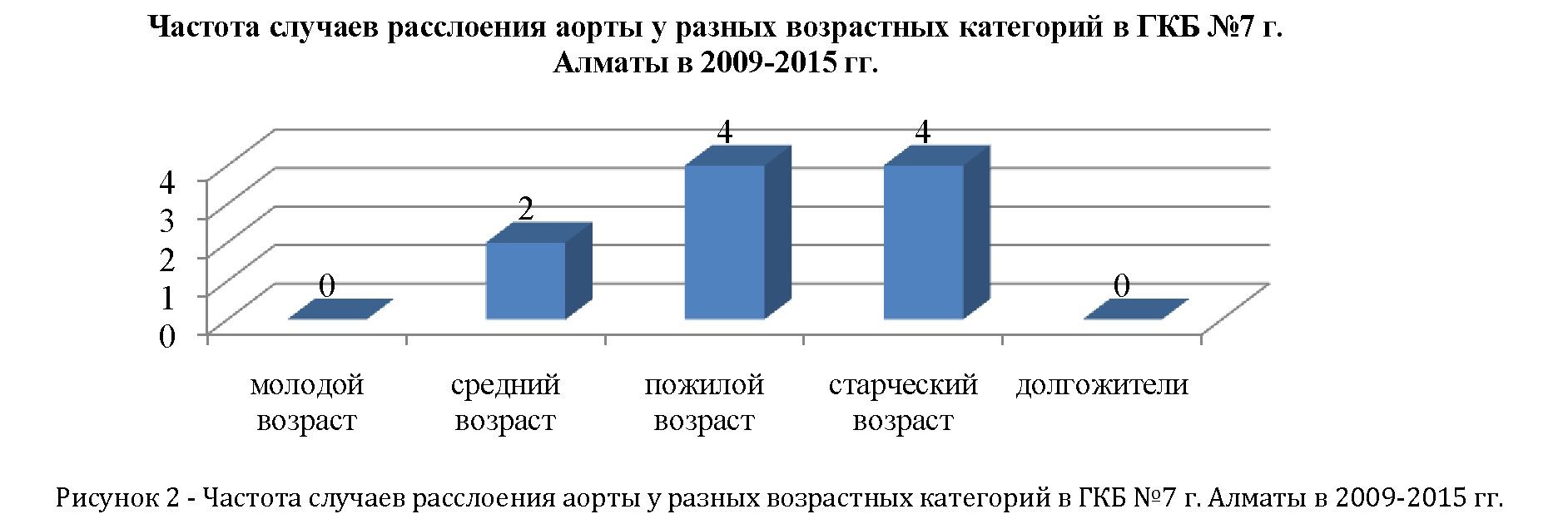
Результаты. Нами были анализированы 11 случаев расслоения аорты, поступивших в экстренном порядке в ГКБ №7 г. Алматы за период времени с 2009 до 2015 гг. Возраст больных от 52 до 86 лет, средний возраст составил 69,09091Ã12,27562 (Рисунок 2). Все рассмотренные пациенты были мужского пола.
У 7 пациентов был выставлен диагноз «I71.3 Аневризма брюшной аорты разорванная». У остальных пациентов были следующие диагнозы: I71.2 Аневризма грудной части аорты без упоминания о разрыве, I71.4 Аневризма брюшной аорты без упоминания о разрыве, I71.6 аневризма грудной и брюшной аорты без упоминания о разрыве, I71.9 Аневризма аорты неуточненной локализации без упоминания о разрыве
Из анамнеза 5 из них страдали ИБС и 1 атеросклерозом, у 4 пациентов в анамнезе была АГ, 2 пациента перенесли ОНМК, у 2 был СД. У 3 пациентов сопутствующих заболеваний не было.
Начальные признаки расслоения аорты, такие как резкие боли в области поражения, потеря сознания, тошнота, рвота появлялись у пациентов от 2 часов до 3 суток до поступления.
У 8 из 11 пациентов при поступлении АД было ниже 100 мм.рт.ст. У остальных пациентов АД было резко повышено. При обследовании выявлялась локальная боль при пальпации и пульсация в данной области.
Лабораторные исследования не выявили особых признаков расслоения аорты, поэтому невозможно провести дифференциальную диагностику между заболевания острого живота и расслоением аорты на основании ОАК,ОАМ, БАК и коагулограммы. У 5 пациентов была отмечена гипокоагуляция. В 8 случаях расслоение аорты выявлялось на УЗИ, с подтверждением КТ-исследования у 5 пациентов, и в 1 случае расслоение аорты было обнаружено на КТ-исследовании. Обзорная рентгенография грудной клетки и ЭхоКГ не выявляли патологию со стороны аорты. Лечение, в основном, заключалось в оперативном вмешательстве, либо в поддерживающей инфузионной терапии.
8 пациентов были проконсультированы ангиохирургами. Операция проведена 4 пациентам. 3 операции были проведены с резекцией и последующим протезированием. 1 операция ограничилась ревизией брюшной полости.
Исход заболевания был летальным в 7 случаях, в 5 из которых пациент скончался в течение суток, 1 пациент отказался от госпитализации, 3 пациента продолжили лечение в стационаре со специализированным отделением. Таким образом, анализируя небольшой материал по актуальной проблеме абдоминальной хирургии, считаем целесообразным сделать следующие выводы:
- Индекс клинической настороженности при расслоении аорты остается довольно низким, что приводит к поздней диагностике заболевания.
- Частым признаком расслоения аорты являются жалобы пациента на резкие боли в животе. Незамедлительное проведение УЗИ в области локализации болей позволяет сократить время диагностики расслоения аорты.
- Антигипертензивное лечение даже при незначительном повышении артериального давления позволяет остановить дальнейшее распространение расслоения тканей по аорте.
- Неэффективность хирургического лечения свидетельствует о поздней диагностике заболевания.
СПИСОК ЛИТЕРАТУРЫ
- Hagan P.G., Nienaber C.A., Isselbacher E.M. et al. The International Registry of Acute Aortic Dissection (IRAD): new insights into an old disease //JAMA. - 2000.-№ 283(7).-С. 897-903.
- Spittell P.C., Spittell J.A., Jr. Joyce J.W. et al. Clinical features and differential diagnosis of aortic dissection: experience with 236 cases (1980 through 1990) //Mayo Clin Proceedings. - 1993.- №68(7).-С. 642-651.
- Eisenberg M.J., Rice S.A., Paraschos A. et al. The clinical spectrum of patients with aneurysms of the ascending aorta //American Heart Journal. - 1993.-№125.-С. 1380-1385.
- DeBakey M.E., Henly W.S., Cooley D.A., et al. Surgical management of dissecting aneurysms of the aorta //The Journal of Thoracic and Cardiovascular Surgery. – 1965.-№49.-С. 130-148.
- Под ред. Сторожакова Г.И., Горбаченкова А.А. Руководство по кардиологии: учебное пособие. В 3 томах //ГЭОТАР-Медиа. - 2008.-Том 2.-360-390.
- Auer J., Berent R., Eber B. Aortic dissection: incidence natural history and impact of surgery //Journal of Clinical and Basic Cardiology. - 2000.-№3.-С. 151-154.
- Hennessy T.G., Smith D., McCann H.A. et al. Thoracic aortic dissection or aneurysm: clinical presentation diagnostic imaging and initial management in a tertiary referral center //Irish Journal of Medical Science. - 1996.-№165.-С. 259-262.
- Khan I.A., Vasavada B.C., Sacchi T.J. Asymptomatic dissection of the ascending aorta: diagnosis by transesophageal echocardiography //The American Journal of Emergency Medicine. - 1999.-№17.-С. 172-173.
- Friese K.K., Steffens J.C., Caputo G.R. et al. Evaluation of painless aortic dissection with MR imaging //American Heart Journal. - 1991.- №122.-С. 1169-1173.
- Khan I.A. Clinical manifestations of aortic dissection //Journal of Clinical and Basic Cardiology. - 2001.-№4.-С. 265-267.
- Rahmatullah S.I., Khan I.A., Caccavo N.D. et al. Painless limited dissection of the ascending aorta presenting with aortic valve regurgitation //The American Journal of Emergency Medicine. - 1999.-№17.-С. 700-701.
- Alverez Sabin J., Vazquez J., Sala A. et al. Neurologic manifestations of dissecting aneurysm of the aorta //Medicina Clínica (Barcelona). - 1989.-№92-С. 447-449.
- Kuhlmann T.P., Powers R.P. Painless aortic dissection: an unusual cause of syncope //Annals of Emergency Medicine. - 1984.-№13.-С. 549-551.
- Beach C., Manthey D. Painless acute aortic dissection presenting as left lower extremity numbness //The American Journal of Emergency Medicine. - 1998.-№16.-С. 49-51.
- Khan I.A., Wattanasauwan N., Ansari A.W. Painless aortic dissection presenting as hoarseness of voice: cardiovocal syndrome; Ortner's syndrome //The American Journal of Emergency Medicine. - 1999.-№17.-С. 361-363.
- Little S., Johnson J., Moon B.Y. et al. Painless left pleural hemorrhagic effusion: an unusual presentation of dissecting ascending aortic aneurysm //Chest. - 1999.-№116.-С. 1478-1480.
- Takahashi M., Ikeda U., Shimada K. et al. Unilateral pulmonary edema related to pulmonary artery compression resulting from acute dissecting aortic aneurysm //American Heart Journal. - 1993.-№126.-С. 1225-1227.
- Nath H.P., Jaques P.F., Soto B. et al. Aortic dissection masquerading as gastrointestinal disease //CardioVascular and Interventional Radiology. -1986.-№9.-С. 37-41.
- von Kodolitsch Y., Schwartz A.G., Nienaber C.A. Clinical prediction of acute aortic dissection //The Archives of Internal Medicine. - 2000.- №160.-С. 2977-2982.
- Cigarroa J.E., Isselbacher E.M., DeSanctis R.W. et al. Diagnostic imaging in the evaluation of suspected aortic dissection: old standards and new directions //The New England Journal of Medicine. - 1993.-№328.-С. 35-43.
- Jagannath A.S., Sos T.A., Lockhart S.H. et al. Aortic dissection: a statistical analysis of the usefulness of plain chest radiographic findings //Results American Journal of Roentgenology. - 1986.-№147.-С. 1123-1126.
- Treasure T., Raphael M.J. Investigation of suspected dissection of the thoracic aorta //The Lancet. - 1991.-№338.-С. 490-494.
- Nienaber C.A., von Kodolitsch Y., Nicolas V. et al. The diagnosis of thoracic dissection by noninvasive imaging procedures //The New England Journal of Medicine. - 1993.-№328.-С. 1-9.
- Clague J., Magee P., Mills P. Diagnostic techniques in suspected thoracic aortic dissection //British Heart Journal. - 1992.-№67.-С. 428429.
- Tomiguchi S., Morishita S., Nakashima R. et al. Usefulness of turboFLASH dynamic MR imaging of dissecting aneurysms of the thoracic aorta. //CardioVascular and Interventional Radiology. - 1994.-№17.-С. 17-21.
- Rofsky N., Weinreb J., Grossi E. et al. Aortic aneurysm and dissection: normal MR imaging and CT findings after surgical repair with the continuous-suture graft-inclusion technique //Radiology. - 1993.-№186.-С. 195-201.
- Solomon S.L., Brown J.J., Glazer H.S. et al. Thoracic aortic dissection: pitfalls and artifacts in MR imaging. //Radiology. - 1990.-№177.-С. 223-228.
- Erbel R., Daniel W., Visser C. et al. Echocardiography in diagnosis of aortic dissection //The Lancet. - 1989.-№330.-С. 457-460.
- Keren A., Kim C.B., Hu B.S. et al. Accuracy of biplane and multiplane transesophageal echocardiography in diagnosis of typical acute aortic dissection and intramural hematoma //Journal of the American College of Cardiology. – 1996.-№28.-С. 627-636.
- Vignon P., Gueret P., Vedrinne J.M. et al. Role of transesophageal echocardiography in the diagnosis and management of traumatic aortic disruption //Circulation. – 1995.-№92.-С. 2959-2968.
- Adachi H., Omoto R., Kyo S. et al. Emergency surgical intervention of the acute aortic dissection with the rapid diagnosis by transesophageal echocardiography //Circulation. – 1991.-№84.-С. 14-19.
- Erbel R., Mohr-Kahaly S., Rennollet H. et al. Diagnosis of aortic dissection: the value of transesophageal echocardiography //The Journal of Thoracic and Cardiovascular Surgery. – 1987.-№35.-С. 126-133
- Petasnick J.P. Radiologic evaluation of aortic dissection. //Radiology. – 1991.-№180.-С. 297-305.
- Dinsmore R.E., Willerson J.J., Buckley M.J. Dissecting aneurysms of the aorta: aortographic features affecting prognosis. //Radiology. – 1972.-№105.-С. 567-572.
- von Kodolitsch Y., Nienaber C.A., Suzuki T. et al. Increased serum concentration of myosin heavy chain in aortic dissection: discussion of 2 cases //Zeitschrift für Kardiologie. – 1997.-№86.-С. 469-473.
- Suzuki T., Katoh H., Tsuchio Y. et al. Diagnostic implications of elevated levels of smooth-muscle myosin heavy-chain protein in acute aortic dissection: the smooth muscle myosin heavy chain study //Annals of Internal Medicine. – 2000.-№133.-С. 537-541.
- Erbel R., Oelert H., Meyer J. et al. Effect of medical and surgical therapy on aortic dissection evaluated by transesophageal echocardiography: implications for prognosis and therapy; the European Cooperative Study Group on Echocardiography //Circulation. – 1993.-№87.-С. 1604-1615.
- Borst H.G., Laas J. Surgical treatment of thoracic aortic aneurysms // Advances in cardiac surgery. - 1993.-№4.-С. 47-87.
- Jamieson W.R., Munro A.I., Miyagishima R.T. et al. Aortic dissection: early diagnosis and surgical management are the keys to survival // Canadian Journal of Surgery. - 1982.-№25.-С. 145-149.
- Carrel T., Pasic M., Vogt P. Retrograde ascending aortic dissection: a diagnostic and therapeutic challenge //European Journal of Cardio- Thoracic Surgery. - 1992.-№7.-С. 146-152.
- Чернявский А.М., Альсов С.А., Ляшенко М.М. и соавт. Применение «гибридного» протеза в реконструкции дуги и проксимального отдела грудной аорты при расслоении аорты I типа по Де Бейки //Грудная и сердечно-сосудистая хирургия. - 2012.-№5.-С.11-15.