С помощью RAPD-анализа изучался полиморфизм ДНК у культурных сортов, расщепляющегося потомства и различных популяций шуйской конопли. С помощью 10 специфичных праймеров выявлены достоверные генетические различия между сортами, популяциями и гибридами. Показано, что способность к накоплению наркотического тетрагидроканнабинола не является доминантным признаком, а преимущественный синтез ненаркотического каннабидиола связан с высокой активностью каннабидиолсинтазы.
В природе больше половины видов растений являются перекрёстноопыляемыми. Такое размножение обусловливает непрерывную рекомбинацию генов. Динамика популяции выражается в изменении частот встречаемости каждого аллеля данного гена. Для определения популяционной структуры проводят анализ по различным генетическим маркерам [1].
С помощью нескольких десятков биохимических маркеров выявлен генетический полиморфизм у более чем 200 видов живых организмов и разработаны основные теоретические положения популяционной генетики (1, 43). Однако использованные маркёры опосредовано определяют генетические различия между таксонами. Например, анализ белков позволяет исследовать полиморфизм только белок- кодирующих последовательностей и только у экспрессирующихся генов.
Открытие метода полимеразной цепной реакции (ПЦР, Polymerase chain reaction, PCR) стало одним из наиболее выдающихся событий в области молекулярной биологии за последние 20 лет. Использование молекулярных ДНК- маркеров [2] позволило идентифицировать гены и выявить генетический полиморфизм различных организмов [3] непосредственно на уровне генов, а не на уровне их продуктов. Одним из 4 модификаций ПЦР является RAPD- метод, преимуществом, которого является простота и скорость проведения анализа [4-6]. В Казахстане, где дикорастущая наркотическая конопля только в Шуйской долине занимает площадь более 1,2 млн.га, ненаркотическая произрастает в половине областей особую актуальность приобретают исследование по популяционному полиморфизму. Это связано с необходимостью как использования её в промышленном производстве, так и разработке методов уничтожения. Исходя из этого, целью нашей работы было изучение полиморфизма популяций и влияния перекрёстного опыления культурной конопли (Cannabis sativa) дикорастущей (Cannabis ruderalis) на генетический полиморфизм потомства
Материалы и методы. Объектом исследования являлись сорт Fedora 17 и его расщепляющееся в Шуйской долине гибридное потомство F1 и F2, а также дикие популяции конопли, произраставшие на территории Меркенского района Жамбылской области и Уйгурского района Алматинской области.
Для анализа брали созревшие и отлежавшиеся более 30 дней семена и выделяли ДНК цетилтриметил аммониум бромидом (СТАВ) с 20 мМ 2-меркаптоэтанолом по общепринятой методике [7]. Чистоту полученных препаратов ДНК проверяли электрофоретическим разделением в агарозном геле.
Для PCR-амплификации использовали девять праймеров. 3.CCGAATTCGC, 4.CTGACCAGCC, 5. ATCTGGTGGT, 6. GGACCCCGCC, 7.TCAGGACGCTAC, C, 12CCTTGACGCA,14. AGCAGCGTCG, 15GTGTGCCCCA, 16.GGGGTGACGA . Шесть из них были наиболее специфичными. Реакционная смесь объемом 20 мкл содержала 50 мМ KCl, 20 мМ трис-HCl, рН 8,4, 3 мМ MgCl2, 0,01% Tween-20, 0,15 мМ каждого dNTP, 0,2 мкМ праймера, 20 нг ДНК и 1 ед. Tag-полимеразы. В пробирки наслаивали 40 мкл минерального масла. PCR- амплификацию проводили в следующем режиме: первые четыре цикла - 1 мин. При 930С, 1,5 мин. При 430С и 2 мин. При 720С; в последующих циклах отжиг вели при 47-550С (всего 35 циклов). Последняя элонгация длилась 10 мин. Продукты амплификации разделяли электрофорезом в 10¿ ПААГ и гели просматривали в GelDoc при длине волны от 260 до 360 нм.
Для определения генетической дистанции по полиморфизму RAPD-спектров и получения матрицы состояния бинарных признаков были использованы алгоритмы Нея и Ли [8]. По матрице состояния были построены дендрограммы генетических дистанции с помощью невзвешенного парногруппового метода с арифметическим усреднением - UPGMA (unweighted pair- group mathematical averige).
Определение содержания каннабиноидов проводили на газожидкостном хроматографе-масс-спектрографе GCMS фирмы “Shimadzu”. Листья для анализа брали на X-XI (фаза молочной - молочно-восковой спелости) и XI-XII (фаза молочно-восковой - восковой спелости) этапах органогенеза. Размельченные листья обычно экстрагировали этанолом или метанолом (100 мг образца доводим до 10 мл, для конечной концентрации каннабиноидов 1мг/мл) в течение 1 часа при 700С или 24 часа при комнатной температуре. Затем надосадочную жидкость декантировали и использовали для нанесения в плазменно-ионизационный детектор (1мкл).
Результаты и их обсуждение. Использованные в работе праймеры обеспечили синтез специфических и воспроизводимых наборов ампликонов. Выявлен полиморфизм исследуемых образцов. Все шесть исследованных образцов конопли имели специфические RAPD-спектры, которые отличались числом, размерами ампликонов (от 90 до 1700 п.н.) и степенью их выраженности на электрофореграмме. Общее число ампликонов в зависимости от праймера колеблется от 56 до 95. Электрофоретические спектры (рис.1 - 4) свидетельствуют о том, что наряду с общими ампликонами, характерными для всех образцов, существуют специфичные фрагменты ДНК.
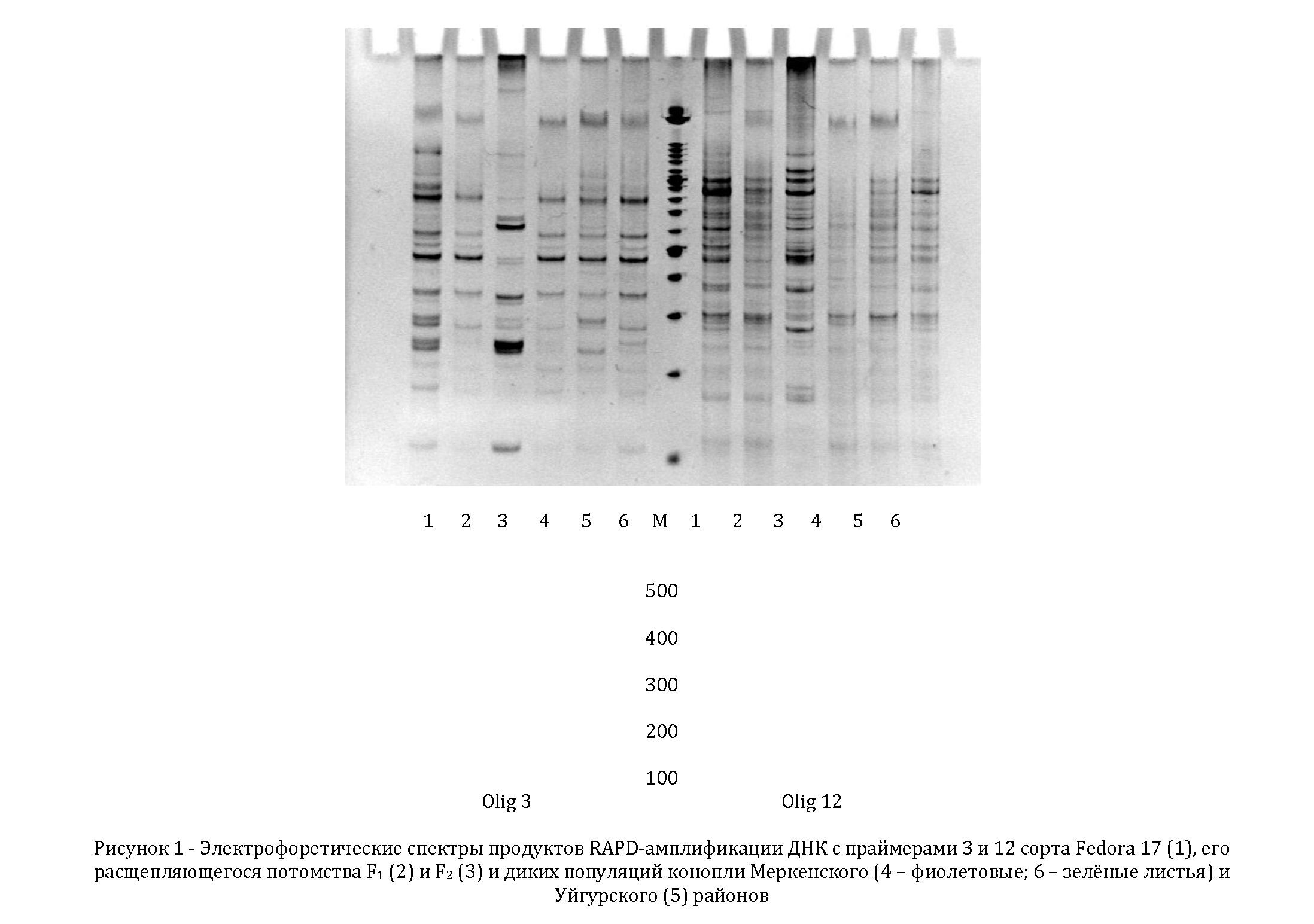
На рис.1 приведён RAPD-спектр 6 образцов, полученный при использовании праймеров 3 и 12. С помощью праймера 3 амплифицирован всего 71 фрагмент. Из них 6 являются общими для всех образцов и имеют размер от 170 до 800 н.п. С помощью данного праймера выявлен полиморфизм ДНК у анализируемых образцов конопли: у образца 3 (потомство F2 сорта Fedora 17) обнаружены специфичные фрагменты длинной 340 и более 1700 н.п., но отсутствуют 4 фрагмента ДНК, длинной около 350, 500, 580 и 1600 н.п., присутствующие у всех остальных образцов. По степени выраженности спектра образец 3 отличается четкими зонами с ампликонами длинной около 110, 240, 250, 610 и 670 п.н. Они присутствуют или отсутствуют в спектре у других образцов. Менее выражена у него зона в 460 н.п., которая у всех остальных является четкой. Дикорастущие популяции из Меркенского – образцы 4 и 6 и Уйгурского (образец 5) районов также отличаются друг от друга по составу ампликонов. Так образец 5 имеет в спектре фрагменты размерм 280 и 610 п.н., отсутствующие у образцов из шуйских популяции, но присутствующие в спектре культурного сорта и его потомства F2. Сходство между уйгурской популяцией и культурным сортом заключается в наличии в спектре фрагмента ДНК в 1050 н.п., который отсутствует у остальных образцов. У дикорастущих популяций в спектре отсутствует ампликон размером 330 н.п., который обычно проявляется у сорта и его F2 потомства. В RAPD-спектре праймера 12 выявлено 10 общих для всех образцов ампликонов размером от 170 до 1000 н.п. Для образца 3 характерно наличие 710, 520, 340 и 240 н.п. фрагментов, отсутствующих у других образцов. Фрагменты длиной около 280, 470, 1100 и 1310 н.п. у него выражены более чётко, чем у исходного сорта. Популяции дикорастущей конопли отличаются между собой в основном лишь по степени выраженности тех или иных фрагментов ДНК в спектре. У них отсутствует фрагмент размером 320 н.п., обычный для культурного сорта и его расщепляющегося в F1 и F2 потомства. Фрагмент размером 1600 н.п. не проявляется в спектре ДНК конопли из Меркенского района с зелёными листьями, в то время как у этой же популяции, но с фиолетовыми листьями, у уйгурской популяции и потомства F1 исходного сорта он присутствует.
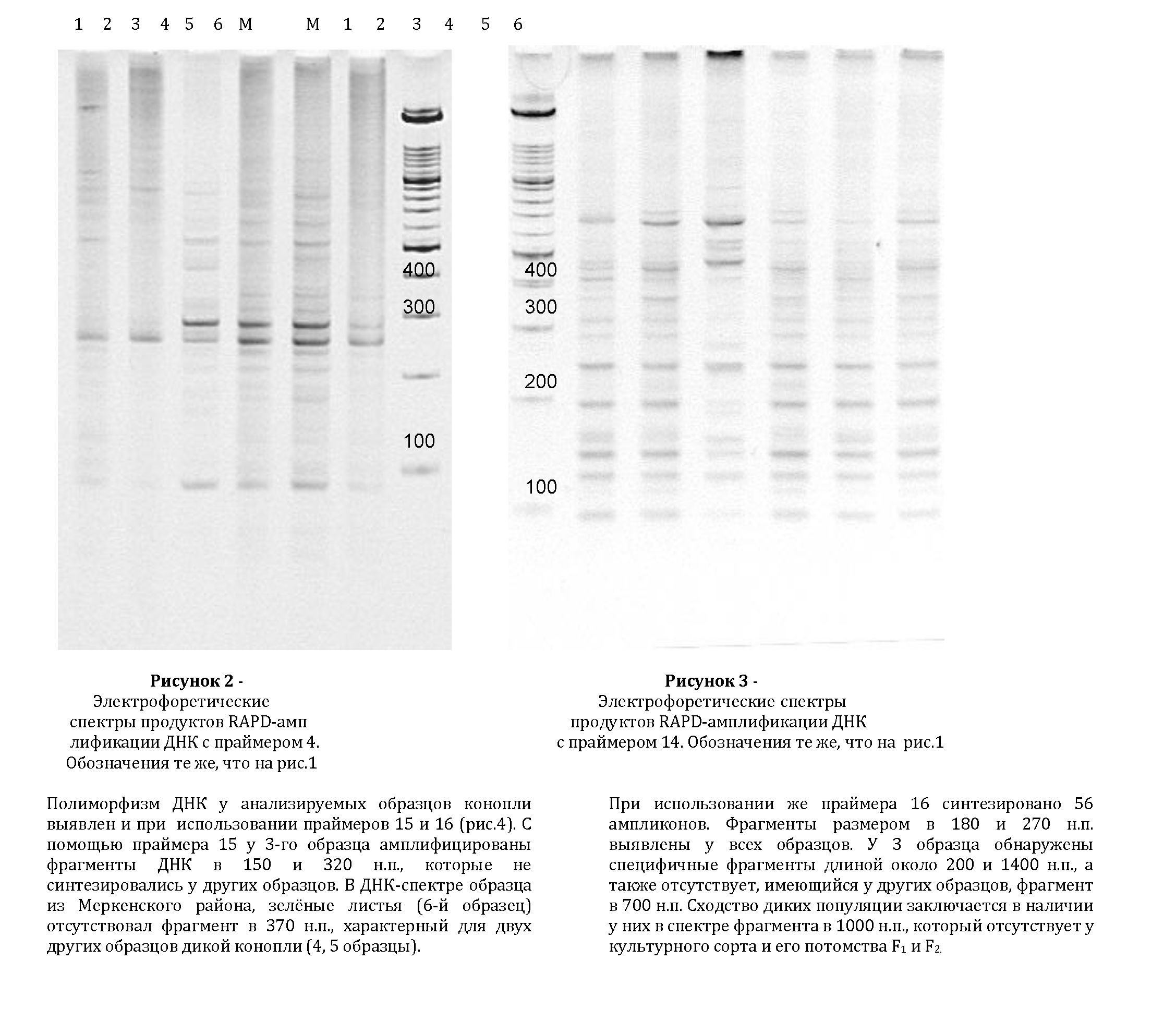
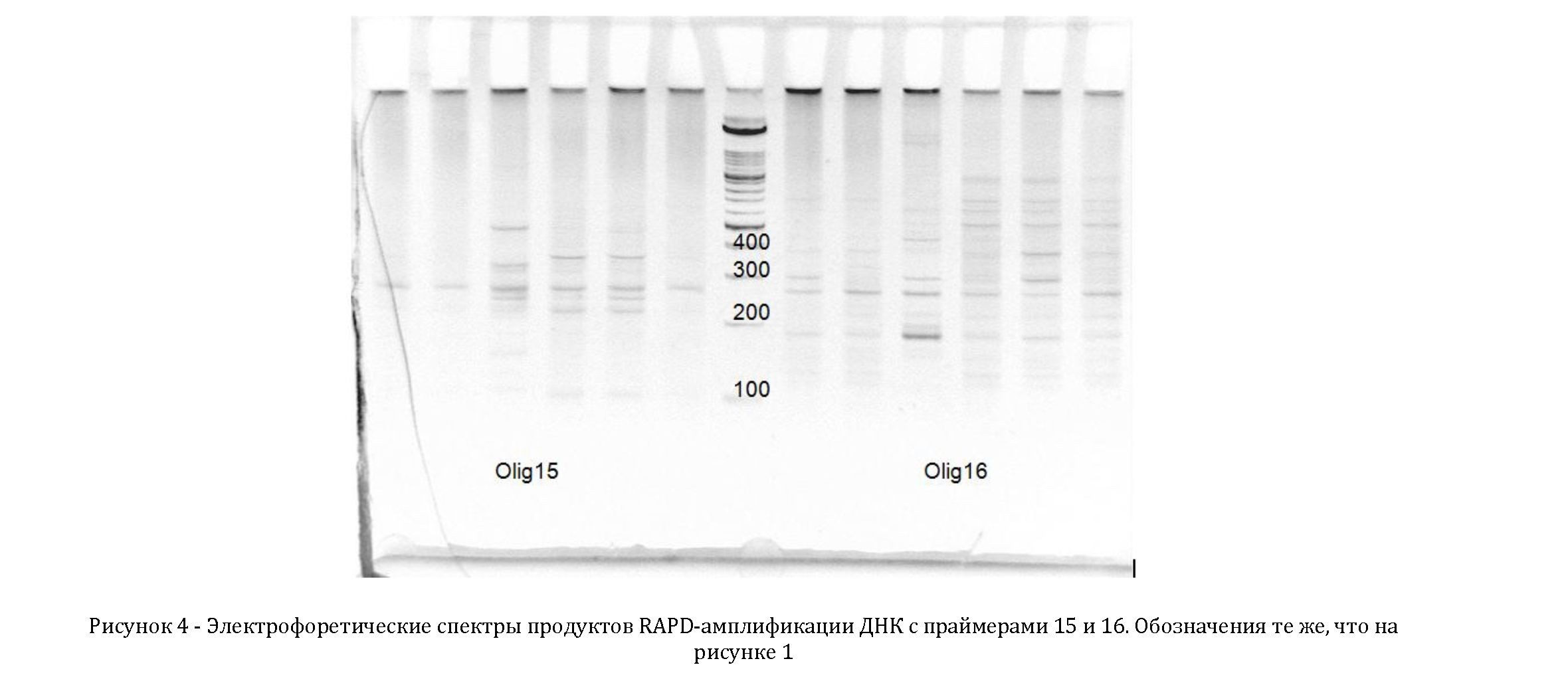
С помощью праймера 4 (рис. 2) амплифицировано два фрагмента ДНК длиной около 90 и 260 н.п., которые являются общими для всех образцов. У сорта Fedora 17 (образец 1) с помощью этого праймера амплифицирован фрагмент ДНК в 1600 н.п., отсутствующий у других образцов. У 3 образца в спектре не отсутствует фрагмент в 720 н.п., присутствующий у других и обнаружен специфичный только для этого образца ампликон в 420 н.п. Специфичный фрагмент в 1500 н.п. выявлен у образца 2. Только у 5 образца в спектре проявляются специфичные фрагменты размером 370 и 460 н.п. В спектре у дикорастущих образцов также присутствуют специфичные фрагменты ДНК длиной 350 н.п., отсутствующие у сорта и его потомства.
На рисунке 3 видно, что праймер 14 обуславливает амплификацию 95 фрагментов. 9 из них размером от 90 до 680 н.п. являются общими для всех образцов. В RAPD- спектре потомства F2 исходного сорта обнаружены специфичные фрагменты размером 180, 270 и 900 н.п., которые не характерны для остальных образцов. Однако у этого образца отсутствуют 280, 320 и 360 н.п. фрагменты присутствующие в спектре у других образцов. Для меркенской конопли (4 и 6 образцы) и потомства F1 сорта Fedora 17 характерно наличие фрагментов в 220 и 720 н.п. В спектре меркенского образца, фиолетовые листья и F2 потомства исходного сорта выявлен специфичный фрагмент в 120 н.п.
В целом, можно сказать, что присутствие в RAPD-спектре у сорта Fedora 17 отдельных фрагментов ДНК и отсутствие их у его потомства F1 и F2 свидетельствует о гетерогенности по данному локусу.
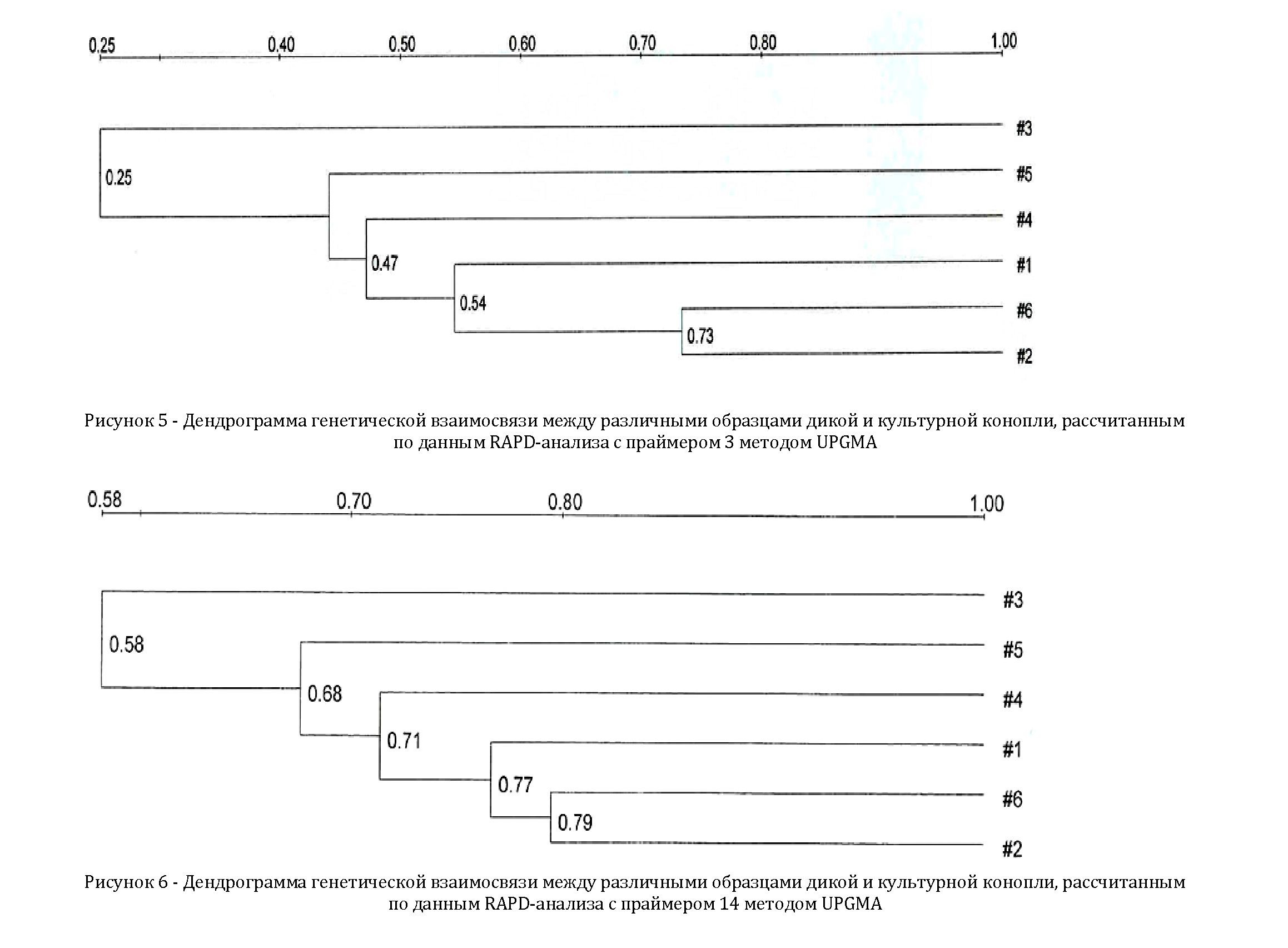
Данные по полиморфизму электрофоретических спектров продуктов RAPD-амплификации ДНК позволили провести кластерный анализ различных образцов конопли с помощью программы UPGMA (рисунок5-8).
Из данных дендрограмм (рис. 5-8) видно, что шуйская популяция (6 образец) и потомство F1 сорта Fedora 17 образуют отдельный кластер. Это может свидетельствовать об их генетическом сходстве. Наиболее близко к ним находится сам сорт Fedora 17, а также 4-й шуйский образец. Из дендрограммы, составленной на основе RAPD-анализа с праймером 15, видно, что дикие популяции из Меркенского и Уйгурского районов (4 и 5 образцы) образуют одну генетическую группу. Самым отдаленным по генетическому родству является потомство F2 сорта Fedora 17.
Таким образом, можно сказать, что генетическая близость шуйской конопли и потомства F1 возможно является результатом перекрестного опыления исходного сорта пыльцой дикой конопли. В то время как наибольшая
отдаленность потомства F2 сорта Fedora 17 объясняется расщеплением его гетерогенных (гетерозиготных) родителей. Наличие разницы в генетической дистанции между популяциями Cannabis ruderalis может быть обусловлено гетерогенной структурой данных популяций. Одним из маркёров популяций у конопли являются каннабиноиды. Одни из них не обладают наркотическим - КБН (каннабинол) и КБД (каннабидиол), а другие - ТГК (тетрагидроканнабинол), ТГКА обладают наркотическим эффектом. Мы попытались изучить наследование этого признака у потомства культурного сорта. В таблице приведены результаты определения содержания каннабиноидов у сорта Fedora 17, его потомства F1 и F2, популяциях Cannabis ruderalis.
|
№ |
Сорт/экотип |
Этап органогенеза |
ТГК, % |
КБД, % |
|
1. |
Fedora 17 F1 |
X-XI |
0,12 |
0,82 |
|
2. |
F2 Fedora 17 |
X-XI (Меркенский р-н) |
0,18 |
1,08 |
|
3. |
F2 Fedora 17 |
XI-XII (Меркенский р-н) |
0,07 |
1,43 |
|
4. |
F2 Fedora 17 |
XI-XII (растение внешне сходное с Cannabis ruderalis; Меркенский р-н) |
0,06 |
1,01 |
|
5. |
Cannabis ruderalis |
XI-XII (растение с фиолетовыми листьями, Меркенский р- н, переправа) |
1,25 |
0,48 |
|
6. |
Cannabis ruderalis |
XI-XII (растение с зелеными листьями, Меркенский р-н, переправа) |
1,32 |
0,14 |
|
7. |
Cannabis ruderalis |
XI-XII (Уйгурский р-н, 1 крупное растение) |
1,5 |
1,0 |
|
8. |
Cannabis ruderalis |
XI-XII (Уйгурский р-н, среднее растение) |
1,0 |
0,66 |
Таблица 1 - Содержание каннабиноидов у европейского сорта, его потомства F1 и популяций дикой конопли
Из приведенных данных видно, что у потомства F1 исходного сорта не наблюдается накопления наркотического соединения - тетрагидроканнабинола (ТГК), хотя несколько возрастает содержание каннабидиола (КБД). У исходного сорта в условиях Европы содержание ТГК не превышало 0,15¿, а КБД находилось примерно на том же уровне. Т.е. накопление ТГК является генетически детерминированным признаком и экологические условия (Шуйская долина) не влияют на накопление наркотического вещества. У дикорастущих шуйских популяций его содержание в сентябре-октябре в прицветниках достигает 8¿, а КБД и КБН -0,12 - 2¿ [9]. Это, по нашему мнению, связано с гомозиготностью дикорастущих популяций по признаку накопления ТГК.

Таким образом, сорт культурной конопли Cannabis sativa, его расшепляющееся потомство F1 и F2, дикорастущие популяции Cannabis ruderalis отличаются друг от друга по структуре ДНК и накоплению каннабиноидов (т.е. генетически неоднородны). Уровень накопления каннабиноидов у конопли, в частности содержание ТГК, по всей видимости, является генетически детерминированным признаком. Можно ожидать, что посевы волокнистых ненаркотических сортов будут изменять генетическую структуру шуйских популяций в сторону низкого содержания ТГК. Различия в уровне накопления ТГК и КБД связаны с неодинаковой активностью их синтаз. Аминокислотная последовательность изоферментов у ТГКА- синтазы, КБД-синтазы неодинакова, что и определяет их каталитические свойства.
СПИСОК ЛИТЕРАТУРЫ
- Сарсенбаев К.Н., Беков А.А.-Х., Рахимбаев И.Р. Изоферменты в хемосистематике высших растений. Алматы: 1982, - 145 с.
- Welsh J., McClelland M. Fingerprinting genomes using PCR with arbitrary primers. Nucler Acids Res., - 1990, - №18. - Р.7213-7218
- Гостимский С.А., Кокаева З.Г., Боброва В.К. Использование молекулярных маркеров для анализа генома растений// Генетика. 1994. Т. 35. №11. С. 1538-1549
- Дорохов Д.Б., Клоке Э. Быстрая и экономичная технология RAPD-анализа растительных геномов// Генетика. - 1996. - №33: - С.476-480
- Оганесян А.С., Кочнева Е.З., Рысков А.П. Маркирование видов и сортов картофеля с помощью метода RAPD PCR// Генетика. - 1996. №32. - С.448-451
- Кочнева Е.З., Оганесян А.С., Рысков А.П. RAPD-маркеры генома картофеля: клонирование и использование для определения межвидовых и межсортовых различий// Молекулярная биология. 1999. - Т.33. - №5. - С.893-897
- Jhingan A.R. A novel technology for DNA isolation// Methods of Mol. Cell. Biol. 1992. - №3. - P.15-22
- Nei M., Li W. Mathematical model for studying genetic variation in terms of restriction endonucleases// Proc. Nat. Acad. Sci. USA. 1979. - №76. - P.5269-5273
- Сарсенбаев К.Н., Кожамжарова Л.С., Айдосова С.С., Ережепов А.Е. Особености волосков конопли (Cannabis L.) и состав каннабиноидов.// Вестник КазНУ им.Аль-Фараби, сер.биол., - №1(22), - 18 – 20, - 2004. – 235 с.