Стремление к максимальному уменьшению дискомфорта, связанного с перенесением операций, выполняющихся в условиях ИК, уменьшению сроков пребывания в стационаре и времени возвращения к обычной жизни привело к распространению минимально инвазивных вмешательств в коронарную хирургию.
Актуальность. Дизайн исследования и основные его итоги были опубликованы ранее [1].Основой для настоящей работы послужил анализ 30 больных ИБС прооперированныхметодом минимально коронарной инвазивной хирургии. В группе обследованных больных было 28 мужчин и 2 женщины в возрасте от 41 до 67 лет (средний возраст 51,9±5,43). Из 30 вмешательств по реваскуляризации миокарда 24 было первичных и 6 повторных. Показаниями к операции служили: 1) выраженная клиника стенокардии, рефрактерная к обычной антиангинальной терапии; 2) повторные операции после ранее проведенных АКШ или ТЛБАП с возвратом стенокардии, без использования ВГА; 3) больные, у которых выполнение стандартной операции по реваскуляризации миокарда с ИК сопряжено с высоким риском.К ним относятся больные с атеросклеротическим поражением восходящей аорты, диффузной васкулопатией сосудов головного мозга и критическим мультифокальным поражением других сосудистых бассейнов, с резким угнетением сократительной способности миокарда, преклонного возраста и сопутствующими заболеваниями, сопровождающимися выраженной почечной и печеночной недостаточностью, обструктивными заболеваниями легких и др.; 4) больные с поражением ствола левой коронарной артерии с так называемыми “защищенными” крупными ветвями и после перенесенной операции АКШ или достаточной естественной коллатерализацией; 5) больные с множественным поражением коронарных артерий, у которых имеется проксимальное поражение крупной ПМЖВ, а остальные КА либо не требуют, либо не пригодны для шунтирования; 6) экономическая целесообразность, 7) нормальная конституция, с широкими межреберными промежутками на рентгенограммах (рисунок 1) .
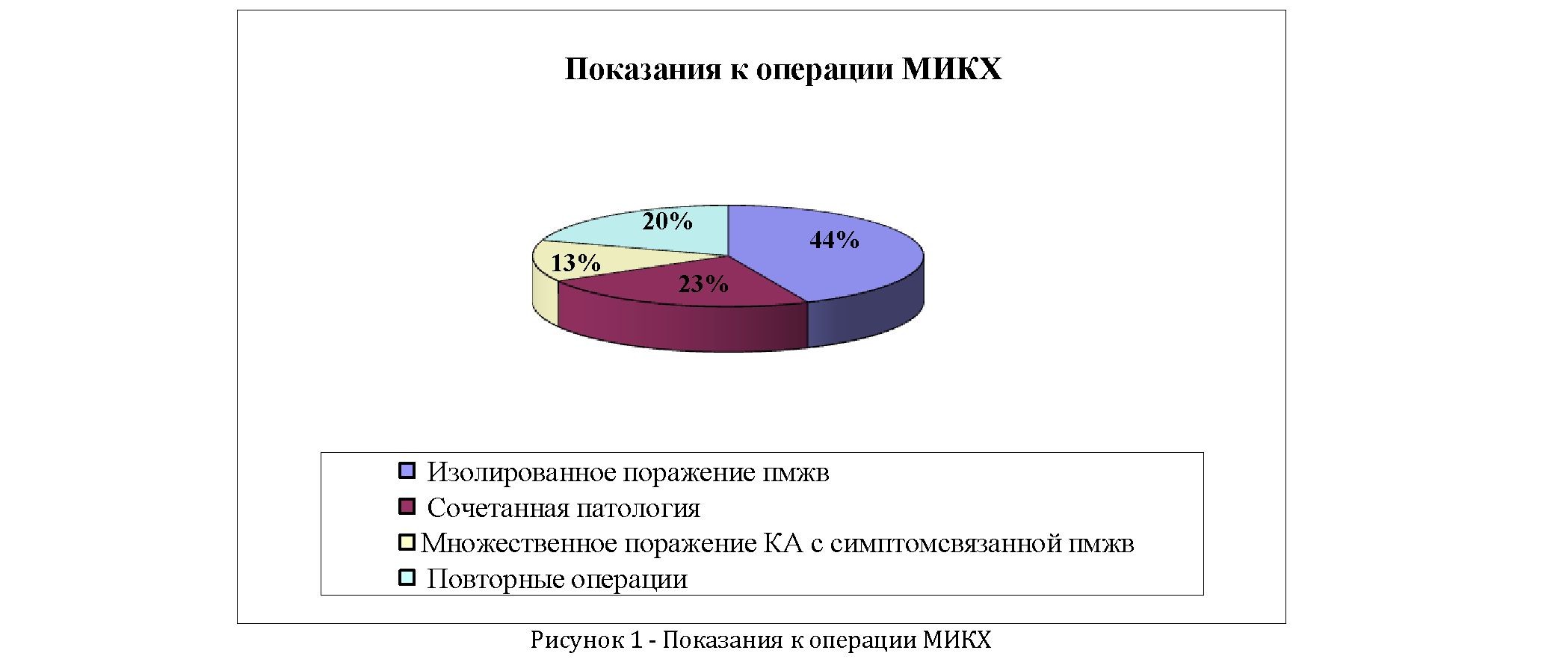
Цель исследования: Анализ ближайшего
послеоперационного периода при процедуре МИКХ Материалы и методы: Следует отметить, что наиболее часто у 13 больных имело место изолированное поражение ПМЖВ, в 7 случаев показанием для МИКХ была сочетанная патология, т.е. больные с высоким риском, которым было нежелательно проведение ИК, 6 больных ранее перенесли операцию АКШ, имелся возврат стенокардии с
симптомсвязанным ПМЖВ. У 4 имелось множественное поражение коронарных артерий с проксимальным поражением пмжв. Согласно данным коронарограмм у всех пациентов имело поражение ПМЖВ, у 4 больных имелось поражение ствола ЛКА. Окклюзия ПМЖВ отмечена у 9 больных и у 4окклюзия - ДВ, ОВ и ПКА окклюзированы в 2 и 1случаях соответственно (таблица 1). Диффузное поражение КА обнаружено у 4 больных.
Таблица 1- Характеристика коронарного русла у больных подвергшихся МИКХ
|
ЛКА n=30 |
ПМЖВ n=30 |
ДВ n=30 |
a.int. n=30 |
ОВ n=30 |
Пкаn=30 |
|
|
До 50% |
3 |
- |
- |
1 |
1 |
3 |
|
50-75% |
1 |
2 |
2 |
0 |
3 |
7 |
|
>75% |
19 |
9 |
1 |
8 |
6 |
|
|
Всего стенозов |
4 |
21 |
11 |
2 |
12 |
16 |
|
Всего окклюзий |
0 |
9 |
4 |
- |
2 |
1 |
|
Всего больных |
4 |
30 |
15 |
2 |
14 |
17 |
Для интраоперационного контроля за глобальной и региональной сократимостью миокарда использовали ЧПЭхоКГ. Все операции выполнены на бьющемся сердце с применением системы OCTOPUS фирмы “Medtronic”.Во всех наблюдениях перед пережатием коронарной артерии осуществляли пробу прекондиционирования в течение 5 минут с последующей реперфузией в течение 2 мин. Диагноз ИБС был установлен на основании клинической картины заболевания, анамнеза и данных клиникоинструментальных методов исследования. Длительность заболевания составила 56,95±10,37 месяцев или 4,7±0,86 года. В анамнезе у 24 пациентов был перенесенный ИМ.Все больные в зависимости от наличия и характера перенесенного в анамнезе ИМ рассматривались по отдельным группам: без инфаркта миокарда (БИМ), с мелкоочаговым инфарктом миокарда (МИМ), с крупноочаговым передне - перегородочным инфарктом миокарда (КПИМ) и с крупноочаговым нижним инфарктом миокарда (КНИМ). Стенокардия напряжения и покоя имела место у всех больных, у 2 пациентов установлена стенокардия II ФК (NYHA), 8 больных имели IIIФК, а у 18 больных ФК IV. Нестабильная стенокардия диагностирована у 1 и у 1 больного безболевая форма ишемии. Средний класс стенокардии составил 3,6. У большинства пациентов отмечены частые приступы стенокардии. Количество потребляемого в сутки НГ в среднем составило 7,75±1,7 таблеток. При обследовании у 13 больных установлено мультифокальное атеросклеротическое поражение артериальной системы. У 6 больных имелось поражение брахиоцефальных артерий, у 4 - артерий нижних конечностей (таблица 2). Артериальная гипертензия установлена у 6 больных, причиной у 3 пациентов был атеросклероз почечных артерий. Обструктивные заболевания легких у 2. Повышение артериального давления у 2 обследованных больных не сопровождалось выраженными нарушениями функции органов мишеней. Компенсированный сахарный диабет отмечен у 3 пациентов. Нарушения ритма сердца и проводимости были диагностированы у 4 больных.
Таблица 2 -
|
К - во больных |
% больных |
|
|
Всего |
30 |
100% |
|
Длительность ИБС (мес) |
56,95±10,37 |
- |
|
Инфаркт миокарда |
24 |
80% |
|
Аневризма ЛЖ |
1 |
3,3% |
|
Без инфаркта миокарда |
6 |
20% |
|
НК Iст |
2 |
6,6% |
|
НК IIА ст |
- |
- |
|
Мультифокальный атеросклероз |
13 |
43,3% |
|
Артериальная гипертензия |
6 |
20% |
|
Нарушения ритма и проводимости |
17 |
56,4% |
|
Сахарный диабет |
3 |
10% |
|
Язвенная болезнь желудка |
4 |
13,3% |
|
Мочекаменная болезнь |
3 |
10% |
|
Экстракардиальные заболевания |
4 |
13,3% |
больных по клинико-анамнестическим данным ВЭМ перед операцией выполнили всем 30 больным. Среди обследованных больных у 73,3% больных отмечалась средняя и высокая толерантность к физической нагрузке, и у 26,6% низкая толерантность к физическим нагрузкам. Средняя толерантность к физическим нагрузкам равнялась 75,8±4,0 Вт. В диагностике коронарной недостаточности нагрузочная проба была наименее информативной у больных с крупноочаговым нижним инфарктом миокарда где процент положительной пробы равнялся 83,3% и исследования прекращались на первых ступенях исследования.
Таким образом, описанная группа пациентов представляла собой тяжелый контингент, для выбора тактики, ведения которых необходимо проведение объективных методов исследования с разработкой критериев операбельности, выбора метода хирургического вмешательства и оценки его эффективности.
Техника операции.
Операция проводилась под общим наркозом, 3 больных проведена сочетанная спинальная анестезия, для подавления инотропной активности использовали β- блокаторы и антогонисты Са. Использовали доступы к сердцу: 1-левопередняя торакотомия в пятом межреберье у 21 больного, 2 - срединная стернотомия у 9 больных, которая была использована при шунтировании двух коронарных артерий, реваскуляризации ПКА, а также при повторных операциях. При проведении левопередней торакотомии разрез чаще всего делался по 5 межреберью от левой парастернальной до передней подмышечной линии, длиной до 4-10см.
Защита миокарда от ишемического повреждения
Первые 10 операций осуществляли под комбинированной (высокой эпидуральной и общей) анестезией, остальные – под общим наркозом. Первично проводили раздельную вентиляцию легких. Применяли фармакологические средства для повышения энергетического резерва миокарда, способствующие защите миокарда от ишемии – ингибиторы трансмембранного переноса аденозина, препараты открывающие К-АТФ каналы (никорандил, кромакалим, панацидил, миноксидил, пинацидил). Всем больным использовали метод “Ischemicpreconditioning” основанный на кардиопротективных свойствах теста окклюзии. Широко использовали различные методы механической разгрузки миокарда. Всем больным интраоперационно проводили чреспищеводную эхокардиографию.Широкое распространение получило применение ß-блокаторов и антогонистовСа. При этом снижается как ЧСС так и минутный объем кровообращения. ЧСС снижается до 30-40 ударов в минуту. Наиболее популярными среди кардиохирургов являются механические стабилизаторы. Для стабилизации миокарда использовали различные устройства с фармакологическим урежением ритма сердца ß-блокаторами или антогонистами кальция, либо спинальной симпатической блокадой (Arom K.V., и соавт., 1996 [8]). Угнетение хронотропного и инотропного воздействия позволяет сохранить сердцу достаточный минимум колебаний, и в отличие от пережатия аорты, и кардиоплегии, предупредить как ишемию так и отек миокарда. При этом в условиях брадикардии сохраняется антеградный кровоток, предотвращающий развитие ишемии - реперфузии и уменьшить потребление О2 предупреждающих ишемию. Сохранение колебаний стенок сердца, поддерживающих дренирование лимфы, предотвращает отек миокарда. Концепция выполнения операций на работающем сердце может оказаться полезной и для защиты миокарда у больных со сниженной функцией левого желудочка из группы с высоким риском выполнения операций в условиях ИК.
Результаты и обсуждение.
Интраоперационноечреспищеводноеэхокардиографическое исследование показало положительную динамику ФВ после окончания операции (таблица 3). Наилучшие результаты наблюдались в группе больных не имеющих в анамнезе инфаркта миокарда.
Таблица 3 - Динамика изменений фракции выброса (ЧПЭхоКГ)
|
Всего (n=30) |
Исход |
Этап операции |
Конец операции |
|
БИМ (n=6) |
52,8±1,4 |
31.2±1,2 |
42,3±2,1 |
|
МИМ (n=6) |
47,5±3,1 |
29,4±1,5 |
38,4±2,2 |
|
КПИМ (n=12) |
45,2±2,1 |
26,4±2,3 |
36,3±3,1 |
|
КНИМ (n=6) |
47,6±2,4 |
27,3±3,1 |
37,3±4,1 |
Ведение ближайшего послеоперационного периода.
Все больные после операции МИКХ, были переведены в реанимационное отделение в состоянии медикаментозного сна на ИВЛ. В первые часы после операции проводился прямой контроль гемодинамики, мониторинг ЭКГ пациента, контроль за газовым составом крови, кислотно-щелочным состоянием и биохимическими показателями, включая ферменты-маркеры ишемии миокарда. Инотропная поддержка в интра/послеоперационном периоде и в реанимации представлена на таблице 4.
Т аблица 4 - Инотропная поддержка на этапах операции
|
Всего n=30 |
Этап операции |
Конецоперации |
Реанимация |
Экстубация |
|
БИМ- (n=6) |
0,11 мкг/кг/мин |
0,42 мкг/кг/мин |
0,13 мкг/кг/мин |
0,1мкг/кг/мин |
|
МИМ- (n=6) |
0,21мкг/кг/мин |
0,61 мкг/кг/мин |
0,21мкг/кг/мин |
0,12мкг/кг/мин |
|
КПИМ(n=12) |
0,26 мкг/кг/мин |
2,71мкг/кг/мин |
0,52 мкг/кг/мин |
0,23 мкг/кг/мин |
|
КНИМ- (n=6) |
0,23мкг/кг/мин |
1,66 мкг/кг/мин |
0,36 мкг/кг/мин |
0,17 мкг/кг/мин |
Допамин при МИКХ применяли в среднем 0,3 мкг/кг/мин. Конец операции сопровождался наибольшей инотропной поддержкой в группе больных с крупноочаговым инфарктом миокарда, где средняя доза кардиотоников составила 2,71 мкг/кг/мин, тогда как в группе больных не имеющих в анамнезе инфаркта миокарда средняя доза составила соответственно 0,42.
Таблица 5 - Ферментативная активность на этапах
|
Время после операции |
Средняя КФК |
Средняя КФК МВ |
% КФК МВ |
|
3 часа |
968,3 |
95,5 |
9,8% |
|
12 часов |
975,6 |
92,3 |
9,4% |
|
18 часов |
965,8 |
90,3 |
9,3% |
|
1 сутки |
602,2 |
46,5 |
7,7% |
На момент экстубации во всех группах больных была минимальная инотропная поддержка и в среднем составила 0,3 мкг/кг/мин.
Анализ ЭКГ в первые часы после МИКХ ишемии не выявил. Анализ общей КФК и КФК МВ не выявил критического повышения этих ферментов (Табл.5).Как следует из таблицы 5, ни в одном случае величина МВ фракции не превышала 10% от общей КФК, а уровень КФК МВ ни на одном из этапов наблюдения не превышал 100 ед, что свидетельствовало об отсутствии повреждения миокарда. С целью предупреждения отека миокарда больным назначали кортикостероиды: дексазон или преднизолон 30 мг/сут.Все больные были экстубированы по показаниям в первые сутки после операции, в среднем через 6,8±4,1 часов после вывоза из операционной. Гемодинамика во всех случаях оставалась стабильной и требовала назначения незначительных доз кардиотоников у отдельных больных. Болевой синдром после операции умеренный, купировался стандартным назначением анальгетиков. Кровопотеря после операции составила в среднем 300±35,4 мл. Угрожающих жизни осложнений во время пребывания в реанимации не зафиксировано. Длительность времени пребывания в отделении реанимации в среднем составила 1,4±1,1 сутки. Срок пребывания больных в стационаре не анализировался, поскольку в определенной степени он был целенаправленно увеличен с целью более подробного обследования больных.
Анализ ближайшего послеоперационного периода показал, что процедура МИКХ достаточно безопасна для больного и требует стандартную интенсивную терапию в отделении реанимации. Преимущества операции следующие:
- Ранняя экстубация и небольшой период пребывания в отделении реанимации;
- отсутствие необходимости длительного использования дорогостоящего оборудования и лекарств в послеоперационном периоде;
- высокая стоимостная эффективность процедуры;
- косметический эффект операции;
- устранение нежелательных воздействий экстракорпорального кровообращения.
Таким образом, на основании представленного анализа можно сделать вывод, что минимально инвазивная хирургия сердца при ИБС, действительно, исключает осложнения, свойственные ИК. Это является сильной стороной выполнения операций на сокращающемся сердце. При этом несмотря на то, что изменение техники потребует переобучения, специалисты считают что для кардиохирурга это не составит больших трудностей. Однако следует отметить, что хотя МИКХ является многообещающим разделом сердечно - сосудистой хирургии, она не совершенна и имеет определенные ограничения. При боковом доступе хирург имеет оперативный простор только в области верхушки сердца. Когда он встречается с такими осложнениями, как кальцинированная коронарная артерия, массивный жир или интрамуральное прохождение сосуда, вероятно, ему стоит отказаться от минимально инвазивной хирургии, быстро перейти на стернотомия и ИК. По этим соображениям министернотомия в нижней части грудины является наиболее практичным доступом. Использование видеотехники в препарировании грудной артерии имеет несомненные преимущества. Использование этой техники позволяет проследить весь ход артерии, и все ее ветви могут быть перевязаны, что исключает возможность развития стил - синдрома.
Малоинвазивная коронарная хирургия уже прочно вошла в повседневную практику многих кардиохирургических Центов мира. По мнению F. Allessandrini [6] МИКХ очевидно является наиболее интересным и перспективным нововведением в коронарную хирургию. По всей видимости, она уже в ближайшем будущем станет применяться рутинно, серьезно вмешавшись в существующее соотношение используемых сегодня в коронарной хирургии методик.
СПИСОК ЛИТЕРАТУРЫ
- Айткожин Г.К. Хирургические подходы к различным методам реваскуляризации миокарда: дис. ... д-р мед. наук - Алматы, 2002. - 367 с.
- Айткожин Г.К. Хирургическое лечение ишемической болезни сердца методом минимально - инвазивной коронарной хирургии с использованием системы «Octopus». - «Хирургия». - №10. - С. 17 - 20.
- Acuff T.E., Landreneau R.G., GriffithB.P., Minimally invasive coronary artery bypuss grafting. //Ann.Thorac.Surg.-1996.-№61.-P.135-137.
- Akins C. W. Reoperation for stenotic saphenous vein bypass grafts without cardiopulmonary bypass // Ann. Thorac. Surg. - 1983. - Vol. 35. № 2.-P. 201-206.
- Akins C.W., Searcher C.A., Pohost G.M. Preservation of interventricular septal function in patients having coronary artery bypuss grafts without cardiopulmonary bypuss.// Am.Heart.J.-1984.-№9- P.364.
- Alessandrini F., gaudino M., Glieca F. et al. Lesions of the target vessel during minimally invasive miocardialre vasculariszation.// Ann.Thorac.Surg.-1997.-№64.-P.1349-1353.
- Allen K.B. Mathey R.G., Robison R.J., et al. Minimally invasive versus conventional reoperative coronary artery bypuss.// Ann.Thorac.Surg.-1997.-№64.-P.616-622.
- Arom K.V., Emery R.W., Nicoloff D.M. Mini-sternotomy for coronary artery bypuss grafting.// Ann.Thorac.Surg.-1996.-№61.-P.1271- 1272.
- Benetti F. International workshop on arterial conduits for myocardial revascularization. UniversitaCattolicadelSacroCuore, Rome.- November 1994.
- Benetti F., Ballester C., Sani G. Et al. Video-assisted coronary artery bypuss surgery.//J.Cardiac.Surg.-1995.- №10- P.620-625.