В статье приведены результаты анализа клинико – нейровизуализационного сопоставления у 48 больных с острым ишемическим инсультом в остром периоде. При оценке неврологического статуса использовались унифицированные международные шкалы (European Stroke Scale, Fugl-Meyer Scale, Motor Assessment Scale) и результаты МРТ – исследования.
Проблема острых нарушений мозгового кровообращения (ОНМК) имеет большую медико-социальную значимость. Она обусловлена их значительной долей в структуре заболеваемости и смертности населения, высокими показателями временных трудовых потерь и уровнем первичной инвалидности [1, 5].
Цель исследования: провести анализ результатов клинико- нейровизуализационного сопоставления в остром периоде ишемического инсульта.
Материалы и методы исследования. Клинико- нейровизуализационная оценка ишемического инсульта (ИИ) в остром периоде проводилась у 48 пациентов, в возрасте от 66 лет. На момент включения в исследование все больные находились в сознании. При оценке неврологического статуса использовались унифицированные международные шкалы (European Stroke Scale, Fugl-Meyer Scale, Motor Assessment Scale) и результаты МРТ - исследования.
Результаты и обсуждения исследования. При оценке неврологического статуса использовалась шкала European Stroke Scale (ESS), достаточно подробно отражающая выраженность двигательного дефицита, который в среднем по группе составил 72±0,3 балла. Исходя из общей тяжести состояния, все больные условно были разделены на 3 группы: в первую группу были включены 6 больных с выраженным неврологическим дефицитом (до 40 баллов по шкале ESS), во вторую - 16 пациентов со средней выраженностью дефицита (41-70 баллов) и в третью - 26 пациентов с легким неврологическим дефицитом (71-100 баллов) (табл. 1).
Таблица 1 - Распределение больных по общей тяжести неврологического дефицита
|
Количество баллов |
До 40 баллов |
41-70 баллов |
71-100 баллов |
|
Количество больных |
6 |
16 |
26 |
|
Процент |
12,5% |
33,3% |
54,2% |
Следует отметить, что из 48 наблюдаемых больных парез руки был только у 29 человек (60,42%). Для характеристики распределения больных по степени выраженности пареза мы выделили группу пациентов, способных выполнить лишь треть анализируемых Fugl-Meyer Scale (FMS) движений (количество баллов менее 18), приблизительно половину (от 19 до 36 баллов) и большую часть необходимых заданий (более 37 баллов). В среднем выраженность пареза руки по FMS составила 10±0,4 балла.
Степень выраженности функционального дефицита по Motor Assessment Scale (MAS) в среднем составила 24±0,2 балла, варьируя в значительной степени: у 8 (16,67%) больных количество баллов было менее 18, что отражает низкую функциональную активность больных, у 21 (43,75%) - 19-36 баллов, то есть средние функциональные возможности, у 19 пациентов (39,58%) - 37-54 баллов, а значит хороший функциональный уровень (таблица 2).
Таблица 2 - Распределение больных по общей выраженности функционального дефицита по шкале MAS
|
Количество баллов |
До 18 баллов |
19-36 баллов |
37-54 баллов |
|
Количество больных |
25 |
13 |
10 |
|
Процент |
52,08% |
27,08% |
20,83% |
Согласно Barthel Index нарушение навыков самообслуживания в значительной степени (менее 40 баллов) при поступлении было у 25 (52,08%) больных, в умеренной степени (41-80 баллов) у 13 пациентов (27,08%) и практически сохранны (более 81 балла) у 10 (20,83%) больных (табл. 3). Средний балл по этой шкале составил 38±0,2.
Таблица 3 - Распределение больных по степени нарушений навыков самообслуживания (согласно Barthel Index)
|
Время проведения МРТ-исследования, часы |
0-6 |
7-24 |
25-48 |
|
Количество больных |
6 |
12 |
30 |
При сопоставлении клинико-неврологических и нейровизуализационных признаков были выявлены следующие особенности. При поступлении у половины больных отмечалась легкая степень тяжести состояния, у остальных - тяжелая и средняя. У 60,4% больных отмечался двигательный дефицит в руке разной степени выраженности, у большинства из них тяжелой и средней степени. Функциональный дефицит у 43,8% больных был средней степени выраженности.
MPT-исследование проводилось в сроки от 1 часа до 48 часов от начала ишемического инсульта. Среднее время, прошедшее с момента появления симптомов до первого MPT-исследования составило 28 часов (табл. 4). Зона инфаркта вовлекала различные структуры головного мозга. Так, лобная доля была поражена у 7 (14,58%), височная доля у 17 (35,42%), теменная доля у 19 (39,58%), глубокие отделы белого вещества полушарий головного мозга с вовлечением лентикулярного ядра у 15 (31,25%), внутренняя капсула - у 9 (18,75%), таламус - у 3 больных (6,25%). Причем у 24 пациентов очаг располагался в левом полушарии, у 23 в правом, а у 1 больного на фоне острой сердечной недостаточности развились острые очаги в обоих полушариях головного мозга.
|
Время проведения МРТ-исследования, часы |
0-6 |
7-24 |
25-48 |
|
Количество больных |
6 |
12 |
30 |
Таблица 4 - Распределение больных по срокам выполнения МРТ-исследования
У большинства больных нарушение кровообращения произошло в бассейне средней мозговой артерии (36 больных - 75%), в бассейне передней мозговой артерии очаг поражения был у 1 пациента (2,08%), задней мозговой артерии - у 5 (10,42%), перфорирующих артерий - у 5 (10,42%), в зоне смежного кровообращения у 1 пациента (2,08%).
При поступлении размер первоначального очага биоэнергетического повреждения, визуализируемого методом ДВ-МРТ, составил 15,8 см3, что было значительно больше очага повреждения по T2df - 6,1 см3, при этом различие объемов статистически достоверно (р<0,001).
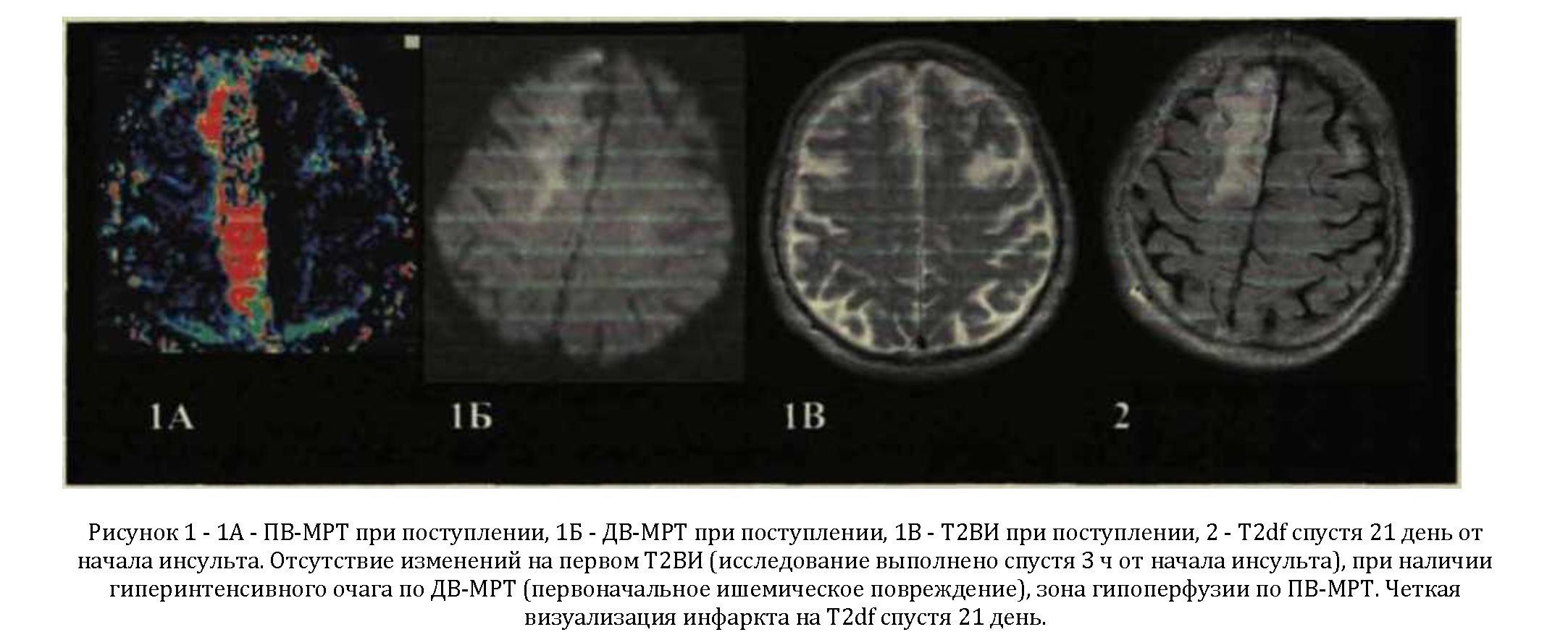
Как уже отмечалось, это объясняется большей чувствительностью метода МРТ в выявлении острого ишемического повреждения мозга. Этот факт подтверждается также отсутствием каких-либо изменений по данным стандартных режимов у трех наших пациентов, в то время как по ДВ-МРТ которое проводилось спустя 1, 3 и 4 часа от начала ИИ, размеры очагов повреждения составили 19,2 см3; 6,5 см3 и 60,6 см3, а их ИКД 75, 55 и 57 х10-3мм2/с соответственно (Рисунок 1).
При сопоставлении тяжести состояния больных при поступлении с объемом структурного повреждения по ДВ- МРТ и T2df взаимосвязи выявлено не было. Так, коэффициент корреляции между исходным количеством баллов по ESS и размером инфаркта по ДВ-МРТ составил - 0,076 (р=0,651), а по T2df- 0,142 (р=0,396).
Степень выраженности изменений по ДВ-МРТ определялась сроками МРТ-исследования. Так, интенсивность сигнала от инфаркта, отражающая выраженность структурных нарушений в веществе мозга, а также ее повышение относительно неповрежденного вещества мозга были прямо пропорциональны срокам проведения МРТ-исследования, выраженных в часах от начала ишемического инсульта, при этом коэффициент корреляции Спирмена составил соответственно 0,53 и 0,39 (р<0,05). По-видимому, интенсивность сигнала от инфаркта по ДВ-МРТ, отражающая выраженность структурных нарушений в веществе мозга, имеет временную зависимость.
На изображениях, полученных в T2df режиме, помимо основного очага у 56% больных (27 человек) визуализировались гиперинтенсивные очаги диаметром менее 2 см, а у 4 человек - более 2 см. Учитывая наличие у них в анамнезе той или иной сердечно-сосудистой патологии и отсутствие ОНМК, обнаруженные изменения мы интерпретировали как последствия хронической недостаточности мозгового кровообращения или немые инфаркты. У всех описанных больных дифференцировка острого инфаркта и более давних изменений на T2df изображениях была затруднена из-за одинаковых показателей интенсивности сигнала от них. Вместе с тем, ДВ-МРТ (при высоких значениях силы диффузионного взвешивания) визуализировало только острое ишемическое повреждение.
Таким образом, для метода ДВ-МРТ в остром периоде ИИ показана высокая чувствительность в выявлении ишемического очага, временная зависимость степени выраженности изменений, возможность дифференцировки острого повреждения от более давних. Достаточно большое прикладное значение имеет и другая методика - МРТ с контрастированием. Согласно работам, выполненным в отделении нейрореанимации, для эффективного лечения и вторичной профилактики ИИ важно выявление его патогенетического подтипа. По нашим данным в ряде случаев МРТ с контрастированием может служить вспомогательным инструментом для распознавания механизма ИИ. Так, у двух больных на МРТ зона гипоперфузии была клиновидной формы, что характерно для закупорки крупной интракраниальной артерии, однако ультразвуковое исследование магистральных артерий головы патологии не выявило. Полученные данные указывали на вероятный кардиоэмболический подтип ИИ, хотя в анамнезе указаний на патологию сердца, способную привести к формированию эмболического материала, не было. Пациенты имели синусовый ритм сердца, и им было проведено суточное мониторирование ЭКГ. Только повторная процедура холтеровского мониторирования выявила пароксизмы мерцания предсердий. То есть данные качественного анализа МРТ изображений головного мозга, а именно выявленная клиновидная форма зоны гипоперфузии, помогла в определении направления диагностического поиска с целью распознавания подтипа ИИ и разработки дальнейшей тактики ведения больного.
У двух больных при проведении МРТ зона гипоперфузии занимала весь бассейн передней и средней мозговых артерий. При дальнейшем обследовании были выявлены в одном случае окклюзия, в другом - критический стеноз (9095%) внутренней сонной артерии на стороне поражения
изменения, в результате чего был диагностирован атеротромботический подтип инсульта.
Таким образом, в ряде случаев МРТ может иметь вспомогательное значение в распознавании подтипов ИИ, определяя дальнейший диагностический поиск.
Кроме того, в редких случаях при проведении МРТ- исследования в пределах 1-2 часов от начала ИИ, когда визуализируемые ДВ-МРТ изменения ещё не развились, МРТ исследование с контрастированием могут иметь решающее значение для верификации диагноза.
СПИСОК ЛИТЕРАТУРЫ
- 1 Верещагин Н.В., Суслина З.А. Современное представление о патогенетической гетерогенности ишемического инсульта // В кн. Очерки ангиневрологии. / Под ред. З.А. Суслиной. - М.: Атмосфера, 2005. - С. 82-85
- Инсульт. Принципы диагностики, лечения и профилактики / Под ред. Н.В.Верещагина, М.А. Пирадова, З.А. Суслиной. - М.: Интермедика, 2008. - 208 с.
- Труфанов Г.Е., Фокин В.А., Пьянов И.В., Банникова Е.А. Рентгеновская компьютерная и магнитно-резонансная томография в диагностике ишемического инсульта. - Спб.: ЭЛБИ-СПб, 2005. - 296 с.
- Barber P.A., Darby D.G., Desmond P.M., et al. Prediction of stroke outcome with echoplanar perfusion- and diffusion-weighted MRI // Neurology. - 2011. - Vol. 51. - P. 418-426.
- Chalela J.A., Merino J.G., Warach S. Update on stroke // Curr. Opin. Neurol. - 2008. - Vol. 17. - P. 447-451.