Проведен сравнительный анализ общего состояния, локального статуса и функционального состояния печени и почек у пациентов в условиях доклинических испытаний до и после лечения препаратом «Аяфрол», а также побочных действий препарата.
Применение препарата «Аяфрол» у больных с гнойной хирургической инфекцией обладает хорошей переносимостью и достаточной безопасностью.
Проблема лечения гнойных ран продолжает оставаться одной из основных в современной хирургии, разработка научно-обоснованных методов местного лечения ран является актуальной, как для теоретической, так и для практической медицины. В этой связи представляется перспективным применение нового отечественного препарата «Аяфрол», разработанного в АО «МНПХ «Фитохимия» (председатель правления - академик НАН РК, д.х.н., профессор Адыкенов С.М.). Препарат «Аяфрол» представляет собой 3% мазь на основе эфирного масла Аянии кустарничковой.
Цель исследования: определения биодоступности фитопрепарата «Аяфрол, мазь 3%» в эксперименте, изучение переносимости и безопасности его применения у больных с гнойной хирургической инфекцией.
Материалы и методы: Определение фармакокинетики хамазулена (основного компонента эфирного масла Аянии кустарничковой) проводили на 40 белых короткошерстных половозрелых крысах одинакового возраста, размера и массы тела методом высокоэффективной жидкостной хроматографии на аппаратах фирмы “Agilent 1260 Infinity”, на базе лаборатории коллективного пользования Карагандинского государственного медицинского университета (заведующий - д.м.н., профессор Азизов И.С.). Под эфирным наркозом с помощью пластикового шаблона производилось моделирование раны с одинаковой площадью 6,0 см2 на дорзальной поверхности животного, затем наносилась навеска мази массой 5 г тонким слоем по всей поверхности раневого дефекта. Через 0,5 ч,1 ч, 2 ч, 4 ч,6 ч, 12 ч и 24 ч после легкого эфирного наркоза производился забор крови у животных путем внутрисердечной пункции. Сыворотку получали путем центрифугирования крови и помещали в морозильную камеру (t=-20ºС) для хранения.
В качестве контроля использовали сыворотку крови интактных животных. Далее проводили статистический анализ измерения концентрации хамазулена в сыворотке крови после местного воздействия мази «Аяфрол».
На этапе первой фазы клинических испытаний, проведено простое открытое клиническое исследование у 30 пациентов в возрасте от 18 до 50 лет с хирургической гнойной инфекцией, находившихся на стационарном лечении в Областной клинической больнице г.Караганды (директор - к.м.н., доцент Абеуов М.Е.). Средний возраст пациентов составил 40,6±10,3 лет, мужчин -10 (33,3%), женщин - 20 (67,7%).
Критериями исключения пациентов из исследования являлись сопутствующие сердечно-сосудистые заболевания в стадии декомпенсации, хроническая печеночная или почечная недостаточность, некоррегируемый сахарный диабет в стадии декомпенсации, психические и онкологические заболевания, наличие в анамнезе указаний на аллергию, острые воспалительные процессы других органов и систем.
Преобладали пациенты с диабетической стопой - 10 (33,3%) и острыми гнойными заболеваниями мягких тканей с локализацией на нижних конечностях - 10 (33,3%), на голове и шее - 5 (16,7%), передней брюшной стенке - 1 (3,33%), ягодичной области - 1 (3,33%), 2 (6,67%) пациентов с острым парапроктитом и 1 (3,33%) с вазотрофической язвой голени, осложненной рожей.
После получения информированного согласия пациентам назначался препарат «Аяфрол» в виде 3% мази, наносимой на раневую поверхность после первичной обработки тонким слоем в течение 14 дней.
Проведен сравнительный анализ общего состояния, локального статуса и лабораторных показателей функционального состояния печени и почек пациентов до и после лечения препаратом «Аяфрол», побочных действий препарата.
Оценка эффективности препарата не входила в задачи данной фазы исследования.
Статистическая обработка результатов проводилась с расчетом средних значений, стандартного отклонения среднего значения, доверительных интервалов, значимость различий в группах определялась в экспериментальных данных методом сравнения доверительных интервалов, в клинических - с помощью непараметрических критериев (критерий знаков Dixon&Mood и Wilcoxon). Для расчетов использовался табличный процессор MS Excel 2010.
Результаты и обсуждение.
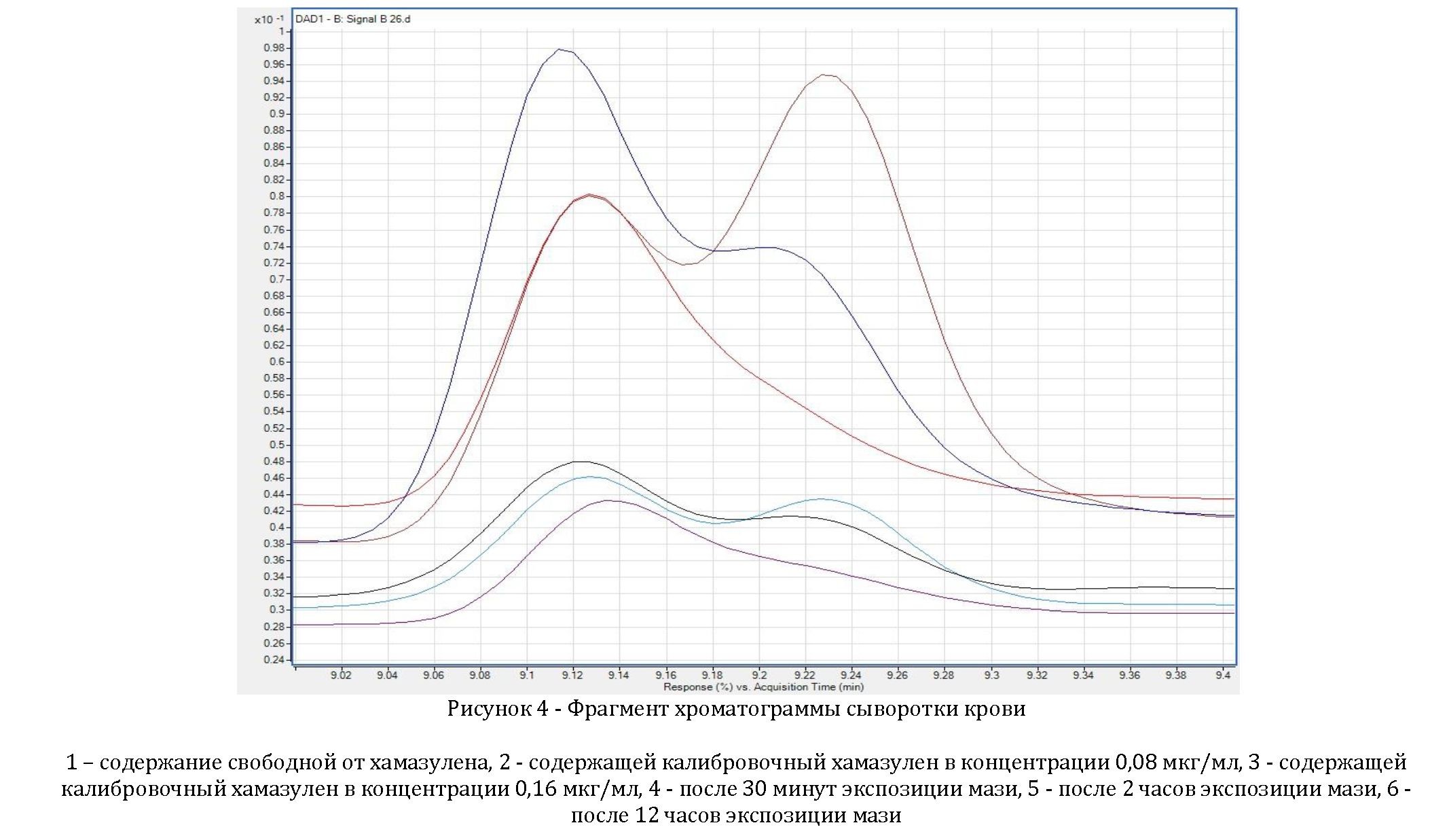
Результаты определения содержания хамазулена в сыворотке крови экспериментальных животных после аппликации фитопрепарата «Аяфрол» представлены в таблицах 1, 2 и на рисунке 4. При местном применении мази
Таблица 1 – Результаты измерения концентрации хамазулена в сыворотке крови после местного воздействия мази с эфирным маслом Аянии кустарничковой.
|
Экспозиция мази |
Площадь хроматографического пика |
Оценка концентрации, мкг/мл |
|
30 мин |
1,64 |
не определяется |
|
30 мин |
2,78 |
0,002 |
|
30 мин |
2,53 |
0,002 |
|
30 мин |
1,69 |
не определяется |
|
30 мин |
2,49 |
0,002 |
|
1 час |
4,53 |
0,011 |
|
1 час |
3,31 |
0,005 |
|
1 час |
3,86 |
0,007 |
|
1 час |
3,49 |
0,006 |
|
1 час |
4,21 |
0,009 |
|
2 часа |
3,58 |
0,006 |
|
2 часа |
7,25 |
0,025 |
|
2 часа |
4,83 |
0,013 |
|
2 часа |
5,79 |
0,02 |
|
2 часа |
4,66 |
0,012 |
|
4 часа |
4,79 |
0,012 |
|
4 часа |
7,60 |
0,026 |
|
4 часа |
5,21 |
0,018 |
|
4 часа |
6,54 |
0,022 |
|
4 часа |
4,76 |
0,013 |
|
6 часов |
4,48 |
0,011 |
|
6 часов |
4,69 |
0,012 |
|
6 часов |
4,59 |
0,012 |
|
6 часов |
5,22 |
0,014 |
|
6 часов |
4,16 |
0,009 |
|
12 часов |
4,74 |
0,012 |
|
12 часов |
3,95 |
0,008 |
|
12 часов |
3,72 |
0,007 |
|
12 часов |
4,12 |
0,009 |
|
12 часов |
3,73 |
0,007 |
|
24 часа |
3,27 |
0,005 |
|
24 часа |
3,68 |
0,007 |
|
24 часа |
2,99 |
0,004 |
|
24 часа |
3,31 |
0,005 |
|
24 часа |
2,63 |
0,002 |
в виде аппликаций на рану, площадью 6 см2, статистически значимое повышение уровня лекарственного вещества в крови и максимальное его содержание обнаруживается через 4 часа, среднее значение - 0,0182 мкг/мл (ДИ=0,0052; δ=0,00593; α=0,05). Через 6 и 12 часов концентрация хамазулена статистически значимо снижается до 0,0116 мкг/мл (ДИ=0,00159; δ=0,00182; a=0,05) и 0,0086 мкг/мл (ДИ=0,00182; δ=0,00207; a=0,05) соответственно, а к 24 часам практически достигает базового уровня, составляющего 0,0046 мкг/мл (ДИ=0,00159; δ=0,00182; a=0,05).
Таблица 2 - Результаты статистического анализа измерения концентрации хамазулена в сыворотке крови после местного воздействия мази с эфирным маслом Аянии кустарничковой.
Примечания:
- * - статистическая значимость различий по отношению к начальной экспозиции 0,5 часа;
- # - статистическая значимость различий по отношению к предыдущему интервалу экспозиции.
|
Концентрация Хамазулена в сыворотке (мкг/мл) |
Длительность экспозиции мази (час) |
||||||
|
0,5 |
1,0 |
2,0 |
4,0 |
6,0 |
12,0 |
24,0 |
|
|
M среднее |
0,0012 |
0,0076 |
0,0152 |
0,0182 |
0,0116 |
0,0086 |
0,0046 |
|
δ |
0,00110 |
0,00241 |
0,00740 |
0,00593 |
0,00182 |
0,00207 |
0,00182 |
|
ДИ, (a=0,05) |
0,00096 |
0,00211 |
0,00648 |
0,00520 |
0,00159 |
0,00182 |
0,00159 |
|
ДИ+ |
0,00216 |
0,00971 |
0,02168 |
0,02340 |
0,01319 |
0,01042 |
0,00619 |
|
ДИ- |
0,00024 |
0,00549 |
0,00872 |
0,01300 |
0,01001 |
0,00678 |
0,00301 |
|
p<0,05 |
*, # |
* |
* |
*, # |
* |
*, # |
|
В ходе клинических испытаний мази «Аяфрол», при поступлении до назначения препарата у всех 30 пациентов отмечены признаки интоксикационного синдрома в виде лихорадки и общей слабости. При выписке после хирургического лечения и применения препарата «Аяфрол» лихорадки не отмечено ни у одного пациента, общая слабость сохранялась у 3 (10%). Локальные изменения при поступлении в виде гнойного отделяемого и некрозов наблюдались у всех 30 пациентов, которые к моменту выписки регрессировали во всех случаях наблюдения. Размеры раны при поступлении - 9,8±12,1 см2 , после лечения - 11,7±15,6 см2. В показателях общего анализа крови и мочи, биохимического анализа крови достоверных различий до и после применения мази «Аяфрол» не выявлено (таблица 3).
|
Показатели |
до (M ±m) |
После (M ±m) |
Уровень значимости различий |
|
Общий анализ крови |
|||
|
Гемоглобин (г/л) |
144,53±13,67 |
137,73±17,22 |
p>0,05 |
|
Эритроциты (х1012)/л |
4,82±0,37 |
4,64±0,49 |
p>0,05 |
|
Лейкоциты (х109)/л |
7,95±3,01 |
5,37±1,38 |
p>0,05 |
|
СОЭ (мм/ч) |
22,60±13,07 |
20,03±11,29 |
p>0,05 |
Таблица 3 - Лабораторные показатели до и после применения препарата «Аяфрол»
|
Палочкоядерные нейтрофилы (%) |
3,37±2,30 |
1,47±0,69 |
p<0,05 |
|
Сегментоядерные нейтрофилы (%) |
67,53±8,06 |
67,17±6,81 |
p>0,05 |
|
Моноциты (%) |
3,52±1,71 |
3,37±1,34 |
p>0,05 |
|
Лимфоциты (%) |
24,73±7,95 |
28,87±6,42 |
p>0,05 |
|
Биохимический анализ крови |
|||
|
АЛТ (нмоль/л) |
129,00±84,00 |
113,98±61,12 |
p>0,05 |
|
АСТ (нмоль/л) |
73,51±31,40 |
67,48±27,06 |
p>0,05 |
|
Щелочная фосфатаза (м МЕ/л) |
665,51±370,44 |
761,95±306,81 |
p>0,05 |
|
Общий билирубин (мкмоль/л) |
14,06±2,45 |
12,98±1,43 |
p>0,05 |
|
Прямой билирубин (мкмоль/л) |
3,63±0,92 |
3,07±0,56 |
p>0,05 |
|
Общий белок (г/л) |
69,85±4,63 |
49,32±69,91 |
p>0,05 |
|
Креатинин (ммоль/л) |
13,91±23,03 |
13,01±21,53 |
p>0,05 |
|
Мочевина (ммоль/л) |
7,1±1,44 |
6,7±1,26 |
p>0,05 |
|
Общий анализ мочи |
|||
|
Относительная плотность |
1019,28±4,52 |
1018,57±3,59 |
p>0,05 |
|
Плоский эпителий (п/зр) |
2,3±1,5 |
2,5±1,3 |
p>0,05 |
|
Лейкоциты (п/зр) |
3,8±2,5 |
3,0±0,9 |
p>0,05 |
Протеинурия при поступлении выявлена у 5(16,7%), при выписке у 6(20,0%), эритроцитурия - у 3 (10%) и у 1 (3,33%) пациентов соответственно, статистически достоверных отличий не выявлено (p>0,05).
Ни в одном случае применения препарата не выявлено местно-раздражающего действия, также не отмечено ни одного случая аллергических реакций.
Таким образом, анализ I фазы клинических испытаний мази «Аяфрол» показал, что использование данного препарата у больных с гнойными ранами не сопровождается клинически значимым резорбтивным или местно-раздражающим эффектом, каким-либо другим побочным действием или аллергией.
Выводы: на основании проведенных доклинических испытаний можно утверждать, что при местном применении фитопрепарата «Аяфрол, на поверхности ран экспериментальных животных, в системном кровотоке концентрация хамазулена не превышает 0,025 мкг/мл. Кумуляции хамазулена в системном кровотоке при длительной (до 24 часов) экспозиции не происходит.
Полученные результаты свидетельствуют о том, что компоненты мази с эфирным маслом «Аянии кустарничковой» предназначены для местного воздействия на раневой процесс, непосредственно в месте контакта с раневой поверхностью.
Применение препарата «Аяфрол» у больных с гнойной хирургической инфекцией обладает хорошей переносимостью и достаточной безопасностью.
СПИСОК ЛИТЕРАТУРЫ
- Марковский В.Б. Ожирение и артериальная гипертония: патофизиологические особенности, диагностика и лечение. - М.: 2010. - С. 55-56.
- Рогоза А.Н., Ощепкова Е.В., Цагареишвили Е.В., Гориева Ш.Б. Современные неинвазивные методы измерения артериального давления для диагностики артериальной гипертонии и оценки эффективности антигипертензивной терапии. - М.: Медика, 2007. - С. 27-33.
- Шевченко О.П., Праскурничий Е.А., Шевченко А.О. Артериальная гипертония и ожирение. - М.: «Реофарм», 2006. - С. 59-61