Представлен метод определения гидазепама в крови и биологических тканях по его фармакологически активному метаболиту N1- дезалкилгидазепаму в варианте двумерной хроматомасспектрометрии. С целью изолирования N1-дезалкилгидазепама предложено два варианта экстракции – жидкостная и твердофазная. Показано, что в случае жидкостной экстракции оптимальным экстрагентом является смесь 1-хлорбутана и этилацетата в соотношении 9:1. Эффективность изолирования жидкостной и твердофазной экстракцией составляет 98 и 94 % соответственно. Линейный диапазон определяемых концентраций составил 201000 нг/мл в крови, и 0,2-10 мкг/г в тканях органов. Предел обнаружения в крови и тканях составил соответственно 3 и 5 нг.
Гидазепам, известный также под названием Диамидазепам, является производным 1,4-бенздиазепина с выраженным анксиолитическим действием и применяется в качестве дневного транквилизатора [1]. В отличие от других препаратов с анксиолитической активностью, гидазепам в терапевтических дозах не проявляет седативный и миорелаксантный эффекты и обладает низкой токсичностью. Вместе с тем, он потенцирует действие алкоголя, наркотических и психотропных препаратов, что обуславливает его немедицинское использование с целью усиления наркотического эффекта или осуществления криминальных действий.
Целью настоящей работы явилась разработка методики определения гидазепама по его активному метаболиту N1- дезалкилгидазепаму в крови живых лиц, а также крови и паренхиматозных органах трупов методом двумерной хроматомасспектрометрии.
Будучи пролекарством, гидазепам подвергается интенсивному метаболизму, в результате которого в организме человека обнаруживаются главным образом его метаболиты [2,3], основным из которых является фармакологически активный N1-дезалкилгидазепам. Именно последний и обуславливает весь спектр фармакологических свойств гидазепама [3]:
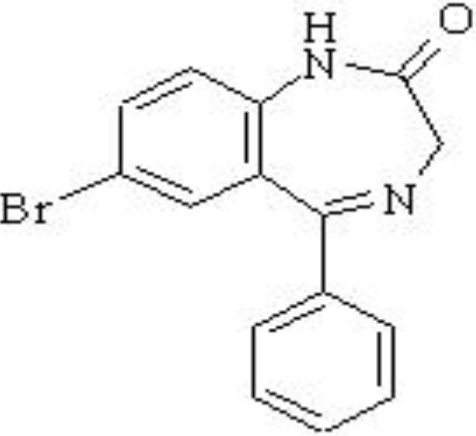
Показано, что в крови человека присутствует только N1- дезалкилгидазепам[1,3]. Литературные данные
относительно его распределения в других органах и жидкостях человека отсутствуют, равно как и данные относительно распределения других его метаболитов. Однако, наши исследования крови и органов трупов, в анамнезе которых было употребление гидазепама, а также крови и мочи принимавших его добровольцев, показали, что в тканях печени и почки, как и в крови, присутствует только N1-дезалкилгидазепам. В желудке и верхнем отделе тонкого кишечника обнаружены, в основном, гидазепам и в небольшом количестве карбоксиметилгидазепам (5-20 %), а в моче - карбоксиметилгидазепам (50-70%), гидазепам (615%), N1-дезалкилгидазепам (10-15%) и глюкуронид 3- гидрокси-N1-дезалкилгидазепама (5-15%).
Pанее, на основании полученных данных, нами был предложен метод обнаружения гидазепама по продуктам его гидролиза в моче [4], принцип и методология которого с успехом была применена для анализа содержимого желудка. В настоящей работе нами представлено определение гидазепама по его активному метаболиту N1- дезалкилгидазепаму в крови живых лиц, а также крови и паренхиматозных органах трупа методом двумерной хроматомасспектрометрии.
Материалы и методы. Стандарты N1-дезалкилгидазепама и феназепам (внутренний стандарт) были приобретены у ОДО “Интерхим” (г. Одесса, Украина). Все органические растворители использовались квалификации “ для ВЭЖХ ” (Merck, Darmstatd, Germany). В качестве реагента для силилирования применялся N,O- бис(триметилсилил)трифторацетамид (BSTFA) содержащий 1 % триметилхлорсилана (Fluka Analytical, Buchs SG, Switzerland). Уксусная кислота, 25 % раствор аммиака, дигидрофофат калия (KH2PO4) - квалификации “х.ч.”. 1М раствор уксусной кислоты готовили путем растворения 5,7 мл уксусной кислоты в 60 мл дистиллированной воды и доведением до общего объема 100 мл. Фосфатный буферный раствор (0,1М, рН=6,0) готовили путем растворения 6,8 г KH2PO4 в 400 мл дистиллированной воды, доведением рН до значения 6,0 под контролем рН-метра 1М раствором КОН и доведением до общего объема 500 мл. Боратный буферный раствор (0,01М, рН=9,2) готовился из фиксанала. Колонки для твердофазной экстракции Bond Elute Certify, 130 мг, 3 мл производства Agilent Technologies (Palo Alto, CA, USA).
Исходные и рабочие растворы. Исходный раствор N1- дезалкилгидазепама с концентрацией 100,0 мкг/мл был приготовлен растворением 10,3 мг N1-дезалкилгидазепама в 100 мл метанола. Pабочие растворы с концентрацией 1,0 и 10,0 мкг/мл готовили путем разведения соответственно 0,1 и 1,0 мл исходного раствора N1-дезалкилгидазепама метанолом до 10,0мл. Pабочий раствор внутреннего стандарта с концентрацией 50,0 мкг/мл был приготовлен растворением 10,2 мг феназепама в 200 мл метаноле.
Оборудование. В работе использовали одноквадрупольный хроматомасспектрометр Agilent 6890N/5973N/FID (Agilent Technologies, Palo Alto, CA, USA), с пневматическим микропотоковым переключателем потока газа-носителя между колонками, позволяющий переключать поток газа носителя с первой колонки на детектор ионизации в пламени (ДИП), или через вторую колонку в массдетектор. Колонка № 1 - НP-5MS 0,25 мм х 30 м, конец колонки соединен с ДИПом, №2 - DB-17MS 0,25 мм х 30 м, конец колонки непосредственно входит в масспектрометр. Аналитические весы для взятия навесок с точностью взвешивания 0,1 мг Mettler-Toledo ML 204/01 (Greifense, Switzerland).
Условия работы хроматографа и массдетектора. Температура испарителя - 250 0С. Программа изменения давления на входе в первую колонку (испарителе): 26,00 psi - 1 мин, увеличение до 40,00 psi со скоростью 4 psi/мин, затем увеличение до 50,22 psi со скоростью 2,00 psi/мин, удерживание 2,91 мин, затем понижение давления до 0,50 psi со скоростью 30 psi/мин и удерживание до конца хроматографического цикла. Программа изменения давления на входе во вторую колонку (пневматический переключатель): 19,35 psi - 1 мин, увеличение до 30,40 psi со скоростью 4 psi/мин, затем увеличение до 38,72 psi со скоростью 2,00 psi/мин и выдержка при данном давлении до конца хроматографического цикла. Pежим ввода пробы - 1 мкл с помощью автоинжектора серии 7683 без деления потока. Температурная программа термостата: 70 0С - 1 мин, нагрев до 210 0С со скоростью - 45 0С/мин, затем нагрев до 320 0С со скоростью - 25 0С/мин, и выдержка при этой температуре 8,49 мин. Температурная программа линии сопряжения хроматографа с масспектрометром - 280 0С, в течении 6,91 мин, затем нагрев до 320 0С со скоростью - 25 0С/мин, и выдержка при этой температуре 8,49 мин. Температура ДИПа - 250 0С. Температура источника ионов - 230 0С, квадруполя - 150 0С, энергия электронов - 70 еВ, напряжение на электроумножителе на 200 В больше чем при автонастройке. Массдетектор настроен для работи в режиме селективного ионного мониторинга (СИМ). С 8,50 до
- минуты скнируются ионы N1-дезалкилгидазепама, а с
- минуты и до конца хроматографического цикла ионы феназепама (внутренний стандарт).
Пробоподготовка. Кровь. Перед экстракцией к 1мл образца крови (сыворотки или плазмы) добавлялось 20 мкл раствора внутреннего стандарта и смесь перемешивалась.
- Жидкость-жидкостная экстракция (ЖЖЭ). К 1 мл объекта добавляли 1мл боратного буферного раствора (рН=9,2), перемешивали, затем смесь экстрагировали 5мл смеси н- хлорбутан - этилацетат (9:1) в течении 5 мин. Для полного разделения слоев пробу центрифугировали 5мин при 3000 об/мин. Органическую фазу отделяли и упаривали при разряжении водоструйного насоса при 40 0С и остаток дериватизировали.
- Твердофазная экстракция (ТФЭ) [5]. 1мл объекта
разбавляли 1 мл 0,1М фосфатного буферного раствора (рН=6,0) и, в случае трупной крови, при необходимости, центрифугировали при 2000 об/мин в течении 10 минут. Подготовленный объект переносили в промытую последовательно 2 мл метанола, 2 мл дистиллированной воды и 2 мл 0,1М фосфатного буферного раствора (рН=6,0) колонку. После загрузки объекта колонка последовательно промывалась 3 мл дистиллированной воды, 1мл 1,0М раствором уксусной кислоты и в конце 3 мл метанола. Далее колонку сушили 5 мин и проводили элюирование аналита 2 мл смеси дихлорметан - i-пропанол - 25 % роаствор аммиака (78:20:2). Элюат упаривали при разряжении водоструйного насоса при 40 0С и остаток дериватизировали.
Дериватизация. К упаренным экстрактам или элюатам добавляли 50 мкл BSTFA и нагревали в герметично закрытой виале 20 мин при температуре 80 0С. 1мкл полученного раствора вводили в хроматограф.
Ткани трупа. 1 г ткани гомогенизировали с 4 мл дистиллированной воды, к 0,5 мл гомогената добавлялось 20 мкл раствора внутреннего стандарта и смесь перемешивали. Затем, перед ЖЖЭ добавляли 1,5 мл боратного буферного раствора (рН=9.2), а перед ТФЭ - 1,5 мл фосфатного буферного раствора (рН=6.0), и гомогенат центрифугировали при 3000 об/мин 10 мин. Далее подготовленные объекты подвергали ЖЖЭ или ТФЭ с последующей дериватизацией как описано для крови.
Калибровка и валидация. Калибровочный график для определения N1-дезалкилгидазепама строили, используя рабочие растворы последнего добавленные в не содержащую данный аналит кровь или гомогенаты тканей. Концентрация внутреннего стандарта в объектах, во всех случаях, составляла 1,0 мкг/мл. Полученные графики использовались для проверки линейности, вычисления предела детектирования и предела количественного определения. Аналогично приготовленные пробы крови и гомогената использовали для нахождения показателей точности, воспроизводимости и возврата, а также для нахождения и коррекции “временных окон” на хроматограммах с целью идентификации. Идентификацию аналита проводилась на основании времени удерживания и анализа масспектральных данных. “Временное окно” на первой колонке составляло 0.10 мин, на второй колонке 0.2 мин, от значения полученного при хроматографировании контрольной пробы содержащей аналит и внутренний стандарт. Хроматографические параметры гидазепама, его метаболитов и их различных дериватов представлены в работе [6]. В режиме СИМ идентичность оценивалась по наличию выбранных масс и отношения их интенсивностейсогласно указаний [7]. Процедуру валидации проводили согласно документа [8].
Результаты и их обсуждение
Экстракция и хроматографическое разделение.
Учитывая отсутствие в литературе информации о влияние
Таблица 1.
Как видно из таблицы, наименее эффективными оказались гексан и гептан, все остальные растворители показали примерно равную эффективность экстракции. Однако, этилацетат и эфир наряду с аналитом в значительной степени извлекают коэкстрактивные вещества, сильно загрязняющие конечные экстракты, а хлороформ и дихлорметан, с практической точки зрения, менее удобны при экстракции небольших объемом в пробирках. Наиболее оптимальным, по нашему мнению, является 1-хлорбутан. Данный экстрагент, по сравнению с этилацетатом и эфиром, в значительно меньшем количестве извлекает коэкстрактивные вещества, находясь по этому критерию наравне с хлороформом и дихлорметаном. Добавление к 1- хлорбутану 1 % этилацетата позволило увеличить степень экстракции N1-дезалкилгидазепама до 98 %, при этом количество экстрагируемых примесей осталось на прежнем уровне. Как альтернативный, изучен вариант изолирования методом ТФЭ. Степень экстракции данным методом составляет 94±5 % (n=5), а полученные экстракты, в отличие от ЖЖЭ, оказались значительно чище.
|
Степень экстракции N1-дезалкилгидазепама (%) Хср±ς, n=5 |
|||||||
|---|---|---|---|---|---|---|---|
|
гексан |
гептан |
хлороформ |
дихлорметан |
эфир |
этилацетат |
1- хлорбутан |
1- хлорбутан этилацетат (9:1) |
|
15±3 |
13±4 |
82±5 |
79±4 |
97±5 |
98±6 |
91±4 |
98±3 |
Хроматографическое разделение выполнено в варианте двумерной хроматомасспектрометрии. Принцип и преимущества данного варианта хроматографического разделения описаны в работе [4].
Валидация метода. В качестве внутреннего стандарта выбран феназепам, как ближайший 7-бромзамещенный химический аналог. С целью увеличения чувствительности и улучшения хроматографических характеристик N1- дезалкилгидазепам подвергался дериватизации с получением триметилсилильного производного. Несмотря на преимущество получения трет-бутилдиметилсилильных производных [6], в масспектре такового производного N1- дезалкилгидазепама, интенсивность кластера молекулярных ионов не превышает 10 %. Последнее обстоятельство послужило основанием в пользу выбора триметилсилильного производного, у которого молекулярный и изотопный ему ионы являются базовыми в масспектре. Для режима СИМ из масспектра N1- дезалкилгидазепама выбраны ионы со значением m/z 371, 373, 385 (М+), 387 и 389. Внутренний стандарт природы экстрагента на изолирование N1- дезалкилгидазепама, на первом этапе мы изучили степень изолирования его наиболее популярными в аналитической токсикологии экстрагентами. Полученные результаты представлены в Таблице 1. прослеживался по ионам со значением m/z 385, 387, 405, 407, 420 (М+) и 422. Критерии выбора ионов изложены в руководстве [7].
Рабочий диапазон концентраций устанавливался, учитывая данные о концентрации N1-дезалкилгидазепама в крови, после однократного и длительного (до 14 дней) приема гидазепама [3], а также анализа построенной прямой на соблюдение линейности. На основании полученных данных рабочий диапазон определения N1-дезалкилгидазепама в крови составил 20-1000 нг/мл, с калибровкой по пяти точкам - 20, 50, 100, 500 и 1000 нг/мл. При определении в биологических тканях, точки калибровочной прямой будут соответствовать концентрациям N1-дезалкилгидазепама в 0,1 г ткани (0,5 мл гомогената соответствует 0,1 г). При необходимости определения концентраций свыше 1000 нг/мл в крови (сыворотке, плазме) или свыше 10 мкг/г в тканях, объект до внесения внутреннего стандарт, может быть разбавлен или взят в соответствующе меньшем количестве. Определение в тканях концентраций менее 200 нг/г возможно при использовании всего (5мл) гомогената. При этом, в зависимости от используемого метода экстракции ткань гомогенизируют в боратном (рН=9,2), или в фосфатном (рН=6,0) буферных растворах. Значения параметров валидации определения N1-дезалкилгидазепама в крови и тканях трупа представлены в таблицах 2 и 3. Параметры "точность” и "возврат” оценивались для трех уровней, соответственно наименьшего, среднего и наивысшего уровней диапазона концентраций. Параметр "воспроизводимость” оценен как среднеквадратичное отклонение (СКО) определения каждого уровня концентраций. Исследование образцов крови и биологических тканей из различных источников (n=10 для обоих объектов) не содержащих N1-дезалкилгидазепама, показало отсутствие влияния матрицы на обнаружение и определение последнего. Определению не мешают диазепам, оксазепам, хлордиазепоксид, медазепам, клоназепам, 7-аминоклоназепам, нитразепам, 7- аминонитразепам, 7-аминофлунитразепам, нордазепам, альпразолам, празепам при совместном присутствии.
Таблица 2.
|
Объект |
Линейность (r2) |
Предел обнаружения (нг) |
Предел количественного определения (нг) |
Воспроизводимость (СКО (%)) |
|
|
20 нг |
50-1000 нг |
||||
|
кровь |
0,99957 |
3 |
10 |
7,2 |
0,9-2,6 |
|
ткани |
0,99961 |
5 |
15 |
9,8 |
1,3-3,4 |
Таблица 3.
|
Точность (%) |
Концентрация аналита (нг) |
Возврат (%), Хср±ς n=5 |
||||||
|
в течении дня |
день ото дня |
ЖЖЭ |
ТФЭ |
|||||
|
кровь |
ткани |
кровь |
ткани |
кровь |
ткани |
кровь |
ткани |
|
|
3,8 |
6,1 |
0,3 |
0,3 |
20 |
97±4 |
45±6 |
94±5 |
53±7 |
|
1,4 |
1,2 |
0,2 |
0,2 |
500 |
98±4 |
55±4 |
94±5 |
57±6 |
|
0,8 |
0,7 |
0,2 |
0,3 |
1000 |
98±3 |
55±5 |
95±6 |
56±6 |
Выводы. Pазработан чувствительный и специфичный метод установления факта употребления гидазепама по обнаружению его фармакологически активного метаболита - N1-дезалкилгидазепама. Возможность исследовать как кровь, так и ткани трупа позволяет использовать его в клинической, наркологической и судебно-медицинской практике. Предел обнаружения в крови и органах составляет 3 нг/мл и 5 нг/г, соответственно. Pабочий диапазон концентраций находится в пределах 20-1000 нг/мл для крови и 0,2-10 мкг/г для органов. Диапазон определяемых концентраций может быть значительно расширен изменением количества взятого на анализ объекта. Последнее обстоятельство особенно актуально ввиду отсутствия данных относительно токсических и смертельных концентраций N1-дезалкилгидазепама в крови и биологических тканях.
СПИСОК ЛИТЕPАТУPЫ
- Жук О.В., Карпинчик В. А. Гидазепам - новый отечественный дневной транквилизатор // Провизор, 2000. - N 17. - С. 33-35
- Савченко М. А., Петюнін Г. П. Дослідження поведінки гідазепаму та його метаболітів в умовах кислотного гідролізу // Буковинський медичний вісник. - 2013. - т. XVII. - №3(67). - ч.1. - С. 143-148.
- Андронати С.А., Воронина Т.А., Головенко Н.Я. и др. Гидазепам. — К.: Наук. думка, 1992. - С. 55-62.
- Savchenko M.A., Petunyn G.P. Determination gidazepam aminobenzophenones by two-dimensional gas chromatography-mass spectrometry (GC-GC-MS) in urine // Journal of Chemical and Pharmaceutical Research. - 2015. - Vol. 7. - № 2. - P. 555-560.
- Agilent bond elut certify and certify II methods manual // Agilent Technologies Publication 5991-4939EN. - 2014. - P. 35.
- Савченко М.А., Петюнін Г.П. Газохроматографічне дослідження, гідазепаму, продуктів його гідролізу та метаболітів // Теорія та практика судовоŕ експертизи і криміналістики. - 2013. - № 1. - С. 312-318.
- Guidance document on analytical quality control and validation procedures for pesticide residues analysis in food and feed. // European commission health & consumer protection directorate-general. - SANCO/12571/2013. - P. 12.
- Guidance for the validation of analytical methodology and calibration of equipment used for testing of iIllicit drugs in seized materials and biological specimens ST/NAR/41. - N.Y.: United Nations, 2009. - P. 35-38.
- Mohammad Nasir Uddin, Victoria F. Samanidou, Ioannis N. Papadoyannis Biosample preparation and gas chromatographic determination of benzodiazepines —a review // Journal of Chromatographic Science. - 2013. - № 5. - P. 587-598.