В статье отражены результаты исследования пациентов с сахарным диабетом 1 и 2 типа. Изложены соотношение между мужчинами и женщинами, возрастной состав, стадии компенсаций и самое главное грозное осложнение заболевания - синдром диабетической стопы (СДС). Были решены вопросы требующего раннего проведения ангиографии сосудов нижних конечностей с последующим выбором методов и тактики реваскуляризации - стентирования или шунтирования.
Актуальность темы: Диабетическая нейропатия является следствием распространенного поражения нейронов и их отростков в центральной и периферической нервной системе, часто необратимого, в силу нарушения при СД процессов регенерации. Из-за диабетической нейропатии чувствительность нервов снижена или полностью потеряна. Поэтому у большинства пациентов повреждения стопы не вызывают болевых ощущений, и они обращаются к врачу намного позже, чем следовало бы и это приводит таким осложнением, как СДС. Если лечение начали с опозданием, то повышается вероятность, что спасти жизнь больному сможет только ампутация.
Термин СДС представляет собой собирательное понятие, обозначающее симптомокомплекс анатомофункциональных изменений стопы, связанных с диабетической нейропатией, микро- и макроангиопатией, остеоартропатией, на фоне которых развиваются тяжелые гнойно-некротические процессы. Исследовательской группой экспертов ВОЗ по сахарному диабету (Женева, 1987) диабетическая стопа выделена в качестве самостоятельного тяжелого осложнения сахарного диабета наряду с поражением глаз, почек, нервной и сердечно-сосудистой систем [3, 4].
Несмотря на повышение эффективности терапии диабетической стопы, 50-70% общего количества ампутаций нижних конечностей приходится на долю больных СД, превосходя общепопуляционные показатели в15-20 раз. Частота ампутаций увеличивается с возрастом и преобладает у мужчин [2, 5].
По данным International Working Group on the Diabetic Foot от 40 до 70% всех ампутаций нижних конечностей связано с сахарным диабетом, в 85% случаев этим ампутациям предшествуют язвенные дефекты [4, 7].
Подобный разброс объясняется отсутствием стандартов исследования и критериев оценки выраженности сосудистых расстройств. Одни авторы регистрируют только клинически выраженные нарушения, другие учитывают данные инструментальных исследований. В результате фактическая распространенность сосудистых поражений превышает регистрируемую: при ретинопатии в 4-5 раз, при нефропатии в 8,6 раза, при макроангиопатии нижних конечностейв 9,5 раза [3, 4, 7].
Ведущий патогенетический фактор ДС-микроангиопатия стоп-появляется чаще и раньше, чем ангиопатия сетчатки и почек.
А.П. Калинин и Б.М. Газетов (1999) выделили три типа диабетического поражения сосудов нижних конечностей [4,
- :
- Микроангиопатия, являющаяся одним из проявлений- нейропатии, с поражением артериол и капилляров.
- Атеросклеротическое поражение артерий голени (реже бедренных и подвздошных сосудов).
- Сочетание микроангиопатии с атеросклерозом.
У лиц молодого возраста преобладают явления микроангиопатии, основные изменения при которой локализуются в области базальных мембран микрососудов и проявляются в форме их аневризматических расширений, утолщения стенок артериол, капилляров и венул вследствие накопления в последних гликопротеинов [3, 1, 7].
Для старших возрастных групп наряду с микроангиопатией характерно также поражение сосудов среднего и крупного калибра-макроаигиопатия, типичное структурное проявление которой крупносегментарный и циркулярный кальциноз. Если для больных, не страдающих СД, характерны сегментарная и локальная облитерация крупных артерий, то у больных СД чаще обнаруживается продольная облитерация всей бедренной и большеберцовой артерий [2, 5, 8].
У длительно болеющих лиц с высокой частотой диагностируется распространенное поражение, как магистральных артерий, так и их дистальных отрезков. У больных СД отмечается более раннее и частое, чем в общей популяции, атеросклеротическое поражение сосудов нижних конечностей в форме облитерирующего атеросклероза дистальных сегментов сосудов-подколенных, большеберцовых артерий стопы, реже - бедренных и подвздошных [6, 9, 10].
Широко используемые консервативные методы терапии позволяют стабилизировать ремиссию процесса при начальных проявлениях критической ишемии, а при язвенно-некротических поражениях должны использоваться как этап подготовки к операции и в послеоперационном периоде [1, 5, 10].
Если эндоваскулярное вмешательство возможно, ему отдается предпочтение в связи с малой инвазивностью. Ограничение длительности эффекта ангиопластики компенсируется легкой повторяемостью и минимальной угрозой для жизни пациента [5, 6]. Развитие эндоваскулярных технологий с применением анте- и ретроградных доступов приводит к уменьшению более длительных и тяжелых для пациента шунтирующих операций [1, 5]. Задача улучшения артериального кровотока для купирования критической ишемии, угрожающей потерей конечности, требует раннего проведения ангиографии сосудов нижних конечностей и реваскуляризации [2, 6].
Показаниям к проведению ангиографии является синдром диабетической стопы и заболевания сосудов нижних конечностей (облитерирующий атеросклероз, аневризмы артерий, тромбоз глубоких вен) [4, 6, 9].
Целю ангиографии артерий нижних конечностей являются дальнейшее уточнение диагноза и определение методов и тактики реваскуляризации - стентирования или шунтирования, а также гибридные методы [5, 7, 10]. Показания для проведения ангиографии артерий нижних конечностей определяются лечащим врачом, который назначает необходимые анализы и исследования, такие как:
- анализы крови: общий, группа крови, Rh-фактор (резус- принадлежность), RW, ВИЧ, пробы на гепатит В и С
- ультразвуковое дуплексное сканирование сосудов нижних конечностей.
Цель исследования: Выявление осложнения сахарного диабета 1 и 2 типа СДС. Ранняя диагностика и определение методов и тактики реваскуляризации - стентирования или шунтирования.
Задачи исследования:
- Определить возрастной состав, частоту по полам, стадий компенсаций и частоту осложнений заболевания.
- Выявит количество больных с СДС.
- Решить вопрос о ранней диагностике, методов исследования пациентов и тактики реваскуляризации сосудов нижних конечностей при данном синдроме.
Материал и методы исследования:
Ретроспективно было изучены результаты диагностики и лечения всех 314 пациентов с сахарным диабетом 1 и 2 типа в условиях стационара НИИ кардиологии и внутренних болезней, который получали лечение в отделения терапии, кардиологии и ОРЭВХ с января 2012 по 1 декабрь 2013 гг.
Результаты исследования:
На рисунке 1 приведено соотношение больных СД, всего госпитализировано 314 пациентов с данным диагнозом, из них 166 (53%) мужчин и 148 (47%) женщин.
32% от общей распространенности диабета. Особую тревогу вызывает «омоложение» СД, так как за последние 15 лет заболеваемость среди лиц в возрасте 30 лет увеличилась на 80% [9].
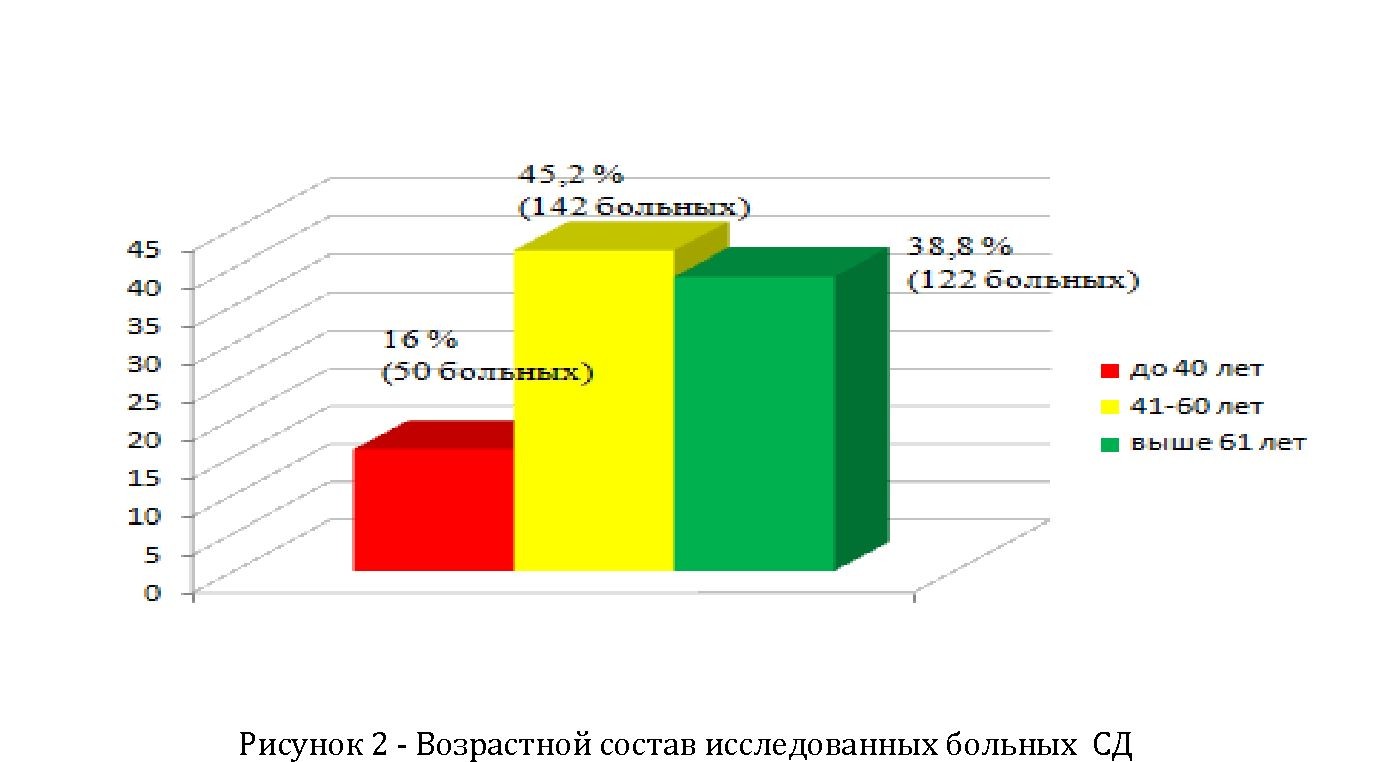
Как видно, основную массу составляют пациенты СД в возрасте от 40 до 60 лет, где показатели 45,2% (142), выше 60 лет 38,8% (122) и до 40 лет 16% (50) больных соответственно. Наибольшая частота язв стоп отмечается в возрасте 45-64 лет [14]. (Рисунок 2)
Возраст пациентов составлял от 14 до 81 лет. В действительности основную массу больных составляют лица с СД 2 (80-95%). По современным характеристикам его называют "болезнью цивилизации", прямую связь с технологией которого можно проследить в развитых и развивающихся странах.
Несмотря на высокие достижения в технологии в условиях неукротимого роста числа больных СД 2 проблемой остается позднее выявление этого заболевания. По данным литературы, Доля не Диагностированного СД Достигает 29–
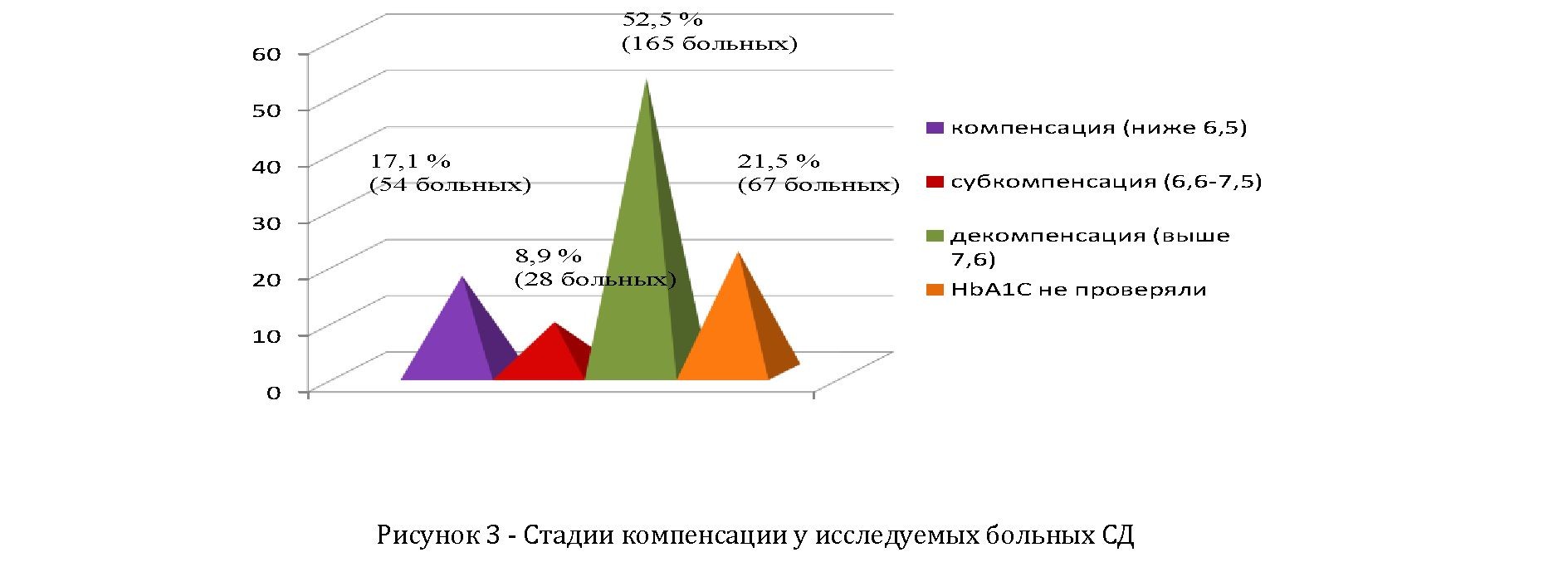
Анализ стадии обменных процессов на основании гликилированного гемоглобина показывает, что большинство количество больных не доходит до компенсации. В действительности среди больных, госпитализированных декомпенсации составляют (165 больных) 52,5%, субкомпенсации (29) 8,9%, и только (54) 17,1 % больных со стадией компенсации, к сожалению 21,5% (67) исследование гликилированного гемоглобина не был проведен связи отсутствием реактива в стационаре.

По данным проспективном многоцентровом исследовании DCCT (Исследование по контролю за диабетом и его осложнениями, 1993 и 1995 гг.) еще раз было продемонстрировано тесная связь между гипергликемией и нейропатией. Посредством интенсивной инсулинотерапии достигнутый оптимальный уровень сахара крови уменьшал невропатических осложнений СД независимо от возраста, пола и длительности заболевания на 64%.
В то же время, данные интервенционного исследования сахарного диабета по методике Киссинджера (Kissinger) (Haupt, 1996) свидетельствуют о том, насколько трудно оптимизировать обмен веществ. Целевые уровни контроля гликемии у подавляющего большинства больных не достигаются (Ю.Н. Сунцов и др., 2008; А. Н. Мураталина, 2009) 68% пациентов с СД 2 типа не достигают контроля гликемии, из них у каждого третьего (29%) уровень гликированного гемоглобина превышает 9% (Рисунок 8, 9).
С другой стороны, по данным зарубежных исследователей многофакторное вмешательство, включая контроль гликемии и других факторов риска, позитивно снижает выраженность ретинопатии, вегетативной нейропатиии, тогда как соматическая нейропатия продолжает развиваться в своем режиме, что требует специальной фармакотерапии [5, 7].
Проблема диабетической микроангиопатии до настоящего времени является актуальной ввиду ее определяющей роли в инвалидизации и смертности больных СД. Как известно в общей структуре причин смерти больных СД лидирующую позицию занимают макрососудистые осложнения, прежде всего инфаркт миокарда и инсульт. Высокая частота сердечно-сосудистых заболеваний обусловлена тем, что СД 2 является одним из важных факторов риска атеросклероза и часто сочетается с другими факторами риска (артериальной гипертензией, дислипидемией, ожирением), усиливая их неблагоприятное действие. Одна из основных причин повышенного риска сердечно-сосудистых осложнений при СД — гипергликемия, инициирующая повреждение эндотелия сосудов, дисфункция которого приводит к развитию атеросклероза.
Как видно на рисунке 4 у большинство больных страдающих СД 1 и 2 типа АГ обнаруживается у 38,2% (120) и ИБС у 40,1% (126) больных, а у 21,7% (68) отсутствует.
Это показывает что у больных СД осложнения со стороны сердечно сосудистой системы встречается часто. По данным Американской диабетической ассоциации (ADA), несмотря на значительные успехи в контроле над уровнем глюкозы крови, артериальной гипертонией (АГ) и дислипидемией, смертность больных СД от ИБС лишь незначительно снизилась у мужчин и существенно увеличилась у женщин, в то время как в общей популяции лиц без СД смертность снизилась более чем на 30% [7, 9, 10]. Как известно, СД приводит к трехкратному повышению риска развития сердечно-сосудистых заболевании (ССЗ) и осложнений у мужчин и 9-кратному - у женщин [4, 5, 7].
У больных с СД чаще отмечаются безболевые формы (немые) формы ИБС, вплоть до безболевого ИМ [7, 8, 10]. В связи с этим всех больных СД после 35 лет необходимо тщательно собрать анамнез и регулярно провести ЭКГ исследование.
Анализ результатов исследования больных СД типа на основании клинического осмотра и УЗДГ сосудов нижних конечностей показало, что у 75 % (234) больных имеются ишемический и нейроишемический форма СДС, а у остальных 25% (80) больных ДПНП. (Рисунок 5)


По данным разных авторов, ее частота колеблется от 8 до 90%, к моменту установления диагноза СД 2 диабетическая нейропатия (ДН) составляет 43% [4]. ДН снижает качество жизни больных, является непосредственной причиной развития диабетической остеоартропатии, нейропатических язв стоп, являясь причиной 50-75% нетравматических ампутаций [2, 6].
Ампутация по праву считается крайним, калечащим методом лечения гнойно-некротического процесса. Малые ампутации при всех преимуществах приводят к изменению биомеханики стопы, при котором без индивидуальной ортопедической коррекции, профессионального ухода за стопами и тщательного контроля специалистов вероятность развития язвенного дефекта в будущем многократно возрастает [8].
СДС развивается в течение жизни у 15% больных сахарным диабетом (СД), и это связано с высокой заболеваемостью, летальностью и финансовыми затратами [4, 5]. Гнойно- некратические осложнения ангиопатий нижних конечностей занимает одно из ведущих мест среди причин госпитализации и глубокой инвалидизации больных СД [10].
Это доказывает, что для ранней диагностики и профилактики и своевременного лечения СДС всем больным СД необходимо провести электронейромиографию и УЗДГ сосудов нижних конечностей [2, 6, 7]. После исследовании в 2012 году 30-ти пациентам из 146 было показано проведение реваскуляризация нижних конечностей, тогда как в 2013 году 19-ти из 168. Кроме этого в 2013 году 7 пациентам была проведена баллонная ангиопластика.
Выводы:
Таким образом, нейроишемическая и ишемическая форма синдрома диабетической стопы без реваскуляризации ведет к одинаково большому количеству высоких ампутаций конечности как у пациентов с выраженными язвеннонекротическими поражениями, так и у пациентов с минимальными поражениями стопы.
Реваскуляризация при минимальном поражении стопы сопровождается достоверно большим количеством сохраненных конечностей, в сравнении с реваскуляризацией при выраженном язвенно-некротическом поражении стопы. Ранняя диагностика и своевременная реваскуляризация при минимальном поражении стопы является оптимальным подходом к лечению нейроишемической формой синдрома диабетической стопы, позволяющим сохранить опорную функцию стопы и избежать ампутации нижней конечности.

СПИСОК ЛИТЕРАТУРЫ
- Грачева Т.В. Физические возможности пациентов в отдаленном периоде хирургического лечения осложненных СДС // Статьи журнала . - 2011. - №3. - С. 44-49.
- Дистальные реконструкции при критической ишемии нижних конечностей у больных старших возрастных групп // Хирургия. - 2009. - № 1. - С. 49-53.
- Дибиров М.Д. Роль реконструктивных сосудистых операций у больных диабетической ангиопатией // Хирургия. - 2009. - №2. - С. 59-63.
- Земляной А.А. Гнойно-некротические поражения нейроишемической формы синдрома диабетической стопы. Новые возможности комплексного хирургического лечения // Эндокринная хирургия. - 2008. - № 1. - С. 11-13.
- Ефимов А.С. «Диабетические ангиопатии». - М.: «Медицина», 1989 . - 288 с.
- Игнатович И.Н., Хирургия и ангиология диабетической стопы. - Минск: БГМУ, 2013. - 304 с.
- Котов С.В. Диабетическая нейропатия»- 2-е изд. - М.: «Медицинское агентство», 2011 . -141 с.
- Калинин А.П. «Хирургические заболевания у больных сахарным диабетом». - М.: «Медицина», 1991. - 256 с.
- Маслова О.В. Эпидемиология сахарного диабета и микрососудистых осложнений // Сахарный диабет. - 2011. - №3. - С. 6-11.
- Bаnks A.M., МсGlаmry R.A. / Neuroarthropathy (Charcot joints) in diabetes mellitus // Journal of American Podiatry Medical Association. - 1989. - V. 79. - Р. 110.