В статье преДставлена оценка программированной клеточной гибели при хроническом миелолейкозе на основании морфологического и молекулярно-генетического анализа.
Учитывая клональное происхождение гемобластозов, изучение апоптоза занимает в настоящее время, ведущее место в гематологической практике [1, 2]. Снижение способности к апоптозу играет существенную роль в развитии многих опухолей. Осуществляется последнее с помощью различных механизмов, анализ которых может быть полезен для понимания существующих и поиска новых путей подавления опухолевого роста. Мутация онкогена нередко сопровождается извращением его функции. Типичным примером такого механизма наработки опухолевого клона является хронический миелолейкоз (ХМЛ), при котором транслокация t(9;22) приводит к образованию химерного гена abl/bcr, продуктом которого является онкобелок, обладающий повышенной тирозинкиназной активностью и служащий важным звеном в передаче антиапоптотических сигналов в клетке [3]. Изучение апоптоза у больных с хроническим миелолейкозом в последние годы является весьма актуальным направлением.
Материал и методы: нами было проведено исследование программированной гибели (апоптоза) клеток крови у больных хроническим миелолейкозом (n = 22). В качестве контрольных показателей для оценки результатов лабораторного исследования использовались данные, полученные при обследовании 10 здоровых людей, являющихся донорами крови. Нами был соблюден принцип паракопий, в контрольную группу вошли люди, подобранные в соответствии с изучаемой группой по возрасту, полу.
Апоптоз выявляли с использованием морфологического и молекулярно-генетического анализа.
Для визуализации клеток с признаками апоптоза и оценки его интенсивности мы проводили прижизненное окрашивание акридин-оранжевым красителем цитологических препаратов периферической крови у больных ХМЛ и в группе контроля (доноры). При апоптозе не нарушается целостность ядерной и цитоплазматической мембраны. Апоптоз-специфические фрагменты ДНК через поры ядерной мембраны выходят в цитоплазму на ранних стадиях апоптоза, что можно обнаружить с помощью флуоресцентного метода прижизненной окраски акридин- оранжевым красителем. Акридин-оранжевый краситель специфически связывается с нуклеиновыми кислотами (ДНК и РНК), однако при связывании с ДНК он флуоресцирует в желто-зеленой области спектра, а при связывании с РНК – в оранжево-красной области спектра. Метод морфологического идентифицирования феномена апоптоза является наиболее чувствительным даже при его очень низкой активности.
Результаты исследования и обсуждение. Нами проводился подсчет количества гранулоцитов с морфоструктурными признаками апоптоза при исследовании 20 тыс. лейкоцитов. Затем расчитывали в процентах апоптотический индекс по отношению к живым клеткам. Результаты исследования представлены в таблице 1.
Таблица 1 - Активность апоптоза в периферической крови больных ХМЛ
|
Показатель |
M±m |
Контроль (n = 10) |
Больные ХМЛ M±m |
(n = 22) |
|
Количество |
||||
|
апоптотических клеток |
492,5±11,61 |
120,7±9,98 |
||
|
p<0,001 |
||||
|
на 20 тысяч лейкоцитов |
||||
|
Апоптотический индекс, |
2,5±0,17 |
0,6±0,21 |
||
|
% |
p<0,001 |
Как следует из таблицы 1, уровень спонтанного апоптоза гранулоцитов существенно различался в сравниваемых группах и был снижен у пациентов с ХМЛ. Так, содержание апоптотических гранулоцитов составляло 120,7±9,98 клеток против 492,5±11,61 клеток в группе контроля (p<0,001). Апоптотический индекс в группе лиц, страдающих ХМЛ, был ниже в 4,2 раза, чем в контрольной группе (p<0,001).
Уменьшение явления апоптоза у больных наблюдалось в гранулоцитах разной степени зрелости. В некоторых образцах вообще не наблюдались признаки апоптоза или наблюдались единичные клетки (рисунок 1).
Как видно на рисунке 1, в мазке периферической крови у больного Д., 42 года при обилии лейкоцитов во всех клетках определялись ядро зеленого цвета, а цитоплазма – оранжевого, т.е. клеток с признаками апоптоза не выявлено. В то же время у обследуемых доноров отмечалось присутствие клеток с апоптозом (рисунок 2).
На рисунке 2 просматриваются клетки как без признаков апоптоза, в которых визуализируется ядро в зеленой области спектра, а цитоплазма в красной области спектра, так и апоптотические клетки с зеленым свечением по всему объему клетки.
Известно, что в эволюции болезни в более злокачественную стадию играет не только увеличение массы опухоли, но и снижение чувствительности патологических клеток к сигналам апоптоза [4].
Считается, что апоптоз является общебиологическим механизмом, ответственным за поддержание постоянства численности клеточных популяций. Идентификация морфологических и биохимических маркеров апоптоза должна в перспективе способствовать более глубокому пониманию механизмов патогенеза заболевания, улучшению дифференциальной диагностики и созданию принципиально новых направлений терапии [5].
Нарушение баланса процессов пролиферации и апоптоза в системе крови лежит в основе развития большинства заболеваний, коррекция этого равновесия - основное направление современной патогенетической терапии болезней крови, в том числе онкогенетической патологии [6]
Снижение уровня спонтанного апоптоза при ХМЛ свидетельствует о редком делении опухолевых клеток, их долгой жизнеспособности и преимуществе перед нормальным гемопоэзом [7].
Для более детального исследования процесса апоптоза при хроническом миелолейкозе нами был проведен также следующий анализ - электрофорез ДНК клеток периферической крови в агарозном геле.
В настоящее время гель-электрофорез ДНК также широко используется для регистрации апоптоз-специфической фрагментации ДНК, так как является одним из наиболее наглядных методов.
Для анализа ДНК использовали ЭДТА-обработанные образцы периферической крови. Из замороженных (-20°С) образцов периферической крови в присутствии ЭДТА была выделена тотальная ДНК. Для выявления апоптоз- специфической «лестницы» ДНК мы использовали агарозный гель высокой концентрации (2%), позволяющий разделить фрагменты ДНК, различающиеся на 10-100 нуклеотидов.
Опытную группу составили 14 человек больных ХМЛ, средний возраст которых 50±4,1 лет. В группу контроля вошли здоровые доноры (n=10), средний возраст которых составил 46,4±3,9 лет.
В результате анализа ДНК клеток крови 14 пациентов ХМЛ и 10 лиц контроля было обнаружено, что апоптоз- специфическая фрагментация ДНК в клетках в виде апоптотической «лестницы» имела место в 7 образцах, а именно: в 5 образцах контрольной группы, что составляет 50,0±16,6 %, и была обусловлена, по-видимому,


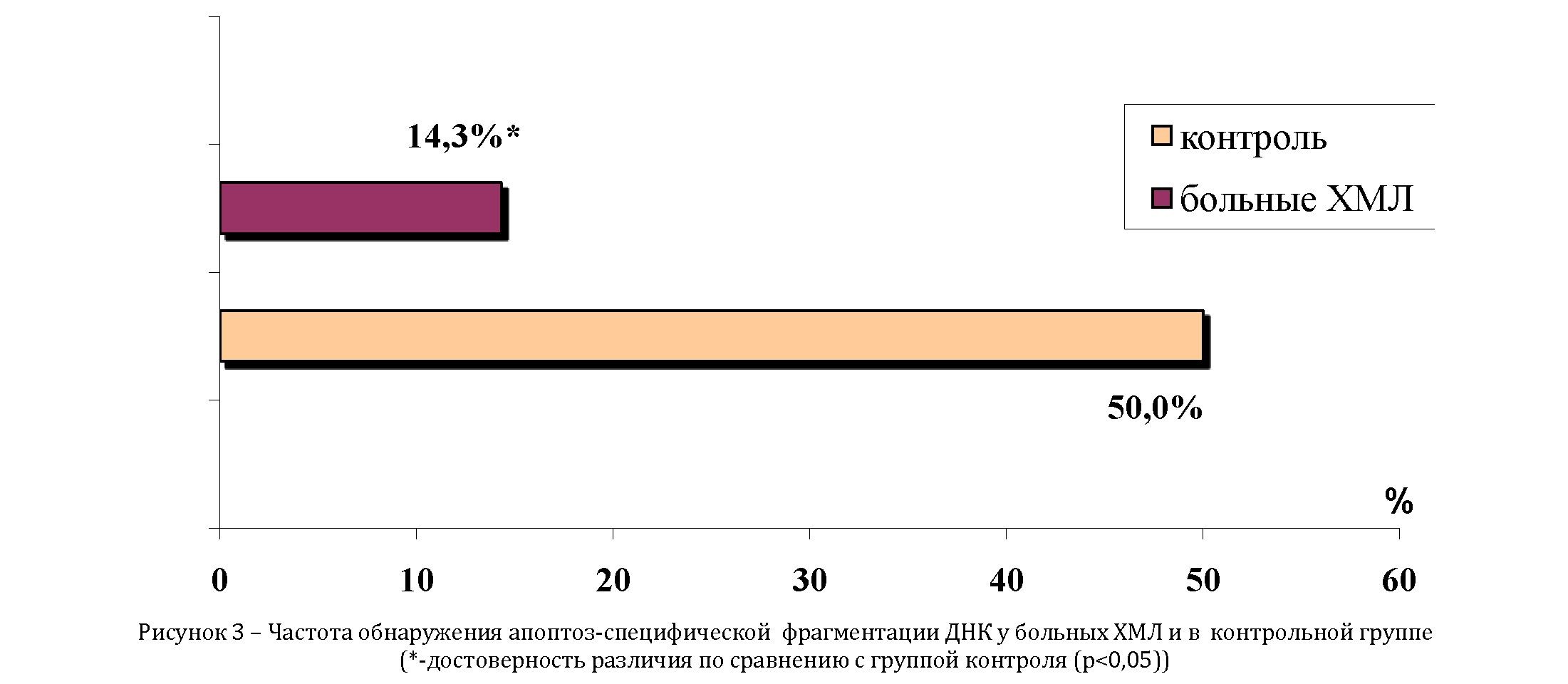
физиологическим апоптозом; в 2 образцах группы лиц с ХМЛ в 14,3±2,6% случаях (рисунок 3).
Во всех других образцах ДНК клеток не была строго фрагментирована. Признаков некротической смерти в исследованных образцах не обнаружено.
При сравнении полученных результатов, следует отразить, что апоптоз-специфическая фрагментация ДНК у больных ХМЛ наблюдалась в 3 раза реже, чем в контроле (p<0,05), что наглядно представлено на рисунке 3.
Очевидно, сниженный уровень апоптоза при ХМЛ по сравнению с таковым у здоровых играет значительную роль в онкогенезе заболевания. Одной из основных характеристик лейкемических клеток является их низкая способность к программированной гибели, а поскольку рост опухоли во многом зависит не только от скорости пролиферации ее клеток, но и от скорости их гибели, можно предположить, что направленная индукция апоптоза в опухолевых клетках может оказаться более эффективным подходом лечения, чем подавление их пролиферации [8,9].
Таким образом, при исследовании апоптоза выявлена низкая активность программируемой клеточной гибели у больных ХМЛ как при морфологическом исследовании, так и при молекулярном. Апоптотический индекс у больных ХМЛ оказался сниженным в 4,2 раза по сравнению с группой контроля. Данное заключение подтверждается молекулярным анализом, при котором апоптоз- специфическая фрагментация ДНК наблюдалась в 3 раза реже у больных ХМЛ, чем в группе здоровых доноров, что подтверждает тезис А.И. Воробьева (2002) о «бессмертии» опухолевой клетки.
СПИСОК ЛИТЕРАТУРЫ
- Mgahon A., Brown D.G., Martin S.J. et al. Fas-mediated in chronic myelogenous leukemia // Cell Death Differ. – 1997. – Vol. 4. – P. 95.
- Петухов В. И. Роль FAS-опосредованного апоптоза в реализации противоопухолевого эффекта альфа-интерферона при хроническом миелолейкозе // Гематология и трансфузиология. - 2000. - № 4. - C. 29-33.
- Барышников А. Ю., Шелепов В. П., Кузнецов С. В. и др. Экспрессия и проявление функциональной активности Fas/APO-1/CD95- антигена, опосредующего апоптоз, при гемобластозах у человека // Гематология и трансфузиология. - 1996. - № 5. - C. 42-44.
- Carlos G.F., Mirjam E., Frank A.E. Apoptosis. Target of Cancer Therapy // Clinical Cancer Research.. - 2002. - Vol. 8. - P. 2024-2034.
- Заботина Т.Н., Соколовская А.А., Кадагидзе З.Г., Барышников А.Ю. Спонтанный и индуцированный апоптоз у больных лимфопролиферативными заболеваниями // Клиническая иммунология. – 2003. - №1. – С. 23-26.
- Козинец Г.И., Макаров В.А. Исследование системы крови в клинической практике. – М.: Триада-Х, 1997 – 480с.
- Michael J. Mauro, Michael W.N. Chronic myeloid leukemia in 2006: a perspective // Нaematologica. - 2006. - Vol.91, №2.- Р.152-158.
- Круглов С.С., Туркина А.Г., Хорошко Н.Д., Абакумов Е.М. и др. Резистентность при терапии гливеком у больных хроническим миелолейкозом в фазе акселерации // Гематология и трансфузиология. – 2007. - №2. - C. 17-24.
- Кузнецов С.В. Новые подходы к лечению хронического миелолейкоза. // Гематология и трансфузиология. – 2007. - №2. - C. 4146.