В последнее время значительное количество исследований посвящено поиску наследственных факторов, предрасполагающих к развитию сосудистых заболеваний мозга. Одно из главных направлений в этих исследованиях - изучение роли генов-кандидатов. В настоящем обзоре нами систематизированы результаты молекулярно-генетических исследований последних лет по изучению связи различных классов «кандидатных генов» с риском развития ишемических инсультов у человека.
В настоящее время достаточно хорошо изучена роль таких факторов риска развития ишемического инсульта, как артериальная гипертензия, атеросклероз, нарушение ритма сердца, инфаркт, курение, сахарный диабет, нарушение липидного обмена, изменения в системе гемостаза, применение оральных контрацептивов, злоупотребление алкоголем и др. [8]. Известно, что тяжесть ишемического инсульта возрастает при сочетании нескольких факторов риска, среди которых значительными являются артериальная гипертензия, гиперхолестеринемия, увеличение уровня липопротеинов низкой плотности, курение. Внедрение в клиническую практику рациональной системы профилактики и лечения артериальной гипертензии, гиполипидемической терапии, эффективной эндартериоэктомии и стентирования брахиоцефальных артерий позволило существенным образом снизить частоту возникновения мозговых катастроф. Вместе с тем данные последних лет показали, что у пациентов с высоким теоретическим индивидуальным риском инсульта фактическая частота его возникновения существенным образом разнится. Все это приводит к обсуждению влияния наследственной предрасположенности и механизмов, лежащих в основе повышения индивидуального риска развития ишемического инсульта [5].
Понятие о генах-кандидатах
Благодаря открытию и внедрению в практику метода полимеразной цепной реакции, развития технологии рекомбинантных ДНК, стало возможным выявление генов- кандидатов, белковые продукты которых могут хотя бы потенциально участвовать в развитии инсульта.
Гены, принимающие участие в развитии ишемического инсульта, подразделены на две категории: 1) увеличивающие риск развития ишемического инсульта, 2) влияющие на сосудистую реактивность, устойчивость ткани мозга к ишемии, размер очага. Эти категории не являются взаимоисключающими. Определение роли конкретного гена в развитии ишемического инсульта является сложной задачей. Это связано с взаимодействием гена с другими факторами риска (артериальная гипертензия, сахарный диабет, повышение уровня фибриногена, нарушение липидного обмена) или модулированием их эффекта, а также с так называемым эффектом генной дозы. Эффект генной дозы - увеличение риска болезни при дефекте определенного гена в совокупности с другими. Часто такие комбинации являются синергическими, увеличивающими риск развития ишемического инсульта. Кроме того, каждому подтипу ишемического инсульта соответствует дефект определенного гена, свои этиология и патогенез. В настоящее время лишь в единичных работах учитывается подтип ишемического инсульта. Наиболее изученной моделью для изучения наследственной предрасположенности в развитии инфаркта мозга является атеротромботический инсульт [6]. Кроме того, риск развития ишемического инсульта увеличивается не только под влиянием полиморфизма с участием одной пары нуклеотидов, но и при сочетании аллелей нескольких генов, т.е. имеет полигенную наследственную предрасположенность.
Имеется множество генов, определенные аллели которых ассоциируются с повышенным риском развития цереброваскулярных заболеваний. Так, широко изучаются полиморфные маркеры, относящиеся к генам системы гемостаза (к генам ФБ, тромбоцитарного гликопротеина, V, VIII и XII факторов свертывания, протромбина, тромбомодулина, генов, белков, участвующих в фибринолизе (tPA, PAI-1), ренин-ангиотензиновой системы, NO-синтетазы, липидов крови и гомоцистеина) [9].
Патогенез тромбообразования у больных ишемическим инсультом
Не вызывает сомнения, что одной из основных причин возникновения ишемических инсультов является тромбоз церебральных артерий: до 50% острых нарушений мозгового кровообращения по ишемическому типу являются тромботическим или эмболическим осложнением атеросклеротического процесса в артериях крупного и среднего калибра. Известно, что процесс тромбообразования зависит от множества факторов: гемодинамических, состояния сосудисто-тромбоцитарного и плазменного компонентов системы гемостаза, стадии развития атеросклеротической бляшки [44]. Р. Вирховым было выделено три фактора, предрасполагающих к развитию тромбозов: 1) нарушение тока крови; 2) повреждение стенки сосуда; 3) изменение реологических свойств крови. Компоненты триады являются лишь относительно самостоятельными и их значимость в патогенезе венозных и артериальных тромбозов неодинакова: ведущие причины развития венозных тромбозов - стаз и дефицит компонентов системы противосвертывания, артериальных - нарушение структуры сосудистой стенки и активация тромбоцитов [2]. Артериальные тромбы состоят в основном из тромбоцитов с небольшим содержанием фибрина и эритроцитов, поэтому их называют «белыми» тромбами в отличие от венозных - «красных» тромбов, состоящих преимущественно из эритроцитов и фибриновых нитей. Различие венозных и артериальных тромбов не является абсолютным. Состав тромба определяется его возрастом. Так, тромбы, обнаруживаемые в церебральных и коронарных артериях при инфарктах, по составу преимущественно «белые».
Нормальное функционирование системы гемостаза обеспечивается сложными взаимодействиями компонентов плазмы, клеток крови и стенки сосудов, которые должны способствовать сохранению жидкого состояния крови в пределах кровеносных сосудов и быстрому тромбированию их поврежденных участков для предотвращения кровоизлияния в ткань. В норме адгезии тромбоцитов к неповрежденному эндотелию не происходит. Это связано с образованием эндотелиальными клетками таких атромбогенных факторов, как простациклин и оксид азота. Основным субстратом образования тромбов является поражение сосудистой стенки атеросклеротическим процессом. Начальные стадии образования атеросклеротической бляшки связаны с накоплением липидов в макрофагах с пролиферацией гладкомышечных клеток и образованием коллагена. Вследствие этих процессов образуется атеросклеротическая бляшка с ядром, в котором содержатся внеклеточные липиды. Ядро заключено в фиброзно-коллагеновую капсулу. Помимо свободного холестерина, в нем содержатся богатые липидами макрофаги, которые разрушаются, и их липидное содержимое увеличивает ядро. При разрывах мелких бляшек тромботические массы проникают внутрь бляшки, происходит стимуляция пролиферации гладкомышечных клеток и дальнейший рост бляшки. Когда она увеличивается настолько, что артерия теряет способность к ремоделированию, возникает гемодинамический стеноз церебральной артерии. Данные механизмы, лежащие в основе развития хронических стенозов, могут приводить к возникновению транзиторных ишемических атак в определенном сосудистом бассейне [3].
Второй возможный вариант развития процесса - быстрое образование тромба на бляшке, которое начинается либо по причине истончения и повреждения эндотелия, покрывающего бляшку, либо вследствие разрыва покрышки бляшки. При этом происходит снижение отрицательного заряда эндотелия и возникновение условий для формирования пристеночных тромбов из агрегатов тромбоцитов и фибрина (рис. 1). Это связано с тем, что активированные в результате контакта с коллагеном поврежденной сосудистой стенки тромбоциты выделяют коллагеназу и эластазу, расщепляющие соответствующие структурные белки, входящие в ее состав. Помимо этого, тромбоциты высвобождают фактор Виллебранда, серотонин, АДФ, продукты превращения арахидоновой кислоты (простагландин PGI 2, тромбоксан А2). Эти биологические активные вещества вызывают вазоспазм, повышение проницаемости эндотелия, отек, усугубляя повреждение стенки сосуда, что в свою очередь усиливает адгезию и агрегацию тромбоцитов с образованием пристеночных тромбов [3].
Разрыв бляшек в местах выраженных стенозов сонных артерий может не сказываться на церебральном кровотоке, так как длительно существующий стеноз в сонной артерии способствует развитию коллатерального кровообращения. С другой стороны, разрыв бляшек, умеренно стенозирующих церебральные артерии, чаще проявляется симптомами острой недостаточности мозгового кровообращения из-за отсутствия развитого коллатерального русла [7].
При возникновении инфаркта мозга большая роль отводится изменениям мозгового и магистрального кровотока артерий головы и шеи с формированием стенозов, окклюзий, патологической извитости. При этом причиной ишемии мозга является ограничение кровотока в атеросклеротически суженных сосудах на фоне временного изменения системного артериального давления под влиянием экстрацеребральных факторов, приводящих к возникновению зон так называемого турбулентного типа кровотока, являющегося одним из условий оседания форменных элементов, в первую очередь тромбоцитов. Это сопровождается повреждением сосудистой стенки, изменением реологических свойств крови, способствуя развитию тромботического ишемического инсульта [1, 10]. Приблизительно у 40% больных развитие инсульта происходит по механизму кардиогенной и артериальной эмболии из распадающихся атером, пристеночных тромбов дуги аорты, магистральных артерий, внутрисердечных тромбов в результате аритмий, эндокардита, ревматизма и др. [4].
Роль фибриногена в тромбообразовании у больных с инфарктом мозга
У больных с ишемической болезнью мозга, в том числе у перенесших ишемический инсульт, имеются изменения тромбоцитарного звена гемостаза. В процессах тромбообразования, в основе которых лежат адгезия и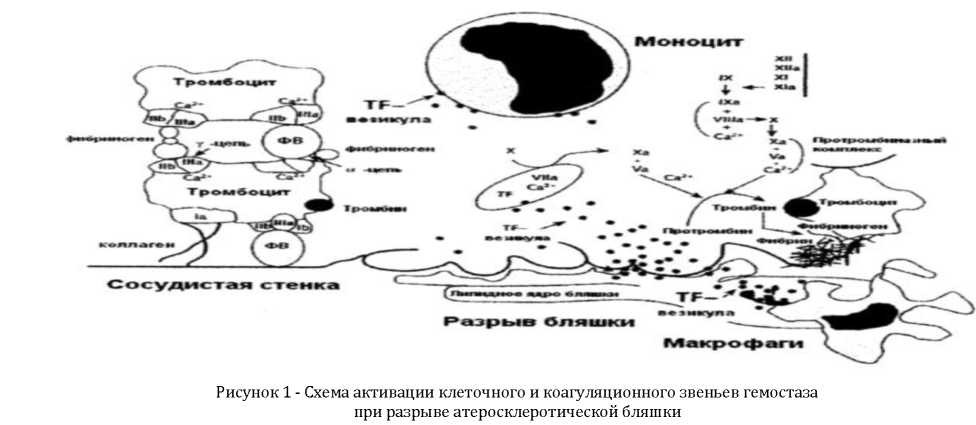
агрегация тромбоцитов, большая роль принадлежит фибриногену (один из факторов свертывания крови, который под действием тромбина превращается в нерастворимый фибрин, составляющий структурную основу тромба). Именно с ним взаимодействуют тромбоциты в области повреждения эндотелия. Фибриноген, иммобилизованный на поверхности эндотелиальных клеток, выполняет роль мостиков, связывающих активированные тромбоциты между собой и с коллагеном субэндотелиальных слоев, взаимодействуя с гликопротеином - специфическим рецептором мембраны тромбоцитов. Известно, что формирование тромбоцитарных агрегатов происходит с помощью этих рецепторова, способных взаимодействовать не только с фибриногеном, но и с фактором Виллебранда, фибронектином и витронектином. Активация GP является ключевым процессом, запускающим агрегацию тромбоцитов. Таким образом, увеличение уровня фибриногена имеет определенное значение в развитии тромботических осложнений.
В международных исследованиях PROCAM (the Prospective Cardiovascular Munster), PRIME (the Prospective Epidemiological Study of Myocardial Infarction), Framingham study, Northwick Park Heart было установлено, что повышение уровня фибриногена увеличивает в несколько раз риск развития инфарктов мозга и сердца. Механизмы, лежащие в основе связи между повышением уровня фибриногена и риском ишемического инсульта, недостаточно ясны. Это может быть обусловлено тем, что фибриноген повышает вязкость крови, агрегацию тромбоцитов и эритроцитов, стимулирует пролиферацию эндотелиальных и гладкомышечных клеток, обеспечивая матрикс для роста клеток, задерживая тромбин, обладающий митогенной активностью. Кроме того, накапливаясь в области атеросклеротической бляшки, фибрин стабилизирует тромбоцитарные агрегаты [11]. Некоторые исследователи рассматривают фибриноген как маркер повреждения эндотелия. Считается, что уровень фибриногена является чувствительным и одним из самых ранних факторов, отражающих повреждение эндотелиальных клеток. Определение его концентрации в сыворотке крови имеет значение для оценки тяжести и распространенности повреждения сосудов. Увеличение уровня фибриногена является прогностически неблагоприятным фактором, ассоциированным с увеличением риска смерти у больных с атеросклеротическим поражением сосудов головного мозга и сердца.
Гены фибриногена находятся на длинном плече 4-й хромосомы. Последовательность каждой из цепей фибриногена кодируется своим геном, однако значительная гомология свидетельствует об их возникновении в результате дупликации одного гена-предшественника.
Фибриноген состоит из трех пар неидентичных полипептидных цепей, обозначаемых α, ß и γ , является симметричной, вытянутой, слегка изогнутой молекулой размером 7x48 нм. N-концевые части всех трех полипептидов образуют центральную область взаимодействия двух половин молекулы фибриногена, которые ковалентно связаны между собой тремя дисульфидными мостиками, далее следует область, в которой все три субъединицы закручены в суперспираль, примерно по середине которой имеется короткая область нарушения регулярности структуры, являющаяся одним из участков специфического расщепления плазмином. За суперспиралью каждая из полипептидных цепей фибриногена образует свою структуру (С-концевые фрагменты) [3, 9]. Пространственная организация С- концевых фрагментов ß- и ү-цепей во многом сходна. Они образуют на концах молекулы фибриногена глобулы, латерально смещенные от оси суперспирали. За счет наличия S-S связи в ß-цепи ее концевая глобула несколько сдвинута к центру молекулы. Глобулярные участки ß- и γ- цепей вместе с дистальной частью суперспирали составляют D-фрагмент фибриногена. Согласно модели J. Weisel и соавт. после спирального участка ɑ-цепи загибаются, и их С-концы взаимодействуют друг с другом вблизи центра молекул. α- и ß-Цепи фибриногена синтезируются как единственные продукты соответствующих генов и состоят из 610 и 461 аминокислотных остатков соответственно. Фибриноген, содержащий удлиненную ү-цепь, менее эффективно взаимодействует с тромбоцитами, снижая их агрегационную активность.
Уровень фибриногена плазмы крови зависит от многих факторов (возраст, пол, низкая физическая активность, артериальная гипертензия, курение, инсулинорезистентность).
Фибриноген является белком острой фазы, его уровень в плазме повышается также при воспалении, инфекциях, травме и стрессе. Регуляция синтеза фибриногена осуществляется на уровне транскрипции. Синтез стимулируется гормонами, жирными кислотами, продуктами деградации фибриногена. Основным механизмом стимулирующего действия является секреция интерлейкина-6 макрофагами и моноцитами в ответ на фагоцитоз продуктов деградации фибриногена.
Курение, вирусные инфекции, воспаление влияют на содержание фибриногена плазмы путем повышения количества лейкоцитов, секреции ими эластазы и интерлейкина-6 - основного стимулятора транскрипции ß- фибриногена в печени. Прекращение курения приводит к некоторому снижению содержания фибриногена, но его уровень все же остается выше, чем у людей, никогда не куривших. Уровень фибриногена плазмы повышается при увеличении уровня глюкозы крови и инсулина. Сильная положительная связь обнаружена между уровнем фибриногена, индексом массы тела и абдоминальным типом ожирения [10]. С возрастом содержание фибриногена также увеличивается. У женщин уровень фибриногена сыворотки крови выше, чем у мужчин, и более заметно его увеличение с возрастом. Прием эстрогенов приводит к снижению фибриногена, с этим хорошо согласуются данные об увеличении уровня в менопаузе. Обнаружена положительная связь фибриногена с липопротеидами низкой плотности и триглицеридами, хотя зависимости между его концентрацией и липидным профилем крови выявлено не было.
Заключение.
Таким образом, все исследования, связанные с изучением генетических факторов риска возникновения инсультов, демонстрирует, что в их развитии задействовано большое число генов, детерминирующих различные звенья патогенеза заболевания. Дальнейшее исследования функций генома, возможно, позволит выявить новые гены предрасположенности к сосудистым заболеваниям мозга.
СПИСОК ЛИТЕРАТУРЫ
- Боголепов Н.К. Церебральные кризы и инсульт. - М: Медицина, 1972. – 392 с.
- Пусев Е.И., Скворцова В.И. Ишемия головного мозга. – М.: Медицина, 2001. – 177 с.
- Панченко Е.П., Добровольский А.Б. Тромбозы в кардиологии // Механизмы развития и возможности терапии. – М.: Спорт и культура, 1999. – С. 55—59.
- Шмидт Е.В., Смирнов В.Е. Вопросы эпидемиологии сосудистых заболеваний головного мозга. – М.: Медицина, 1972. – 392 с.
- Aalto-Setala К., Palomaki Н., Miettinert Н. et al. Genetic risk factors and ischaemic cerebrovascular disease: role of common variation of the genes encoding apolipoproteins and angiotensin-converting enzyme // Ann Med. – 1998. - №30. – Р. 224—233.
- Adams H.P.Jr., Bendixen B.H., Kappelle L.J. et al.Classification of subtype of acute ischemic stroke. Definitions for use in a multicenter clinical trial. TOAST. Trial of Org 10172 in Acute Stroke Treatment // Stroke. – 1993. - №24. – Р. 35—41.
- Bansal В.С., Sood A.K., Bansal C.B. Familial hyperlipidemia in stroke in the young // Stroke. – 1986. - №17. – Р. 1142—1145.
- Balleisen L., Bailey J., Epping P.H. et al. Epidemiology study on factor VII, factor VIII and fibrinogen in an industrial population, I: baseline data on the relation to age, gender, body weight, smoking, alcohol, pill using and menopause // Thromb Haemost. – 1985. - №54. – Р. 721—723.
- Baumann R.E., Henschen A.H. Human fibrinogen polymorphic site analysis by restriction endonuclease digestion and allele-specific polymerase chain reaction amplification: identification of polymorphisms at positions A 312 and В 448 // Blood. – 1993. - №82. – Р. 2117—2124.
- Broderick J., Brott T., Kothari R. et al. The Greater Cincinnati/Northern Kentucky Stroke Study: preliminary first-ever and total incidence rates of stroke among blacks // Stroke. – 1998. - №29. – Р. 415—421.
- Brown E.T., Fuller G.M. Detection of a complex that associates with the b-fibrinogen G-455-A polymorphism // Blood. – 1998. - №92. – Р. 3286—3293.