Исследование показало, что в спектрах ЭПР от печени мышей с имплантами сплава I-BOND 02 содержащий никель, меняются параметры и растет интенсивность сигнала СР. Это согласуется с морфологическими данными о том, что у мышей с вживлением имплантов с содержанием никеля наблюдали видимые признаки болезненных изменений в частности, облысение. Можно принять наличие сигнала СР с параметрами ΔHpp 2,5 Гс компоненты g ~2,0007 в печени мышей как признак патологии или воспалительного процесса.
Полученные экспериментальные данные демонстрируют возможность применение ЭПР для изучения патологических процессов путем анализа изменений выявленных сигналов ЭПР в крови и тканях.
В современной ортопедической стоматологии широко используется протезирование сплавами, в основном, содержащими такие металлы, как кобальт, никель, хром и другие. Длительный контакт с материалом протезов, и не только в ортопедической стоматологии, не всегда остается без последствий для живого организма*1,2+. Влияние их на здоровье человека при возможном проникновении в биологические ткани и жидкости может выражаться в различных патологиях и потому представляет актуальную проблему для современной медицины. Это тем более важно, учитывая постоянное насыщение окружающей человека среды тяжелыми металлами и вредными микроэлементами. При разработке новых стоматологических сплавов большое значение имеет изучение их биосовместимости.
Метод электронного парамагнитного резонанса (ЭПР) основан на явлении поглощения энергии микроволнового, или сверхвысокочастотного (СВЧ) излучения неспаренными электронами, содержащимися в изучаемых биологических объектах *3,4,5+.
Применение электронного парамагнитного резонанса (ЭПР) для решения медицинских задач основано на том, что спектры ЭПР крови или тканей могут содержать информацию о наличии и состоянии отдельных характерных компонент крови, в частности, о наличии разных форм гемоглобиновых комплексов, их метаболизме, содержании ряда свободных радикалов и микроэлементов*6,7,8+. Однако для корректного анализа биообразцов необходимо разработать методику получения спектров ЭПР, а также выявления в них признаков, связанных с наличием или влиянием вредных примесей.
Предметом нашего исследования является - разработка методики для ЭПР - спектроскопического исследования проб биологических тканей подопытных животных с имплантами стоматологических сплавов. Регистрация и обработка спектров биопрепаратов подопытных животных для изучения биосовместимости стоматологических сплавов путем анализа ЭПР - спектров биопроб.
Материалы и методы: для изучения биосовместимости проведен эксперимент на лабораторных животных (мышах, которые находились в стандартных условиях вивария КазНМУ имени С.Д.Асфендиярова), в котором подопытным мышам была проведена имплантация в область шейного отдела позвоночника пластин, изготовленных из сплавов (I-BOND NF, I-BOND 02, IMG, Stomet-1kz, Stomet -2kz) в виде дисков диаметром 5 мм, толщиной 0,6 мм. Импланты оставлялись на длительный срок. По истечении 1,5 месяцев со дня вживления диски были извлечены у части животных и взята первая серия биопроб - крови, печени, костей вблизи импланта, а также челюстные кости и зубы, а через 3 месяца - получена серия проб от оставшихся животных. Образцы крови хранились в замороженном виде, размораживались перед регистрацией, пробы печени и тканей - в формалине.
Разработка алгоритма приготовления проб и получения спектров биологических ЭПР - образцов Метод ЭПР, кроме многочисленных достоинств, - чувствительности, селективности и др., имеет ряд ограничений - дороговизна аппаратуры, требования к квалификации оператора. Но более существенное с точки зрения работ с биопробами - необходимость максимального удаления влаги. В данной работе выбор методики подготовки биообразцов крови и тканей экспериментальных животных определялся как задачей сохранения информации об интересующих компонентах, так и требованиями метода ЭПР к оптимизации условий - снижения диэлектрических потерь из-за присутствии влаги.
Существуют разные способы подготовки биопроб для выделения исследуемых компонент - сушка, лиофилизация или, возможно, замораживание. При работе с биологическими пробами часто используют варианты стабилизации проб путем высушивания на субстратах, добавление «консервантов» и пр.
Для исследования крови и тканей, полученных от лабораторных животных, была специально отработана методика приготовления ЭПР - образцов из нативной, т.е. жидкой крови и печени. Задача для крови была решена оригинальным приемом. В резонаторе спектрометра была скомпонована система крепления образцов, которая влияла на распределение компонент СВЧ - поля. Образцы крови помещали в капиллярные ампулы фирмы Брюкер емкостью 10 мкл диаметром ~0,5 мм таким образом, что проба крови занимала объем в центре по высоте. Количество образца подбирали экспериментально, с контролем массы и высоты. Затем капилляр с образцом крови помещали в измерительную ампулу, которая уже помещалась в диэлектрическую трубку-держатель в резонаторе спектрометре. Таким образом, было снижено влияние диэлектрических потерь мощности на самом образце и реализована достаточная чувствительность спектрометра т.к. магнитная компонента СВЧ - поля концентрирована по оси сферического резонатора.
Образцы печени подопытных мышей, хранившиеся в формалине, помещались на фильтровальную бумагу для удаления остаточной влаги, затем от них отделяли скальпелем пробу для ЭПР - анализа с контролем массы. Размеры проб должны быть достаточны, чтобы считать их представительными, с другой стороны, влажный образец снижает добротность и, следовательно, чувствительность, и затрудняет настройку СВЧ - тракта на резонанс. Потому брались образцы 7-10 мг, которые помещали в тонкостенные кварцевые измерительные ампулы диаметром 3 мм, была отработана методика внесения биопробы в ампулу, взвешивание проводилось перед измерением и после сушки. Измерительные ампулы помещали в диэлектрическую систему крепления в резонаторе.
Опробованы варианты записи спектров высушенных на воздухе срезов печени, прослежена трансформация спектра в ходе сушки. Костные пробы готовили по методике, используемой для приготовления зубной эмали, отделена фракция 0,2-0,8 мм.
Таким же образом методика получения и обработки спектров ЭПР отрабатывалась в процессе проведения работ.
Спектры записывали на спектрометре ESP300E фирмы Брюкер (Германия), частота ~9,7 Ггц, со сферическим резонатором высокой добротности при комнатной температуре.
Отработка методики регистрации спектров ЭПР биологических образцов
Для исследования «нативных» препаратов – жидкой крови и тканей, полученных от лабораторных животных, были выбраны комплекты параметров регистрации..
Вследствие высокой чувствительности аппаратуры к внешним факторам, а также наличия собственных шумов компонентов схемы (СВЧ - детектор, приемник и пр.), примесных сигналов от пустой ампулы, регистрировался и аппаратурно вычитался спектр поглощения без образца – фоновый спектр освобожденной от образца ампулы в резонаторе при идентичных условиях регистрации для каждого набора условий. Было прослежено влияние выдержки при комнатной температуре на вид спектров ЭПР. В работе изучены биообразцы контрольной группы от 5 групп мышей с вживлением имплантов (хромокобальтовые, хромоникелевые сплавы). Это означает, что в случае проникновения ионов металлов в биологические ткани лабораторных животных, могли быть получены сигналы от парамагнитных состояний элементов, входящих в состав изучаемых сплавов. Были испробованы варианты записи спектров исходных (выдержанных в формалине) и высушенных на воздухе срезов печени, прослежена трансформация спектра в ходе сушки.
Подготовка к проведению ЭПР - исследования крови и тканей экспериментальных животных включала также подбор условий регистрации спектров, которые могут существенно отличаться в зависимости от задачи. Проведена работа по выбору комплектов параметров регистрации, удобных и оптимальных для выявления особенностей спектров и признаков влияния имплантов. Записывали спектр в широком диапазоне развертки, достаточном для регистрации всех возможных сигналов. В резонаторе спектрометра ESP300E помещен сопровождающий эталон для контроля поля и интенсивности спектров - оксид магния с ионами двухвалентного марганца в решетке, позволяющий контролировать также колебания чувствительности. В спектрах разных биообразцов важная информация заключена в интервале g-факторов между 3 и 4 компонентами СТС (сверхтонкой структуры) спектра Mn (2+) в MgO. Для регистрации таких компонент, как метгемоглобин, трансферрин и др., прописывали спектр в развертке магнитного поля, соответствующей g- факторам данных компонент. С использованием написанной для этой задачи мини-программы проведены серии автоматической записи спектров с варьированием параметров – мощности СВЧ, амплитуды модуляции.
После проведения рекогносцировочных измерений спектров в разных вариантах развертки магнитного поля и с варьированием условий регистрации были выбраны комплекты параметров.
Таблица 1 - Параметры регистрации спектров биологических образцов, использованные в работе
|
Параметры поля |
СВЧ |
Модуляция 100 kHz |
Временные параметры |
||||
|
Центр поля Fc, G |
Развертка, G |
Мощность СВЧ, мВт |
Частота, GHz |
А мод., G |
К-т усиления |
С (время конверсии) ms |
Постоянная времени синхр. детектора |
|
Для спектров печени |
|||||||
|
В широком диапазоне |
|||||||
|
2428 |
3850 |
2,52 |
9,73 |
3,375 |
2*E+5 |
40,96 |
40,96 |
|
В узком диапазоне. |
|||||||
|
3450 |
96 |
0,5 |
9,73 |
3,375 |
1*E+5 |
20,48 |
40,96 |
|
Для спектров крови |
|||||||
|
В широком диапазоне |
|||||||
|
2428 |
3850 |
2,5 |
9,73 |
3,375 |
2*E+ 5 |
20,48 |
40,96 |
|
2428 |
3850 |
0,31-0,4 |
9,729 |
2,389 |
2*E +5 |
40,96 |
40,96 |
|
В узком диапазоне. |
|||||||
|
3539 |
727 |
2,5 |
0,73 |
2,389 |
2*E +5 |
40,96 |
20,48 |
|
3454 |
120 |
12,6 |
9,73 |
1,939 |
1,25E+5 |
20,48 |
40,96 |
Спектры ЭПР биологических образцов подопытных животных
Для изучения биосовместимости стоматологических ортопедических сплавов по спектрам ЭПР биообразцов, полученных от подопытных мышей с вживленными им имплантами – дисками, изготовленными из таких сплавов, были исследованы образцы крови, печени и костной ткани от 5-ти групп животных.
1 группа- I-ВОÑ⑉ NF, 1-ВОÑ⑉ 02, - IMG без примесей, 2, 3, 4 группы – те же сплавы, с содержанием примеси лома в количестве (10, 20 и 30)% ,
5 группа – животные с имплантами сплавов опытных образцов Stomet-1kz, Stomet -2kz.
Спектры ЭПР биологических образцов записывались, прежде всего, в широком диапазоне развертки магнитного поля. Этот способ регистрации спектра поглощения СВЧ - мощности исследуемым образцом используется на практике, чтобы регистрировать все имеющиеся в образце парамагнитные компоненты, т.е. компоненты, содержащие неспаренные электроны с разным энергетическим состоянием, для которых поглощение квантов СВЧ - излучения данной энергии индуцируется в разных магнитных полях. По техническим причинам более осуществимо и используется в производимой в мире аппаратуре (Германия, США, Россия, Белоруссия, Япония) сканирование не по частоте СВЧ - излучения, а по напряженности магнитного поля. Связь между частотой СВЧ - излучения источника и
напряженностью магнитного поля, при которой наблюдается резонансное ЭПР - поглощение энергии СВЧ - излучения, определяется соотношением, в которое входит величина g-фактора, характеризующая данный тип неспаренных электронов. Эта величина меняется при изменении локальных условий, наличия вблизи других парамагнитных частиц, ядерных спинов и других факторов.
Выбранный нами диапазон развертки магнитного поля в единицах g-фактора включает весь спектр возможных сигналов - от проявлений линий поглощения форм гемоглобина и трансферрина до интервала, где проявляются признаки присутствия в образце свободных радикалов – клеточных компонент, церулоплазмина, возможные парамагнитные комплексы ионов металлов, а также линии спектра сопровождающего эталона.
Для извлечения и анализа содержащейся в спектрах ЭПР информации необходима детализация, выбор интересующих «объектов», подбор условий и регистрация отдельных участков спектра, а затем анализ их особенностей, что и было сделано в процессе работы для всех изученных образцов.
Спектры ЭПР образцов печени в широкой развертке магнитного поля позволяют на основе имеющихся в них особенностей выбрать нужные интервалы для более детальной записи при выбранных условиях и сравнения разных образцов.
Спектр на рисунке 1 приведен со шкалой в единицах g- факторов, содержит довольно интенсивную асимметричную линию с g-фактором ~2,2÷2.36, на фоне которой можно наблюдать ряд сигналов.
Асимметричная линия, которая показана на рисунке стрелкой, вероятно, связана с парамагнитными комплексами железа, а также содержит вклад от линий поглощения низкоспиновых форм гемоглобина и церулоплазмина. Метод ЭПР является эффективным методом для изучения парамагнитных частиц, присутствующих в биологических системах. К парамагнитным частицам, имеющим важное биологическое значение, относятся два основных типа соединений - это свободные радикалы и металлы переменной валентности (Fe, Cu, Mn и др.) или их комплексы.
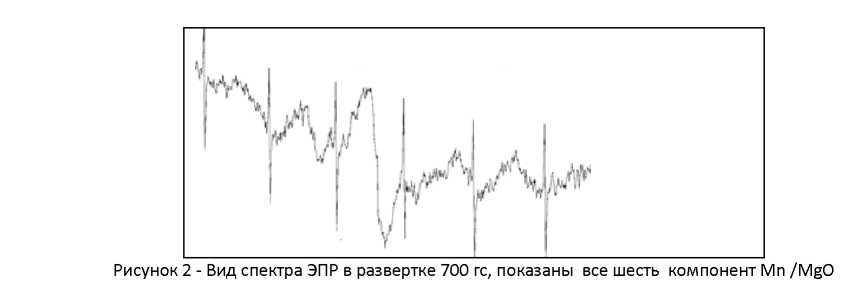
В области значений g-фактора ~ (1,9 - 2,2) наблюдается сверхтонкая структура (СТС) из 6-ти компонент иона двухвалентного марганца в оксиде магния, эталонного образца поля и концентрации. Эта СТС показана 2-мя вогнутыми линиями.
При записи спектра с эталоном Mn(2+)/MgO в интервале между 3 и 4 линиями СТС регистрируются относительно узкие сигналы свободных радикалов (СР), требующие подбора особых параметров регистрации. На рисунке 2 приведен спектр в развертке ~700 гс.
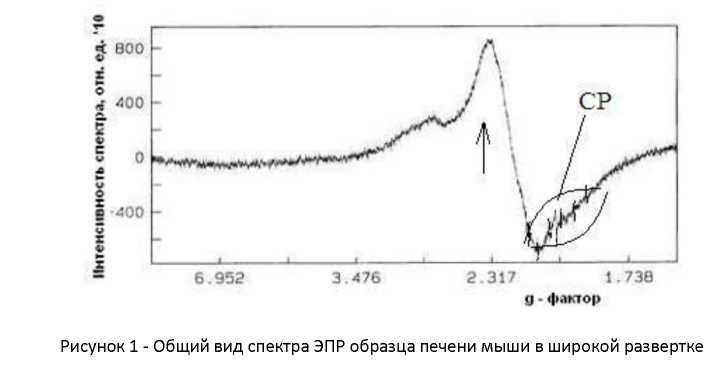
Для выделения этих и других ЭПР - сигналов и определения их параметров проведены регистрации спектров исследуемых образцов в разных диапазонах и операции вычитания из них фоновых спектров ЭПР резонатора с пустой измерительной ампулой, записанных в соответствующих диапазонах и при идентичных условиях.
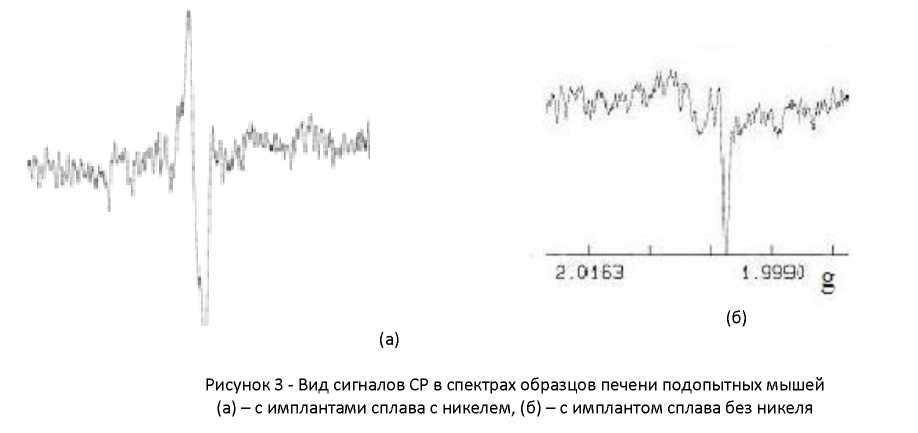
В результате получены различные сигналы ЭПР (g~ 2,00), два типа из которых показаны внизу на рисунке 3а и б.
Полученные ЭПР - сигналы были близки по форме для спектров, записанных от образцов печени мышей с имплантами импортных сплавов (сигнал 1 на рисунке. 4, g-фактор ~ 2,001). Сигналы отличались по параметрам (g-фактор, ширина и форма линии, интенсивность) от сигналов ЭПР для мышей 5-й группы, которым были вживлены диски из отечественных сплавов. Интенсивность сигналов от свободных радикалов в 5-й группе также была ниже, особенно интенсивные сигналы ЭПР получены для 1-й и 2-й групп. Введение добавок лома более 10 % не оказывает влияния на вид и интенсивность спектров ЭПР.
1 группа -- I-BOND NF, I-BOND 02, IMG, без добавок. Наложение двух типов ЭПР-сигналов
g ~2,0005, ширина ΔHpp 0,015 Гс, он преобладает в 1 сплаве,
2, 3 и 4 группа - I-BOND NF, I-BOND 02, IMG, с добавками 10, 20 и 30% лома.
ЭПР-сигналы g ~2,0005, ширина ΔHpp 0,02 Гс, более широкой ΔHpp 2,5 Гс компоненты g ~2,0007.
5 группа
ЭПР- сигнал g ~2,0005, ширина ΔHpp 0,015 Гс.
Обсуждение результатов:
При оценке концентрации парамагнитных центров (ПМЦ) амплитуды сигналов нормировали во всех случаях на массу и выбранные одинаковые условия регистрации. Но необходимо учитывать, что в спектрах ЭПР определяются не абсолютные интенсивности.
По литературным данным, подобный сигнал наблюдали как в крови, так и в тканях подопытных животных и человека, и приписали его наложению двух сигналов от динитрозильных комплексов железа в ромбической и аксиальной симметрии. Сигнал ЭПР в ромбической симметрии появляется от железа в комплексе с альбумином. В других случаях можно наблюдать железо, связанное в аксиальной симметрии.
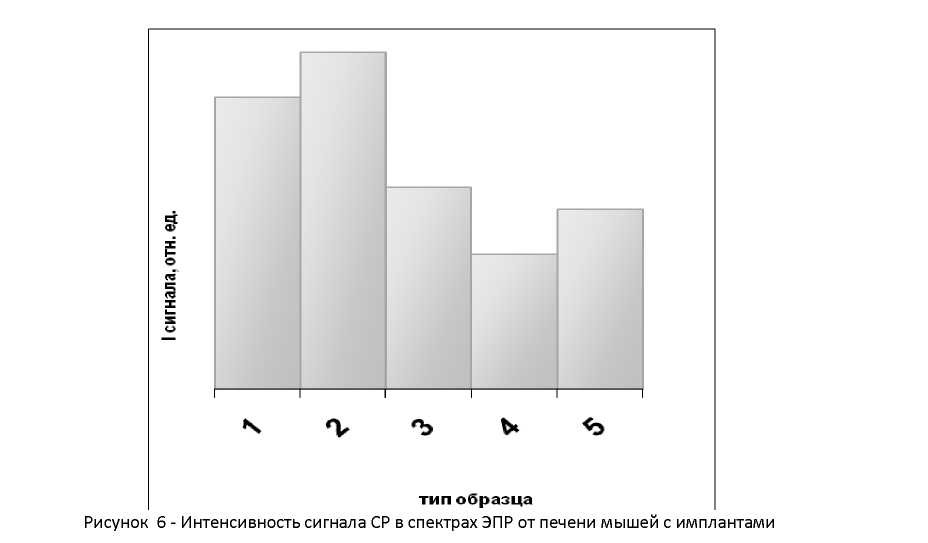
В спектрах печени мышей с имплантами сплавов 1 и 2 наблюдали сигналы, по форме представляющие наложение двух типов сигналов разной ширины. Параметры более узкой компоненты g ~2,0005, ширина ΔHpp 0,015 Гс, она преобладает в 1 сплаве, сигнал более широкой ΔHpp 2,5 Гс компоненты g ~2,0007 наблюдался в спектре для группы 2.
Для сравнения на рисунке 6 показаны изменения спектров динитрозильных комплексов железа (g 2.03) и трансферрина (g 4.3) в крови. В спектрах печени мышей с вживленными имплантами сплавов наблюдали лишь слабые сигналы трансферрина.
В спектре печени мышей из группы с вживленными имплантами сплавов Stomet-1kz, Stomet -2kz выделен только узкий анизотропный сигнал (g=2,00045, ΔHpp 0,02Гс), рисунок 4.б, по по форме и параметрам его можно отнести радикалам окисленной аскорбиновой кислоты в семихинонной форме, наблюдаемым в ЭПР.
Полуколичественные сравнения сигналов показали, что для случая никель-хромового импланта сигнал с преобладанием более широкой ΔHpp 2,5 Гс компоненты g
~2,0007 был и по интенсивности значительно больше, до 30%, чем для сплава 3 и почти вдвое больше, чем сигнал в спектрах образцов печени с имплантами Stomet-1kz,
Stomet -2kz.


I-ВОÑ⑉ 02
I-ВОÑ⑉ NF,
IMG,
Stomet-1kz,
Stomet -2kz.
Таким образом, в спектрах ЭПР от печени мышей с имплантами сплава 1-ВОÑ⑉ 02 меняются параметры и растет интенсивность сигнала СР. Это согласуется и с морфологическими данными о том, что у мышей с
Спектры ЭПР образцов крови подопытных животных Проведено изучение влияния ортопедических сплавов по спектрам ЭПР биообразцов, полученных от групп подопытных мышей с имплантами 5 сплавов:
1 группа - 1-ВОÑ⑉ NF, 1-ВОÑ⑉ 02, - IMG, 2-, 3, 4- те же сплавы, с добавкой лома 10, 20 и 30 % , 5 – без добавок сплавы Stomet-1kz, Stomet -2kz.
Как и для печени, спектры ЭПР - образцов крови подопытных животных записывались сначала в широком
вживлением имплантов с содержанием никеля наблюдали видимые признаки болезненных изменений, в частности, облысение. Можно принять наличие сигнала СР с параметрами ΔHpp 2,5 Гс и g ~2,0007 в печени мышей как признак патологии и / или воспалительного процесса.
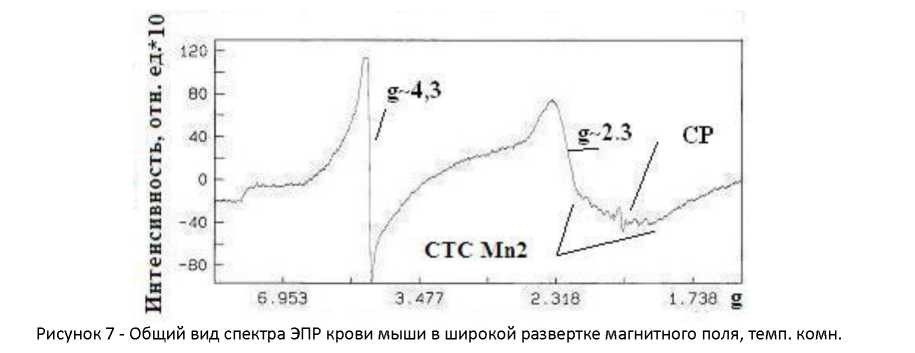
диапазоне изменения магнитного поля, что позволило получить развернутую картину. Спектр образцов крови подопытных мышей в широкой развертке показан на рисунке 7.
В спектрах крови животных регистрируется наличие большего числа информативных признаков. Затем все спектры прописаны в более узких диапазонах развертки магнитного поля и при соответствующих условиях регистрации.
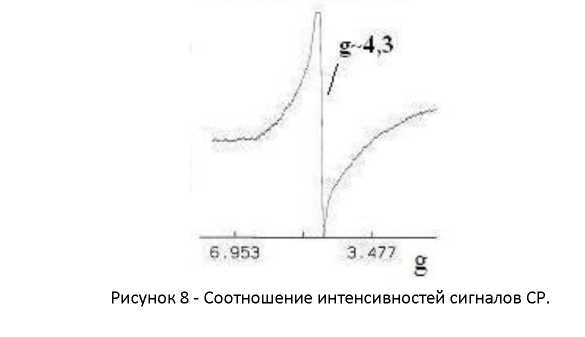
Гемоглобин, миоглобин и цитохромы характеризуются сравнительно широким сигналом ЭПР в диапазоне значений g-фактора 2.07-1.98 и, как правило, триплетной сверхтонкой структурой при g = 2.01 (у нас 2,013). эти сигналы регистрируются и в полученных спектрах ЭПР мышей с Co-, Ni- имплантами. В крови мышей группы с имплантами сплавов предложенного Казахстанскими учеными состава также наблюдался подобный сигнал (g=2,0015), шириной ΔHpp 21 Гс, однако в значительно более низкой концентрации, соотношение интенсивностей сигналов СР показано на рисунке 8.
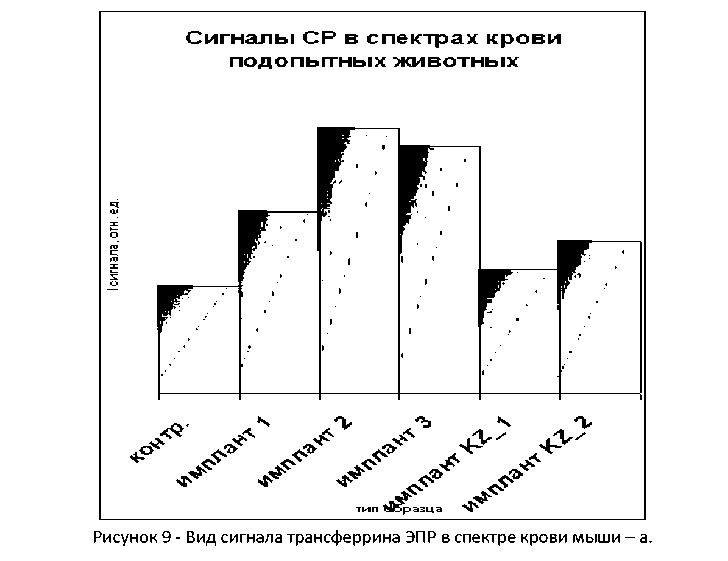
Интенсивность сигналов СР в спектрах образцов крови от мышей с имплантами - б.
Спектры крови изученных экземпляров подопытных мышей содержат интенсивный анизотропный сигнал трансферрина - этот (Fe3+) железо-транспортный белок, регулятор пероксидного окисления липидов, - дает широкую линию gɪ =4.3, g∣∣ = 9.3 *5+, рисунок .
Железо (3+) в гемовой структуре метгемоглобина проявляется сигналами в высокоспиновой области, g~6.00. в записанных спектрах крови мышей есть довольно слабое поглощение в этой области (рисунок 10), а также при более высоком значении g - фактора.
Метгемоглобин ^etHb) - ферридезоксигемоглобин в высокоспиновом состоянии *9+.образуется в самих эритроцитах в ходе следующей реакции:
Hb (Fe++) O2 + NO = Hb(Fe+++) + NO3
Поэтому было задумано исследовать сам NO, метгемоглобин и церулоплазмин. Именно вместе эти маркеры могут свидетельствовать и об оксидативном стрессе и о воспалении (церулоплазмин).
Система оксида азота (NO) у человека обладает широким спектром биорегуляторного действия *13+. Сейчас трудно назвать функцию организма, в регуляции которой NO не принимал бы участия. Он является уникальным медиатором межклеточного взаимодействия, участвующим в поддержке гомеостатических параметров организма в формировании базального тонуса сосудов, улучшения реологических свойств крови путем регуляции процессов агрегации ее форменных элементов, стабилизации проницаемости сосудистой стенки, обладает свободнорадикальными свойствами * 10+. Благодаря малым размерам и отсутствию заряда NO легко преодолевает клеточные мембраны органов и тканей организма NO - короткоживущая молекула, время полужизни которой не превышает 10 секунд, после чего она преобразуется в нитриты *11+.
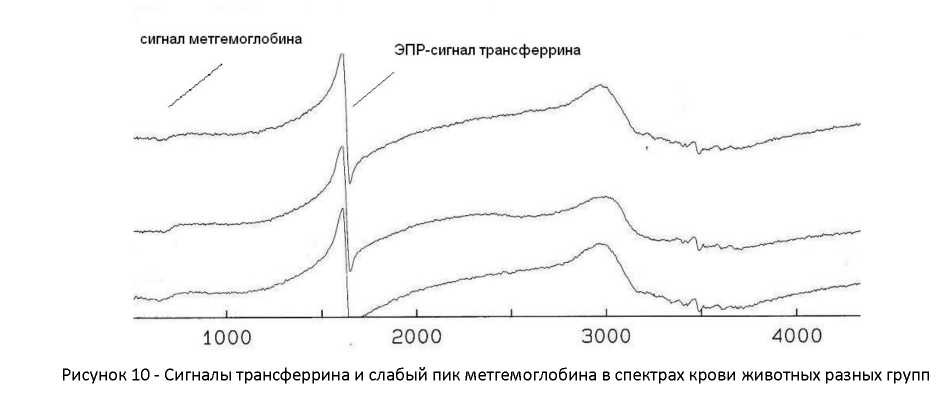
Превышение концентрации метгемоглобина до 5- 15% (а в последние годы отмечается и до 20-30 % от общего уровня гемоглобина крови) отражает патологические проявления, в частности, изменения функций ЦНС, инактивации некоторых ферментов и т.д. и инициирует различные патологические состояния в организме человека. В проведенных исследованиях не обнаружено существенных различий в содержании метгемоглобина и церулоплазмина в тканях мышей под воздействием испытанных имплантантов по сравнению с контрольными животными, поэтому эти данные в работе не анализируются.
В области (g -фактора) g ~ 2.03 в изученных пробах наблюдался сигнал с боковыми компонентами, сходный с сигналом динитрозильных комплексов негемового железа Fe-(NO)2, который имеет триплетную структуру. Прямой количественный метод электроннопарамагнитного резонанса (ЭПР) позволяет определить в тканях скорость генерации NO по включению в комплексы с двухвалентным железом и диэтилдитиокарбаматом (ДЭТК) и дальнейшим образованием парамагнитных мононитрозильных комплексов железа (МНКЖ) с ДЭТК *12+.
Можно предположить, что при контакте с вживленными имплантами характерны как проявления нитрозильных комплексов, так и оксидных форм гемоглобина (гидроксикомплексы железа), что сказывается в наличии налагающихся максимумов поглощения в данной области g - факторов. Аналогичные сигналы дают гемихромы - низкоспиновые формы метгемоглобина (g ~ 1,8 - 3,0) в ромбической симметрии.
В образцах тканей животных с носительством имплантантов в течение 3 месяцев характер полученных результатов, в общем, повторял аналогичные проявления, описанные выше (1,5 - месячные эксперименты). Мы считаем, что данное обстоятельство связано с адаптацией мышей к имплантантам за столь длительный период.
Для развития начатых исследований в направлении изучения перечисленных объектов предполагается более эффективно разделить сигналы разных спин-систем и идентифицировать детально полученные ЭПР - сигналы. Таким образом, наличие значительных количеств никеля в ортопедических сплавах можно считать нежелательным. Полученные экспериментальные данные демонстрируют возможность применения ЭПР для изучения патологических процессов путем анализа изменений выявленных сигналов ЭПР в крови и тканях.
Список литературы
- Гожая Л.Д. Аллергические заболевания в ортопедической стоматологии. - М.: Медицина,1988. - С.44-45.
- Алтынбеков К.Д. Выбор конструкционных протезных материала согласно регистрации реакции организма и тканей полости рта.//Проблемы стоматологии. - 2000. - №2. - С.42-45.
- Аленчева Н.И., Лакомова Ф.Ф., Лакомов Е.И. и др. Биологические аспекты применения электронного парамагнитного резонанса.//Вестник новых медицинских технологий. - 1998. - Т.5. - №3-4. - С.93-97.
- Максина А.Г., Дайняк Б.А. Использование метода спиновых меток и зондов в медицинских исследованиях.//Медтехника. - 1991. - №6. - С.17-18.
- Резникова И.И., Максина А.Г., Дайняк Б.А. и др. Использование ЭПР- спектроскопи для решения актуальных медицинских задач.//Медтехника. - 1992. - №6. - С.43-44.
- Тимошин А.А., Орлов П.Р., Ванин А.Р. и др. Динитрозильные комплексы железа- новый тип гипотензивных препаратов.//Жур.Рос.Хим.Общества им. Д.И.Менделеева. - 2007. - Т .51. - №1. - С.88-92.
- Изюмов Д.С., Домнина Л.В., Непряхина О.К. и др. Митохондрии как источники активных форм кислорода при окислительном стрессе. Исследование с помощью новых митохондриально - направленных анти-оксидантов на основе «ионов Скулачева».//Биохимия. - 2010. - Т.75. - В. 2. - С.149-157.
- Кадыржанов К.К., Надиров Б.Н., Пивоваров С.П. и др. Начальный опыт применения ЭПР для медицинской диагностики в Казахстане и перспективы дальнейшего развития. Тезисы 4-й Межд. Конфер. «Ядерная и радиационная физика». - Алма- Ата: 2013. - С. 472-473.
- Ванин А.Ф. Оксид азота в биологии: история, состояние и перспективы исследований. Биохимия. - 1998. - Вып. 7. - С. 867869.
- Ванин А.Ф. Оксид азота в биомедицинских исследованиях // Вестник. Рос. АМН. - 2000. - №4. - С. 3-5.
- Лев Н.С. Патогенетическая роль оксида азота при бронхиальной астме // Рос. вестн. перинатол. педиатр. -2000. - № 4. - С. 48 - 51.
- Раевский К.С., Башкатова В.Г., Вицкова Г.Ю. и др. Судороги, вызываемые введением N-метил-⑉, L-аспартата, сопровождающиеся усилением генерации оксида азота и процесс-сов перекисного окисления липидов в мозге крыс // Экспер. клин. фармакол. - 1998. - Т. 61. - № 1. - С. 13 - 16.
- Moncada S., Palmer R.M.J., Higgs E.A. Nitric oxide: physiology, pathophysiology and pharmacology // Pharmacol.Rev. - 1991. - Vol. 43. - № 1. - P. 109 - 142.