АННОТАЦИЯ
Выполнен обзор литературных источников, опубликованных в международных научных изданиях. Приведены данные по эффективности и переносимости альфаферона при хроническом гепатите В и С.
До настоящего времени проблема терапии хронической HBVи HCV-инфеĸций является окончательно неразрешенной и чрезвычайно актуальной. В связи с этим в современной гепатологии широко применяют новые подходы, принципы и способы лечения больных хроническим вирусным гепатитом (ХВГ). Основные средства терапии ХВГ интерфероны (INF) [1, 2], которые тормозят репликацию вирусов гепатита BnC (HBV, HCV). Интерфероны являются цитокинами, а по химической структуре гликопротеинами, и обладают противовирусными, иммуномодулирующими и антипролиферативными свойствами. Существуют 2 главных типа интерферонов:
- • I тип это -ɑ, -ß, -ω и -τ, которые продуцируются моноцитами, макрофагами, лимфоцитами-0, а также фибробластами. Они оказывают преимущественно противовирусное действие благодаря блокированию синтеза нуклеиновых кислот вирусов, снижению их онкогенных свойств, увеличению иммуноцитотоксичной активности, направленной на пораженные вирусом гепатоциты, а также уменьшению фибринообразования.
- • II тип это INF-γ, продуцируемые активными Т-лимфоцитами, которые обладают выраженными иммуномодулирующими свойствами при незначительной противовирусной активности.
Для противовирусной терапии инфицированных вирусом гепатита C используют преимущественно INF-α. Нативныйì NF-Otnl (Wellferon(W) один из первых интерферонов, который был применён для лечения вирусной инфекции.
Более совершенной формой лейкоцитарного интерферона является LeINF-otn3 (Alfaferon®, AlfaWassermann), получаемый из лейкоцитов здоровых доноров, состоящий из 18 подтипов человеческого INF-Ot 2а, 2Ьи 2сс молекулярной массой 17-27 kDa. Их процентное соотношение аналогично природному. Соответствие интерферонов, которые входят в состав альфаферона, интерферонам, синтезированным клетками в физиологических условиях, составляет 75-85 %. Le-INF-otn3 метаболизируется преимущественно в клетках-мишенях, лишь незначительное его количество выводится почками. Поскольку период полувыведения препарата составляет 18-36 ч, его назначают каждые 48 ч [3]. Особенностью Le-INF-otn3 является отсутствие образования антител к интерферонам, в том числе нейтрализующих.
При ХВГ-C противовирусная эффективность пегилированных форм альфа-интерферона (реĝINF) в сочетании с рибавирином составляет 40-60 %. Пегилированные интерфероны состоят из частиц рекомбинантного INF-Ot и молекул полиэтиленгликоля, который обеспечиваетподдержание высокой концентрации препарата в крови в течение нескольких суток, что позволяет применять препарат 1 раз в неделю.
Однако в терапии ХВГ-С остается много спорных позиций, связанных как с недостаточной эффективностью терапии peg-INF, так и с высокой частотой побочных эффектов peg-INF, что требует преждевременной отмены препарата. У некоторых категорий пациентов большая длительность действия peg-INF является скорее недостатком, чем преимуществом. К таким категориям относятся пациенты, находящиеся на гемодиализе, пациенты с гемофилией, пациенты с циррозом печени, пациенты с высоким риском прогнозированной лейкопении и тромбоцитопении в процессе предстоящего лечения. Установлено, что противовирусная эффективность INF-Ot Зп сопоставима с эффективностью остальных интерферонов, но имеет лучший профиль безопасности. На сегодняшний день проведено более 500 клинических исследований применения альфаферона в лечении ХВГ-С, в том числе одна треть из них при комбинированном применении с рибавирином. Данные, опубликованные в международных научных изданиях, свидетельствуют о том, что Le-INF-Ot обладает лучшим профилем безопасности по сравнению с другими рекомбинантными ɑ-интерферонами (rINF-α). Эффективность и переносимость терапии с применением альфаферона в сочетании с рибавирином изучена:
- у первичных пациентов с HCV,
- у пациентов с рецидивами после завершения лечения другим INF-α,
- у пациентов, не ответивших на предыдущий курс лечения другим INF-α.
В этих исследованиях выявлен лучший устойчивый вирусологический ответ (УВО) при комбинации альфаферон + рибавирин у первичных пациентов по сравнению с rINF-α (47 и 33 % соответственно) при длительности курса лечения 24 недели. Продемонстрирована четкая взаимосвязь между УВО и генотипом HCV Альфаферон более эффективен при HCV генотипа 2 и 3 10-25 % в монотерапии и 4181 % при применении комбинации альфаферон+рибавирин по сравнению с 8 % в монотерапии и 36-42 % в комбинированной терапии при HCV 1 генотипа. При естественном течении HCV-инфеĸции риск перехода острой фазы в хроническую составляет 50-84 % больных [4].
Nomura et al. [5] получили стойкий вирусологический ответ (CBO) на лечение INF-otn3 в 87 % больных острым вирусным гепатитом С. При этом не было зафиксировано необходимости в отмене терапии или снижении дозы препарата. D. М. Simon et al. [6] одними из первых провели многоцентровое исследование по оценке противовирусной эффективности и побочных эффектов INF-αn3 у больных ХГС. Из обследованных 57 % были заражены генотипом lHCV-инфеĸции, остальные генотипами 2 и 3. Недельная доза INF-αn3 составляла 30 млн. МО. Через 48 недель терапии CBO был достигнут у 24 % пациентов.
Т. Lapinsky et al., М. Dibovska, R. Flysyak [7] оценивали эффективность, переносимость, частоту побочных действий альфаферона у 24 больных (8 женщин и 16 мужчин, средний возраст 47 лет), инфицированных вирусом С, которым не было показано лечение пегилированными интерферонами.
Противопоказаниями к применению пегилированных интерферонов были:
- цирроз печени со значительной тромбоцитопенией (11 чел.);
- состояние после перенесенного ишемического инсульта с развитием гемипареза (1 чел.);
- лейкопения (3 чел.);
- предыдущая непереносимость пегилированного интерферона INF-Ot (9 чел.).
Инфицирование генотипами 1, 3, 4 HCV-инфеĸции подтверждено соответственно у 16 (66,5 %), 3 (12,5 %) и 5 (21 %) больных. Лечение пациентов проводили INF-Ot Зп (Alfaferone®, AlfaWasseimann) в дозе 9 млн. МО/неделя (в 3 приёма), а также рибавирином (Meduna®, AlfaWassermann) в дозе 8001200 мг/сут. в зависимости от массы тела. Терапия проводилась на протяжении 6 мес. независимо от генотипа, а при печеночной недостаточности на протяжении 12 мес. Оценку эффективности проводили через 24 недели после завершения лечения. В процессе лечения альфафероном у всех больных наблюдалось уменьшение активности аланинаминотрансферазы (АЛТ). CBO получен у 7 из 24 больных (29 %). У остальных отмечено снижение виремии в среднем от 1,5 х IO6 (÷2,5 х IO6) до 2,6 X IO3 (±6,1 X IO3) МО/мл. CBO отмечен у 4 больных (17 %) генотипом 1. Среди 11 пациентов с циррозом печени элиминация HCVRNA подтверждена в 2-х случаях (18 %). У остальных средняя виремия уменьшилась от 3,9 х IO5 (±8,9 X IO5) до 4,1 х IO3 (±8,9 х IO3) МО/мл. Ни в одном случае не возникла необходимость в досрочном прекращении лечения или в уменьшении дозы препарата. В течение первых 4 недель лечения INF-α Зп у 50 % пациентов наблюдался гриппоподобный синдром. В дальнейшем он развился у 8 % больных. Не было выявлено изменений в месте инъекций, отсутствовали симптомы депрессии. Так, лишь у 13 % пациентов подтверждена эмоциональная лабильность. Наименьшее количество нейтрофилов, выявленное у больных с циррозом печени в начале терапии INF-Ot Зп, составляло 960/мĸл, тромбоцитов 66000/мĸл. Перед лечением среднее количество лейкоцитов, нейтрофилов и тромбоцитов в крови больных циррозом печени было более низким в сравнении с больными гепатитом C без цирроза. Через 6 мес. Лечения количество лейкоцитов, нейтрофилов и тромбоцитов изменилось несущественно, а их снижение у больных циррозом печени было меньшим, чем у больных без цирроза.
В исследованиях D. Dibovska, W. Halota установлены меньшая частота и тяжесть побочных действий при лечении альфафероном в сравнении с другими препаратами интерферона [8].
В период 2002-2005 гг. наблюдались 25 пациентов (6 женщин, 8 мужчин, средний возраст 38 лет; 11 детей в возрасте 9-17 лет, средний возраст 12,5 лет), инфицированных HBV и/или HCV Альфаферон назначался по 3 MO 3 раза в неделю. Лечение применено 2-м больным с острым вирусным гепатитом C в течение 24 недель. У 11 больных ХГС применена терапия, комбинированная с рибавирином, который дозировали в зависимости от массы тела. Лечение длилось в зависимости от терапевтического эффекта 12-48 недель. Из пролеченных альфафероном 10 пациентов, имевших хроническую HBV-инфеĸцию, получали препарат в дозе 6 MO 3 раза в неделю в течение 24 недель. Лечение человеческим интерфероном по 3 MO 3 раза в неделю и рибавирином проведено 2-м больным с коинфекцией HBV±HCV. Лечение длилось 48 недель. В 6 случаях выбор человеческого интерферона был обусловлен предыдущей неэффективной терапией. В эту группу входили 4 пациента с ХГС и 2 пациента с ХГВ. Больным, зараженным HCV-инфеĸцией, предварительно применяли рекомбинантный интерферон, а у инфицированных HBV ламивудин. В 3-х случаях в процессе лечения вследствие плохой переносимости рекомбинантный интерферон был заменён альфафероном, что позволило завершить терапию. В эту группу входил 1 пациент с ХГС и 2 инфицированных HBV±HCV. В 16 случаях этиологическое лечение применено впервые. Альфаферон хорошо переносился. Среди побочных действий чаще наблюдали гриппоподобные реакции (9 больных) и расстройства психики (8 случаев) в виде чрезвычайной раздражительности, депрессии, агрессии и бессонницы. У 2-х пациентов эти расстройства стали причиной прерывания лечения. Выявленные до лечения лейкопения и тромбоцитопения существенно не изменились в процессе терапии альфафероном, и не возникло необходимости в прерывании лечения. Количество тромбоцитов в крови менее 50 тыс. в 1 мл не было противопоказанием к применению лейкоцитарного интерферона. Из 2-х пациентов с острым вирусным гепатитом C у одного была достигнута эрадикация HCV, у другого лечение было прервано из-за появления побочного действия. В группе больных ХГС у 5 из 11 пациентов достигнут CBO, в том числе у 2-х пациентов, которые ранее без эффекта лечились рекомбинантным интерфероном, а также у пациента, которому в процессе лечения проведена замена рекомбинантного интерферона на альфаферон в связи с побочными реакциями на предыдущий интерферон. Несколько ниже оказалась эффективность лечения у больных ХГВ и ХГВ±ХГС. У 1-го пациента с ХГВ произошла сероконверсия HbeAg∕antiHbe, а также получен отрицательный результат на наличие HBVDNA, у 2-х HbeAg отрицательных пациентов достигнут CBO. У остальных больных была применена другая методика лечения (рекомбинантный интерферон и ламивудин) без существенного эффекта. Однако ни у одного из двух больных, инфицированных HBV±HCV, не удалось достичь терапевтического эффекта.
В лечении ХВГ, как и других заболеваний, именно первичная терапия является наиболее эффективной. В то время как эффект от последующих курсов противовирусного лечения, как правило, худший. Неэффективность терапии у больных ХВГ способствует развитию циррозапечени, каждый год персистенции HBV и HCV увеличивает риск печеночной недостаточности или развития первичного рака печени.
L. Benvegnu et al. [9] в ходе 7,5-летнего наблюдения больных циррозом печени вирусной этиологии подтвердили развитие печеночной недостаточности у 35 % инфицированных вирусом гепатита В, у 31 % вирусом гепатита C и у 53 % вирусом гепатита В и C [9]. У 26 % инфицированных пациентов развился рак печени. Эти результаты являются обоснованием для необходимости проведения противовирусной терапии всем больным ХГВ и ХГС, в том числе и лицам с компенсированным циррозом печени вирусного происхождения.
D. Kozielewicz et al. [10] исследовались 23 пациента (15 женщин и 8 мужчин) в возрасте 17-68 лет (средний возраст 52 года) в 20032008 гг. с целью оценки эффективности и безопасности применения натурального лейкоцитарного интерферона альфа (альфаферона) в комбинации с рибавирином у больных с циррозом печени, связанным с ВГС. При этом 17 пациентов относились к классу А по тяжести печеночной недостаточности согласно классификации Чайлд-Пью, 6 пациентов к классу В. У 17 пациентов определялся генотип Ib, у 6 генотип 3aHCV, 13 пациентов получали лечение впервые. У 8 пациентов терапия по поводу цирроза печени проводилась повторно, а в 2-х случаях предыдущий курс лечения был прерван из-за побочных реакций после применения пегилированного интерферона (ПЭГ-интерферона). Лечение продолжалось в течение 48 недель независимо от генотипа HCV Параметром оценки биохимической эффективности была нормализация активности АЛТ (<40 ед./л), критерием вирусологической эффективности неопределяемая вирусная нагрузка в плазме крови, которые измерялись непосредственно после окончания лечения (HBO) и после 6-месячного периода наблюдения (УВО). Терапевтическая безопасность оценивалась путем мониторинга побочных эффектов лечения. Повышенный уровень АЛТ до начала лечения был обнаружен у 20 из 23 пациентов. Во время терапии нормализация уровня АЛТ была достигнута у 50 % из них, а через 6 мес. она сохранялась у 9 из 20 пациентов. HBO был достигнут у 6 из 19 пациентов и УВО у 3 больных. Наиболее часто выявляемыми побочными эффектами были легкие психические расстройства (у 12 пациентов). Тромбоцитопения и лейкопения, имевшиеся до начала лечения, во время лечения не усиливались. Тяжелые побочные эффекты, вызванные применением исследуемого препарата и приведшие к прекращению лечения, были выявлены у 3-х больных (инфекция мочевыводящих путей, депрессия, миастения), из них 2 больных относились к классу А по классификации ЧайлдПью и 1 больной к классу В. У 1-го пациента лечение было прекращено в связи с развитием гепатоцеллюлярной карциномы (ГЦК).
Таким образом, авторами сделаны следующие выводы:
- Лечение натуральным лейкоцитарным интерфероном альфа (альфафероном) в комбинации с рибавирином у больных с циррозом печени, связанным с HCV, представляется безопасным терапевтическим методом.
- Альфаферон, применяемый у пациентов с тромбоцитопенией и нейтропенией, не обострял эти гематологические нарушения и показывал высокую безопасность.
- Альфаферон хорошо переносится пациентами как класса А, так и класса В по шкале Чайлд-Пью.
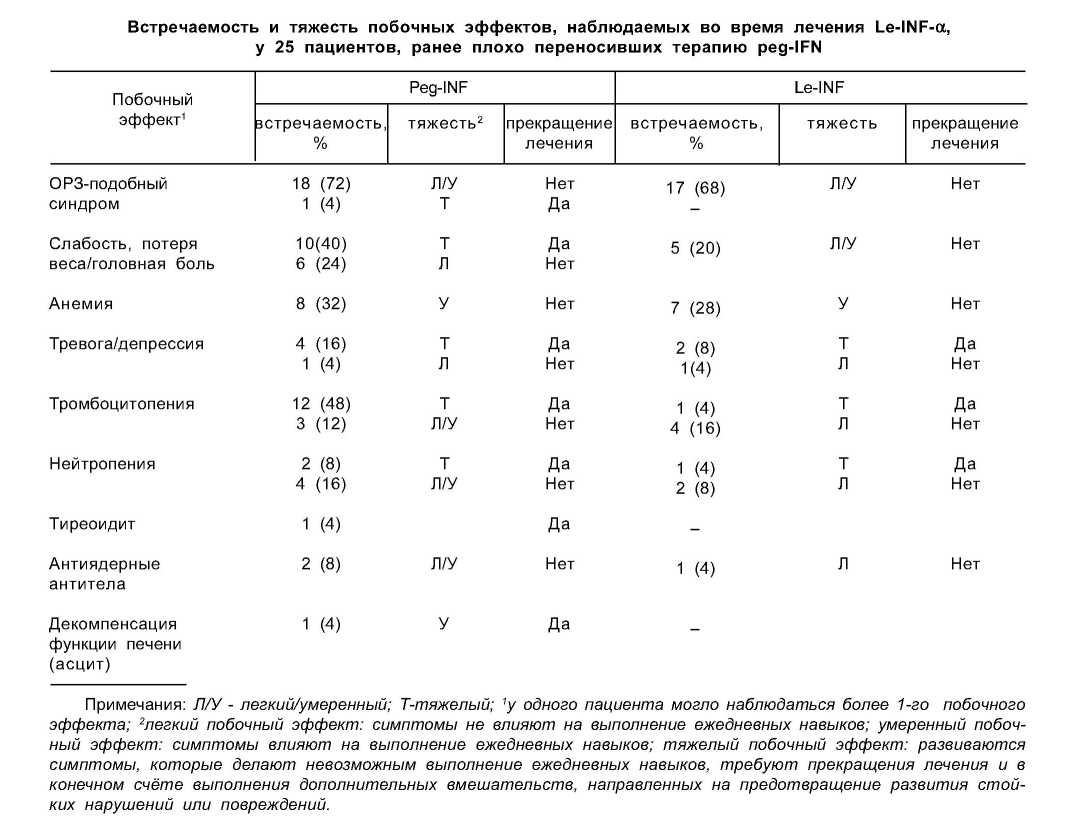
L. Е. Adinolfi et al. [11] анализировали результаты лечения Le-INF-α и рибавирином пациентов XTC с низкой толерантностью к реĝINE В исследование были включены 25 пациентов с ХГС. Генотип 1 вируса гепатита C установлен у 80 %, а цирроз у 68 % больных. У 13 пациентов (52 %) наблюдалась тромбоцитопения. Le-INF-Ot вводился в дозе 3 млн. ME 3 раза в неделю плюс рибавирин по 800 или 1000 мг/день при 2/3-м и 1-м генотипах вируса гепатита C соответственно. Курс лечения составил 48 недель. После окончания терапии за больными наблюдали еще 24 недели. Комплайенс лечения считался удовлетворительным, если пациент получал 80 % запланированного объёма терапии. В общей сложности 22 больных (88 %) завершили полный курс лечения с Le-INF-Ot. Заслуживает внимания тот факт, что побочные эффекты, которые вызвали прекращение лечения, отмечены только у 3-х пациентов при приёме Le-INF-Ot (р‹О‚ООİ) (у 2-х развились тревога и депрессия, у 1-го гематологическая токсичность: тромбоцитопения 3-й степени 34 000 клеток/мкл). При лечении peg-INF лечение прекращено у 12 пациентов: у них развилась тромбоцитопения
3-й степени (>10 000 и <50 000 клеток/мкл). наблюдаемых при назначении этих двух раз13 таблице приведено сравнение распростных видов INF.
раненности и тяжести побочных эффектов,
Как видно из приведенных данных, назначение Le-INF-Ot приводило к значительно меньшей гематологической токсичности по сравнению с peg-INF (4 и 48 % соответственно; p<0,02). Общая частота УВО 32 %, которая среди пациентов с циррозом и хроническим гепатитом составила соответственно 24 и 50 %. Как и ожидалось, эффективность лечения была существенно выше среди пациентов, инфицированных 2и 3-м генотипами вируса гепатита С, чем среди инфицированных 1-м генотипом (60 против 25 % соответственно).
Полученные авторами данные свидетельствуют о том, что назначение Le-INF-Ot может быть эффективной терапевтической альтернативой у пациентов с ХГС, плохо переносящих лечение peg-INF. По мнению авторов, более высокая переносимость Le-INF-Ot связана с тем, что он включает в себя множество молекулярных разновидностей.
A. Iacobellis et al. [12] изучали эффективность и побочные действия пегилированного INF-Ct у 66 больных с циррозом печени. В процессе интерферонотерапии 4 больных умерли из-за ухудшения функционального состояния печени. В связи с этим до применения rINF необходимо более тщательно оценивать функциональное состояние печени.
INF-Ot Зп может быть препаратом выбора для лиц с противопоказаниями к лечению пегилированными INF-Ot [13]. Установлено, что терапия INF-Ot Зп вызывает меньшее число побочных реакций, чем лечение peg-INF, улучшая функциональное состояние печени. В сравнительном исследовании, в котором оценивался профиль гематологической безопасности альфаферона у 72-х пациентов и rINF у 204-х пациентов, показана достоверно меньшая частота развития тромбоцитопении и лейкопении в группе альфаферона по сравнению с рекомбинантным интерфероном (rINF).
Примерно в 25 % случаев причина неудач в лечении хронического вирусного гепатита кроется в образовании нейтрализующих антител к интерферону. В сравнительных исследованиях, в которых изучалась частота обнаружения нейтрализующих антител к различным подтипам INF-а (INF-α2a, INF-α2b и лейкоцитарный INF-Oi) на 3-м месяце лечения ХГС частота появления нейтрализующих антител при использовании INF-α2a достигает 20 %, INF-α2b 7 %, тогда как Le-INF-Oi (альфаферон) 0 %. Более того, Т. Santantonio et al. установили дополнительно положительное влияние альфаферона на снижение уровня уже существующих противоинтерфероновых антител в сыворотке больных, пролеченных ранее пегилироваанным INF-Oi [14].
М. Malaguamera et al. считают, что альфаферон можно использовать у лиц, инфицированных HCV с наличием антинуклеарных (ANA), антимитохондриальных (AMA) аутоантител, наличием аутоантител к гладкой мускулатуре (ASMA), а также микросомного антигена печеночных и почечных клеток (LKM) [15].
Развитие неврологических и психиатрических побочных эффектов (депрессии) на фоне проводимого лечения ХГС различными модификациями "коротких" интерферонов имеет огромное медико-социальное значение. В сравнительном исследовании 90 пациентам был назначен альфаферон. Через 6 мес. лечения ни у одного пациента не наблюдались тяжелые неврологические и психиатрические нарушения, связанные с применением альфаферона [16].
Препаратами выбора для лечения ХГС и далее остаются пегилированные INF-Oi. Тем не менее, когда лечение этими препаратами невозможно, безопасной альтернативой является применение альфаферона. Причем этот препарат должен использоваться в тех ситуациях, где зафиксирована его лучшая переносимость у пациентов, ранее прервавших лечение другими INF в связи с непереносимостью. У пациентов с рецидивом или отсутствием ответа на лечение rINF, а также находящихся на гемодиализе, страдающих гемофилией, циррозом печени, высоким риском прогнозируемых лейкои тромбоцитопении в ходе предстоящего лечения [17].
Таким образом, данные многочисленных научных работ позволяют сделать вывод, что преимущества альфаферона перед другими INF-Oi заключаются в лучшей субъективной переносимости препарата, достоверно меньшей частоте побочных эффектов при сопоставимой или более высокой противовирусной активности.
Целесообразность применения препарата альфаферона обусловлена следующими его свойствами, а именно:
- наличием множества подтипов INF-Oi. Различные, подобные эндогенным, подтипы интерферонов в препарате альфаферон обладают различной противовирусной активностью, способностью стимулировать клетки природных киллеров и ингибировать клеточный рост. Результаты экспериментальных исследований подтвердили, что смесь подтипов INF-Oi обладают большей биологической активностью по сравнению с индивидуальными компонентами;
- отсутствием иммуногенности. В клинических исследованиях было показано, что альфаферон может восстанавливать терапевтический вирусологический ответ у пациентов, у которых развилась резистентность к рекомбинантным INF-Oi, обусловленная выработкой антител;
- эффективностью, сравнимой с другими препаратами INF-oι. В случаях первичных пациентов, а также пациентов с рецидивами и отсутствием ответа на предшествующий курс лечения препаратами INF-Oi;
- наименьшей токсичностью среди всех препаратов INF-Oi, а также способностью альфаферона восстанавливать способность к вирусологическому ответу на лечение у пациентов, лечение которых было прекращено из-за тяжелых побочныхэффектов или недостаточного эффекта.
ЛИТЕРАТУРА
- Gish R. G., Gadano А. С. Chronic hepatitis В: current epidemiology in the Americas and implications for management // J. Viral Hepat. 2006. V. 13. P. 787-798.
- Sy T Jamal M. M. Epidemiology of hepatitis C virus (HCV) infection //lnt. J. Med. Sci. 2006. V 3. P. 41-46.
- Halota W, Pawlowska M., Andrejczyn M. Interferonyalfa w Ieczeniu przewleklychzakazen HCV// Przeglad Epidemiologiczy. 2004. V 58. S. 405-411.
- Balan V. et al. A phase I∕II study evaluating escalating doses of recombinant human albumininterferon-alpha fusion protein in chronic hepatitis C patients who have failed previous interferon-alphabased therapy// Antivir. Then 2006. V 11. P. 35-45.
- Nomura H. et al. Short-term interferon-alpha therapy for acute hepatitis C: a randomized controlled trial // Hepatol. 2004. V 39. P. 1213-1219.
- Simon D. M. et al. Treatment of chronic hepatitis C with interferon alfa-3n: a multizenter, randomized, open-label trial // Hepatol. 1997. V 25. P. 445-448.
- Lapinsky T., Dibovska M., Flysyak R. Human leukocyte interferon-alfa (INF-а n3) in treatment the patients with chronic HCV-hepatitis // Twoje Zdrowie. 2008. № 1.
- Dibovska D., Halota W. Interferon-alpha in clinical practice // Przeglad Epidemiologiczy. 2007; 6: 17-22.
- Benvegnu L. et al. Natural history of compensated viral cirrhosis: a prospective studi on the incidence and hierarchy of major complications // Gut. 2004. V 53. P. 744-749.
- Kozielewicz D., Dybowska D., Halota B., Drozdz. Natural leukocyte interferon alpha is well tolerated by patients with HCV-related cirrhosis and Coexisling thrombocytopenia andleucopenia // J. infection. 08/07/2011. ClinicalArlicle.
- Adinolfi L.E., Durante-Mangoni E., Salzillo M., Marrone A., Tripodi M.-F., Restivo L., Merola A., Zampino R., Ruggiero G. Leukocyte interferon-alpha and ribavirin for treatment of chronic hepatitis C patients intolerant to pegylated-interferon // Intern Emerg Med. 2009; 4:485-90.
- Iacobellis A. et al. Peginterferon alfa-2b and ribavirin in patients with hepatitis C virus and decompensated cirrhosis: a controlled study // J. Hepatol. 2007. V 46. P. 206-212.
- Tripi S. et al. Leucocyte interferon-alpha for patients with chronic hepatitis C intolerant to other alpha-interferons// Biodrugs. 2003. V 17. P. 201-205.
- Santantonio T. et al. Nciilralizing antibodies to interferon alpha in a chronic hepatitis C patient non-responder to pegylated interferon // J. Hepatol. 2006. V 45. P. 759-761.
- Malaguarnera M. et al. Intravenous immunoglobulin plus interferon-alpha in autoimmune hepatitis C // Biodrugs. 2004. V 18. P. 63-70.
- Анастасий И. А. Инструкция по медицинскому применению лекарственного средства альфаферон. 2009. № 4 (60).
- Голубовская О. А. Возможности применения человеческого лейкоцитарного интерферона в лечении хронического гепатита C // Клиническая инфектология и паразитология. 2012. № 2. С. 123-129.