В последние годы вопросам вскармливания детей посвящено самое большое число научных исследований в педиатрии. Если изначально основное внимание ученых было направлено на изучение норм потребления пищевых веществ, разработку оптимально сбалансированных рационов и профилактику дефицитных состояний, то за последние двадцать лет взгляд на проблему вскармливания детей во многом изменился. В последние годы среди педиатров и нутрициологов стала формироваться концепция пищевого программирования, согласно которой, характер питания ребенка в первые годы жизни предопределяет (программирует) особенности его метаболизма на протяжении всей последующей жизни, и, как следствие, предрасположенность к определенным заболеваниям и особенностям их течения. В свете данной концепции разработка рекомендаций по питанию детей раннего возраста должна проводиться не только с позиции оптимизации качественного и количественного состава рациона, обеспечивающего потребности растущего организма в настоящий момент, но и с учетом возможности влияния характера питания на метаболизм в последующем [1,2].
Основанием для появления гипотезы пищевого программирования послужили результаты исследований, проведенных еще в середине ХХ века. В 1964 году G.Rose указал на то, что среди сибсов пациентов, страдающих ишемической болезнью сердца, показатели неонатальной смертности почти в 2 выше, чем в контрольной группе. Такие данные позволили ему предположить, что больные ИБС изначально являются потомками «конституционально более слабого рода» [3]. Эти исследования определили необходимость дальнейшего изучения взаимосвязи особенностей внутриутробного развития и предрасположенности к определенным заболеваниям в последующем.
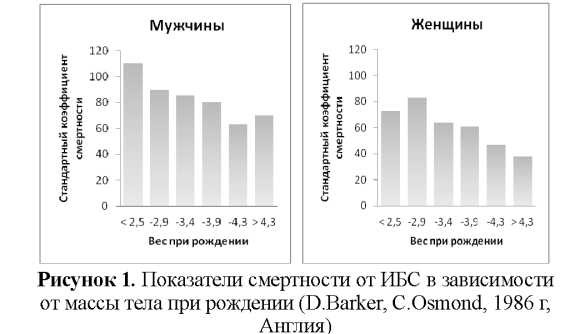
Первой фундаментальной работой этого направления явилось крупное исследование, проведенное D.Barker и C.Osmond в Великобритании [4]. Анализируя имеющиеся эпидемиологические данные, авторы обратили внимание на тот факт, что в тех регионах, где в начале ХХ века отмечались наиболее высокие показатели младенческой смертности, частота сердечнососудистой патологии была также выше среднепопуляционной. Поскольку смертность младенцев в раннем возрасте тесным образом связана с массой тела детей при рождении, данное наблюдение позволило предположить, что выжившие маловесные дети составляют группу риска по развитию сердечнососудистых заболеваний. Анализируя в дальнейшем данные по развитию 15726 мужчин и женщин, рожденных за период 1911-1930 годов, D.Barker установил, что рождение детей с малой массой тела менее 2500 граммов, увеличивает почти в 2 раза показатели летальности от ишемической болезни сердца (рис. 1).
Кроме того, установлено, что в группе пациентов, родившихся маловесными, достоверно чаще встречались случаи гипертонической болезни, сахарного диабета II типа, отмечалось повышение уровня общего холестерина, липопротеидов низкой плотности, аполипопротеина В, фибриногена. Следует отметить, что продолжительность гестации не влияла на частоту развития вышеуказанных заболеваний, что свидетельствовало о том, что именно дети с внутриутробной гипотрофией, а не недоношенные, составляют группу риска. Аналогичные данные были получены в последующем в нескольких крупных эпидемиологических исследованиях. Так, в работе Rich-Edwards J.W. с соавт. (1997), проанализировавших данные по заболеваемости 70297 медицинских сестер в США, было показано, что частота ИБС у пациенток, родившихся с массой тела менее 2500 г, составляла порядка 15%, снижаясь до 4% в случае рождения детей со средней массой (3200 г и более) [5]. Изучение историй развития 14611 мужчин и женщин, родившихся в 1915 – 1929 годах в Швеции, показало, что дефицит каждых 1000 г массы тела при рождении повышает на 70% риск развития ишемической болезни сердца у мужчин [6]. В 1996 году C.Law, проанализировав результаты 34 научных исследований, указал на наличие четкой корреляции между низкой массой тела при рождении и повышенным артериальным давлением в препубертатном периоде [7]. Отрицательная зависимость между массой новорожденного и склонностью к артериальной гипертензии в последующем была подтверждена результатами крупных исследований в Швеции, США, Хорватии [8-10].
Многочисленные научные исследования определили взаимосвязь между низкой массой тела при рождении и развитием нарушений углеводного обмена в последующие годы [11-16]. Низкая масса ребенка при рождении часто является признаком дефицита питательных веществ в антенатальном периоде и отражает усилия плода по адаптации к неблагоприятным условиям внутриутробного существования. Исходя из данного положения, изучение последствий нарушения питания на ранних этапах развития позволило сформулировать концепцию «программирования» питанием.
Термин «пищевое программирование» предложил A.Lucas в 1991 году. Он полагал, что программирование питанием осуществляется только в определенные периоды жизни, так называемые «критические» периоды или «критические окна». Воздействия средовых факторов в эти моменты повышенной чувствительности имеют долговременные последствия для здоровья и жизни человека. Следует отметить, что изучением вопроса возможного программирующего влияния питания на ранних этапах развития исследователи начали заниматься еще задолго до утверждения концепции «пищевого программирования». Так, в 1962 году McCance, в исследованиях на крысах показал, что крысята, получившие в первые 3 недели жизни меньше молока, значительно отставали в росте от своих сверстников, которые вскармливались адекватно. При этом увеличение объема питания в дальнейшем не позволило компенсировать задержку роста. В случае уменьшения объема питания животных в более поздние сроки долгосрочного влияния на рост не наблюдалось, из чего следует, что критическим периодом для «программирования» роста животного явился первый месяц жизни [17]. В последующем ряд аналогичных исследований на животных подтвердили роль пищевого программирования в становлении обменных процессов в организме, формировании поведенческих реакций, способности к обучению, предрасположенности к развитию ожирения, атеросклероза, артериальной гипертензии, сахарного диабета [18-20]. Так, в исследовании J.Smart (1986) показано, что недостаточное питание в критические периоды развития мозга у животных оказывает необратимое влияние на его размер, число нейронов, поведение, память и другие показали развития нервной системы [21]. Согласно данным D.Hill (2000), недостаточное белковое питание плодов крыс приводит к снижению числа клеток поджелудочной железы и нарушению секреции инсулина [22]. K.Park с соавт. в 2003 году доказали взаимосвязь между избыточным питанием в раннем возрасте и склонностью к ожирению после достижения половой зрелости у приматов [23].
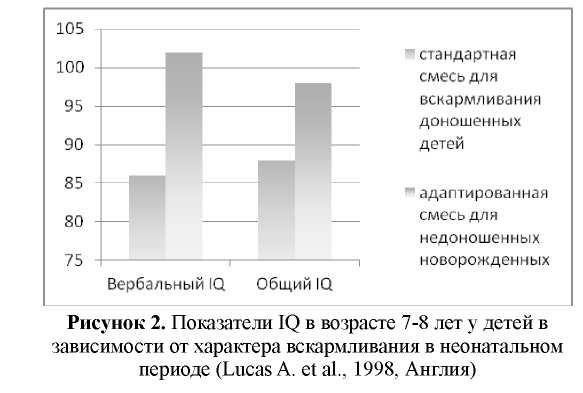
Фундаментальным исследованием программирующего влияния питания на развитие детей стала работа Алана Лукаса. В 90-х годах ХХ века он опубликовал данные по 15-летнему наблюдению за 926 недоношенными детьми [24]. Целью исследования была оценка показателей психомоторного развития недоношенных детей в зависимости от характера вскармливания. Обследуемые пациенты были рандомизированы в группы в зависимости от характера питания на первом месяце жизни (грудное молоко, специализированная обогащенная смесь для недоношенных детей или стандартная смесь для вскармливания здоровых доношенных новорожденных). При динамическом наблюдении за детьми было установлено, что к возрасту 7,5 лет худшие показатели IQ были отмечены в группе детей, получавших стандартную смесь (рис. 2). Коэффициент интеллекта (IQ) детей, находившихся на естественном вскармливании, был сравним с таковым при кормлении специализированной адаптированной смесью.
Наряду с исследованием Лукаса, ряд крупных работ, проведенных за последние 25 лет доказали, что как недостаток питательных веществ в целом, так и нехватка отдельных микронутриентов может существенным образом влиять на психомоторное развитие детей, формирования памяти и способности к обучению [25, 26]. Большое количество доказательств получено к настоящему времени о защитном действии грудного молока в отношении возможности развития ишемической болезни сердца, гипертонии, ожирения, метаболического синдрома, аутоиммунных заболеваний, патологии желудочнокишечного тракта.
Поиск возможных механизмов влияния нарушения питания плода и новорожденного на предрасположенность к определенным заболеваниям в старшем возрасте продолжается до настоящего времени. Еще в 1962 году J.Neel сформулировал теорию «экономного генотипа», пытаясь объяснить относительно высокую частоту сахарного диабета в состоятельных слоях населения [27]. Согласно данной теории гены, предопределяющие развитие диабета в историческом аспекте, могли создавать преимущество их носителям для выживания. Например, в эпоху неолита, когда земледелие и животноводство начали вытеснять охоту из повседневной жизни человека, нехватка пищи отмечалась практически повсеместно. Выживали в таких условиях преимущественно те, кто был способен в период относительного достатка пищи интенсивно запасать питательные вещества, в том числе и за счет накопления жировой массы, и «экономно расходовать» их в период голода.
Другим ярким примером того, как особенности метаболизма, позволяющие выжить в неблагоприятных условияхсуществования,способныоказыватьдолгосрочное влияние на здоровье индивида, являются данные, полученные при наблюдении за популяцией индейцев Пима, которые на протяжении 2000 лет населяли штат Аризона в США. Первые представители данной популяции
жили еще в эпоху палеолита на пустынных территориях континента в чрезвычайно тяжелых условиях окружающей среды, часто сталкиваясь с нехваткой пищи. Первые контакты индейцев Пима с европейцами датируются 1860 годом. Следует заметить, что до середины ХХ века среди 28 наиболее часто встречаемых в популяции заболеваний не упоминалось о сахарном диабете. Однако с середины 60-х годов прошлого века ожирение, сахарный диабет II типа и желчнокаменная болезнь стали наиболее частыми заболеваниями среди данного населения [28]. В настоящее время показатели заболеваемости инсулиннезависимым сахарным диабетом среди индейцев Пима являются самыми высокими в мире. Эти данные свидетельствуют о том, что неблагоприятные условия существования способствовали отбору генов, ответственных, в частности, за быстрое накопление жировой массы, что в условиях достатка может явиться причиной развития ожирения, формирования инсулинорезистентности и нарушений углеводного обмена.
Данные популяционных исследований в сочетании с собственными наблюдениями позволили в дальнейшем Баркеру сформулировать теорию «экономного фенотипа» дляобъяснениявозможныхмеханизмовпрограммирующего влияния питания на состояние обмена веществ организма. Доказательства взаимосвязи между наличием внутриутробной гипотрофии и предрасположенностью к метаболическим нарушениям и патологии сердечнососудистой системы позволили предположить, что плод, испытывая нехватку питательных веществ вследствие недостаточного их поступления в организм беременной женщины или нарушения трансплацентарного транспорта, стремится адаптироваться к неблагоприятным условиям существования, замедляя темпы роста, развивая повышенную способность к запасанию жира и инсулинорезистентность. Кроме того, стремление «экономно» расходовать доступные питательные вещества может приводить к снижению плотности капилляров в большинстве тканей с формированием эндотелиальной дисфункции, уменьшению количества функционирующих нефронов в почках, нарушению механизма отрицательной обратной связи в гормональных системах [29]. Подобная адаптация организма к особенностям питания, начиная с ранних стадий развития, получила название «метаболического импритинга» [30].
Метаболический импритинг на ранних стадиях развития может касаться лишь определенной группы клеток, однако в процессе дальнейшего их деления особенности функционирования, сформированные в процессе адаптации, могут распространиться на ткани, органы и системы организма (табл. 1).
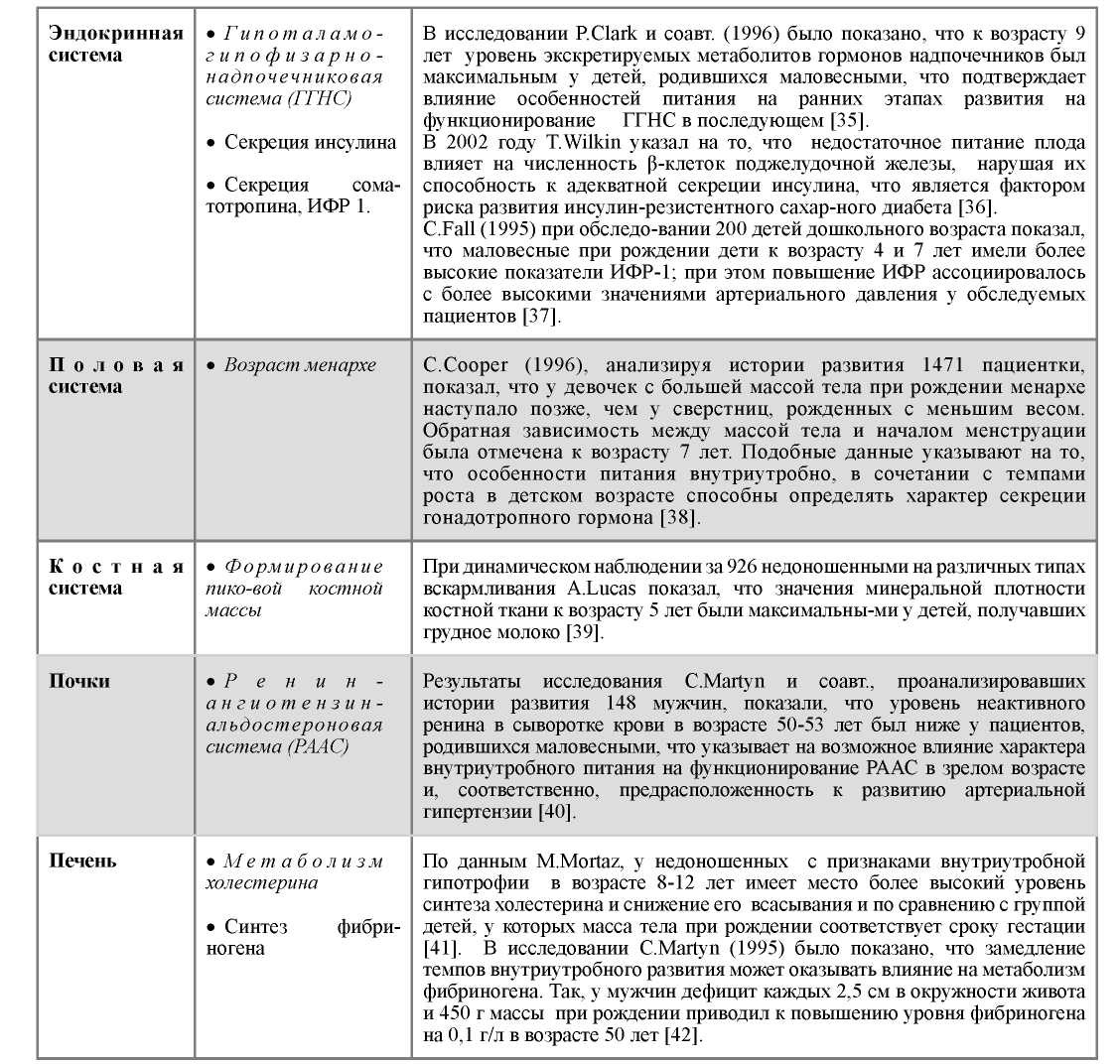
Таблица 1 - Программирующее влияние внутриутробного питания на различные структуры и функции организма [адаптировано из 31]
|
органы и системы |
структуры и физиологические процессы |
данные научных исследований |
|
сердечнососудистая система |
|
В исследовании C.Martyn и соавт. (1995), в которое вошло 337 пациентов с известными массо-ростовыми показателями при рождении, показана взаимосвязь между задержкой вну-триутробного развития и предрасположен-ностью в зрелом возрасте к повышению АД в сочетании со снижением эластичности стенок сосудов туловища и конечностей [32]. Результаты исследований CLeeson (2001), M.Franco (2006) указывают на наличие сосудистой эндотелиальной дисфункции у пациентов, родившихся маловесными. При этом, по данным CLeeson, по силе воздействия в качестве фактора риска развития атеросклероза данное состояние сравнимо с курением [33, 34]. |
33
Последующие исследования ученых показали, что не только малая масса тела при рождении, но и так называемый «скачок роста» в раннем возрасте определяет предрасположенность к развитию «программируемых заболеваний». В частности, в исследованиях на животных было показано, что ускорение роста в критические периоды развития особи влияет на состояние углеводного обмена, предрасположенность к ожирению и продолжительность жизни у крыс, скорость отложения жировой массы у рыб [43]. На роль раннего постнатального питания детей и прибавки в весе на первом году жизни в качестве фактора риска развития артериальной гипертензии указали Y.Cheung с соавт. (2000), которые на протяжении 30 лет наблюдали за ростом, развитием и характером артериального давления у 122 субъектов, родившихся массой тела менее 2500 г. Было показано, что более высокие массо-ростовые показатели у детей в возрасте 6-18 месяцев сопровождались более высоким уровнем артериального давления в возрасте 30 лет [44]. Близкие результаты получены в работах A.Singhal с соавт. (2003), которые отметили, что повышенная прибавка массы тела у недоношенных детей на первом году жизни приводила в возрасте 13-16 лет к более высоким показателям уровня проинсулина в плазме крови, то есть являлась фактором риска развития инсулинорезистентности и диабета 2 типа [45]. Исследования, проведенные в Великобритании в 2000 году, показали достоверную корреляцию ожирения у детей в возрасте 5 лет с прибавкой массы тела в первом полугодии жизни [46].
34
Объяснить данные наблюдения может помочь теория экономного фенотипа Баркера и понимание процессов метаболического импритинга. Особенности функционирования органов и систем, помогающие выжить плоду в условиях внутриутробного дефицита питательных веществ, при последующем их избыточном поступлении (что отражается в интенсивном росте и прибавке в весе рожденного маловесным ребенка) могут предопределять развитие ожирения, инсулинорезистнтности, артериальной гипертензии в более старшем возрасте.
Таким образом, на основании имеющихся данныхможно полагать, что внутриутробный период и первый год жизни ребенка являются критическими этапами развития, когда воздействие неблагоприятных факторов, к числу которых относится неадекватное питание, существенно сказывается на состоянии здоровья ребенка в последующем. Обеспечение беременной женщины необходимыми питательными веществами в сочетании с рациональным вскармливанием младенца с первых минут жизни является залогом здоровья, как для ребенка, так и для будущего взрослого.
CписоК литератУры
- Захарова И.Н., Дмитриева Ю.А., Суркова Е.Н. Отдаленные последствия неправильного вскармливания детей. Учебное пособие для врачей / М.:2011. – 70с.
- Захарова И.Н., Дмитриева Ю.А., Суркова Е.Н. Отдаленные последствия неправильного вскармливания детей /Вопросы практической педиатрии. -2010.-т.5.- №4.-с.52-57
- Anderson J.W. et al. Brest-feeding and cognitive development: a meta-analysis. American journal of clinical nutrition, 70: 525-535 (1999).
- Barker DJP, Hales CN, Fall CHD, Osmond C, Phipps K, Clark PMS. Type 2 (non-insulin-dependent) diabetes mellitus, hypertension and hyperlipidaemia (syndrome X): relation to reduced fetal growth. Diabetologia 1993;36:62–7.
- Barker DJP, Osmond C. Infant mortality, childhood nutrition, and ischaemic heart disease in England and Wales. Lancet 1986; 1:1077-81.
- Barker DJP. Mothers, babies and health in later life. Edinburgh: Harcourt Brace & Co Ltd, 1998.
- Cheung YB, Low L., Osmond C. et. al. Fetal growth and early postnatal growth are related to blood pressure in adults. Hypertension, 2000; 36:795-805.
- Clark PM, Hindmarsh PC, Shiell AW, Law CM, Honour JW, Barker DJP. Size at birth and adrenocortical function in childhood. Clin Endocrinol 1996; 45:721–6.
- Cooper C, Kuh D, Egger P, Wadsworth M, Barker DJP. Childhood growth and age at menarche. Br J Obstet Gynaecol 1996; 103:814–7.
- Curhan GC, Chertow GM, Willett WC, et al. Birth weight and adult hypertension and obesity in women. Circulation 1996;94:1310–5.
- Curhan GC, Willett WC, Rimm EB, Stampfer MJ. Birthweight and adult hypertension and diabetes in US men. Am J Hypertens 1996; 9:11A.
- Dobbing J., Sands J. Vulnerability of developing brain. IX. The effect of nutritional growth retardation on the timing of the brain growth-spurt. Biol. Neonate 1971; 19:363-378.
- Eriksson JG, Forsen T, Tumilehto J. Early growth and coronary heart disease in later life: longitudinal study. B.Med.J. 2001; 322:949-953.
- Fall CHD, Pandit AN, Law CM, et al. Size at birth and plasma insulin-like growth factor-1 concentrations. Arch Dis Child 1995; 73:287–93.
- Franco MC, Christofalo DM et al Effects of low birth weight in 8- to 13-year-old children: implications on endothelial function and uric acid levels. Hypertension. 2006 Jul; 48(1):25-6.
- Godfrey KM and Barker DJP. Fetal nutrition and Adult Desease. American Journal of Clinical Nutrition, Vol. 71, No. 5, 1344S-1352s, May 2000.
- Hahn P. Effect of litter size on plasma cholesterol and insulin and some liver and adipose tissue enzymes in adult rodents. J. Nutr. 1984; 114:1231-1234.
- Hales CN, Barker DJP, Clark PMS, et al. Fetal and infant growth and impaired glucose tolerance at age 64. BMJ 1991;303:1019–22.
- Hill DJ, Duville B. Pancreatic development and adult diabetes. Ped.Res. 2000; 48:269-274.
- Knowler WC, Pettitt DJ, Saad MF, Bennett PH. Diabetes mellitus in the Pima Indians: incidence, risk factors and pathogenesis. Diabetes Metabol Rev 1990;6:1-27.
- Kolacek S, Kapetanovic T, Luzar V. Early determinants of cardiovascular risk factors in adults. B. Blood pressure. Acta Paediatr 1993;82:377–82.
- Law CM, Shiell AW. Is blood pressure inversely related to birthweight? The strength of evidence from a systematic review of the literature. J Hypertens 1996;14:935–41.
- Leeson CP, Kattenhorn M, Morley R. et.al. Impact of low birth weight and cardiovascular risk factors on endothelial function in early adult life. Circulation, 2001; 103:1264-1270.
- Leon DA, Koupilova I, Lithell HO, et al. Failure to realise growth potential in utero and adult obesity in relation to blood pressure in 50 year old Swedish men. BMJ 1996;312:401–6.
- Lithell HO, McKeigue PM, Berglund L, Mohsen R, Lithell U-B, Leon DA. Relation of size at birth to non-insulin dependent diabetes and insulin concentrations in men aged 50–60 years. BMJ 1996; 312:406–10.
- Lucas A. Programming by Early Nutrition: An Experimental Approach. The Journal of Nutrition Vol. 128 No. 2 February 1998, pp. 401S-406S.
- Lucas A. Programming by Early Nutrition: An Experimental Approach. The Journal of Nutrition Vol. 128 No. 2 February 1998, pp. 401S-406S.
- Martyn CN, Barker DJP, Jespersen S, et al. Growth in utero, adult blood pressure and arterial compliance. Br Heart J 1995;73:116–21.
- Martyn CN, Lever AF, Morton JJ. Plasma concentrations of inactive renin in adult life are related to indicators of foetal growth. J Hypertens 1996;14:881–6.
- Martyn CN, Meade TW, Stirling Y, Barker DJP. Plasma concentrations of fibrinogen and factor VII in adult life and their relation to intra-uterine growth. Br J Haematol 1995;89:142–6.
- McCance R. A. Food growth and time. Lancet 1962; 2:271-272.
- Metcalf NB, Monaghan P. Compensation for a bad start: grow now, pay later. Trends in Ecology and Evolution 2001;16:254-60.
- Mortaz M, Fewtrell MS, Cole T. et.al. Birth weight, subsequent growth, and cholesterol metabolism in children 8-12 years old born preterm. Arch.Dis.Child. 2001, 84:212217.
- Neel JV. Diabetes mellitus; a thrifty genotype rendered detrimental by `progress'? Am J Hum Genet 1962;14:353-62.
- Ong K, Ahmed M, Emmett P, et.al Association between postnatal catch-up growth and obesity in childhood: prospective cohort studies. BMJ, 2000:320:967-971.
- Park KS, Kim SK, Kim MS, et.al. Fetal and early postnatal protein malnutrition cause long-term changes in rat liver and muscle mitochondria. J.Nutr. 2003; 133: 3085-3090.
- Phillips DIW. Insulin resistance as a programmed response to fetal undernutrition. Diabetologia 1996;39:1119–22.
- Rich-Edwards JW, Stampfer MJ, Manson JAE, et al. Birth weight and the risk of cardiovascular disease in a cohort of women followed up since 1976. BMJ 1997;315:396–400.
- Rose G. Familial patterns in ischaemic heart disease. Br J Prev Soc Med 1964;18:75–80.
- Singhal A., Fewtrell C., Cole T., Lucas A. Low nutrient intake and early growth for later insulin resistance in adolescents born preterm. Lancet. 2003, 28;361 (9376); 2248-9.
- Smart J. Undernutrition, learning and memory: reviewof experimental studies. Proceedings of XII International Congress of Nutrition, London. John Libbey Company 1986; 74-8.
- Smart J. Undernutrition, learning and memory: review of the experimental studies. In: Taylor TG, Jenkins NK, eds. Proceeding of XII international congress of nutrition. London: John Libbey, 1986:74-78.
- Snoek A., Remacle C., Reusens B., Hoet J. J. Effect of a low protein diet during pregnancy on the fetal rat endocrine pancreas. Biol. Neonate 1990; 57:107-118.
- Waterland R.A., Garza C.. Potential mechanisms of metabolic imprinting that lead to chronic disease. American Journal of Clinical Nutrition, Vol. 69, No. 2, 179-197, February 1999.
- Weaver L. Early Catch-up growth-balancing the interests of the child. Nutritional Programming: implications for infant feeding. Proceedings of an international symposium, Barcelona, 2005.
- Wilkin T, Metcalf B, Murphy M, et. al. The relative contribution of birth weight, weight change and current weight to insulin resistance in contemporary 5-year-olds. Diabetes. 2002;51:3468-3472.