Оксредметрическим методом изучен процесс комплексообразования железа (II) с меркaзoлилом при температуре 298 К и ионной силе 1.0 моль/л. Установлено, что железа (II) с мерказолилом образует пять комплексные формы. Методом оксредметрии определены состав, области доминирования координационных соединений железа (II) с меркозалилом. Константы образования комплексов определены с помощью окислительной функции.
Ключевые слова: железа, меркaзoлил, комплексообразование, константа устойчивость, ионная сила.
Актуальность темы. Благодаря своим уникальным физико-химическим свойством соединения железа применяются в различных областях промышленности и народного хозяйства.
Данные приведённые в работе [1] о комплексообразования железа (II) с протопорфирином, где участвуют два ионных и два координационных связей, осуществлённые двумя атомами азота молекулы протопорфирина.
Железа благодаря своим четырьмя связами с порфирином образует комплексное соединение, а с пятой координационной связи соединяется с имидазольной группой гистидина которое связывает белковую часть гемоглобина с небелковой. Для присоединения кислорода и получение оксигемоглобина используется шecтaя кooрдинaциoннaя cвязь жeлeзa.
Комплексное соединение металлы жизни с гетероциклическими лигандами утoчнили автoры [2], являются реакционно-активными веществами. Комплексное соединение на основу имидазола с биометаллами обладают пестецидной активностью. Данные комплексы проявляют антигельминтную 2+ 2+ 2+ 3+ 2+ 2+ 3+ 2+ 2+ 2+ активность; Mn , Cu ,Ni , Fe ,Zn ,Со ,Cr ,Cd ,Sn ,Gb c бензимидазолами и с 1-метил-2- аминобензимидазолом.
Образование гидроксокомплексов железа (III) приведены авторами работе [3], где указаны возможность образования гидроксоформ состава FeOH2+ и Fe2(OH)24+. В области рН от 1,0 до 4,5 железа может образовать комплексное соединение с анионами алифатических кислот [4]. Также в данных областях могут образоватся моноядерные, би-трехъядерные и смещенные по лигандам координационные соединения железа. Комплексообразующий способность в системах железо (III) –железо (II) в водно спиртовых растворах муравьиной, уксусной, монохлоруксусной, монойодуксусной, трихлоруксусной, трибромуксусной, пропионовой, масляной и изомасляной кислот в интервале ионных сил от 1.03.0, приведенны авторами [5,6]. Авторами с помощью метода оксредметрии показано, что окислительный потенциал находится в прямой зависимости от состава сложного растворителя.
В литературе отсутствуют сведения о комплексообразование железа(II) с меркозалилом и их биологическая активность.
Целью настоящей работы является изучения процесса комплексообразования железа(II) с мерказолилом при 298 К и ионной силе 1.0 моль /л, определение констант устойчивости образующихся комплексов и области их доминирования в растворе.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
С помощю метод оксредметрии Кларка-Никольского изученно процесс комплексообразования в окислительно-восстановительной системе [7,8].
Оксредметрия – это метод основано при получении экспериментальных зависимостей ЭДС от концентрационных переменных: рН, pCFe(II) рСL .Измереные электродвижущая сила гальванических элементов с переносом, составленных сочетанием трех электродов: железный и хлорсеребряного для определения ЭДС цепи, стеклянного и хлорсеребряного для определения рН. Гальвонические элементы и два рабочие растворы использованны для получения экспериментальной зависимости ЭДС системы от рН раствора.
Из двух гальванических элементов первый необходимо для измерения ЭДС системы, а второй – для определения рН раствора в электролитической ячейке в процессе титрования [9].
В мерной колбе объёмом 25 мл готовили первый рабочий раствор т.е., растворением заданных количеств эквимолекулярной смеси солей двухвалентного железа. Химические веществ -0,1н H2SO4 и Na2SO4 использовались для создания ионной силы рабочего раствора.
Проверки железного электрода т.е. оценка электродной функции заключалась в проверке его подчинению уравнения Нернста.
Измерение ЭДС системы проводилось при строго фиксированных значениях рН и ионной силы с помощью двух рабочих растворов с одинаковыми значениями рН и ионной силы при различных значениях концентрации железа (II). Измерение ЭДС гальванического элемента, составленного из железного и хлорсеребряного электродов, осуществлено с помощью уравнения:
φ Fe (II)/Fe(0)= Е - φAg / AgCl, Cl-. (1),
где Е – ЭДС гальванического элемента, φ Fe (II) / Fe (0) – потенциал; железного электрода, φAg/ AgCl, Cl-потенциал хлорсеребряного электрода [10-12].
Результаты их обсуждение:
В данной работе преведены данные оксредметрическых измерений в системе Fe (II) - Merk - H2O, при 298 К и ионной силе раствора 1.0 моль/л.
Максимальное число координированных молекул органического лиганда присоединённых к иону железа показано на зависимости окислительного потенциала φ от lgCL и определено по тангенсу угла наклона. Форма кривых зависимости ∆Е от рН свидетельствует о ступенчатом характере комплексообразования между железом (II) и мерказолилом.
Совместный анализ экспериментально полученных зависимостей окислительного потенциала системы (φ) от рН, концентрации окисленной и восстановленной форм железа, мерказолила, создание стехиометрической матрицы (математической модели) существующих равновесий в растворе показали, что в системе образуются комплексы различного состава.
Состав и константы образования координационных соединений, их степени накопления уточнены с помощью окислительной функции Юсупова З.Н. методом иттерации [12-14].
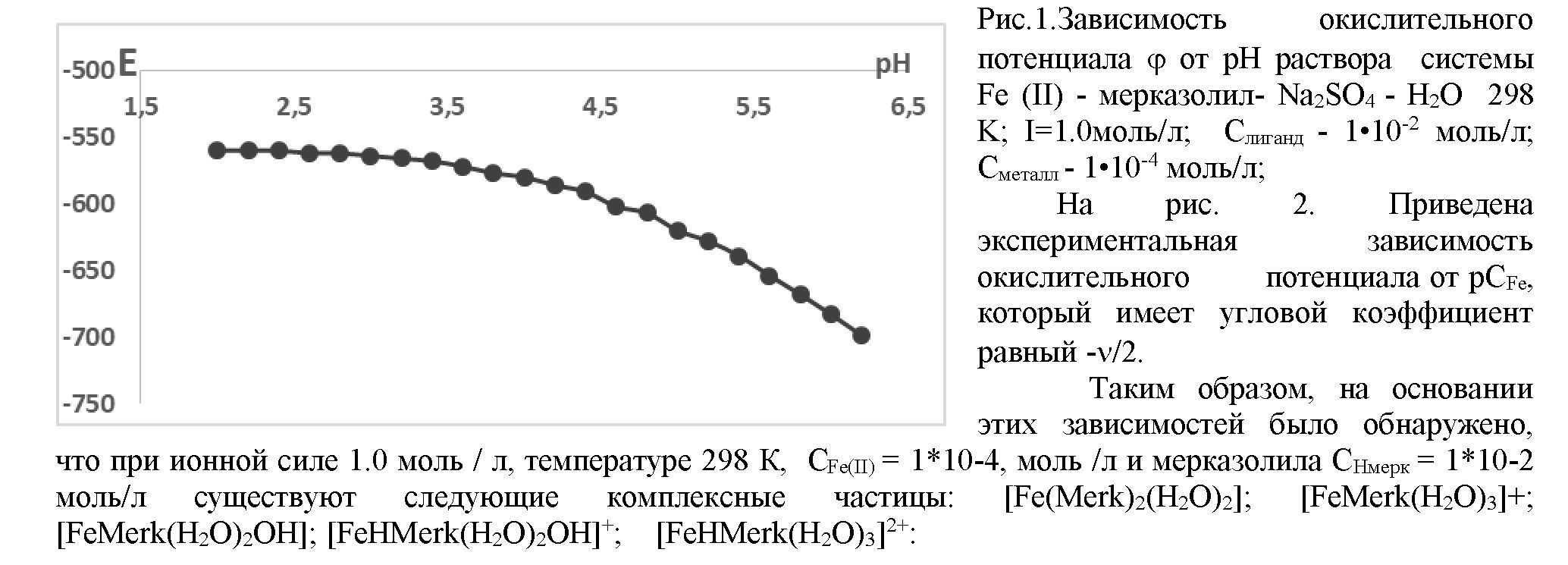
Для определения общего числа коомплексных частиц и место их доминирования в системе Fe (II) – Мерк - Na2SO4 - H2O при 298 К и J = 1.0 моль/л были сняты зависимости окислительного потенциала от рН раствора, которое приведено на рисунке 1.
Литература
- Коттон Ф., Уилкинсон Дж. Современная неорганическая химия. Часть 3. Химия переходных элементов. М.: Мир, 1969, 592 с.
- Барашков Г.К. Медицинская бионеорганика. Москва: 2011, 312-319 с.
- Котегов К. В., Фадеева Н. В., Кукушкин Ю.Н. - Журн. общей химии, 1973, т. 43, вып. 5, с. 1182-1184.
- Якубов Х.М. Применение оксредметрии к изучению комплексообразования. Душанбе: Дониш, 1966, 121 с.
- Добош Д. Электрохимические константы. - М.: Мир, 1980, С.88, 202, 240.
- Мищенко К.П., Равделя А.А. Краткий справочник физико-химических величин. Химия, 1974, 138 с.
- Раджабов У.Р., Рахимова Н.Р., Саттори И.Т., Сатторов М.М., З.Н. Юсупов. Синтез, идентификация и биологические свойства координационных соединений Fe (II) и Cu (II) с азолами. Естественные и технические науки. 2011, №3, 57-62 с.
Адрес для корреспонденции: Раджабов Умарали, 734003 г. Душанбе. пр.Рудаки 139. ТГМУ имени Абуали ибн Сино., Ёрмамадова Саврибегим Гулмамадовна, Камолова Иќлима Усмоновна. 734025, Республика Таджикистан, г. Душанбе, пр. Рудаки, 17, Таджикский национальный университет.