АННОТАЦИЯ
В статье изучена возможность использования методов компьютерной химии для изучения механизма действия известного цитотоксического лекарственного средства - азатиоприна на пролиферативную активность мононуклеарных клеток периферической крови человека. Анализ полученных квантово-химических характеристик азатиоприна выявил высокую реакционную способность его молекулы, что подтверждается положительными значениями теплоты образования и потенциала ионизации.
Ключевые слова: методы компьютерной химии, молекулы, иммунная система, квантовохимический анализ.
Ранее уже отмечалось, что компьютерная химия - одна из динамично развивающихся отраслей современной науки. Она охватывает химические науки, физическую химию, молекулярную биологию, фармацию, фармакологию и т.д. Относительно мало использована компьютерная химия в иммунобиологии. Наши исследования направлены на восполнение этого пробела.
Современные компьютерные технологии, в частности, Structure Activity Relationships (SAR), способны воссоздать структуру любого биологического объекта в трехмерном изображении, а технологии компьютерного конструирования (Computer Assisted Design/CAD) используются для построения новых молекул, которые теоретически обладают способностью вступать во взаимодействие с ферментом или рецептором. Полученная информация широко используется при компьютерном моделировании процесса взаимодействия. Мы предположили о возможности использования методов компьютерной химии для изучения механизма действия азатиоприна на пролиферативную активность мононуклеарных клеток периферической крови человека.
Как известно, существуют первичные и вторичные органы иммунной системы, которые ответственны за размножение, созревание и функционирование иммунокомпетентных клеток. Ранее отмечалось, что система мононуклеарных фагоцитов составляет, после лимфоцитов, вторую крупную популяцию клеток иммунной системы. Она включает клетки первого уровня - происходящие из единой стволовой клетки костномозговые предшественники - монобласт и промоноцит; клетки второго уровня - мононуклеарные фагоциты в виде циркулирующих в крови моноцитов и зрелых тканевых макрофагов /3, 4, 5, 6/.
Мононуклеарные фагоциты обеспечивают неспецифическую защиту организма за счет своей фагоцитарной функции. Секретируемые макрофагами молекулы выполняют эффекторные и регуляторные функции. При формировании специфического иммунного ответа макрофаги выполняют функцию презентации антигена: захваченный макрофагами антиген подвергается переработке в фаголизосомах. Образующиеся в результате ограниченного протеолиза пептидные фрагменты антигена комплексируются с молекулами антигенов главного комплекса гистосовместимости класса 2 и выставляются на мембране макрофага в форме, доступной для распознавания Т-лимфоцитами.
Следует отметить такую важную функцию макрофагов, как секреция цитокинов. В частности, синтез и секреция интерлейкина-1, способствует активации Т-лимфоцитов при ответе на внедрение антигена. При этом макрофаги, под влиянием лимфоцитарных продуктов, мобилизуются в очаг иммунного воспаления. Другие интерлейкины стимулируют пролиферацию ранних клеточных предшественников, Т-клеток, антиген-активированных В- и Т-клеток, эозинофилов, синтез тучных клеток, стимулируют хемотаксис нейтрофилов и другие важные иммунные реакции [7, 8]
Активированные макрофаги выполняют функции основных эффекторных клеток клеточноопосредованного иммунного ответа. Макрофаги также принимают участие в эффекторной фазе гуморального иммунного ответа, захватывая и уничтожая патогенные бактерии, опсонизированные специфическими антителами и комплементом. Для этого на мембране макрофагов экспрессированы специальные рецепторы для иммуноглобулинов FcR и для комплемента - CR1 [3, 4, 5, 6, 7].
Таким образом, макрофаги являются одним из важнейших компонентов неспецифической защиты организма. Следовательно, важнейшее значение имеет также изучение влияния различных иммунокомпетентных лекарственных средств на функционирование макрофагов. В нашей работе изучена возможность компьютерного моделирования действия известного цитотоксического лекарственного средства - азатиоприна - на систему макрофагов.
Как известно, азатиоприн - конкурентный антагонист гипоксантина, по химическому строению и биологическому действию близок к пуриновым основаниям; оказывает иммунодепрессивное и цитостатическое действие. Включаясь в метаболические реакции, нарушает синтез нуклеиновых кислот, конкурирует с гипоксантином и гуанином за гипоксантин-гуанин- фосфорибозилтрансферазу, переводящую пуринетол в тиоинозиновую кислоту (ТИК). ТИК подавляет ряд реакций с участием инозиновой кислоты (ИК), включая превращение ИК в ксантиновую и адениловую кислоты. В ходе метилирования ТИК образуется метаболит, блокирующий глутамин-5-фосфорибозилпирофосфат аминотрансферазу - фермент, инициирующий путь пуринового синтеза рибонуклеотидов. В связи с потерей способности клеток образовывать ТИК возможно развитие резистентности опухолевых клеток к азатиоприну. Иммунодепрессивное действие обусловлено гипоплазией лимфоидной ткани, снижением количества Т-лимфоцитов, нарушением синтеза Ig, появлением в крови атипичных фагоцитов и подавлением клеточноопосредованных аллергических реакций [9, 10, 11, 12, 13].
Препарат применяют для профилактики реакции отторжения при трансплантации почек, лечения ревматоидного артрита, хронического активного гепатита, СКВ, дерматомиозита, узелкового периартериита, приобретенной гемолитической анемии, идиопатической тромбоцитопенической пурпуры, гангренозной пиодермии, псориаза, болезни Крона, неспецифического язвенного колита, миастении, пузырчатки, синдрома Рейтера, лучевого дерматита, псевдогипертрофической миопатии. [9, 10, 11, 12, 13]
.Материалы и методы.
Подготовка образца крови.
Эксперименты проводили на периферической крови, полученной от одного здорового донора. Забор крови производили натощак из локтевой вены с соблюдением правил асептики в одноразовый 50-миллилитровый пластиковый контейнер, содержащий стерильный 6 % раствор ЭДТА. Объемное соотношение кровь/ЭДТА составляло 20/1. Затем кровь перемешивали с полиглюкином в соотношении 1:1 и инкубировали при комнатной температуре в течение 1-1,5 ч. По завершению инкубации взвесь клеток без эритроцитов декантировали в чистый контейнер и центрифугировали при 1000 об./мин в течение 10 мин при комнатной температуре. Удаляли надосадочную жидкость, клеточный осадок разбивали постукиванием по дну контейнера и добавляли 1 мл среды RPMI-1640. Все процедуры выполняли в стерильном кабинете.
Фракционирование мононуклеаров на градиенте плотности.
В центрифужную пробирку вносили 1 мл изопака (Sigma, США) с плотностью 1,076 г/мл. Затем осторожно наслаивали 1 мл клеточной суспензии. Осаждали на центрифуге 3К30 при 3000 об./мин в течение 20 мин при температуре ротора 8оС. По окончанию центрифугирования интерфазное кольцо клеток собирали в 50-милилитровый контейнер, добавляли 20 мл среды RPMI- 1640 и отмывали от примесей изопака центрифугированием при 1000 об./мин в течение 10 мин при комнатной температуре. После центрифугирования супернатант удаляли, встряхивали клеточный осадок постукиванием по дну контейнера и добавляли к осадку 1 мл полной культуральной среды RPMI-1640, содержащей 10% фетальной телячьей сыворотки (ФТС), 4 мМ L-глутамина, 100 мг/мл стрептомицина и 100 МЕ/мл пенициллина.
Оценка количества и жизнеспособности мононуклеарных клеток.
Для оценки жизнеспособности клеток в суспензии использовали тест на исключение красителя трипанового синего. К суспензии клеток добавляли равное количество раствора трипанового синего, перемешивали встряхиванием и подсчитывали количество окрашенных и неокрашенных клеток в гемоцитометре Горяева под микроскопом.
Культивирование клеток.
Суспензию полученных клеток доводили до концентрации 106 кл./мл полной культуральной средой и вносили по 200 мкл в 96-луночный планшет. Клетки культивировали при 37оС в атмосфере с 5% СО2 и 95% влажности в СО2-инкубаторе в течение 48 ч. В опытные ячейки вносили тестируемый препарат в концентрации, равной концентрации рекомендуемой разовой дозе препарата из расчета на 5 л крови.
Приготовление рабочих разведений препаратов.
Рабочие разведения азатиоприна готовили следующим образом: таблетку азатиоприна (5 мг) тщательно растирали в ступке и растворяли в 5 мл среды RPMI-1640. Полученную взвесь центрифугировал и при 5000 об./мин в течение 5 мин. Супернатант стерилизовали, пропуская через стерильный мембранный фильтр с диаметром пор 0,22 мкм. Раствор азатиоприна в концентрации 640 мкг/мл добавляли в ячейки с клетками в объеме 20 мкл на каждые 180 мкл клеточной суспензии, получая конечную концентрацию препарата 64 мкг/мл
-
- Оценка пролиферации клеток в МТТ-тесте /14/.
За 4 ч до окончания культивирования в каждую ячейку вносили по 250 мкг/мл МТТ (3-(4,5- диметилтиазол-2-ил)-2,5-дифенилтетразолиум бромид). По окончанию опыта из лунок удаляли супернатант, образовавшиеся кристаллы формазана растворяли ДМСО и колориметрировали при 570 нм.
Индекс пролиферации (ИП) клеток вычисляли по формуле:
ИП=О/Кх100%,
где О - среднее значение экстинкции из 5 повторов в опыте, К - то же самое в контроле (в отсутствии лекарственного препарата). /9/
Определение цитокинов.
В части ячеек, в которые не вносили МТТ, определяли продукцию цитокинов с помощью иммуноферментного анализа, используя коммерческие тест-системы (IFND , IL-1D , IL-15, - R&D Systems, Великобритания; IL-13, IL-12 - Diaclone, Франция) согласно прилагаемым инструкциям. По окончанию инкубации планшеты центрифугировали для осаждения клеток (10 мин при 400g). Бесклеточные супернатанты собирали, замораживали и хранили при -70оС до определения в них цитокинов.
Компьютерный химический анализ
Была изучена молекулярная механика и реакционная способность ликопида.
Расчеты осуществлены с применением метода Хартри-Фока в полуэмпирическом приближении РМ3 (Parametrization Method 3) /15, 16/
Статистический анализ
Полученные данные обрабатывали методами математической статистики, используя прикладную программу Microsoft Excel. Вычисляли среднюю арифметическую, среднюю квадратическую ошибку средней арифметической и достоверность различия средних (Р), используя функцию ТТЕСТ.
. Результаты исследования.
Анализ влияния азатиоприна на пролиферативную активность мононуклеарных клеток периферической крови человека показал, что в исследованной концентрации он весьма умеренно снижал на пролиферацию при культивировании в течение 48 ч (рисунок 1).
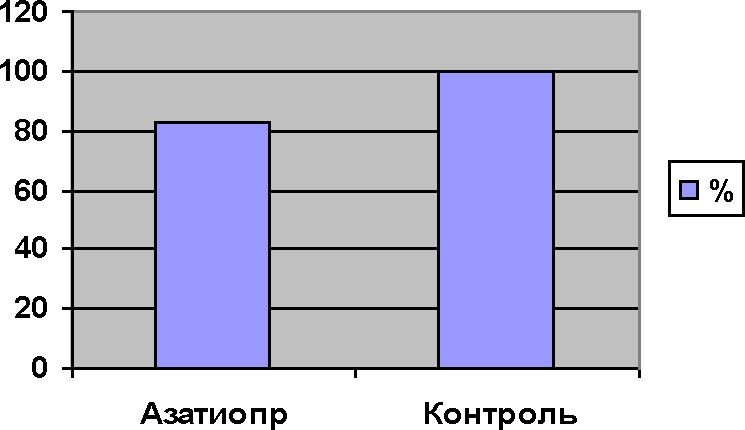
Рисунок 1 - Влияние азатиоприна на пролиферацию мононуклеарных клеток периферической крови человека.
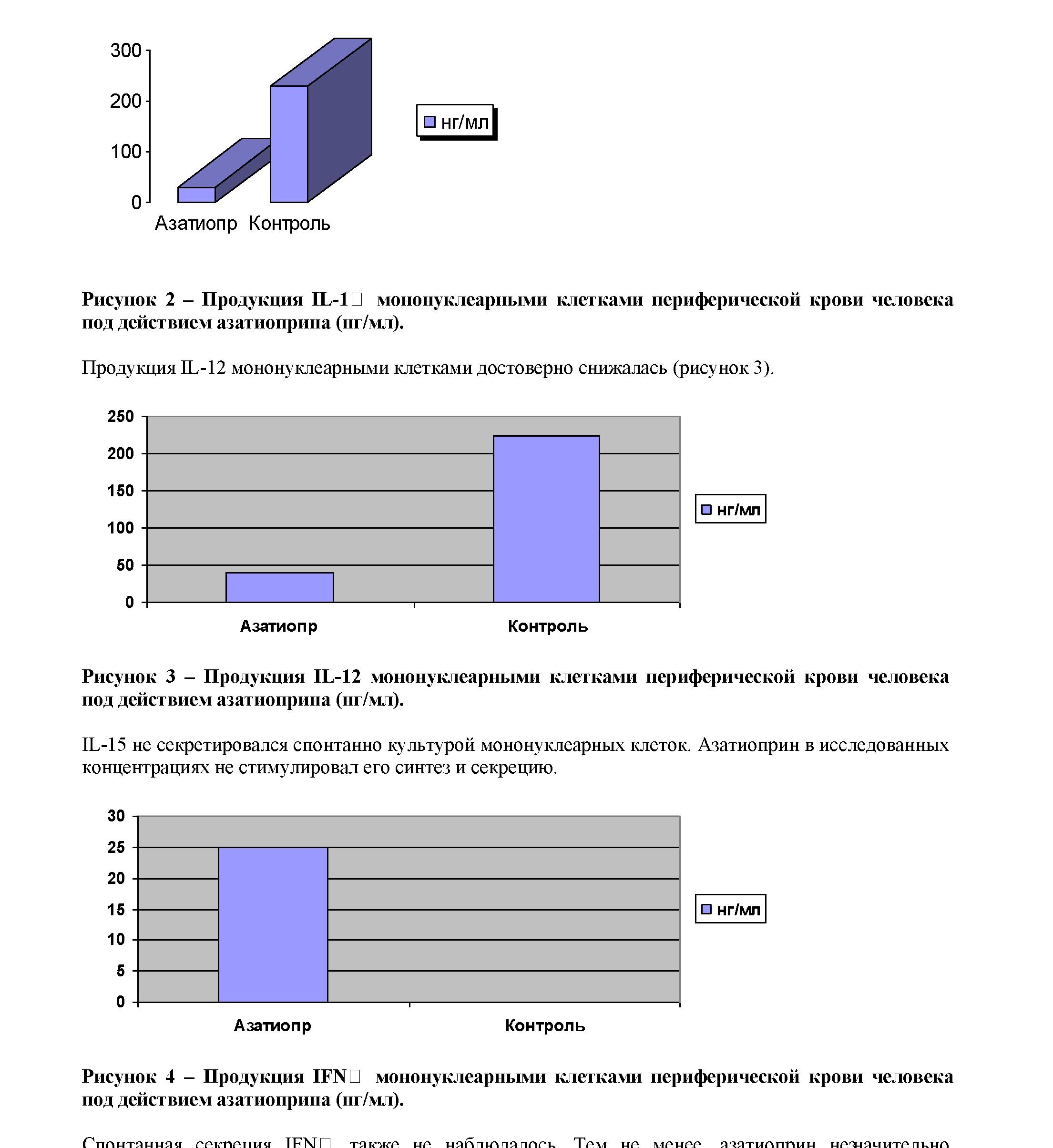
Оценка продукции цитокинов культурой мононуклеарных клеток под действием азатиоприна показала следующие результаты:
- продукция IL-1 □ достоверно (P<0,05) снижалась (рисунок 2)..,
стимулировал продукцию этого цитокина (рисунок 4)..
В то же время он не влиял на продукцию супрессорного цитокина IL-13.
Таким образом, действие азатиоприна на мононуклеары в основном проявляется через супрессию цитокинов. Тем не менее, продукция IFND недостоверно увеличивалась при одновременном отсутствии влияния на продукцию супрессорного цитокина IL-13. То есть данный препарат в наших исследованиях показал умеренно выраженную способность активировать цитотоксические макрофаги и естественные киллеры, что свидетельствует в пользу наличия у него противовоспалительных свойств и, в целом, иммуномодулирующего действия в невысоких концентрациях.
Из литературных данных известно, что IFND повышает продукцию других цитокинов и антимикробную активность лейкоцитов [17, 18, 19]. То есть в низких концентрациях данных
препарат показывает не только цитотоксические, но и в некоторых аспектах, иммуномодулирующие свойства.
Квантово-химические характеристики азатиоприна представлены в таблице 1.
Для анализа нами отобраны: теплота образования (AHf, ккал/мол), полная энергия (Etot ), потенциал ионизации (IP), полная электронная энергия (Eel), энергия отталкивания ядер (Enn). Это основные квантово-химические характеристики, которые позволяют оценить стабильность соединения, его способность преодолевать биологические барьеры и взаимодействовать с различными биологическими структурами.
Теплота образования (энтальпия образования, ДНГ) - тепловой эффект реакции образования химических соединений из простых веществ в стандартном состоянии. Данная характеристика также служит показателем стабильности соединения, так как дает количественную оценку энергии, необходимой для разрушения молекулы химического вещества. Отрицательная величина обозначает высокую стабильность вещества. Положительное или нулевое значение означает, что вещество быстро распадается. Расчет теплоты образования позволяет дополнительно оценить правильность расчета Etot: обе энергетические характеристики при правильном расчете должны иметь примерно одинаковые значения.
Полная энергия (Etot ) - сумма кинетической и потенциальной энергий, т.е. общий
энергетический потенциал молекулы. Она характеризует стабильность соединения и, следовательно, возможность создания из него перспективной для фармацевтического производства лекарственной формы. С другой стороны количественная характеристика стабильности позволяет оценить возможности гидролиза вещества в организме и продолжительность его действия.
Потенциал ионизации (IP) - это физическая величина, определяемая отношением наименьшей энергии, необходимой для однократной ионизации атома (или молекулы), находящегося в основном состоянии, к заряду электрона. Потенциал ионизации — мера энергии ионизации, которая равна работе вырывания электрона из атома или молекулы и характеризует прочность связи электрона в атоме или молекуле. Потенциал ионизации характеризует растворимость соединения в различных средах и его реакционную способность. Чем выше значение потенциала ионизации, тем лучше растворимость соединения и его способность вступать в различные реакции. Исходя из выше изложенного очевидно, что потенциал ионизации - один их основных показателей, характеризующих способность биологически активного вещества вступать во взаимодействие с теми или иными молекулами. Следовательно - это важный показатель для понимания механизма взаимодействия биологически активного вещества с рецепторами или другими молекулами-мишенями клеточных структур организма млекопитающих.
Полная электронная энергия (Eel) характеризует величину энергии, необходимую для передачи электронов из одной системы (в данном случае молекулы) в другую квантовую систему. Чем ближе к нулю или положительному значению эта величина, тем менее стабильна локализация электронов на внешней оболочке молекулы или атома.
Энергия отталкивания ядер (Enn) характеризует энергию, необходимую для разрыва межъядерных связей в молекуле химического вещества. Чем ближе к нулю или положительному значению эта величина, тем менее стабильно химическое вещество.
Анализ полученных результатов свидетельствует, что структура азатиоприна обладает высокой реакционной способностью (положительные значения теплоты образования и потенциала ионизации). Положительное значение теплоты образования свидетельствует об относительной нестабильности данной молекулы. Однако отрицательные значения Etot и Eel показывают наличие достаточной стабильности данного вещества в индифферентных средах (например, вне организма человека).
В то же время уровень потенциала ионизации показывает, что молекула азатиоприна относительно хорошо растворима в воде, следовательно, относительно быстро выводится из организма. Литературные данные свидетельствуют о том, что при приеме внутрь азатиоприн хорошо всасывается из желудочно-кишечного тракта (максимальная концентрация в крови появляется в пределах 2 часов после введения), однако период полувыведения составляет около 5 часов, что свидетельствует о достаточно быстром выведении этого препарата [20, 21, 22]
Следует отметить, что высокая реакционная способность, в целом, предполагает наличие относительной легкости взаимодействия данной молекулы с различными биологическими структурами, что хорошо согласуется с данными о его высокой биологической активности и относительно высокой токсичности.
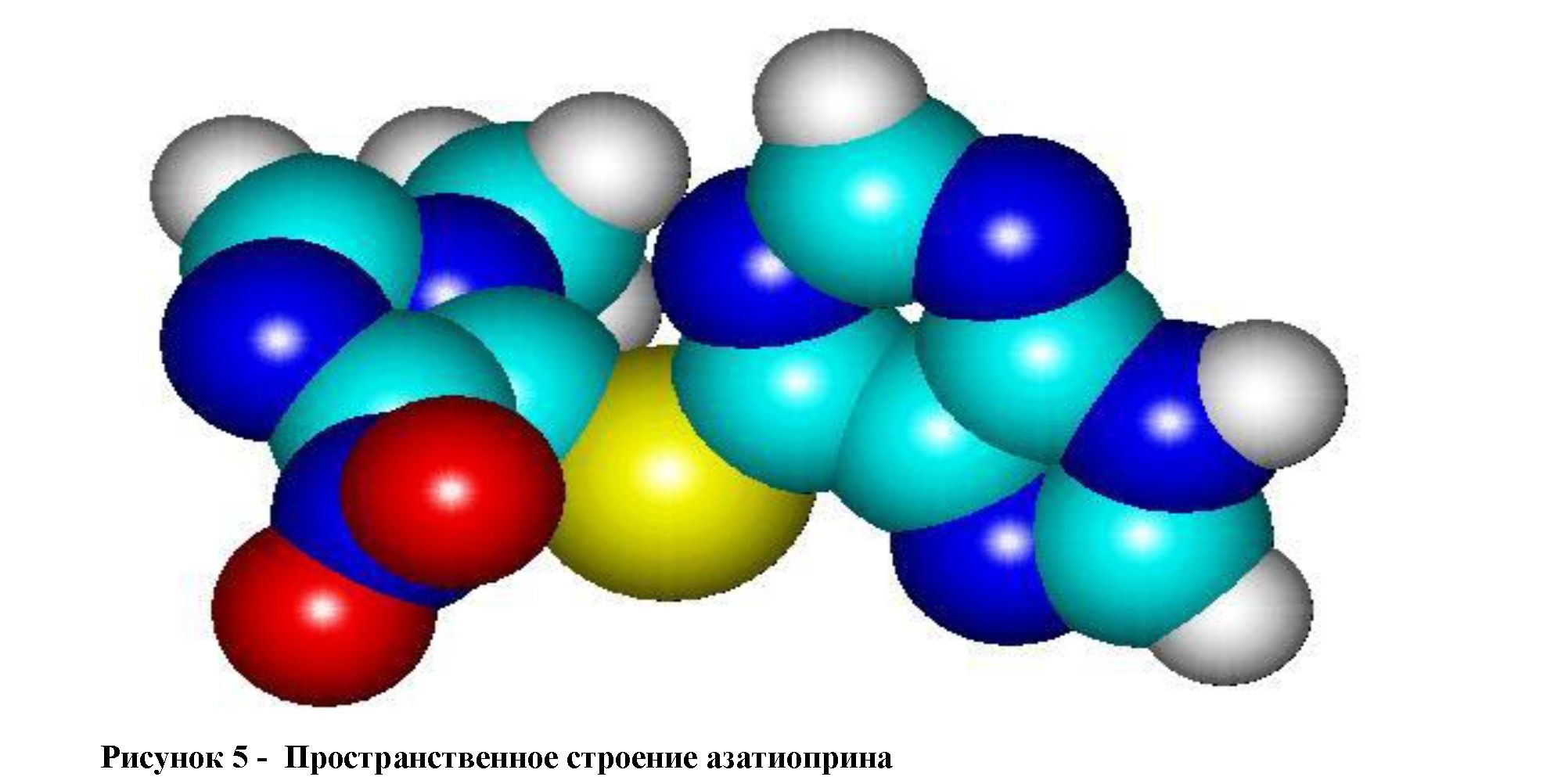
Исследования в области молекулярной механики азатиоприна свидетельствуют: все циклы плоские, отклонения менее 1о. Угол C-S-C =104.6o. 5-членный цикл повернут относительно 6членного на 99о. Группа NO2 повернута относительно 5-цикла на 91о, т.е. сопряжения с С=С 5-цикла отсутствует (порядок связи C15-N16 = 0.857).
Указанные особенности наглядно представлены в рисунке 5: молекула азатиоприна значительно меньше, чем молекула циклоспорина, все плоскости плоские, из-за чего доступны для взаимодействия все её фрагменты.
|
Наименование препарата |
AHf, ккал/мол |
Etot, ккал/мол |
IP, эВ |
Eel, ккал/мол |
Enn ккал/мол |
|
Азатиоприн |
97.13 |
-3078.65866 |
9.473 |
-19824.26110 |
16745.602439 |
Таблица 1- Основные энергетические характеристики азатиоприна: теплота образования AHf, полная энергия Etot, потенциал ионизации IP, полная электронная энергия Eel энергия отталкивания ядер Enn
Полученные методами компьютерной химии данные о высокой биологической доступности азатиоприна хорошо согласуются с выше представленными результатами, свидетельствующими о его высокой биологической активности и, в частности способности влиять на индукцию цитокинов. То есть методы компьютерной химии, позволяют достоверно прогнозировать выраженность биологической активности иммунокомпететных лекарственных средств типа азатиоприна.
Выводы: Компьютерные химические исследования имеют ценность при прогнозировании биологической активности иммунокомпетентных лекарственных средств с цитотоксическими свойствами и дают новые сведения о биологических эффектах этих препаратов.
62
ЛИТЕРАТУРА
- Nicolova N., Javorska J. Approaches to Measure Chemical Similarity// Review QSAR Comb. Sciences, 2003, 22, 1006 - 1026
- Perun T.J., Propst C.L. Computer-Aided Drug Design: Methods and Applications (Hardcover) Marcel Dekker Ink New-York and Basel, 2010, 485 с
- Фрейдлин И.С. Иммунная система и ее дефекты. www.MedBookAide
- Ройт А. Основы иммунологии. М.: Мир, 1991. - 328 с.
- Benjamini E., Sunshine G., Leskowitz S. Immunology, a short course. WILEY-LISS, New York, 1996, 451 p.
- Bona C., Bonilla F. Textbook of immunology, second ed., Harwood Acad. Publ., Amsterdam, 1996, 406 p.
- Gordon S., Clarke S., Greaves D., Doile A. Molecular immunobiology of macrophages: recent progress // Current Opinion in Immunology, 1995, v. 7, P. 24
- Лутай М.И., Гавриленко Т.И., Корнилина Е.М., Якушко Л.В., Ломаковский А.Н., Лутай Я.М. Цитокининдуцирующая активность мононуклеаров периферической крови у больных со стабильной и нестабильной стенокардией. http://banner.kyev.ua
- Секачева М.И. Лекарственная терапия воспалительных заболеваний кишечника: что выбрать практическому врачу?//Русский медицинский журнал, 2005, т 7, №1, с 50 - 56
- Румянцев В.Г. Стратегия медикаментозной терапии болезни Крона // Лечащий врач, 2005, №6. www.proctolog.ru
- Руденко И.Б. Цитостатики в дерматовенерологии. //Здоров’я Украіни, №126 http://health.ua.com
- Никитин И.Г., Сторожаков Г.И. Современные аспекты терапии аутоиммунного гепатита. http://Pharmateca.ru
- Ананьева М.Н., Николенко Ю.И., Звягина Т.В., Гринь В.К., Щукин И.Н., Баркалов А.П., Михайличенко В.Ю. Новые подходы к иммунокорригирующей терапии системной красной волчанки в эксперимента на животных и у больных.// Украина, Вестник гигиены и эпидемиологии, т 6, № 1, 2002, с 47 - 50
- Carmichael J., DeGraff W.G., Gazdar A.F., Minna J.D. Mitchell J.B. Evaluation of a tetrazolium-based semiautomated colorimetric assay: assessment of chemosensitivity testing//Cancer Research.-1987.-V. 47.-P.936-942
- Хедвиг П.. Прикладная квантовая химия. М.: Мир, 1977.
- Пчелкина З. Различные приближения для расчета электронной структуры твердых тел: область применения и ограничения. Лаборатория рентгеновской спектроскопии. Институт физики металлов. УрО РАН, г Екатеринбург http://impo.imp.uran.ru.
- Барбуто Х.А.М., Херш Э.М., Салмон С.И. Иммунофармакология. В кн: Базисная и клиническая фармакология (ред Катцунг Б.Г.). С-Петербург, 2000, т.2, с 463 - 486.
- Schroder K, Hertzog PJ, Ravasi T, Hume DA Interferon-gamma: an overview of signals, mechanisms and functions. // J Leukoc Biol. 2004 Feb;75(2), p 163-89.
- Ganesh Raghu, M.D., Kevin K. Brown, M.D., Williamson Z. Bradford, M.D., Ph.D., Karen Starko, M.D., Paul W. Noble, M.D., David A. Schwartz, M.D., Talmadge E. King, Jr., M.D. A Placebo- Controlled Trial of Interferon Gamma-1b in Patients with Idiopathic Pulmonary Fibrosis //The New England Journal of Medicine, Vol 350, No 2, 2004, p 125 - 133
- Машковский М.Д.. Лекарственные средства. М.: Медицина, 2000.
- Оксфордский справочник по клинической фармакологии (ред Г. Грэхам-Смит), М.: Медицина, 2000 г.
- Лоуренс Д.Р., Беннет П.Н., Браун М.Дж. Клиническая фармакология. М.: Медицина, 2002 г, с 540 - 561