АННОТАЦИЯ
В нашей работе изучена возможность компьютерного моделирования действия известного иммуномодулятора ликопида на систему маркофагов с использованием квантово-химических расчетов. Полученные результаты хорошо согласуются с данными о высокой биологической активности ликопида и, в частности с его способностью стимулировать индукцию цитокинов даже в том случае, когда мононуклеар самостоятельно не индуцирует их. Цитокининдуцирующее действие ликопида также хорошо согласуется с данными о потенциале ионизации, свидетельствующими о том, что данный препарат обладает высокой биодоступностью, в том числе и в клетки. То есть методы компьютерной химии, и, в частности, квантовой химии, позволяют в определенной степени прогнозировать выраженность биологической активности иммунокомпететных лекарственных средств типа ликопида.
Ключевые слова: иммуномодулятор, индукция, цитокины, ликопид, квантовая химия.
Компьютерная химия - одна из динамично развивающихся отраслей современной науки. В сферу её интересов входят химические науки, физическая химия, молекулярная биология, фармация, фармакология и т.д. Одним из наиболее перспективных применений компьютерной химии, на наш взгляд, является иммунобиология.
Как известно, компьютерная химия состоит из двух основных разделов: квантовой химии и молекулярной механики.
Методами квантовой химии изучается стабильность структур новых соединений, их реакционная способность и, следовательно, взаимодействие с различными другими химическими (в том числе и биологическими) структурами.
Современные компьютерные технологии, например, Structure Activity Relationships (SAR), способны воссоздать структуру любого биологического объекта в трехмерном изображении, а технологии компьютерного конструирования (Computer Assisted Design/CAD) используются для построения новых молекул, которые теоретически должны обладать способностью вступать во взаимодействие с ферментом или рецептором. Полученная информация широко используется при компьютерном моделировании процесса взаимодействия [1, 2].
Исходя из этого, мы предположили о возможности использования методов компьютерной химии для изучения механизма действия биологически активных веществ на пролиферативную активность мононуклеарных клеток периферической крови человека.
Как известно, существуют первичные и вторичные органы иммунной системы, которые ответственны за размножение, созревание и функционирование иммунокомпетентных клеток.
Последние находятся в состоянии рециркуляции (обмена) клетками между кровью, лимфой и лимфоидными органами. Это необходимо для реализации специфического иммунного ответа, так как иммунная система должна быть готова ответить на любой из множества чужеродных антигенов, попадающий в любой участок тела. Поскольку каждый отдельный антиген распознается лишь очень небольшой частью популяции лимфоцитов, только постоянная рециркуляция может создать условия для встречи каждого антигена с единичными лимфоцитами, несущими специфические для него антиген-распознающие рецепторы. В органах иммунной системы, где происходит эта встреча, разыгрывается взаимодействие антиген-специфических лимфоцитов с другими клетками, выполняющими роль вспомогательных, участвующими в запуске иммунного ответа и в его эффекторной фазе, к которым относятся дендритные клетки, мононуклеарные фагоциты, гранулоциты и др. [3]
Наиболее крупную популяцию иммунокомпетентных клеток составляют лимфоциты.
Вторую крупную популяцию клеток иммунной системы составляет система мононуклеарных фагоцитов, которая включает происходящие из единой стволовой клетки костномозговые предшественники - монобласт и промоноцит, циркулирующий в крови моноцит и зрелые тканевые макрофаги. Мононуклеарные фагоциты обеспечивают в значительной степени неспецифическую защиту организма за счет своей фагоцитарной функции. Секретируемые макрофагами молекулы выполняют эффекторные и регуляторные функции.
При формировании специфического иммунного ответа макрофаги выполняют функцию представления (презентации) антигена. Для этого захваченный макрофагами антиген подвергается переработке в фаголизосомах. Образующиеся в результате ограниченного протеолиза пептидные фрагменты антигена комплексируются с молекулами антигенов главного комплекса гистосовместимости класса 2 и выставляются на мембране макрофага в форме, доступной для распознавания Тлимфоцитами. Кроме того, секретируемые макрофагами цитокины, в частности интерлейкин-1, способствуют активации Т-лимфоцитов при их ответе на антиген. Участие макрофагов в эффекторной фазе специфического иммунного ответа проявляется, в частности, их мобилизацией в очаг иммунного воспаления под влиянием лимфоцитарных продуктов. Другие цитокины лимфоцитарного происхождения, в частности интерферон-гамма, способны активировать макрофаги: повысить их микробицидность и цитотоксичность. Такие активированные макрофаги выполняют функции основных эффекторных клеток клеточно-опосредованного иммунного ответа. Макрофаги также принимают участие в эффекторной фазе гуморального иммунного ответа, захватывая и уничтожая патогенные бактерии, опсонизированные специфическими антителами и комплементом. Для этого на мембране макрофагов экспрессированы специальные рецепторы для иммуноглобулинов FcR и для комплемента - CR1 [3, 4, 5, 6, 7].
Таким образом, макрофаги являются одним из важнейших компонентов неспецифической защиты организма. Следовательно, важнейшее значение имеет также изучение влияния различных иммунокомпетентных лекарственных средств на функционирование макрофагов.
В нашей работе изучена возможность компьютерного моделирования действия известного иммуномодулятора ликопида на систему маркофагов с использованием квантово-химических расчетов.
Как известно, ликопид — синтетический аналог универсального фрагмента клеточных стенок бактерий — глюкозаминилмурамилдипептида (ГМДП), оказывающего иммуномодулирующее действие. ГМДП входит в состав клеточных мембран всех бактерий и является природным модулятором иммунной системы, поэтому воздействие на организм человека ликопида в наибольшей степени приближено к процессу естественной иммунорегуляции [8].
.Материалы и методы.
Подготовка образца крови.
Эксперименты проводили на периферической крови, полученной от одного здорового донора. Забор крови производили натощак из локтевой вены с соблюдением правил асептики в одноразовый 50-миллилитровый пластиковый контейнер, содержащий стерильный 6 % раствор ЭДТА. Объемное соотношение кровь/ЭДТА составляло 20/1. Затем кровь перемешивали с полиглюкином в соотношении 1:1 и инкубировали при комнатной температуре в течение 1-1,5 ч. По завершению инкубации взвесь клеток без эритроцитов декантировали в чистый контейнер и центрифугировали при 1000 об./мин в течение 10 мин при комнатной температуре. Удаляли надосадочную жидкость, клеточный осадок разбивали постукиванием по дну контейнера и добавляли 1 мл среды RPMI-1640. Все процедуры выполняли в стерильном кабинете.
Фракционирование мононуклеаров на градиенте плотности.
В центрифужную пробирку вносили 1 мл изопака (Sigma, США) с плотностью 1,076 г/мл. Затем осторожно наслаивали 1 мл клеточной суспензии. Осаждали на центрифуге 3К30 при 3000 об./мин в течение 20 мин при температуре ротора 8оС. По окончанию центрифугирования интерфазное кольцо клеток собирали в 50-милилитровый контейнер, добавляли 20 мл среды RPMI- 1640 и отмывали от примесей изопака центрифугированием при 1000 об./мин в течение 10 мин при комнатной температуре. После центрифугирования супернатант удаляли, встряхивали клеточный осадок постукиванием по дну контейнера и добавляли к осадку 1 мл полной культуральной среды RPMI-1640, содержащей 10% фетальной телячьей сыворотки (ФТС), 4 мМ L-глутамина, 100 мг/мл стрептомицина и 100 МЕ/мл пенициллина.
Оценка количества и жизнеспособности мононуклеарных клеток.
Для оценки жизнеспособности клеток в суспензии использовали тест на исключение красителя трипанового синего. К суспензии клеток добавляли равное количество раствора трипанового синего, перемешивали встряхиванием и подсчитывали количество окрашенных и неокрашенных клеток в гемоцитометре Горяева под микроскопом.
Культивирование клеток.
Суспензию полученных клеток доводили до концентрации 106 кл./мл полной культуральной средой и вносили по 200 мкл в 96-луночный планшет. Клетки культивировали при 37оС в атмосфере с 5% СО2 и 95% влажности в СО2-инкубаторе в течение 48 ч. В опытные ячейки вносили тестируемый препарат в концентрации, равной концентрации рекомендуемой разовой дозе препарата из расчета на 5 л крови.
Приготовление рабочих разведений препаратов.
Рабочие разведения ликопида готовили следующим образом: таблетку ликопида (1 мг) тщательно растирали в ступке и растворяли в 5 мл среды RPMI-1640. Полученную взвесь центрифугировали при 5000 об./мин в течение 5 мин. Супернатант стерилизовали, пропуская через стерильный мембранный фильтр с диаметром пор 0,22 мкм. Раствор ликопида в концентрации 2 мкг/мл добавляли в ячейки с клетками в объеме 20 мкл на каждые 180 мкл клеточной суспензии, получая конечную концентрацию препарата 0,2 мкг/мл.
Оценка пролиферации клеток в МТТ-тесте /9/.
За 4 ч до окончания культивирования в каждую ячейку вносили по 250 мкг/мл МТТ (3-(4,5- диметилтиазол-2-ил)-2,5-дифенилтетразолиум бромид). По окончанию опыта из лунок удаляли супернатант, образовавшиеся кристаллы формазана растворяли ДМСО и колориметрировали при 570 нм.
Индекс пролиферации (ИП) клеток вычисляли по формуле:
ИП=О/Кх100%, где О - среднее значение экстинкции из 5 повторов в опыте, К - то же самое в контроле (в отсутствии лекарственного препарата) [9].
Определение цитокинов.
В части ячеек, в которые не вносили МТТ, определяли продукцию цитокинов с помощью иммуноферментного анализа, используя коммерческие тест-системы (IFND , IL-IIZI, IL-15, - R&D Systems, Великобритания; IL-13, IL-12 - Diaclone, Франция) согласно прилагаемым инструкциям. По окончанию инкубации планшеты центрифугировали для осаждения клеток (10 мин при 400g). Бесклеточные супернатанты собирали, замораживали и хранили при -70оС до определения в них цитокинов.
Компьютерный химический анализ
Была изучена молекулярная механика и реакционная способность ликопида.
Расчеты осуществлены с применением метода Хартри-Фока в полуэмпирическом приближении РМ3 (Parametrization Method 3) [10].
Статистический анализ
Полученные данные обрабатывали методами математической статистики, используя прикладную программу Microsoft Excel. Вычисляли среднюю арифметическую, среднюю квадратическую ошибку средней арифметической и достоверность различия средних (Р), используя функцию ТТЕСТ.
. Результаты исследования.
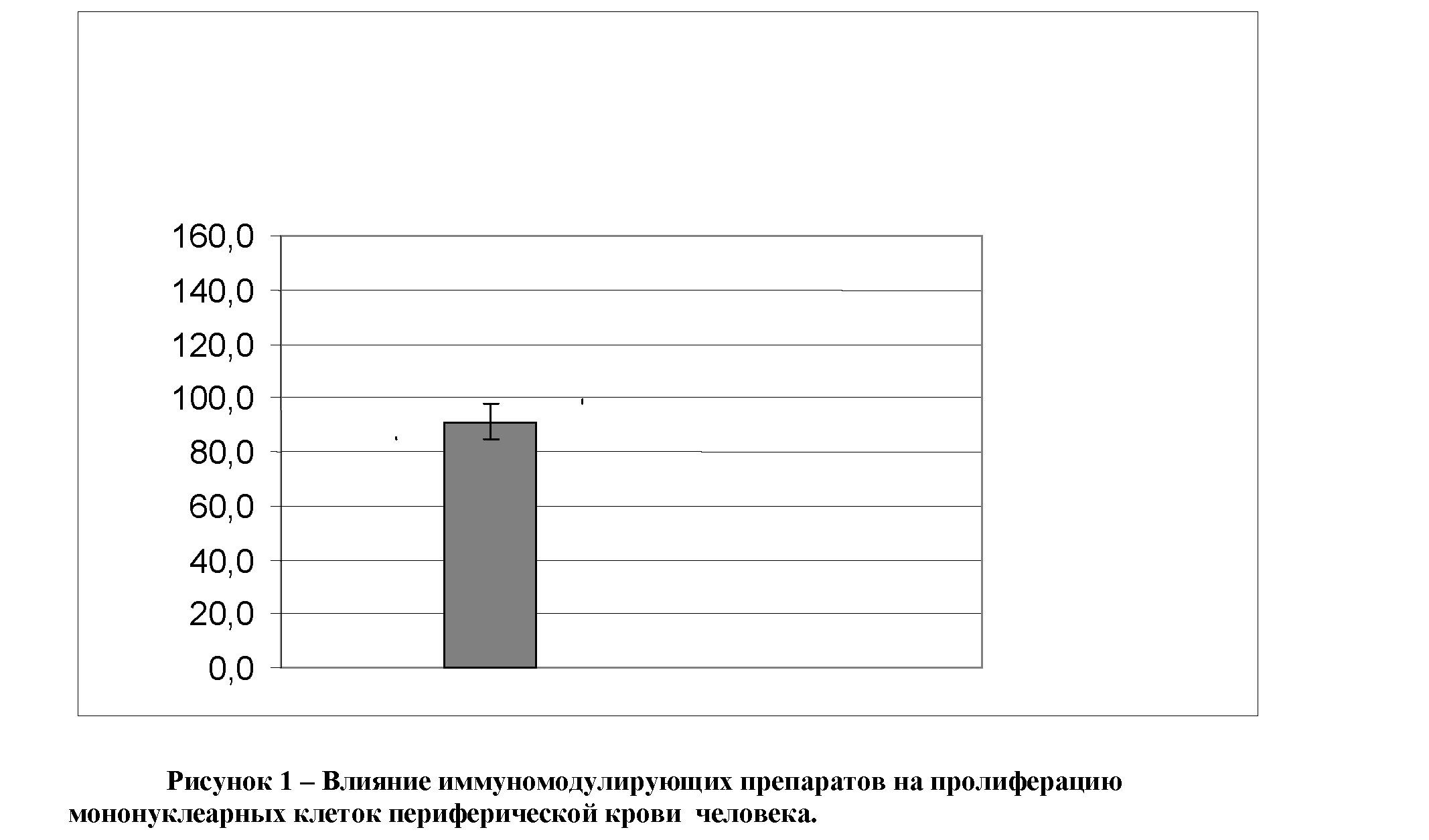
Анализ влияния ликопида на пролиферативную активность мононуклеарных клеток периферической крови человека показал, что в исследованной концентрации он не оказывал значимого воздействия на пролиферацию при культивировании в течение 48 ч (рисунок 1).
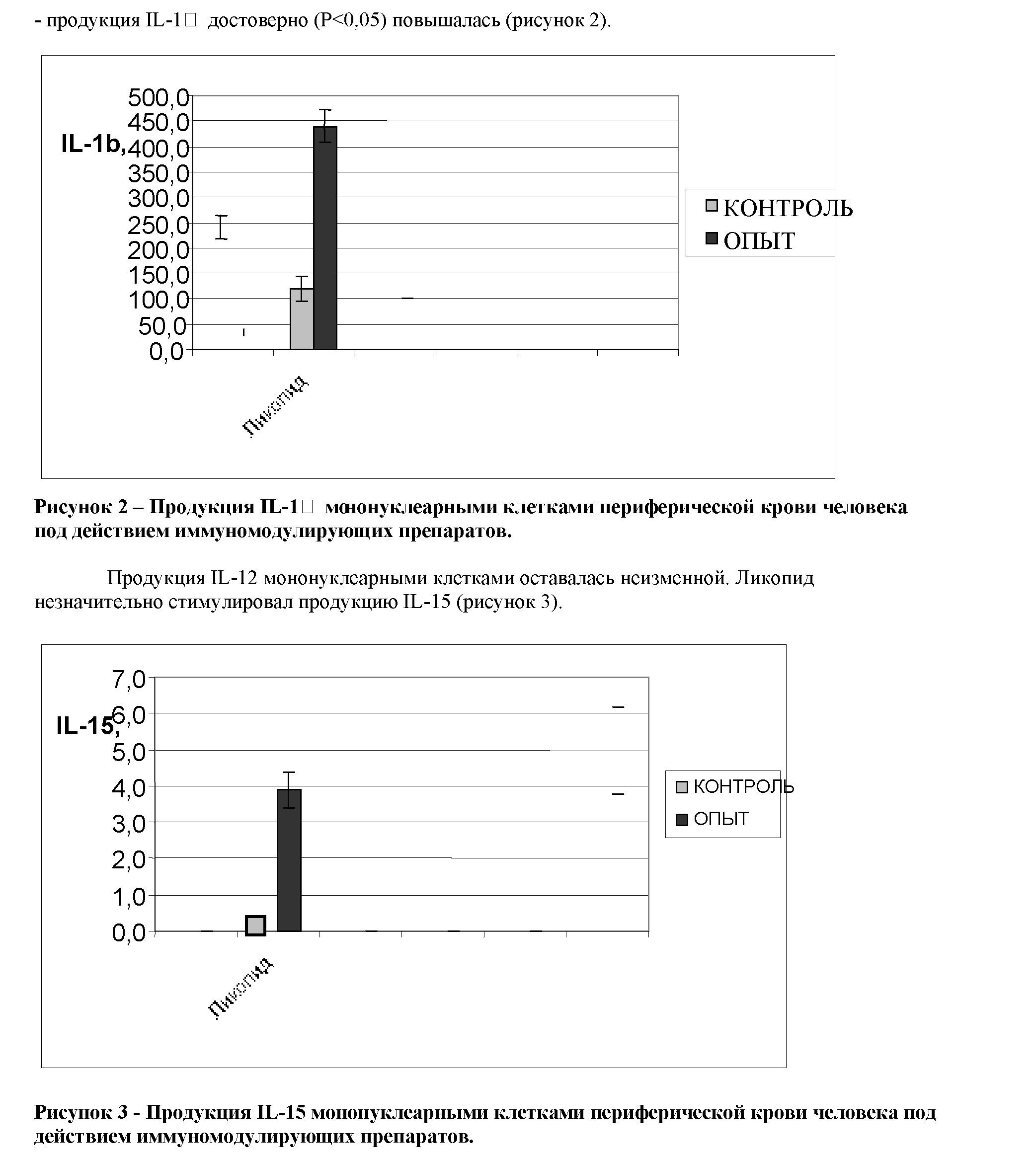
Оценка продукции цитокинов культурой мононуклеарных клеток под действием ликопида показала следующие результаты:
Ликопид значимо (более 250 нг/мл, в контроле - 0 нг/мл) стимулировал продукцию IFND (P<0,05).
В то же время он не влиял на продукцию супрессорного цитокина IL-13.
Таким образом, действие ликопида на мононуклеары в основном проявляется через стимуляцию цитокинов, даже в тех случаях, когда не обнаруживается их естественная продукция в процессе культивирования.
Квантово-химические характеристики ликопида представлены в таблице 1.
 68
68
Для анализа нами отобраны: теплота образования (AHf, ккал/мол), полная энергия (Etot ) и потенциал ионизации (IP). Это основные квантово-химические характеристики, которые позволяют оценить стабильность соединения, его способность преодолевать биологические барьеры и взаимодействовать с различными биологическими структурами.
Теплота образования (энтальпия образования, ДИ!) - тепловой эффект реакции образования химических соединений из простых веществ в стандартном состоянии. Данная характеристика также служит показателем стабильности соединения, так как дает количественную оценку энергии, необходимой для разрушения молекулы химического вещества. Отрицательная величина обозначает высокую стабильность вещества. Положительное или нулевое значение означает, что вещество быстро распадается. Расчет теплоты образования позволяет дополнительно оценить правильность расчета Etot: обе энергетические характеристики при правильном расчете должны иметь примерно одинаковые значения.
Полная энергия (Etot ) - сумма кинетической и потенциальной энергий, т.е. общий
энергетический потенциал молекулы. Она характеризует стабильность соединения и, следовательно, возможность создания из него перспективной для фармацевтического производства лекарственной формы. С другой стороны количественная характеристика стабильности позволяет оценить возможности гидролиза вещества в организме и продолжительность его действия.
Потенциал ионизации (IP) - это физическая величина, определяемая отношением наименьшей энергии, необходимой для однократной ионизации атома (или молекулы), находящегося в основном состоянии, к заряду электрона. Потенциал ионизации — мера энергии ионизации, которая равна работе вырывания электрона из атома или молекулы и характеризует прочность связи электрона в атоме или молекуле. Потенциал ионизации характеризует растворимость соединения в различных средах и его реакционную способность. Чем выше значение потенциала ионизации, тем лучше растворимость соединения и его способность вступать в различные реакции. Исходя из выше изложенного очевидно, что потенциал ионизации - один их основных показателей, характеризующих способность биологически активного вещества вступать во взаимодействие с теми или иными молекулами. Следовательно - это важный показатель для понимания механизма взаимодействия биологически активного вещества с рецепторами или другими молекулами-мишенями клеточных структур организма млекопитающих.
Анализ квантово-химических характеристик свидетельствует о том, что, в целом, ликопид обладает высокой стабильностью (отрицательные значения теплоты образования, низкий уровень полной энергии, который свидетельствует о необходимости приложения больших энергетических усилий для разрыва межатомных связей). Положительное значение потенциала ионизации свидетельствует об относительно высокой растворимости и реакционной способности. То есть, этот препарат относительно легко преодолевает биологические барьеры, хорошо абсорбируется в ткани и, в частности, в иммунокомпетентные органы и клетки, что подтверждается литературными данными о его высокой биологической активности
Таблица 1 - Основные энергетические характеристики ликопида
|
Наименование препарата |
Теплота образования AHf, ккал/мол |
Полная энергия Etot, ккал/мол |
Потенциал ионизации IP |
|
Ликопид |
-539.15 |
-8673.622 |
9.170 |
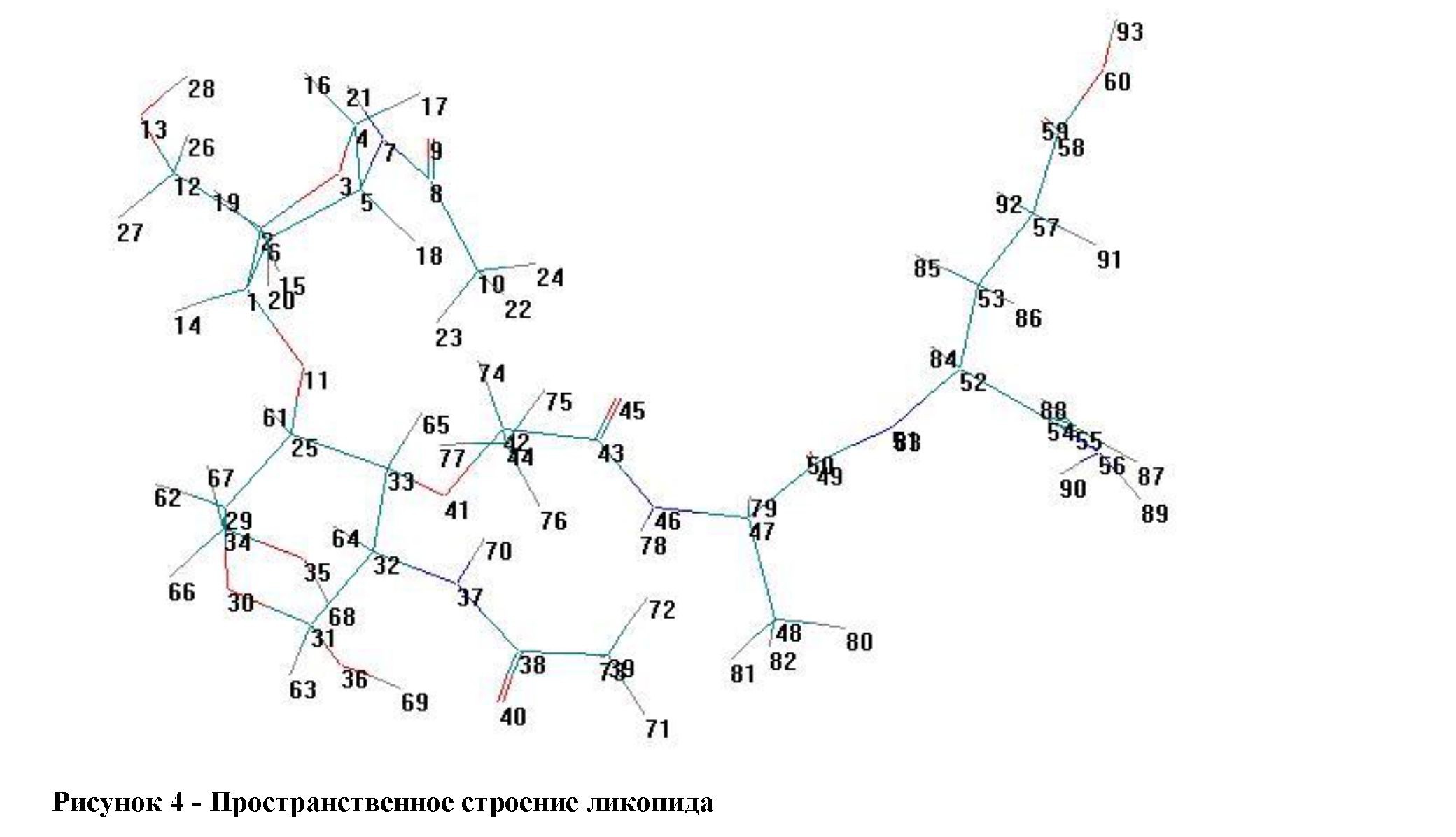
Исследования в области молекулярной механики ликопида свидетельствуют, что оба пирановых кольца имеют конформацию в форме кресла (рис 4). То есть, в целом, структура ликопида «открыта» для различного рода взаимодействий, ядра расположены в относительной глубине структуры, что предопределяет поверхностное положение электронных орбиталей. При этом электронные орбитали не перекрываются, то есть вся структура ликопида предполагает наличие донорно-акцепторных взаимодействий и, следовательно, относительно высокую аффинность к многим биологическим структурам.
Полученные результаты хорошо согласуются с выше представленными данными о высокой биологической активности ликопида и, в частности с его способностью стимулировать индукцию цитокинов даже в том случае, когда мононуклеар самостоятельно не индуцирует их. Цитокининдуцирующее действие ликопида также хорошо согласуется с данными о потенциале ионизации, свидетельствующими о том, что данный препарат обладает высокой биодоступностью, в
том числе и в клетки. То есть методы компьютерной химии, и, в частности, квантовой химии, позволяют в определенной степени прогнозировать выраженность биологической активности иммунокомпететных лекарственных средств типа ликопида.
Выводы:
Компьютерные химические исследования имеют определенную ценность при прогнозировании биологической активности ипммуномодуляторов и дают новые сведения о биологических эффектах этих лекарственных средств.
СПИСОК ЛИТЕРАТУРЫ
- N. Nicolova, J. Javorska - Approaches to Measure Chemical Similarity// Review QSAR Comb. Sciences. - 2003. - 22, P. 1006 - 1026.
- T.J. Perun, C.L. Propst - Computer-Aided Drug Design: Methods and Applications (Hardcover) // Marcel Dekker Ink New-York and Basel. - 2010. - 485 p.
- Фрейдлин И.С. Иммунная система и ее дефекты // MedBookAide. -medbookaide.ru/ books/ fold9001/ book2032/content.php.
- Ройт А. Основы иммунологии // М.: Мир. - 1991. - 328 с.
- E. Benjamini, G. Sunshine, S. Leskowitz - Immunology, a short course // WILEY-LISS. - New York, 1996. - 451 p.
- C. Bona, F. Bonilla - Textbook of immunology, second ed., // Harwood Acad. Publ. - Amsterdam, 1996. - 406 p.
- S. Gordon, S. Clarke, D. Greaves, A. Doile - Molecular immunobiology of macrophages: recent progress // Current Opinion in Immunology, 1995. - V. 7. - P. 24-8.
- J. Carmichael, W.G. Degraff, A.F. Gazdar, J.D. Minna, J.B. Mitchell - Evaluation of a tetrazolium-based semiautomated colorimetric assay: assessment of chemosensitivity testing // Cancer research. - 1987. - V. 47. - P. 936 - 942.