АННОТАЦИЯ
В работе представлена клиническая и лабораторная характеристика 115 больных с инфравезикальной обструкцией различной этиологии, прошедших углубленное обследование при условии комплексного хирургического лечения. Целью исследования явилось углубленное изучение метаболических процессов тиолового обмена детрузора мочевого пузыря у наблюдаемых больных. Полученные данные, касающиеся изменений содержания в крови больных тиоловых и дисульфидных групп белков, глютатиона, а также уровня активности глютатионовых ферментов подтвердили наличие у наблюдаемых пациентов состояния оксидантного стресса, который приводит к нарушениям тиолового статуса в биологических жидкостях и тканях мочевого пузыря, и позволили раскрыть его существенные патогенетические механизмы.
Сделан вывод о целесообразности коррекции глютатионового статуса при комплексном хирургическом лечении больных с инфравезикальной обструкцией.
Ключевые слова: инфравезикальная обструкция, метаболические процессы, тиоловый статус, оксидантный стресс.
Введение.
Патологические состояния, обладающие общими морфо-функциональными чертами и закономерностями развития, объединенные понятием «инфравезикальная обструкция» (ИО) - клинически ассоциированы с симптомами нижних мочевых путей (СНМП) более, чем у 30% мужчин и 25% женщин в возрастных группах старше 60 лет. Современные данные подтверждают, что названный пропорциональный уровень достигает соответственно 45% и 35% в возрастных группах старше 70 лет. [1,2,3.5,7 ]
Патогенетически значимым относительно ИО является ряд факторов, обуславливающих прогрессию этого патологического состояния. К ним относятся:
механические факторы ( ДГПЖ, стенотические изменения шейки мочевого пузыря и уретры);
чрезмерная а-адренегргическая активность, определяющая рост уретрального давления;
снижение стромально-эпителиального соотношения и связанных с ним структурными изменениями тканей мочевого пузыря;
нейротрансмиттерные нарушения (угнетение не адренергических и не холинергических действующих факторов);
влияние воспалительного процесса в мочеполовой системе. [3,4 ]
Клинические проявления СНМП у больных с ИО обусловлены снижением эластических свойств, ишемией детрузора, а также ультраструктурными изменениями, в частности оксидацией протеинов, связанными с нарушениями энергетического метаболизма в тканях мочевого пузыря и уретры.[6,8,9 ]
Ишемия детрузора и ее следствие развитие хронической гипоксии его тканей приводят к развитию состояния гипоксического стресса, к которому наиболее чувствительными выявились стромальные элементы, в отличие уротелиальных и мышечных компонентов детрузора. [8,9,10 ]
Анализ данных, полученных нами ранее, относительно уровня содержания глутатиона и изменений активности глутатионовых ферментов в крови больных с ИО свидетельствует о наличии состояния оксидативного стресса, что является важным патогенетическим звеном в развитии и прогрессировании инфравезикальной обструкции. [11], а полученные результаты следует рассматривать как клинико-биохимическое обоснование целесообразности коррекции глутатионового статуса в комплексном хирургическом лечении больных с ИО.
Целью исследования явилась оценка клинической эффективности метаболизм- корригирующей терапии в комплексном хирургическом лечении больных с ИО в условиях наличия биоенергетических нарушений в организме пациентов в целом и в детрузоре.
Материалы и методы.
Под наблюдением находились 115 больных с инфравезикальной обструкцией и продолжительностью заболевания от 2 до 14 лет, которые в соответствии с результатами предшествовавшего детального обследования подлежали хирургическому лечению. Клинические проявления СНМП были обусловлены ДГПЖ второй степени в 74 наблюдениях (63,3%), стенозом шейки мочевого пузыря в 20 случаях (17,4%), стриктурами и стенозами уретры, имевшими место у 21 пациента (18,3%). Возраст больных находился в пределах от 65 до 83 лет. Ранее консервативному лечению подвергались 72 (62,6%), хирургическим методам лечения - 11 (9,6%), не получали лечение - 32 (27,8%) пациента.
Уродинамическими исследованиями установлено, что средняя объемная скорость мочеиспускания у наблюдаемых больных составляла 4,8±0,8мл/сек, а максимальная 9,7±1,4 мл/сек. Биохимические исследования проводились с использованием крови и мочи больных с ИО, которым проводились предварительные клинические обследования. В плазме крови определяли активность глутатион^-трансферазы, а в гемолизате крови - активность глутатион-пероксидазы и глутатион-редуктазы. В депротеинизованном и нейтрализованном экстракте крови определяли содержание тиоловой и дисульфидной формы глутатиона. Аналогичному исследованию были подвергнуты биоптаты тканей мочевого пузыря. Одновременно определялось содержание тиоловых и дисульфидных групп белков в крови и моче пациентов.
В последующем в 37 (32,2%) случаях выполнена ТУРП, в 14 (12,2%) наблюдениях - трансуретральная инцизия шейки мочевого пузыря, у 16 (13,9%) больных - внутренняя оптическая уретротомия и у 48 (41,7%) больных черезпузырная аденомэктомия. С целью коррекции выявленных изменений метаболического гомеостатаза больных, а также восстановления нарушений биоэнергетических процессов тиолового обмена тканей детрузора, нами назначался 59 больным из исследуемой группы (І) в послеоперационном периоде препарат КудесанQ10. Последний обладает выраженным антиоксидантным эффектом, активирует окислительно-восстановительные процессы, стимулирует процессы клеточного дыхания и синтез АТФ в митохондриях клеток.
Препарат назначался по 34,5 мг per os 1 раз в день на протяжении трех недель. Контингент больных группы сравнения II, в которую входило 56 пациентов, были подвергнуты традиционному комплексному хирургическому лечению по поводу ИО разной этиологии.
Таблица 1 - Изменения уродинамических показателей у больных І и II группы на фоне комплексного хирургического лечения.
|
Периоды обследова ния больных подгрупп Іа(откр опер) Іб(эндо), ІІа(откр опер) ІІб(эндо) |
Уродинамические показатели |
|||||
|
Объем мочевого пузыря (У),мл |
Максимальна я скорость мочеиспуска ния (Qmax), мл/с |
Средняя скорость мочеиспуска ния (Qavr), мл/с |
Ускорение потока мочи (Ға)мл/с |
Індекс внутренне го давления (R), у.о. |
Степень обструкц ии по номогра мме Боярина |
|
|
До лечения Іа(п=25) |
381,2±18,7 |
9,5±1,6 |
4,3±1,2 |
3,3±0,6 |
0,37±0,08 |
5,8±0,4 |
|
ІІа(п=23) |
379,3±17,9 |
9,4±1,5 |
4,4±1,3 |
3,4±0,7 |
0,38±0,04 |
5,9±0,6 |
|
После лечения Іа(п=25) |
292±14,3 |
21,3±1,5* |
10,9±1,2* |
6,2±0,4* |
0,19±0,08* |
2,9±0,7* |
|
ІІа(п=23) |
299,4±14,7 |
16,9±1,2 |
7,7±1,1 |
6,0±0,3* |
0,23±0,06 |
3,0±0,5* |
|
До леченияІб (n=34) |
380,1±16,3 |
9,8±1,7 |
4,7±1,4 |
3,5±0,7 |
0,35±0,02 |
5,7±0,5 |
|
ІІб (n=33) |
378,7±15,4 |
9,6±1,7 |
4,6±1,5 |
3,3±0,2 |
0,36±0,08 |
5,8±0,7 |
|
После лечения Іб(п=34) |
279±13,9 |
24,7±1,6* |
11,2±1,3* |
6,5±0,4* |
0,18±0,07* |
2,6±0,2* |
|
ІІб (n=33) |
287,5±15,1 |
17,3±1,4 |
7,9±1,3 |
6,3±0,4* |
0,18±0,06* |
2,8±0,3* |
*Разница статистически достоверна в сравнении с данными до начала лечения (p<0,05)
С целью оценки влияния характера и объема хирургической травмы на процессы восстановления детрузора под влиянием, комбинированной с хирургическим лечением энерготропной и метаболизм-корригирующей терапии контингент наблюдаемых больных (115 человек) был разделен на две группы - I (59 больных), которая состояла из подгруппы Ia (25 больных), подвергавшихся открытым хирургическим вмешательством и Іб (34 пациента), которые подлежали эндоскопическим операциям, а также группу ІІ (56 человек), в которую соответственно входили подгруппа ІІа (23 больных), оперированных открытым способом, и подгруппа ІІб (33 пациента), подлежащих эндоурологических операциям.
Результаты и их обсуждение.
Клиническая эффективность применения метаболизм-коррегирующей, энерготропной терапии определялась по результатам клинико-лабораторных, функциональных, углубленных биохимических исследований, а также в соответствии с оценкой изменения уровня «качества жизни» согласно данным анкетирования больных и 20 здоровых лиц референтной группы.
Интегративно-сравнительная оценка эффективности проведенного комплексного лечения больных предусматривала изучение изменений уродинамических показателей, выраженности СНМП, регионального кровотока мочевого пузыря, а также психосоматического статуса больных.
Характеристика изменений уродинамических показателей представлена в таблице 1.
Таблица 2 - Изменения клинической симптоматики у больных І и ІІ групп на фоне комплексного хирургического лечения.
|
Периоды обследования больных подгрупп Іа(откр опер) Іб(эндо), ІІа(откр опер) ІІб(эндо) |
Клинические симптомы |
||||
|
Дизурия, % |
Ноктурия, % |
Дневное кол-во мочеисп. |
Частота императивных позывов к мочеисп. |
Інтервалы между мочеисп., час |
|
|
До лечения Ь(п=25) |
92,0±5,9 |
3,6±0,7 |
14,7±1,2 |
2,8±0,4 |
1,4±0,6 |
|
Па(п=23) |
91,3±5,6 |
3,5±0,6 |
14,6±1,3 |
2,7±0,6 |
1,5±0,8 |
|
После лечения Ь(п=25) |
16,0±1,8* |
0,4±0,03* |
8,1±1,3* |
0,4±0,05* |
2,7±0,2* |
|
Па(п=23) |
26,1±1,9* |
1,2±0,04* |
10,2±1,6 |
1,6±0,7 |
2,1±0,3 |
|
До лечения Іб (n=34) |
82,3±4,4 |
2,7±0,4 |
12,6±1,4 |
2,2±0,3 |
1,8±0,3 |
|
ІІб (n=33) |
81,8±4,6 |
2,8±0,3 |
12,7±1,4 |
2,3±0,5 |
1,7±0,4 |
|
После лечения Іб(п=34) |
20,6±1,9* |
1,4±0,2* |
8,4±1,5* |
0,5±0,07* |
3,1±0,6* |
|
ІІб (n=33) |
24,2±1,8* |
1,5±0,3* |
9,8±1,7 |
0,9±0,08* |
2,6±0,6 |
* Разница статистически достоверна в сравнении с данными до начала лечения
Представленные данные убедительно свидетельствуют о том, что проведенное комплексное лечение достоверно улучшает функциональные показатели нижним мочевых путей у больных исследуемой группы, в то же время позитивная динамика у больных группы сравнения (II) имеет менее выраженный характер.
Характеристика клинических особенностей течения послеоперационного периода у больных исследуемой (I) группы и группы сравнения (II) представлена в таблице 2.
Исходя из представленных данных проведение комплексного хирургического лечения у больных (I) группы обеспечивает статистически достоверное снижение частоты дизурии, ноктурии, императивных позывов, позволяет оптимизировать продолжительность интервалов между мочеиспусканиями. В ограниченном количестве наблюдений, сохранение выраженности СНМП в послеоперационном периоде связано с активизацией хронической инфекции мочевых путей у больных подвергавшихся удалению или разрушению вторичных камней мочевого пузыря. Одновременно следует отметить, пациентов группы сравнения (II) показатели характеризующие детрузорные функции накопления и опорожнения были восстановлены не в полной мере, что обусловливало необходимость последующей амбулаторной медикаментозной реабилитации больных.
Результаты исследований изменений психосоматического статуса и уровня качества жизни исследуемых больных (I) группы и группы сравнения (II), представлены в таблице 3.
Таблица 3 - Изменения психосоматического статуса и уровня качества жизни исследуемых больных І и ІІ групп на фоне комплексного хирургического лечения.
|
Периоды обследования больных подгрупп Іа(откр опер) Іб(эндо), ІІа(откр опер) ІІб(эндо) |
Параметры исследования |
||||
|
Уровень астенического синдрома (по анкете астении MFI- 20) |
Болевой синдром, % |
Качество сна |
Депрессивные проявления |
Уровень качества жизни (Qol) в баллах |
|
|
До лечения Іа(п=25) |
68,7±4,5 |
84,0±2,6 |
12,02±2,11 |
13,9±2,13 |
5,4±0,6 |
|
Па(п=23) |
68,2±4,3 |
82,6±2,3 |
12,07±2,13 |
13,7±2,11 |
5,3±0,5 |
|
После лечения Ь(п=25) |
49,4±3,3 |
20,0±1,2* |
23,78±2,11* |
7,6±1,4* |
1,9±0,05* |
|
Па(п=23) |
52,3±3,2 |
26,1±1,4* |
19,13±2,12 |
8,7±1,6 |
2,6±0,09* |
|
До лечения Іб (n=34) |
59,8±3,1 |
52,9±2,2 |
12,97±1,47 |
13,2±1,9 |
4,8±0,4 |
|
ІІб (п=33) |
59,2±3,2 |
51,5±2,1 |
12,83±1,42 |
13,4±1,8 |
4,7±0,3 |
|
После лечения 16(п=34) |
47,1±3,2* |
14,7±1,1* |
23,97±1,93* |
7,2±1,5* |
1,7±0,06* |
|
ІІб (п=33) |
43,9±3,8* |
18,2±1,5* |
19,89±1,61 |
7,0±1,3* |
1,6±0,05* |
* Разница статистически достоверна в сравнении с данными до начала лечения (p<0,05)
Полученные данные продемонстрировали выраженные позитивные изменения психосоматического статуса больных, что обусловило статистически достоверное повышение уровня (качества жизни) больных исследуемой группы. Положительные изменения психосоматического статуса и уровня «качества жизни» больных (II) группы в большей мере было присущим пациентам группы (Пб), комплексное лечение которых включало малотравматичное эндоскопическое лечение. Часть контингента больных подгруппы Па, которые были подвержены традиционному открытому хирургическому лечению, на амбулаторном этапе получала дополнительную медикаментозную терапию.
Изучены также изменения регионального артериального и венозного кровотока в мочевом пузыре больных Iu Пгрупп, которые представлены в таблице 4.
Таблица 4 - Изменения регионального артериального и венозного кровотока моченого пузыря у исследуемых больных І та ІІ групи на фоне комплексного хирургического лечения.
|
Периоды обследов ания больных подгруп п Іа(откр опер) Іб(эндо), ІІа(откр опер) ІІб(эндо) |
Параметри дослідження |
||||||
|
Макс. Систолич . скорость ^max), м/с |
Макс. Диастол ич. скорость ^max), м/с |
Пульсовой индекс (Ri/од) |
индекс перифер. сосудистог о давленя (Ri), м/с |
Плотнос ть сосудист . рисунка, мм2 |
Пиков ая систол. скорос ть кровот ока в артери ях, мм/с |
Линейна я скорость кровоток а в венах, мм/с |
|
|
До лечения Ь(п=25) |
0,091±0,0 22 |
0,037±0, 003 |
1,57±0,15 |
0,448±0,07 5 |
0,84±0,0 6 |
8,26±0, 21 |
1,94±0,1 4 |
|
Па(п=23) |
0,90±0,01 9 |
0,036±0, 002 |
1,55±0,14 |
0,476±0,06 2 |
0,83±0,0 5 |
8,25±0, 19 |
1,93±0,1 2 |
|
После лечения Іа(п=25) |
0,179±0,0 14* |
0,043±0, 005 |
1,29±0,12 |
0,639±0,11 * |
0,98±0,0 07 |
8,79±0, 03 |
2,93±0,1 3* |
|
Па(п=23) |
0,161±0,0 12 |
0,040±0, 004 |
1,34±0,13 |
0,640±0,15 |
0,96±0,0 6 |
8,58±0, 02 |
2,21±0,1 4 |
|
До лечения Іб (n=34) |
0,171±0,0 11 |
0,035±0, 007 |
1,47±0,13 |
0,479±0,02 9 |
1,01±0,0 3 |
8,11±0, 19 |
2,17±0,1 6 |
|
ІІб (n=33) |
0,170±0,0 12 |
0,036±0, 08 |
1,45±0,14 |
0,477±0,02 3 |
1,02±0,0 3 |
8,12±0, 18 |
2,16±0,1 5 |
|
После лечения Іб(п=34) |
0,312±0,0 21* |
0,058±0, 004 |
1,17±0,11* |
0,634±0,12 * |
1,14±0,1 3 |
10,11± 0,04* |
3,21±0,1 6* |
|
ІІб (n=33) |
0,231±0,0 15 |
0,049±0, 006 |
1,19±0,12* |
0,636±0,11 * |
1,12±0,1 4 |
9,57±0, 05 |
3,19±0,1 4* |
* Разница статистично достоверна в сравнении с данными до начала лечения (p<0,05)
Исходя из вышеприведенных данных, региональный артериальный и венозный кровоток в мочевом пузыре больных исследуемой группы в результате комплексного хирургического лечения характеризуется значительными позитивными изменениями, что в большей мере относится к больным, подвергавшимся эндоурологическим инвазивным вмешательствам (подгруппа Іб). Следует отметить, что представленные положительные изменения у больных группы сравнения в большей мере относились к параметрам венозного кровотока и эластических свойств периферических сосудов, в то время как адекватное восстановление артериального кровотока происходило в несколько более поздние сроки.
Оптимизация региональных уродинамических показателей обусловливает эффективное восстановление уродинамики нижних мочевых путей, устранение патологической симптоматики, существенное повышение уровня «качества жизни» в большей мере имевшие место у больных, перенесших эндоурологические вмешательства исследуемой (І) группы.
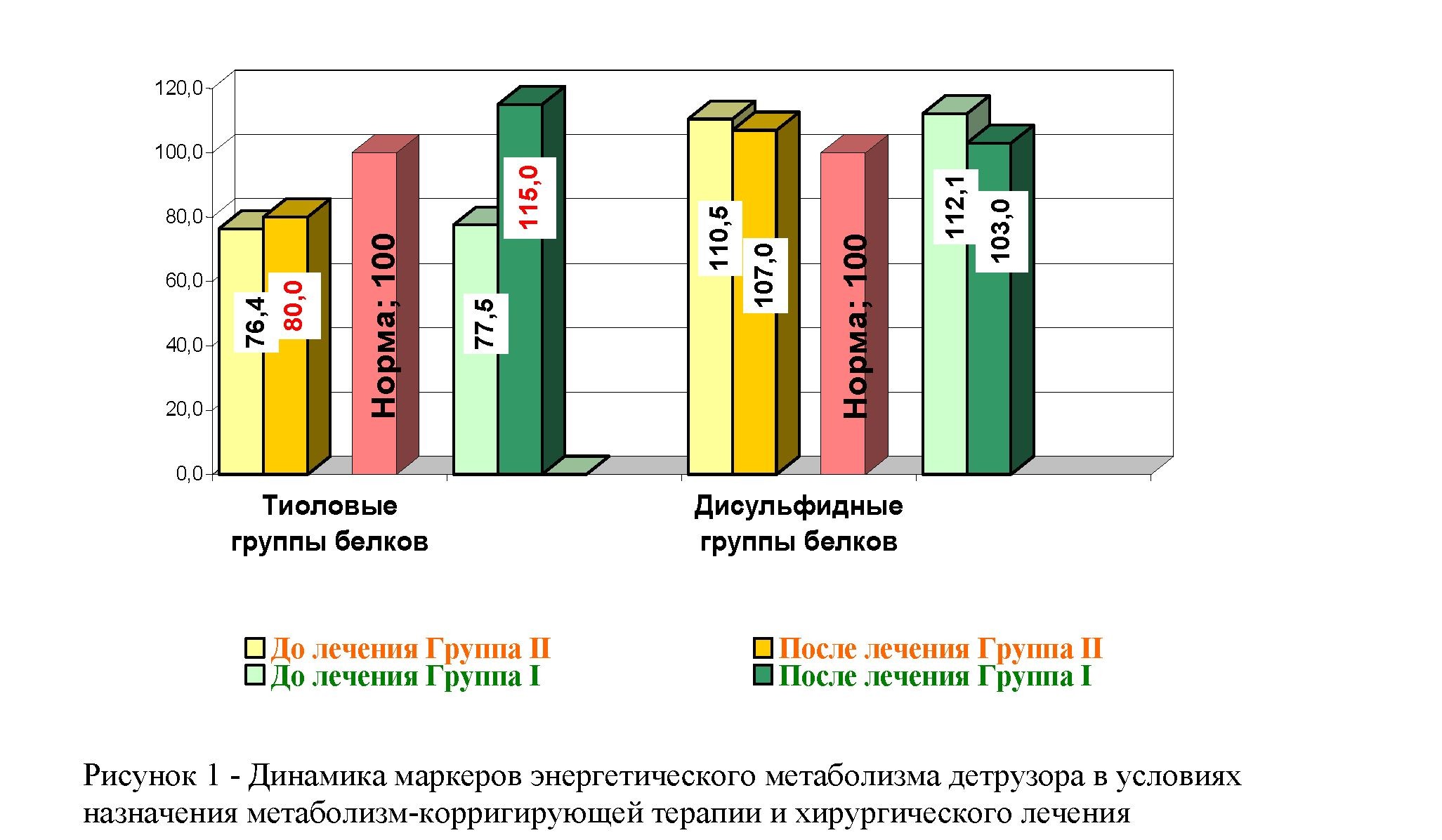
В целях изучения влияния энерготропной терапии на энергетический метаболизм детрузора, нами исследованы тиоловые и дисульфидные группы белков в ткани детрузора у больных подвергнутых хирургическому лечению по поводу инфравезикальной обструкции.(Рис.1)
Нами установлено, что при проведении традиционного хирургического лечения (группа сравнения ІІ) уровень тиоловых белковых групп в плазме крови оставался пониженным по отношению к норме и составлял 80,0% (p <0,01) в то время, как в исследуемой группе (І) при проведении комплексного хирургического лечения с одновременным назначением метаболизм-корректирующего препарата было обнаружено существенное повышение уровня тиоловых групп белков в 115,0% по отношению к соответствующему значение показателя до начала лечения.
Использование нами в комплексном хирургическом лечении метаболизм- корригирующего лечения позволило в значительной степени снизить уровень нарушений тиол-дисульфидного обмена и повысить восстановительный потенциал глютатионовои системы в организме больных с инфравезикальной обструкцией.
Заключение.
Анализ полученных клинико-биологических данных позволяет сделать ряд заключений. Так, у больных с ИО наблюдается существенное нарушение тиолдисульфидной системы в тканях мочевого пузыря и в организме в целом. Про это свидетельствует существенное снижение состава тиоловых групп белков в крови, а также по данным углубленных биохимических исследований, в моче и тканях детрузора. У больных выявлено снижение восстановительного потенциала глутатионовой системы на рубеже угнетения активности ферментов, которые обеспечивают окислительновосстановительные преобразования глутатиона и регенерацию окисленных тиоловых групп белков (глутатион-редуктаза, глугатион^-трансфераза). Выявленные нами нарушения тиол-дисульфидной системы играют важную роль в реализации биоэнергетических процессов и транспортных мембранных реакций. Все представленное следует рассматривать как важную патогенетическую ступень угнетения функциональной возможности детрузора.
Так при общем благоприятном течении послеоперационного периода, и отсутствии тяжелых осложнений в обеих группах больных, положительные изменения основных клинических и функциональных показателей оказались более значимыми у пациентов I (исследуемой) группы. У лиц I (исследуемой) группы происходило более полное восстановление функциональной способности НСШ, имело место достоверное улучшение клинической симптоматики и выраженная положительная динамика в психосоматическом статусе, которая обусловила существенное повышение «качества жизни» больных, одновременно наблюдалось более эффективное восстановление регионального артериального и венозного кровотока мочевого пузыря, что в целом обеспечило высокий лечебный эффект и адекватную функциональную реабилитацию больных.
СПИСОК ЛИТЕРАТУРЫ
- Мазо Е. Б. Гиперактивный мочевой пузырь у больных пожилого возраста [Электронный ресурс] / Е. Б. Мазо, М. Е. Школьников, Г. Г. Кривобородов. — Режим доступа : http://www.consilium-medicum.com (31)
- Ткачук В. Н. Доброкачественная гиперплазия предстательной железы / В. Н. Ткачук, А. Э. Лукьянова. — СПб.: СпецЛит, 2003. — 109 с.(79)
- Урология : учебник / Н. А. Лопаткин, А.Г.Пугачев, О. И. Аполихин и др.; под ред. Н. А. Лопаткина. — 5-е изд., перераб. и доп. — М.: ГЭОТАР-МЕД, 2004. — С. 335-367.(83)
- Пушкарь Д. Ю. Новый взгляд на патогенез и лечение доброкачественной гиперплазии предстательной железы. Мировой опыт : материалы сателлитного симпозиума / Д. Ю. Пушкарь, А. Е. Вишневский. — М., 2002. — 32 с. (106)
- Возианов А. Ф. Атлас - руководство по урологии (в трёх томах) / А. Ф. Возианов, А. В. Люлько // - Днепропетровск: Днепр-VAL, —2001. (27)
- Temml C, Heidler S, Ponholzer A, Madersbacher S. Prevalence of the Overactive Bladder Syndrome by Applying the International Continence Society Definition. //European Urology. 2005 Oct; Vol. 48, Issue 4; Pages 622-627 (5)
- Тиктинский О. Л. Заболевания предстательной железы : руководство I О. Л. Тиктинский, С. Н. Калинина. — СПб.: Питер, 2006. — 464 с. (78)
- Coyne K, Payne C, Bhattacharyya S, et al. The impact of urinary urgency and frequency on health-related quality of life in overactive bladder: Results from a national community survey. //Value Health 2004;7:451.(7)
- Martin C. Michel, Christopher R. Chapple. Basic mechanisms of urgency: preclinical and clinical evidence.// Eur Urol 2009; 56: 298-308.(8)
- Milson I, Abrams P, Cardozo L, Roberts RG, Thuroff J, Wein AJ. How widespread are the symptoms of overactive bladder and how are they managed? A population-based prevalence study. //BJU Int 2001; 87: 760-6 (6)
- Borisov K.O, Kostyev F.I. Features of metabolic homeostasis in patients with infravezical obstruction. / / Urology-2011. - № 3. - P.28-31.