Одной из актуальных проблем современной хирургии и интенсивной терапии является лечение пациентов с разлитым острым перитонитом, так как летальность пациентов колеблется от 40 до 84 %, достигая при септическом шоке 100% [1,2]. Особенностями предоперационного состояния по поводу перитонита является их экстренность, тяжелое или крайне тяжелое состояния больных, как правило пожилого и старческого возраста, обусловленная невозможностью полной коррекции волемических нарушений, высокой травматичностью самой операции, выраженностью воспалительного стресс-ответа, индуцированного хирургической инфекцией [1,4]. Дальнейшее развитие этого процесса зависит от проведение адекватного анестезиологического обеспечение во время оперативного вмешательства.
Целью исследования: явились улучшение результатов лечения пациентов с осложненной абдоминальной хирургической инфекцией путем оптимизации анестезии как компонента комплексной программы интенсивной терапии.
Материал и методы. Ретроспективно проводила исследование истории болезни у 98 пациентов в возрасте от 45 до 75 лет с разлитым гнойным перитонитом, находившихся на лечении в отделении реанимации и интенсивной терапии в больнице скорой медицинской помощи г. Шымкента. Из них -68
мужчины, 30- женщин.Источниками разлитого острого перитонита были червеобразный отросток (36,7%) при перфоративном, флегмонозном, гангренозном аппендиците, желчный пузырь (21,4%) при наличии гангренозного,флегмонозного,перфоративного холецистита, поджелудочная железа (11,2%) при остром деструктивном панкреатите, панкреонекрозе, перфоративной язве желудке и 12 перстной кишке (10,2%), острой кишечной непроходимости (20,4%). Нозологическая структура и половой состав абдоминальной хирургической инфекции представлена в таблице № 1
|
№ |
Нозология |
% |
мужчины |
Женщины |
|
1 |
Желчный перитонит |
21,4 |
14 |
7 |
|
2 |
Аппендикулярный перитонит |
36,7 |
24 |
12 |
|
3 |
Деструктивный панкреатит |
11,2 |
10 |
1 |
|
4 |
ОКН |
20,4 |
11 |
9 |
|
5 |
Перфоративная язва желудка |
10,2 |
9 |
1 |
|
Всего |
77 |
30 |
Все пациенты находились в разных фазах абдоминального сепсиса, который диагностировали согласно критериев Чикагской согласительной конференции ACCPZ SCCM[2]. Общая летальность составила 16,6%. Репрезентативность исследования обеспечивала стандартизацией пациентов по принципам интенсивной терапии ( хирургическая санация и дренирование очага инфекции, антибактериальная терапия, гемодинамическая и респираторная поддержка, детоксикация). Обследование пациентов включало развернутые общеклинические и биохимические анализы крови.В комплексной оценке степени эндогенной интоксикации (ЭИ) учитывала ее объективно-клинические проявления и уровень лейкоцитарного индекса интоксикации (ЛИИ). Прогнозирование и исход разлитого острого перитонита проводили с помощью МПИ. Все пациенты оперированы в условиях мультимодальной комбинированной анестезии после предоперационной подготовки, объем которой зависел от степени дегидратации, т.е. от объема патологических потерь.
Если степень дегидратации не более 10 % массы тела объем инфузии составлял 25-35 мл/кг, а при дегидратации более 10 % массы тела объем инфузии увеличивали до 30-50 мл/кг под контролем минутного диуреза, гематокрита. Во время оперативного вмешательство в качестве основного анестетика применяла пропофол в дозе 0,3-4,0 мг/кг х час. Анальгетический компонент анестезии обеспечивала фентанилом, миорелаксацию -аркуроном. Катетеризацию эпидурального пространства начинала до введения пациента в наркоз и проводили на уровне Th12 -L1 . Перидуральную анестезию осуществляла 0,5 % раствором бупивикаина после тест-дозы 3 мл, в начальной дозе 8мл, затем фракционное введение по 5 мл до окончание операции каждые 2 часа и в послеоперационном периоде каждые 6 часов по 5 мл 0,5% раствора. В некоторых случаях несмотря на такое сочетание анестезии, выполнялась интраоперационная новокаиновая блокада рефлексогенных зон и корня брыжейки тонкой, поперечно-ободочной и сигмовидной кишки. Результаты лечения оценивали по длительности нахождения пациентов в отделении интенсивной терапии, частоте развития послеоперационных осложнений и летальности.
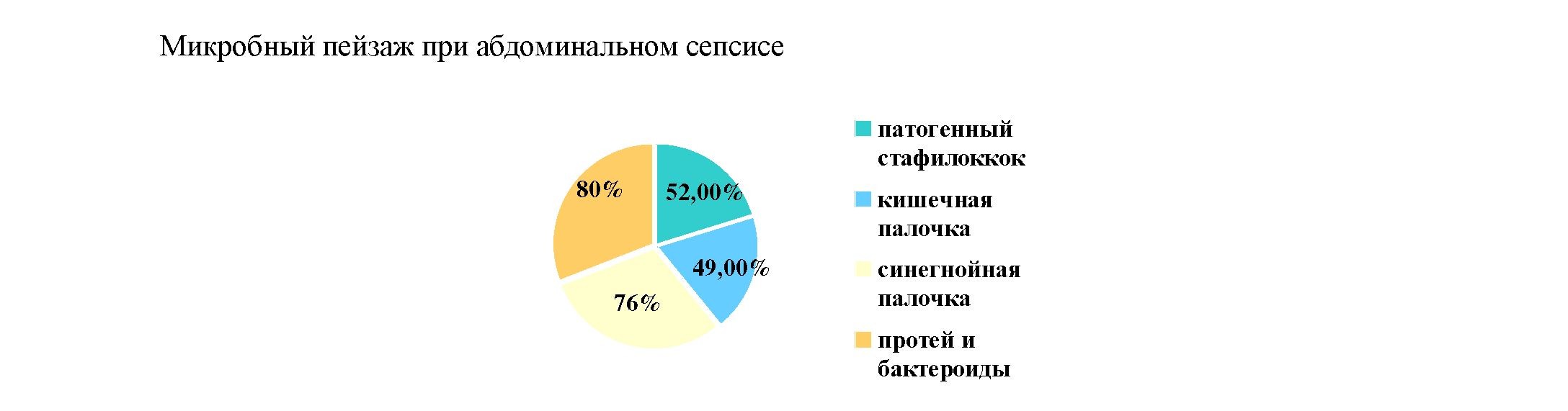
Результаты и их обсуждение. Тяжесть состояния у всех пациентов была обусловлена развитием синдрома энтеральной недостаточности( угнетение двигательной активности, секреторной, переваривающей и всасывающей функций кишки) с выраженной эндогенной интоксикацией, артериальной гипотонией, обусловленной общей дегидратацией, гипонатриемией. Средний балл по шкале МПИ составил 25,55 ±6,67. Осложненная интраабдоминальная инфекция у пациентов имела полимикробную этиологию. Микробиологическая экосистема перитонеальных экссудатов при абдоминальном сепсисе выглядела таким образом: патогенный стафилококк составил-52 %, кишечная палочка- 49%, синегнойная палочка- 76%, протей и бактероиды- 80 %.
По стадиям течения патологического процесса и степени тяжести эндогенной интоксикации пациенты разделены на три группы: I группу составили пациенты с наличием признаков синдрома системного воспалительного ответа (CBO) и компенсированным вариантом эндогенной интоксикации ( ЛИИ 2,8 ±0,7). У больных этой группы все признаки эндогенной интоксикации и ответной реакции на воспаление удалось предотвратить на 4-5 сутки после операции. Летальных исходов в этой группе не было. II группу составили пациенты с признаками полиорганной недостаточности ( тяжелый сепсис), субкомпенсированным вариантом течения ЭИ ( ЛИИ 6,1± 0,04) на фоне сниженных компенсаторноадаптационных процессов. Обратный регресс эндогенной интоксикации наступала к 8 дню, а у пациентов, прооперированных по техническим причинам не в условиях мультимодальной анестезии, прогрессировал эндотоксикоз, ухудшение общего состояния с клинико-лабораторными проявлениями полиорганной недостаточности. Летальность в этой группе составила 21,1 %.
III группу составили пациенты с декомпенсированным вариантом эндогенной интоксикации ( ЛИИ 7,2±0,08), острой печеночно-почечной недостаточностью с ярко выраженной клинико-лабораторными данными, сложными нарушениями водно-электролитного обмена, декомпенсированным метаболическим ацидозом, гиперосмолярным синдромом, нестабильной гемодинамикой, что требовало применение вазопрессоров (тяжелый сепсис, септический шок). Положительная динамика клинико-лабораторных показателей у этих пациентов наблюдались на 3-е сутки после операции. Они заключались в достоверном регрессе энцефалопатии (с 10,4 ± 1,7 до 12,5 ± 2,4 баллов по шкале Глазго), увеличении темпа диуреза на 45 ± 4,1 %, стабилизацией гемодинамики, что потребовались снизить дозы вазопрессоров , нормализации осмолярности, азотемии в плазме крови по сравнению с исходными показателями. Однако положительная динамика носила мозаичный характер, особенно пациентов с неадекватной санацией очага инфекции, что требовало проведения активных методов детоксикации.
Летальность в этой группе составила 32,4%. У пациентов с острым разлитым перитонитом достижение положительных результатов возможно только при условии разрешения хирургической проблемы на фоне проведения комплексной программы интенсивной терапии, одним из компонентов которой являлась мультимодальная комбинированная анестезия во время оперативного вмешательства с продленной эпидуральной анестезией в послеоперационном периоде. Положительной стороной такого сочетания являлось максимальное обеспечение адекватной анестезии у пациентов с эндотоксикозом, полиорганной недостаточностью на фоне сопутствующей патологии во время операции (использование малых доз наркотических анальгетиков, адекватная защита от хирургической агрессии вследствие нормализации нейроциркуляторных и нейрогуморальных реакций пациента, максимальная релаксация).
Продленная эпидуральная анестезия в послеоперационном периоде у пациентов с острым разлитым перитонитом приводит к восстановлению чревного кровотока, увеличению регионарного кровообращения в органах брюшной полости, уменьшению степени ишемических повреждений, предупреждает транслокацию бактериальной флоры, повышает тонус кишечника и раннему восстановлению моторики в сочетании со снижением проницаемости микрососудистого русла. Все это являлось мерой профилактики синдрома интраабдоминальной гипертензии, что существенно улучшило течение заболевания. Комплекс интенсивной терапии на фоне периоперационного эпидурального блока как его компонента, позволил оптимизировать лечебный процесс и значительно снизить летальность.
Выводы: 1.Использование мультимодальной комбинированной анестезии у больных с интраабдоминальной инфекцией обеспечивала надежную антиноцицептивную защиту от хирургической агрессии, что позволило избежать назначения и уменьшить дозу и кратность введения наркотических анальгетиков во время операции и в раннем послеоперационном периоде.
2.Как компонент интенсивной терапии мультимодальная анестезия у больных с острым разлитым перитонитом в послеоперационном периоде предупреждает развитие ателектазов и пневмоний, приводит к раннему восстановлению моторики кишечника, снижению интраабдоминального давления, восстановлению перфузии спланхнической зоны.
ЛИТЕРАТУРА
- Гринев М.В., М.И. Громов, В.Е. Комраков (2001). Хирургический сепсис. СПб-M.: ОАО «Типография”Внешторгиздат”», 350 с.
- Костюченко А.А., Бельских А.Н., Тулупов А.Н. (2000). Интенсивная терапия послеоперационной раневой инфекции и сепсиса. СПб: Фолиант, 448 с.
- Авдеева М.Г., Шубич М.Г. Патогенетические механизмы инициации синдрома системного воспалительного ответа (обзор литературы)// Клиническая лабораторная диагностика. - 2003. - № 6. - С. 3-10.
- Васильков В.Г., Сафронов А.И., Купцова М.Ф. соавт. Критерии выбора методов детоксикации при перитоните// Вестник интенсивной терапии. - 2005. - №6. - С. 12-14.
- Векслер Н.Ю., Бояринов Г.А., Макаров Н.А. и соавт. Тактика ведения больных с диффузным перитонитом с позиций анестезиолога-реаниматолога// Вестник интенсивной терапии. - 2004. - №5. - С. 178-180.