Функциональная активность гепатоцитов определяется состоятельностью ферментов монооксигеназной системы. Однако до сих пор нет ответа на вопрос, каким образом индукторы и ингибиторы монооксигеназ влияют на активность нитрергической системы. Известно, что маркерами активности последней являются оксид азота (NO), эндотелиальная (eNOS) и индуцибельная NOS (iNOS ) NO-синтаза и пероксинитрит (ONO2-) .Исследования проводились на 48 белых беспородных крысах-самцах массой 180-250 г, которых разделили на серии и группы в зависимости от условий опыта. Выявленные корреляционные связи между показателями монооксигеназной системы и NOS свидетельствуют об их четкой обоюдной функциональной зависимости, которая, к сожалению, до сих пор не учитывается в экспериментальной и клинической фармакологии, а также при терапии больных, в курс лечения которых назначают индукторы и ингибиторы лекарственного метаболизма.
В последние годы исследователи проявляют интерес к межсистемным и межорганным взаимосвязям на уровне жизнедеятельности клетки, особенно в органах, ответственных за функционирование всего организма, поддержание его гомеостаза при всевозможных патологических ситуациях, возникающих как внутри организма, так и на фоне привнесенных в него извне причин [1,2]. Из-за особого структурно-функционального положения и значения печени особое место отводится гепатоцитам, поскольку их функционирование подвергается постоянному влиянию эндогенно образовывающихся и экзогенно поступающих ксенобиотиков [3,4]. Печеночная паренхима обладает способностью нивелировать все эти угрозы. Функциональная активность гепатоцитов определяется состоятельностью ферментов
монооксигеназной системы [5,6]. Физиологическая стабильность и гибкая приспособляемость этой системы в полной мере можно оценить и проследить на фоне применения индукторов или ингибиторов лекарственного метаболизма. Доказано, что первые повышают активность монооксигеназ, а вторые, напротив, снижают их активность [7,8]. Однако до сих пор нет ответа на вопрос, каким образом индукторы и ингибиторы монооксигеназ влияют на активность нитрергической системы. Уже известно, что маркерами активности последней являются оксид азота (NO), эндотелиальная (eNOS) и индуцибельная NOS (iNOS ) NO-синтаза и пероксинитрит (ONO2-) [9,10].
Цель исследования – изучение активности монооксигеназ и параметров NO-системы в микросомах гепатоцитов на фоне действия индуктора бензонала и ингибитора циметидина.
Материалы и методы. Исследования проводились на 48 белых беспородных крысах-самцах массой 180-250 г,
которых разделили на серии и группы в зависимости от условий опыта. Первая серия - группы животных, которым в течение 6 суток внутрижелудочно вводили 1% водную суспензию бензонала в дозах 25, 50 и 100 мг/кг; вторая - группы животных, которым внутрижелудочно вводили 1% водный раствор циметидина в аналогичных дозах. Животные содержались в стандартных условиях вивария и рационе кормления. Забой экспериментальных крыс, находившихся под рауш-наркозом, проводили посредством мгновенной гильотинной декапитации. В выделенных с помощью препаративной ультрацентрифуги VAC-601 (Германия) при 105000g микросомальных фракциях ткани печени определяли на двухлучевом спектрофотометре с компьютерной обработкой типа UV-2100 (Ltd, Китай) содержание цитохромов Р-450, Р-448, Р-420 и b5классическим методом Т. Omura, R.Sato[11]; активность микросомальных ферментов: НАДФН-цитохром с-редуктазу (НАДФН-цит.С-ред.) по C.H.Williams, H. Kamin [12]; бенз(а)пи- ренгидроксилазу (Б(а)ПГ) -по C.H.Yang, L.P.Kicha [13];N- деметилазу амидопирина (N-АП) - по A. Bast, J. Nordhosck
- ; анилингидроксилазу (АГ) - по А.И. Арчакову и соавт.
- ; глюкоза-6-фосфатазу (Г-6-Фаза) - по N.S. Gnosh, N.C. Kar [24]; микросомальный белок (мг/мл) - по O.H.Lowry и соавт.
Одновременно в выделенных микросомах и в сыворотке крови определяли содержание NO по основным стабильным его метаболитам - NO2- и NO3- - по методу П.П. Голикова и соавт. [17]; активность еNOS - по В.В. Сумбаевой, И.М. Ясинской [22]; активность iNOS и концентрацию пероксинитрита (ONOO-) - по М.Ю. Раваевой, Е.Н.Чуян [18]. Полученные данные обрабатывали методом вариационной статистики. Достоверными считали результаты, удовлетворяющие р<0,05.
Результаты и обсуждение. Действие бензонала характеризовалось дозозависимым повышением активности всех изучаемых ферментов монооксигеназной системы (Таблица 1).
Одновременно существенно изменялись показатели NO- системы. При этом в дозах 25 и 50 мг уровень NO, активность eNOS повышались, а активность iNOS и содержание ONO2-, напротив, снижались. В дозах 75 и 100 мг/кг, наряду с повышением уровня NO и активности eNOS, наблюдалось статистически значимое возрастание активности iNOS и содержания ONO2- (Таблица 2).
При введении животным циметидина, по мере увеличения его дозы с 10 до 100 мг/кг, отмечалось постепенное угнетение количественных показателей цитохромов P-450,
b5, активности ферментов N-AП, АГ. Ферменты НАДФН-цит. с-ред и Г-6-Фаза в дозах 10 и 25 мг/кг практически оставались в пределах контрольных значений, а в дозах 75100 мг/кг снижались (Таблица 2).
При использовании циметидина в дозах 10 и 25 мг/кг уровень NO и активность (eNOSконституитивной) повышались; одновременно увеличивалась экспрессия iNOS и ONO2-. В дозах 75 и 100 мг/кг при сохранении высокого уровня NO и активности eNOS (на уровне действия препарата в дозе 10-25 мг/кг) активность iNOS и содержание ONO2- динамично возрастали.Следовательно, реакция систем цитохрома Р-450 и NOS в микросомах печеночной ткани неоднозначна на действие различных по своей химической природе ксенобиотиков.
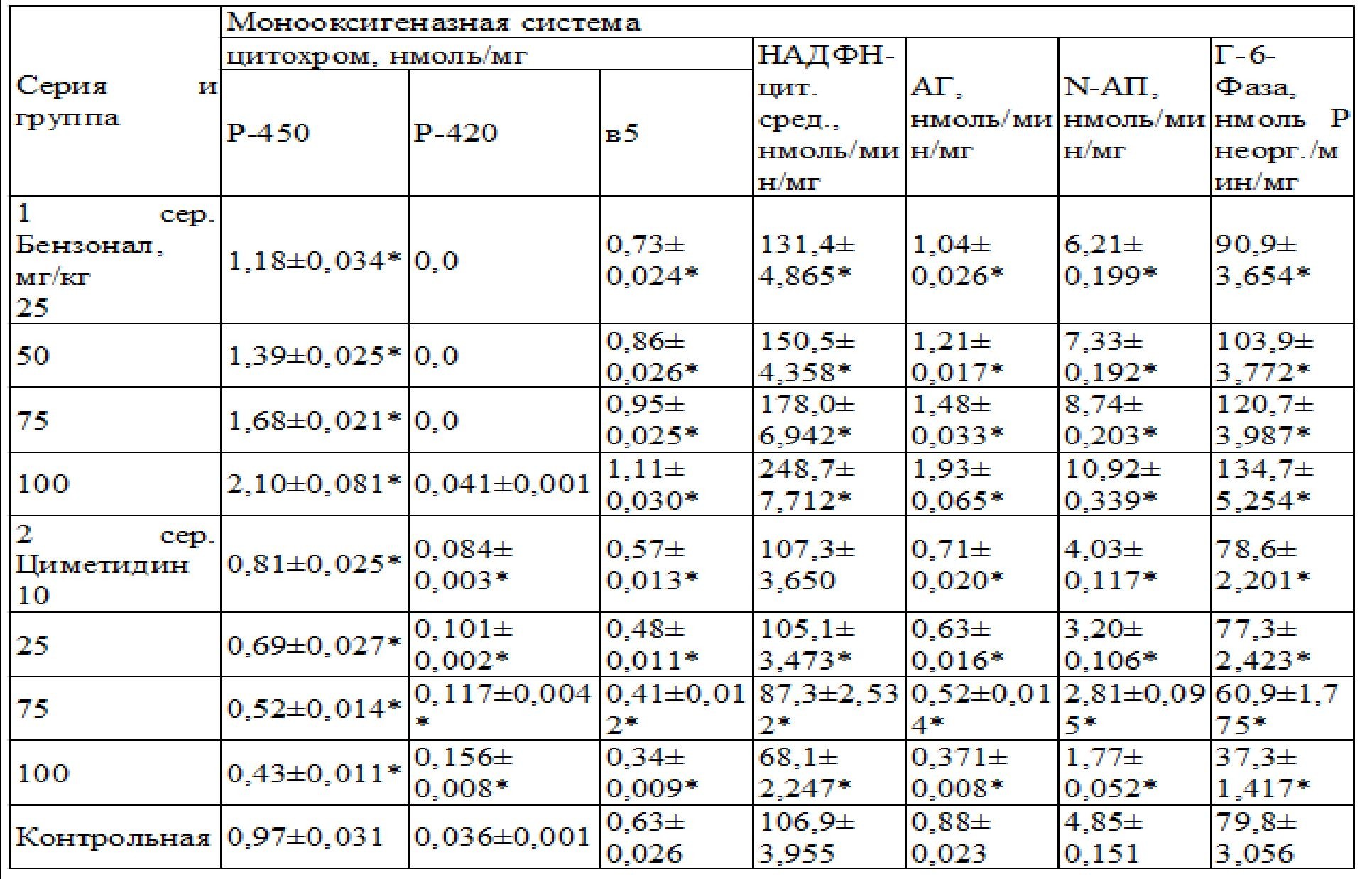
Таблица 1 - Активность монооксигеназ в микросомах печени крыс при действии бензонала и циметидина, M±m
Примечание: здесь и далее * - р<0,05 по сравнению с контролем
Таблица 2 - Активность NOS в микросомах печени крыс при действии бензонала и циметидина, M±m
|
Серия и группа |
Hитpepгичecĸaя система |
|||
|
NO. мĸмoль/мг |
eNOS, м км о ль/мин/мг |
INOSz MKM ОЛЬ /ми H,■■'м г |
ONO⅛- MKM ОЛЬ/м г |
|
|
1 сер. Бензонагг мг/ĸг 25 |
6s45±0s238* |
19z59±0z744* |
0,08Qtí),002* |
0z065±0z002* |
|
50 |
8z17±0z272* |
23z16±018 lơ* |
0z070±0z002* |
0z060±0z002* |
|
75 |
9;Ū8±0306* |
28z54±0z82Sβ |
0=12÷C∣=003* |
0z067±0z002* |
|
100 |
13,L±O,458* |
33z,62±lz042* |
0,15⅛003* |
OzO78±OzOO3* |
|
2 сер. Циметидин 10 |
7,62±0,223* |
20z83±0z558∙ |
0z12÷0z003* |
0z089±0z002* |
|
25 |
8.80⅛0J43* |
24.77⅛〇781* |
0,15⅛03003* |
0z093±0z002* |
|
75 |
llz59±0z374* |
22,9(Ж),842* |
0,21⅛00б· |
0z105±0z003* |
|
100 |
16J5±03531 * |
25161⅛01721* |
0z26±0z006* |
0z119±0z0034 |
|
Контрольная |
5z52±0z164 |
17z42±0z627 |
0z10±0z002 |
OzOSOiOzOOl 6 |
Ответные биохимические проявления в этих системах зависят как от фармакологических свойств препарата, так и от введенной дозы. Свойственное бензоналу индуктивное действие на систему цитохрома P-450 [28], а также повышение содержания NO, экспрессия eNOS, проявляющиеся при введении малых доз индуктора (25-50 мг/кг), можно рассматривать с позиций необходимости увеличения контакта активного центра цитохрома Р-450 с ксенобиотиками. Для этого необходим приток кислорода, который должен поступить в гепатоцит через механизмы усиления процессов микроциркуляции в печеночной ткани. Поэтому подъем активности eNOS и NO при индукции системы цитохрома Р-450, по-видимому, связан с необходимостью усиления экспрессии ферментов монооксигеназной системы. Доказано, что увеличение eNOS и, соответственно, расслабляющего фактора эндотелия сосудов NO приводит к повышению процессов микроциркуляции и более эффективному обеспечению тканей кислородом [19,20]. В дальнейшем, с увеличением активности микросомальных ферментов, возрастает количество продуктов «летального синтеза», одним из элементов реализации которого является возрастание активированных форм кислорода, свободных радикалов, осуществляющих стимуляцию активности iNOS (неконституитивная форма NOS) [21]. При этом активная зона iNOS с большей готовностью доступна к связыванию с кислородом и образованию радикала ONO2-, обладающего цитотоксическим и мембранолитическим свойствами [22,23]. ONO2- угнетает ферментативную активность систем жизнеобеспечения клетки, стимулирует лизосомальные ферменты, процессы ускоренного апоптоза и некроза [24]. Возрастание активности iNOS и ONO2- в микросомах под действием индукторов лекарственного метаболизма, возможно, связано с истощением запасов аргинина, необходимого субстрата для синтеза NO, с участием изоформцитохрома P-450 [25] и eNOS [26,27]. При назначении ингибиторов монооксигеназ повышение активности NO и eNOS, несомненно, обусловлено необходимостью обеспечения микросомальных ферментов кислородом. Но вместе с тем, аргинин как субстрат для активирования цитохрома Р-450, в большей степени расходуется, по-видимому, для активации как eNOS, так и iNOS. При этом перенасыщение клеток NO и iNOS, возможно, в еще большей степени тормозит реакции ферментов системы цитохрома Р-450. Возрастание активности iNOS как следствие гиперэкспрессия NO при высоких концентрациях циметидина (75, 100 мг/кг), происходит на фоне угнетения активности микросомальных ферментов НАДФН-цит. с- редуктазы и Г-6-Фазы - главных лимитирующих факторов функционирования цитохрома Р-450 [28].
По-видимому, НАДФН-цит. c-редуктаза и Г-6-Фаза являются основными мессенджерами возможной взаимосвязи между системой цитохрома P-450 и NOS. Чтобы подтвердить эту гипотезу, нами изучены корреляционные отношения между НАДФН-цит. c-редуктазой, Г-6-фазой и цитохромом Р-450 и активностью NOS, уровнем NO, активностью eNOS и iNOS и содержанием ONO2-. Как видно из полученных данных, при назначении бензонала рост содержания цитохрома Р-450, НАДФН-цит. с-редуктазы и Г-6-Фазы напрямую коррелирует (р≤0,001) с увеличением параметров NO и eNOS и противоположно (р≤0,001) - с экспрессией iNOSи ONO2-. При назначении циметидина наблюдается отсутствие связи между сниженными параметрами НАДФН-цит. с-редуктазы и Г-6-Фазы и количеством цитохрома Р-450 с уровнем NO, активности eNOS, iNOS и ONO2- при малых дозах препарата (от 10 до 25 мг/кг), обратная сильная зависимость угнетения активности ферментов монооксигеназ и степенью гиперэкспрессии NOS, ONO2-, iNOS и прямая с угнетенной активностью eNOS при назначении высоких доз (75 и 100 мг/кг) циметидина.
Заключение. Таким образом, реакция монооксигеназных ферментов и NOS в микросомах при действии индуктора бензонала проявляется в синхронном режиме ее интенсификации. При действии ингибитора монооксигеназной системы циметидина угнетение скорости реакций монооксигеназ характеризуется нарастанием активности NOS как за счет ее конституитивной (eNOS), так и неконституитивной (iNOS) с одновременным повышением в микросомах содержания NO и ONO2-. Выявленные корреляционные связи между показателями монооксигеназной системы и NOS свидетельствуют об их четкой обоюдной функциональной зависимости, которая, к сожалению, до сих пор не учитывается в экспериментальной и клинической фармакологии, а также при терапии больных, в курс лечения которых назначают индукторы и ингибиторы лекарственного метаболизма
Выводы.
- Монооксигеназная и NOS- системы синхронно стимулируются в микросомах печени при назначении индуктора лекарственнго метаболизма бензонала с увеличением дозы от 25 до 100 мг/кг
- При назначении ингибитора монооксигеназной системы циметидина снижение экспрессии ферментов системы цитохрома Р-450 происходит на фоне экспрессии NO, конституитивной и неконституитивной форм NOS - eNOS и iNOS, значительного увеличения уровня пероксинитрита ONO2-.
- Выявленная корреляция между ферментами монооксигеназной системы и NOS свидетельствует об их функциональной зависимости и ответной реакции при действии на организм различных по природе этиологических факторов.
СПИСОК ЛИТЕРАТУРЫ
- Ванин А.Ф. Оксид азота - регулятор клеточного метаболизма // Соросовский образоват. - 2001. - №11. - С. 7-12.
- Minamiyama Y., Jmaoka S., Takemura S. et al. Escape from tolerance of organic Nitrite by induction of cytochrome P450// Free Radical Biology et Medicine. - 2001. - Vol.31. - №11. - P. 1498-1508.
- Durante W., Johnson F.K., Johnson R.A. Arginase: a critical regulator of nitric oxide synthesis and vascular function// Clin. Exp. Pharmacol. Pgysiol. - 2007. - Vol. 34. - №9. - P. 906-911.
- Kuczeriszka M., Olszynski K.H., Gasioroeska A. et al. Interaction of nitric oxide and the cutochrome P-450 system on blood pressure and renal function in the rat: dependence on sodium intake// ActaPgysiologica. - 2011. - Vol. 201. - №4. - Р. 493-502.
- Саратиков А.С., Новожеева Т.П., Венгеровский А.И. Эффективность ферментиндуцирующих средств при экспериментальном поражении печени тетрахлорметанолом// Экспер. и клин.фармакол. - 2003. - №4. - С. 48-49.
- Сивков А.С., Пауков С.В., Рувинов Ю.В., Кукес И.В. Индивидуальная безопасность фармакотерапии при оценке активности изофермента цитохрома Р-450 3А4 (СYP3А4)// Клин.мед. - 2010. - №2. - С. 61-67.
- Симон В.А. Цитохром Р-450 и взаимодействие лекарственных веществ// Рос.журн. гастроэнтерол., гепатол., колопроктол. - 2002. - №6. - С. 25-30.
- Getz G.S. Argenine/Arginase NO// Arteriosclerosis, Thrombosis and Vascular. Biol. - 2006. - Vol. 26. - P. 237-240.
- Ляхович В.В., Вавилин В.А., Зенков Н.К., Меньщикова Е.Б. Активированные кислородные метаболиты в монооксигеназных реакциях// Бюл. СО РАМН. - 2005. - №4. - С. 7-12.
- Манухина Е.Б.. Дауни Х.Ф.. Маллет Р.Т., Меньшев И.Ю. Защитные и повреждающие эффекты периодической гипоксии: роль оксида азота// Вестн. РАМН. - 2007. - №2. - С. 25-33.
- Omura T., Sato R. The carbon monoide-binding pigmenr liver microsomes. Evidence for its hemoprotein nature// J. Biol. Chem. -1964. - Vol. 230. - № 2. -P. 2370-2378.
- Williams C.H., Kamin H. Microsomal triphosphopyridine nucleotide - cytochrome c-reductases of liver // J. Biol. Chem. -1961. -Vol. 237. - № 2. -P. 587-595.
- Yang C.H., Kicha L.P. A direct fluorometric assay of benzo/a/pyrene - hydroxylase// Analyt. Biochem. -1978. -Vol.84. -P.154-163.
- Bast A., Nordhook J. Product inhibition during the hepatic N-demethylation of aminopyrine in the rat// Biochem. Pharmacol. -1981. -Vol. 30. - № 1. -P. 19-24.
- Гидроксилирование производных анилина и аминоантипирина (1-фенил-2,3-диметил-аминопиразолон-5) в эндоплазматическомретикулуме печени/ А.И. Арчаков, И.Н. Карузин, В.Н. Тверитапов, И.С. Кокарева// Биохимия. -1975. - Т.40. - Вып.1. - С.29-32.
- O.H. Lowry, N.G. Rosenbrough, N.J. Farr, R.J. Randall Protein measurement with the Folin phenol reagent // J. Biol. Chem.-1951.-Vol.193. - N1. - P.265-275.
- Оксид азота и перекисное окисление липидов как факторы эндогенной интоксикации при неотложных состояниях/ П.П. Голиков, Н.Ю. Николаева, И.А. Гавриленко и др.// Пат. Физ. и эксп. тер. - 2000. -№2. - С.6-9.
- Раваева М.Ю., Чуян Е.Н. Изменение активности системы синтеза оксида азота под действием низкоинтенсивного миллиметрового излучения// Ученые записки ТНУ им. В. И. Вернадского. Серия «Биология, химия». - 2011. - Т. 24 (63). - № 4. - С. 260-268.
- Марков Х.М. Молекулярные механизмы дисфункции сосудистого эндотелия// Кардиология. - 2005. - №12. - С. 62-72.
- Моисеев С.В. Лекарственная гепатотоксичность// Клин.фармаколю и тер. - 2005. - №14 (1). - С. 10-14.
- Зинчук В.В. Дисфункция эндотелия и кислородсвязывающие свойства гемоглобина// Кардиология. - 2009. - №7-8. - С. 81-89.
- Лукьянова Л.Д. Роль биоэнергетических нарушений в патогенезе гипоксии// Пат.физиол. - 2004. - №2. - С. 2-11.
- Покровский В.И., Виноградов Н.А. Оксид азота, его физиологические и патофизиологические свойства // Тер.арх. - 2005. - №1. - С. 82-87.
- Лукьянова Л.Д., Дудченко А.М., Цыбина Т.А., Германова Э.Л. Регуляторная роль митохондриальной дисфункции при гипоксии и ее взаимодействие с транскрипционной активностью// Вестн. РАМН. - 2007. - №2. - С. 3-13.
- Кукес В.Г., Сычев Д.А., Ших Е.В. Изучение биотрансформации лекарственных средств - путь к повышению эффективности и безопасности фармакотерапии // Врач. - 2007. - №1. - С. 2-5.
- Арчаков А.И., Лисица А.В., Петушкова Н.А., Карузина И.И. Цитохромы Р-450, лекарственная болезнь и персонифицированная медицина. Ч. 1 // Клин.мед. - 2008. - №2. - С. 4-8.
- Кукес В.Г., Сычев Д.А., Гасанов Н.А. Проблемы клинической фармакокинетики на современном этапе// Клин.мед. - 2007. - №2. - С. 58-63.
- Райс Р.Х., Гуляева Л.Ф. Биологические эффекты токсических соединений. - Новосибирск: 2003. - 208 с.