Лабораторные животные занимают исключительное положение в биомедицинских исследованиях, так как полученные с их использованием знания могут быть применены к человеку. Описываются и предлагаются методология эксперимента с использованием лабораторных животных, критические точки исследований и способы их решения. Отмечается значение концепции «Three Rs».
Исследования с использованием лабораторных животных имеют свои особенности и традиции. [1,2]. К наиболее распространённым видам лабораторных животных относятся мыши, крысы, морские свинки, кролики и собаки, реже используются хомяки. В западной научной традиции существует специальная дисциплина – наука о лабораторных животных (Laboratory animal science, LAS). Она в равной степени отдалена как от ветеринарии, так и от физиологии животных. Основной её целью является содействие гуманному и научно обоснованному использованию лабораторных животных в биомедицинских исследованиях [2]. LAS тесно связана с этическими и юридическими проблемами науки. Ранее европейскими учёными была сформулирована достаточно универсальная концепция «The Three Rs», заключающаяся в замене высокоорганизованных животных низкоорганизованными или другими моделями (Replacement), в уменьшении количества используемых животных (Reduction) и в улучшении условий их содержания и использования (Refinement) [2]. В настоящее время в мире эта новая область знания активно развивается.
Значение экспериментов на животных трудно переоценить. Лабораторные животные являются хорошей моделью организма человека [1,2], вследствие чего планированию и использованию лабораторных животных в экспериментах уделяется особое внимание. Поскольку перед исследователем часто возникает вопрос выбора методологии проведения исследований с использованием в них лабораторных животных, целью настоящей статьи является описание в краткой и доступной форме планирования и содержания эксперимента с использованием лабораторных животных.
Гипотеза.
Любое научное исследование начинается с постановки проблемы и спецификации предмета исследования, а это довольно сложный и критичный шаг, так как ему предшествует достаточно большая экспериментальная и теоретическая работа. Следует отметить, что научная проблема от ненаучной отличается прочной опорой на точно установленные факты и подтверждённые теоретические знания. Научное исследование предполагает систематическое и экспериментальное исследование гипотезы – предположения, которое должно быть экспериментально проверяемым.
В процессе постановки проблемы и формулирования гипотезы необходимо тщательное изучение специализированной литературы об исследуемом явлении или предмете даже в тех случаях, когда проблема кажется на первый взгляд новой. Важно также обсуждение выдвигаемых предположений с научным руководителем и коллегами, имеющими определённый опыт и знания в изучаемой области.
По мнению философа Карла Поппера, познание не может начаться с ничего и не может начаться с простого наблюдения, то развитие познания заключается главным образом в модификации более раннего знания [3]. Поэтому изучению новой проблемы предшествует предыдущая собственная практика, или работы других исследователей. Для поиска информации по изучаемой проблеме используются различные электронно-поисковые системы и базы данных. Так, для токсикологических исследований наиболее доступны «Comparative Toxicogenomics Database», «Available Data on Individual Studies», «Pathology incidence rates for completed chronic and pre-chronic studies», «Collected in the Toxicology Database Management System», «PubMed» и т. д. Существуют также коммерческие базы данных.
После проведения предварительного анализа и проверки проблемы на степень её изученности или доказанности, например, токсических свойств какого-либо вещества, принимается решение о продолжении исследований. Если проблема изучена на достаточном уровне, то, как правило, исследование планируется заново или отклоняется вовсе. После тщательного анализа материалов и публикаций по изучаемой проблематике с их критической оценкой выдвигается гипотеза, которая не может содержать абстрактные, обобщающие положения и, как было отмечено ранее, должна подлежать экспериментальной проверке.
Основываясь на выдвинутой гипотезе, исследователь предполагает существование некоторых закономерностей, связей и отношений изучаемых параметров и явления. На этом этапе также важно обсуждение выдвигаемых предположений и способов их проверок с коллегами при определённом скептицизме.
Таким образом, на каждом этапе планирования аспект «вопрос – гипотеза – предположение коллеги» исследуется с жёсткой критической позиции. Выдвинутые гипотезы проверяются экспериментом.
Виды экспериментов.
Выделяют поисковый, пилотный и подтверждающий эксперименты, каждый из которых служит в той или иной степени подтверждению, отвержению или выдвижению новых гипотез.
В поисковых экспериментах на передний план выходят развитие выдвигаемой гипотезы и идентификация проблемы. Иногда одновременно проверяются несколько гипотез. При этом может осуществляться выработка дополнительной или совершенно новой гипотезы и предположений, объясняющих изучаемое явление или процесс. На этом этапе изучаются не только природа и закономерности явления, но и определяется причинноследственная связь между переменными величинами. В поисковых токсикологических экспериментах выявляется биомаркер повреждающего действия исследуемого вещества. Эти эксперименты небольшие и более гибкие в исполнении, без обязательного или ограниченного статистического анализа результатов. Поэтому в определённом смысле поисковый вид эксперимента является противоположным подтверждающему [4,5].
Пилотный вид эксперимента имеет некоторое сходство с поисковым в части «вторичности» статистического анализа или небольшого размера выборки. Но при этом пилотный эксперимент более узок в решении определённых проблем и незаменим для предварительной оценки методологии более крупного исследования. На этом этапе оцениваются размеры эффекта, вариации изучаемых признаков, чувствительность и пределы обнаружения уже выбранных методов измерения. Это даёт возможность определить необходимый объём выборки для статистической проверки гипотезы в большом эксперименте или уточнить некоторые параметры, например, для токсикокинетических исследований, когда совершенно неизвестно, каков будет профиль фармакокинетической кривой, и неясно, с какой частотой следует отбирать кровь для измерения содержания вещества в крови [6].
Большинство биомедицинских исследований относятся к поисковому типу эксперимента, так как они на первый взгляд более результативны и реализуемы и у исследователя появляются возможности избирательного выбора результатов, экономии средств и времени. Тем не менее, бремя доказательства или опровержения гипотезы лежит на подтверждающем эксперименте, который является более трудоёмким, затратным и наиболее значимым. Одной из основных его задач становится формальная проверка гипотезы. К такому типу экспериментов можно отнести GLP-исследование, когда результат проверки статистической гипотезы является основным заключением о безопасности исследуемого вещества.
Все три вида эксперимента применимы в крупных и масштабных исследованиях, например, в разработке новых лекарств, в изучении новых явлений или процессов. В некоторых случаях можно обойтись поисковыми или пилотными исследованиями, если изучаемое явление или предмет новые, и они могут быть эффективны при выработке или первичной проверке нескольких гипотез. Однако решающим ответом может быть только подтверждающий эксперимент.
Расчет количества лабораторных животных на эксперимент.
Часто исследователю необходимо ответить на вопрос о количестве животных, использованных в эксперименте, и определить оптимальное их количество. Для этого используются несколько подходов.
Достаточно простым является «ресурсное уравнение» по Mead (1) [2].
Если число E выше 20, то количество животных в группах следует уменьшить, и наоборот. Однако этот метод используется только тогда, когда невозможно предположить размер эффекта и стандартного отклонения. Такой подход может быть применим в поисковых и пилотных работах, где гипотеза не проверяется и оценивается лишь уровень различия между группами. В то же время он менее надёжен, чем, например, анализ мощности.
Приемлемыми являются метод анализа мощности и метод по уравнениям 2 и 3, основанный на предварительных исследованиях. Значение σ берётся из пилотных, схожих и аналогичных исследований, в том числе литературных источников [7].
Например, исследуемое вещество в сравнении с контрольным воздействием вызывает уменьшение веса на 20 г (δ) при среднем весе морских свинок 400 г со стандартным отклонением (σ) в 23 г. Для мощности теста в 80%, уровня достоверности 0,05 и значений zα 1,96 и zβ 0,84 (критические значения Z стандартного нормального распределения):
В настоящее время доступны специальные программы, предназначенные для математического анализа и статистической обработки результатов исследований.
Из-за сильного разброса или отклонения величин измеряемых параметров (веса, гематологии, клинической химии и т.д.) использование представленных подходов может быть затруднено, а в некоторых случаях, особенно при использовании формулы (1), даже неприменимым. Не вдаваясь в подробности причин отклонений измеряемых величин, которые связаны с индивидуальными вариациями особенностей лабораторных животных, используют для работ стандартизованные по генетическому признаку (изогенные линии), здоровью (SPF-животные), постоянству и контролю среды содержания, а также по весу, возрасту, полу и т. д. Этот подход позволяет в значительной степени сократить количество используемых в эксперименте животных.
Рандомизация и ослепление.
Довольно часто исследователи пренебрегают рандомизацией и еще чаще – ослеплением эксперимента. Однако их важность можно показать на двух примерах.
Так, были проверены 53 исследования на воспроизводимость, в результате 47 оказались невоспроизводимы. При этом одной из причин низкой воспроизводимости результатов исследований оказалась
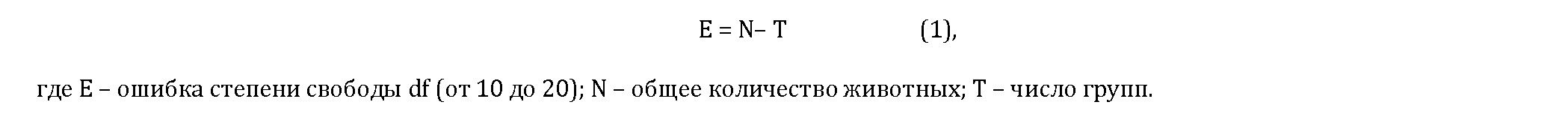

kaznmu.kz · KaзHМУ · №1-2016
неправильная рандомизация экспериментальных животных или полное её отсутствие [8].
Влияние ослепления на результат было продемонстрировано в проверке гистологических исследований слайдов из экспериментов по канцерогенезу, где (хотя этот вопрос остаётся открытым для обсуждения) информирование или, наоборот, сокрытие целей исследований от специалиста-гистолога может повлиять на заключение [9].
Большинство пакетов со статистическими программами имеют функцию рандомизации. Некоторые учебники по биостатистике также включают таблицы случайных чисел
. Иногда можно обойтись и более простым, хотя и менее надёжным способом вытягивания номера из мешка.
Статистический анализ.
Результаты экспериментов следует оценивать с помощью статистических методов даже тогда, когда очевидно, что это не изменит любую интерпретацию. Выбор того или иного подхода в статистической обработке зависит от целей исследований и от качества оцениваемых параметров. Этой проблематике посвящено множество литературы [7] и поэтому нет необходимости в подробном описании процедуры статистической обработки результатов.
Некоторые особенности работы с лабораторными животными.
Довольно часто исследователи используют животных без достаточного обоснования, когда некоторые виды токсикологических тестов уже адаптированы для проведения в условиях in vitro и могут быть успешно внедрены в рутинную работу. Например, тест на бактериальные эндотоксины или на пирогенность заменен LAL-тестом in vitro включающего лизат амебоцитов мечехвоста. В настоящее время изучение местнораздражающего действия проводят в культуре клеток кожи человека или изолированных роговиц глаз после убоя сельскохозяйственных животных и т. д. [10]. Поэтому лабораторных животных используют только тогда, когда невозможно получить адекватные результаты другими подходами, например, in silico, in vitro, in ovo, ex vivo и т.д. (прим. Replacement).
Другой проблемой является отработка инвазивных процедур на живых животных. Во-первых, это не гуманно, а, во-вторых, стрессовая реакция организма животного включает значительные перестройки нейроэндокринной системы. Для таких работ используют различные симуляторы или трупы животных после другого эксперимента, но с условием, что они не были заражены и не подвергались химическому воздействию потенциально опасными веществами.
Отдельно стоит отметить уход и манипуляции с животными. Лабораторные животные, как правило, неагрессивны и легко приручаются. Животные быстро привыкают к персоналу, который постоянно за ними ухаживает или работает. Поэтому смену персонала по возможности следует исключить.
Нельзя в одной комнате содержать мышей и крыс, проводить манипуляции при переходе от одного вида животного к другому без смены спецодежды, а в некоторых случаях необходимо принять душ. Наилучший подход тот, при котором определённый специалист, ухаживающий за животными, и исследователь работают только с одним видом животных. Это вызвано тем, что запах и феромоны мышей и крыс могут вызвать стрессовую реакцию, поскольку в природе эти животные конкурентны. Кроме того, существует риск перекрёстной контаминации инфекционными агентами (бактерии, грибки, вирусы). Во всяком случае, до и после работы принимают душ, а спецодежду отправляют на дезинфекцию.
Важно знать, что ни в коем случае нельзя брать животных пинцетом, корнцангом и т.д. Не рекомендуется долго держать крыс за хвост. Нежелательно лишать животных воды более чем на 3 часа и пищи более чем на 24 часа. Корм и питьевая вода должны быть качественными и обеспечивать физиологические потребности животных. Неполноценный корм приводит к различным метаболическим нарушениям и заболеваниям животных. Для маркировки следует использовать только безопасные и безболезненные способы. Запрещается ампутация пальцев и кончика хвоста. При длительных манипуляциях животных помещают в специальный подогреваемый до физиологических температур станок, роговицу глаз защищают от высыхания обработкой специальным гелем, а животных наркотизируют газовой или инъекционной анестезией (прим. Refinement). После таких инвазивных процедур животных помещают в специальные реанимационные камеры.
Нередко конечной точкой эксперимента является эвтаназия. В таких случаях не рекомендуется умерщвлять животных ингаляцией эфиром и, тем более, хлороформом, а также методом механической асфиксии. Лучшим способом эвтаназии является ингаляционный наркоз галотаном или углекислым газом. Приемлемы декапитация и цервикальная дислокация для мышей и крыс весом до 180 г или инъекция более крупных животных сверхвысокими дозами барбитуратов. Однако последний метод оказывает сильное влияние на уровень стрессовых гормонов в крови животных, и поэтому должно учитываться при выборе способа эвтаназии [11].
Если животное погибло во время эксперимента и при этом явно отсутствует вина исследователя (неправильная фиксация животного, неправильное или избыточное введение вещества, в том числе и анестетика, приведшего к смерти животного), то смертность учитывается в первичных данных как воздействие изучаемого фактора (вещества, физического воздействия, терапия и т.д.). Но в любом случае при некропсии экспертное заключение о причине смерти животного должен дать патоморфолог.
Вводимое исследуемое вещество не должно обладать сильным раздражающим свойством на слизистые оболочки или вызывать химические ожоги. Следует использовать канюли или зонды только соответствующего размера и не превышать допустимые для каждого вида животного объёмы вводимых веществ. Например, максимально допустимый объем однократного введения вещества внутрь составляет для мышей 0,8 мл, для крыс – 2 мл.
Все используемые животные должны содержаться в соответствии с потребностями данного вида в условиях окружающей среды, происходить от известного питомника и сопровождаться справкой об их здоровье. Ни в коем случае нельзя использовать в эксперименте больных и старых животных, из неизвестного источника, смешанных из разных партий.
Представленные требования не являются исчерпывающими и отражают лишь самые важные проблемы, с которыми может столкнуться любой исследователь.
Заключение.
Чрезвычайно важную роль лабораторных животных в биомедицинских исследованиях трудно переоценить. На исследователя возлагается большая моральная и юридическая ответственность, поскольку результаты исследований будут экстраполированы на человека. В то же время полученные новые знания имеют некоторые ограничения. Поэтому в экспериментах с использованием лабораторных животных необходимо исходить из позиции целесообразности и гуманности их использования, не следуя расчёту «чем больше, тем лучше». Эти основополагающие принципы выражены концепцией «Three Rs» – Replacement, Reduction и Refinement. Каждый исследователь должен сверять с ней выдвигаемые гипотезы и планируемые эксперименты и точно следовать ей. Особое внимание необходимо уделять планированию экспериментов. Тщательная подготовка к эксперименту с использованием различных источников информации позволит в значительной степени снизить риски возникновения ошибок в методологии проводимых исследований с использованием лабораторных животных.
СПИСОК ЛИТЕРАТУРЫ
- Turner P.V., Brab Th., Pekow C., Vasbinde M.A. Administration of substances to laboratory animals: routes of administration and factors to consider // J. Am. Assoc. Lab. Anim. Sci. - 2011. - Vol.50. - No.5. - P.600-613.
- Principles of Laboratory Animal Science. Eds. LFM. Van Zutphen, V. Baumans, A.C. Beynen. - Amsterdam: Elsevier, 2001. - 416 p.
- Поппер К. Предположения и опровержения. Рост научного знания. - М.: Ермак, 2004. - 638 с.
- Festing M.F., Altman D.G. Guidelines for the design and statistical analysis of experiments using laboratory animals // ILAR J. - 2002. - Vol.43. - No.4. - P. 244-258.
- Kimmelman J., Mogil J.S., Dirnagl U. Distinguishing between Exploratory and Confirmatory Preclinical Research Will Improve Translation // PLOS Biology. - 2014. - Vol.12. - No.5. - P.1-4.
- Preclinical drug development. Edited by Mark C. Rogge and David R. Taft. - Taylor & Francis Group. - 2005. - 570 p.
- Сергиенко В.И., Бондарева И.Б. Математическая статистика в клинических исследованиях. - М.: ГЭОТАР-Медиа, 2006. - 304 с.
- Begley C.G., Ellis L.M. Drug development: Raise standards for preclinical cancer research // Nature. - 2012. - Vol. 483. - P. 531-533.
- Holland T., Holland C. Unbiased histological examinations in toxicological experiments (or, the informed leading the blinded examination) // Toxicologic Pathology. - 2011. - Vol.39. -P. 711-714.
- Kandarova H., Letasiova S. Alternative methods in toxicology: pre-validated and validated methods // Interdiscip. Toxicol. - 2011. - Vol.4. - No.3. - P.107-113.
- OECD Environment, Health and Safety Publications. Series on Testing and Assessment. No. 57. Detailed review paper on thyroid hormone disruption assays // ENV/JM/MONO. - 2006. - №24. -P. 434-438.