В настоящей работе представлен обзор литературных данных по актуальной проблеме резистентности грамотрицательных микроорганизмов к бета-лактамным антибиотикам, описаны их молекулярные механизмы. Даны классификационная характеристика различных групп и подгрупп β-лактамаз, молекулярная эпидемиология энтеробактерий, продуцирующих β- лактамазы расширенного спектра Действия и металло^-лактамазы.
Актуальность. Формирование и распространение резистентности к бета-лактамным антибиотикам у грамотрицательных бактерий является одной из наиболее актуальных проблем современной антимикробной химиотерапии.
Бактерии семейства Enterobacteriaceae в совокупности занимают ведущее место в этиологической структуре нозокомиальных инфекций в российских стационарах. Так, по данным многоцентрового эпидемиологического исследования антибиотикорезистентности возбудителей нозокомиальных инфекций (Марафон) в 25 стационарах 18 городов России в 2011 – 2012 гг. энтеробактерии составил 33,7% всех выделенных бактериальных возбудителей. Наиболее частыми видами были Klebsiella pneumoniae (16,9%), Escherichia coli (7,9%) [1]. Сходные показатели распространенности нозокомиальных инфекций, вызванных энтеробактериями, были отмечены в аналогичных исследованиях, проведенных ранее: 30,1% в 2002 – 2004 гг. и 34,5% в в 2006 – 2007 гг. [2, 3].
Рост резистентности к антибактериальным препаратам отмечается как среди возбудителей нозокомиальных инфекций, так и среди возбудителей внебольничных инфекций и представляет собой социально – экономическую проблему, так как при этом увеличивается длительность госпитализации, стоимость лечения, ухудшается прогноз выздоровления больных, ухудшается эпидемиологическая ситуация в плане распространения в обществе резистентных штаммов.
Описаны следующие молекулярные механизмы устойчивости бактерий к антибиотикам: 1) модификация мишени, на которую действует лекарственное средство; 2) ферментативная инактивация антибиотика; 3) активное выведение антибиотика из микробной клетки (эффлюкс); 4) предотвращение проникновения лекарства к мишени (защита мишени); 5) нарушение проницаемости внешних структур микробной клетки. [4, 5].
Модификация мишени действия. Мишенями действия β- лактамов являются ферменты – пенициллиносвязывающие белки (ПСБ), участвующие в синтезе клеточной стенки бактерий. В результате модификации у некоторых ПСБ уменьшается сродство к ß-лактамам, что проявляется в повышении МПК этих препаратов и снижении клинической эффективности. Гены модифицированных ПСБ локализованы на хромосомах. Среди грамотрицательных бактерий устойчивость, связанная с модификацией ПСБ, встречается реже.
Активное выведение β-лактамов из микробной клетки. Многие ß-лактамные антибиотики могут активно выводиться грамотрицательными бактериями. Известны, как минимум, 4 больших системы эффлюкса, участвующих в выведении экзогенных веществ из клетки у P.aeruginosa и обеспечивающих природную устойчивость данного возбудителя к антибиотикам.
Нарушение проницаемости внешних структур грамотрицательных бактерий. Внешняя мембрана грамотрицательных микроорганизмов является препятствием для проникновения ß-лактамов внутрь клетки. Транспорт антибиотика через внешнюю мембрану осуществляется через каналы, образованные особыми белками – поринами. В результате мутаций возможна полная или частичная утрата поринов, приводящая к неспособности антимикробного агента проникнуть внутрь клетки и, как следствие, к устойчивости штамма. Данный механизм устойчивости встречается практически среди всех грамотрицательных бактерий, обычно в сочетании с другими механизмами. Мутации в структуре порина OprD вместе с продукцией гена AmpC являются причиной устойчивости к имипенему у Pseudomonas aeruginosa. Также дефекты OprD формируют устойчивость у Klebsiella spp. [6].
Ферментативная инактивация антибиотика. Продукция β-лактамаз. Наиболее распространенным механизмом устойчивости микроорганизмов к ß-лактамным антибиотикам является их ферментативная инактивация в результате гидролиза одной из связей ß-лактамного кольца ферментами ß-лактамазами. Комплексы, образуемые ß- лактамазами и беталактамными антибиотиками не стабильны, что позволяет одной молекуле ß-лактамазы гидролизовать множество молекул антибиотика.
Известно более 500 ферментов, различающихся по следующим важным свойствам:
Субстратному профилю. Способность ß-лактамаз к преимущественному гидролизу тех или иных ß-лактамных антибиотиков, например, пенициллинов, цефалоспоринов, карбапенемов или препаратов разных группп в равной степени.
Чувствительности к действию ингибиторов. Для преодоления устойчивости, связанной продукцией бактериями ß-лактамаз, были разработаны соединения (клавулановая кислота, сульбактам, тазобактам), ингибирующиющие активность этих ферментов и защищающие антибиотики от разрушения. К сожалению, перечисленные ингибиторы подавляют активность не всех ß-лактамаз.
Характеру пролỵкuии (стабильной, на высоком или низком уровне, или индуцибельной). Эта характеристика, наряду с субстратным профилем фермента, определяет возможность формирования резистентности. Значимый уровень устойчивости может быть достигнут только при постоянной продукции необходимого количества фермента или индукции его синтеза в присутствии ß-лактамного субстрата. В то же время, продукция ß-лактамаз на низком уровне является недостаточной для проявления клинически значимой резистентности у многих видов бактерий.
Локализации кодирующих генов. Видоспецифические ß- лактамазы кодируются хромосомно. Гены приобретенных ферментов чаще локализуются на конъюгативных плазмидах и мобильных генетических элементах, что способствует их быстрому внутри- и межвидовому распространению.
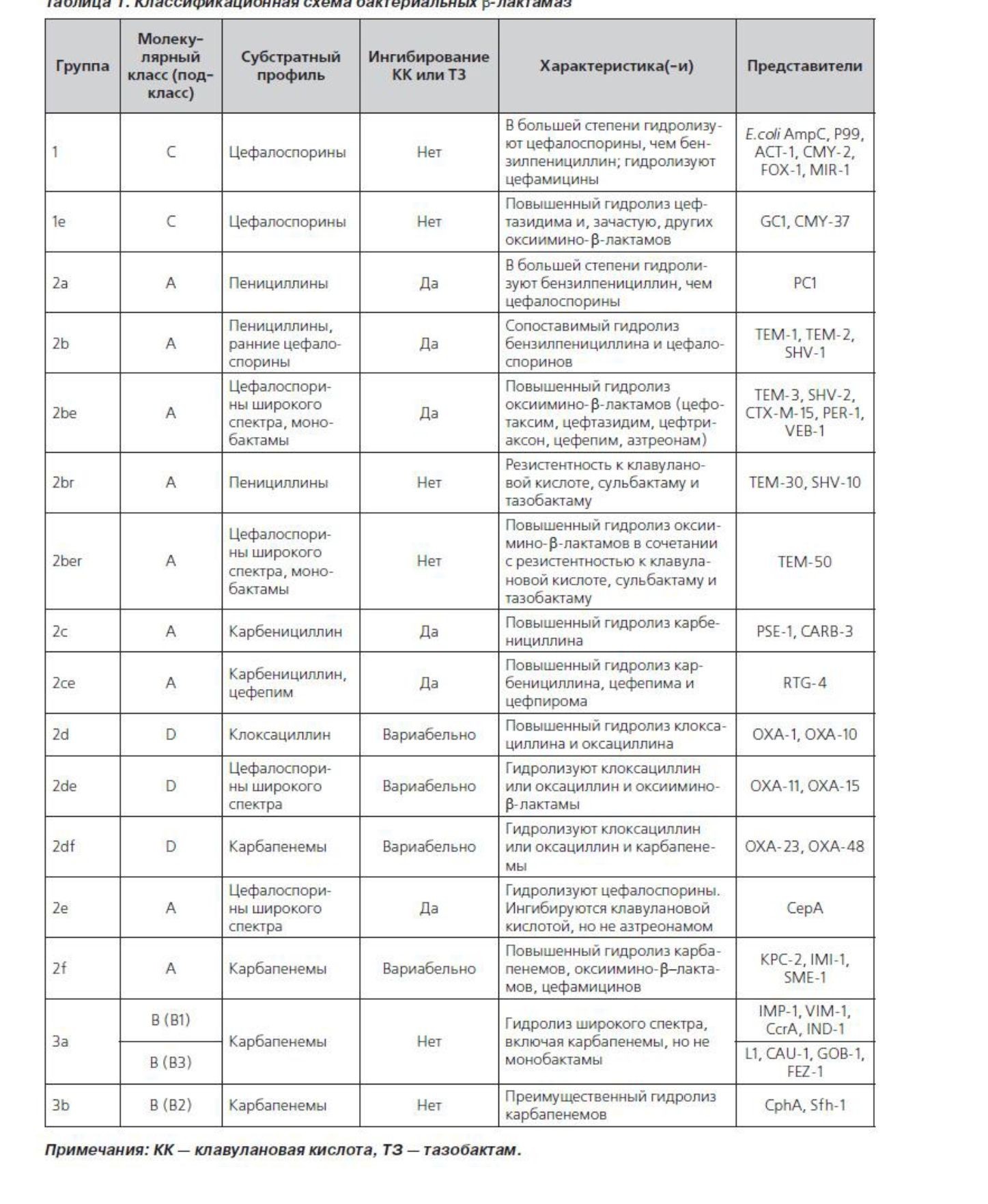
Существует две классификации ß-лактамаз: функциональная и молекулярная. Функциональная классификация базируется на субстратной специфичности ферментов (от пенициллиназ и цефалоспориназ с узким спектром активности до b-лактамаз расширенного спектра действия (БЛРС) и карбапенемаз) и их чувствительности к ингибиторам (клавулановой кислоте, сульбактаму и тазобактаму). Молекулярная классификация основана на первичной аминокислотной структуре и структуре активного центра ферментов. Все известные ß-лактамазы делят на 4 молекулярных класса (A, B, C, D) в зависимости от степени гомологии аминокислотных последовательностей. Группы A, С и D являются протеазами серинового типа (по аминокислоте, находящейся в активном центре фермента), а группа B в активном центре содержит один или два атома цинка, в связи с чем их еще называют металло-ß- лактамазами (МБЛ). Наибольшей популярностью в настоящее время пользуется классификация K. Bush et al., в которой учитываются и функциональные, и структурные особенности b-лактамаз. Впервые она была опубликована в 1995 г. [7] и доработана в 2010г. (таблица 1) [8].
Цефалоспориназы группы 1. Гены, кодирующие выработку этих ферментов, локализуются на хромосомах многих представителей семейства Enterobacteriaceae и некоторых других видов микроорганизмов. У многих видов бактерий, включая Citrobacter freundii, Enterobacter cloacae, Serratia marcescens и Pseudomonas aeruginosa, экспрессия AmpC низкая, но индуцируется при экспозиции к некоторым ß-лактамам, таким как амоксициллин, ампициллин, имипенем и клавулановая кислота [9]. Если они вырабатываются в больших количествах, эти ферменты способны обусловить резистентность к карбапенемам, в особенности к эртапенему [10, 11]. Хотя перенос генов AmpC на плазмиды, наблюдаемый в последнее время, создает реальные предпосылки для их широкого распространения, в настоящее время плазмидные ß-лактамазы 1 группы встречаются реже, чем БЛРС (ß-лактамазы группы 2be).
Представители новой подгруппы 1e представляют собой варианты ферментов группы 1 с повышенной активностью в отношении цефтазидима и других оксииминоß-лактамов. Они получили название «AmpCß-лактамазы расширенного спектра» (ESAC) и включают в себя GC1 у E.cloacae и ряд других, в том числе плазмидных, ß-лактамаз [12-14]. AmpCß- лактамазы, описанные у P.aeruginosa, отличаются повышенной активностью в отношении имипенема [15]. Клиническое значение резистентность приобретает, как правило, при сочетании выработки ß-лактамаз с мутациями пориновых белков [16].
Сериновые ß-лактамазы группы 2. Это наибольшая группа ßлактамаз, во многом благодаря растущей идентификации БЛРС в последние 20 лет.
Пенициллиназы подгруппы 2a представляют собой сравнительно небольшую группу ß-лактамаз с ограниченным спектром гидролитической активности. Они являются ведущими ß-лактамазами у грамположительных кокков, включая стафилококки и изредка энтерококки. Они гидролизуют преимущественно пенициллин и его производные (ампициллин и др.) и в 10 и более раз меньше — цефалоспорины, карбапенемы или монобактамы. Гены, кодирующие их выработку, локализуются на хромосомах, хотя некоторые стафилококковые пенициллиназы являются плазмидными.
В подгруппе 2b объединены ß-лактамазы, легко гидролизующие пенициллины и ранние цефалоспорины (цефалоридин, цефалотин). Они высокочувствительны к ингибиторам ß-лактамаз (клавулановая кислота, тазобактам, сульбактам).
К подгруппе 2be относятся БЛРС. БЛРС гидролизуют оксииминоцефалоспорины (цефотаксим, цефтазидим, цефтриаксон, цефуроксим и цефепим) и монобактамы (азтреонам), но не цефамицины (цефокситин, цефотетан) и не карбапенемы (имипенем, меропенем, дорипенем и эртапенем). Эти ферменты ингибируются классическими ингибиторами ß-лактамаз (клавулановая кислота, сульбактам и тазобактам). Большинство БЛРС принадлежит к классу А и включает в себя типы SHV и TEM, возникшие в результате точечных мутаций в активном участке «родительских» ß-лактамаз, приведших к аминокислотным заменам, что и вызвало расширение спектра действия этих ферментов на цефалоспорины II - IV поколений (TEM1, TEM- 2 и SHV1) [17]. БЛРС обычно локализуются на крупных плазмидах, где нередко располагаются и гены, кодирующие резистентность к другим классам антибиотиков — аминогликозидам и котримоксазолу [18].
К этой же группе относятся многочисленные ß-лактамазы типа CTX-M. Первое сообщение о ß-лактамазах CTX-M (что означает active on CefoTaXime, ist isolated in Munich, т.е. активные в отношении цефотаксима и впервые выделенные в Мюнхене) датируется 1986 г. [19]. Ферменты этого типа кодируются генами, которые были захвачены мобильными генетическими элементами в хромосомах бактерий Kluyvera spp., распространенных в окружающей среде [20, 21]. Гены, кодирующие выработку ß-лактамаз CTX-M, ассоциируются с различными генетическими платформами, которые часто локализуются на плазмидах [22]. Хотя БЛРС типа CTX-M относятся к классу А, они не родственны другим ß- лактамазам, как, например, типа TEM или SHV. Ферменты типа CTX-M активнее гидролизуют цефотаксим и цефтриаксон, нежели цефтазидим. Однако точечные мутации поблизости от активных центров некоторых ферментов, принадлежащих к группам CTX-M-1 и CTX-M-9, значительно повысили их способность гидролизовать цефтазидим [23,24].
Описаны географические различия в распространенности тех или иных групп CTX-M, и только продуценты CTX-M-15 встречаются повсеместно. Hаиболее частые в России и Европе варианты ß-лактамаз CTX-M типа - это CTX-M-15, CTX-M-3, CTX-M-14 [24,25,26].
В подгруппу 2br вошли ß-лактамазы широкого спектра (сопоставимы по активности в подгруппой 2b), но с приобретенной устойчивостью к клавулановой кислоте. Все они относятся к типам TEM или SHV. Hи одного фермента типа CTX-M с подобными свойствами до настоящего времени описано не было.
БЛРС с разной выраженностью устойчивости к клавулановой кислоте объединены в подгруппу 2ber. В ряде случаев такая резистентность довольно умеренная.
Пенициллиназы подгруппы 2c гидролизуют карбенициллин и тикарциллин со скоростью, превышающей 60 % от таковой при гидролизе бензилпенициллина, в то время как оксациллин и клоксациллин гидролизуются в 2 и более раза медленнее бензилпенициллина [7]. За последнее десятилетие описано немного новых ß-лактамаз данной подгруппы — возможно, в связи с тем, что в настоящее время карбенициллин в клинической практике почти не используется и большинство исследователей не тестирует стабильность этого антибиотика [8, 27]. Ферменты данной подгруппы легко ингибируются клавулановой кислотой и тазобактамом.
Подгруппа 2ce включает в себя недавно описанную карбенициллиназу расширенного спектра действия RTG4 (CARB10) с повышенной активностью в отношении цефепима и цефпирома [28].
В подгруппу 2d входят ß-лактамазы, гидролизующие оксациллин и клоксациллин со скоростью, превышающей 50 % от таковой при гидролизе бензилпенициллина, в связи с чем они получили название «OXA-ферменты». В настоящее время это вторая по численности подгруппа ß-лактамаз. Они также с легкостью гидролизуют карбенициллин. Многие ферменты этой подгруппы ингибируются хлоридом натрия.
В новую подгруппу 2de вошли оксациллин и клоксациллин- гидролизующие ß-лактамазы с расширенным спектром активности в отношении оксиимино-ß-лактамов, но не карбапенемов [8]. Они чаще обнаруживаются у изолятов
P.aeruginosa [29]. Резистентность к цефтазидиму обычно выражена в существенно большей степени, чем к цефотаксиму или азтреонаму.
OXA-ферменты, входящие еще в одну новую подгруппу 2df, гидролизуют карбапенемы. Они чаще обнаруживаются у Acinetobacter baumannii. Гены, кодирующие их выработку, обычно локализуются на хромосомах [30], хотя у некоторых представителей семейства Enterobacteriaceae описана плазмидная локализация генов [7, 31]. Фермент OXA-48 и его модификация - OXA-181, характерные для энтеробактерий имеют плазмидную локализацию и представляют одну из основных угроз, с которой связывают распространение устойчивости к карбапенемам. Карбапенемазы проявляют активность, более выраженную по отношению к имипенему, чем к меропенему. Бензилпенициллин и оксациллин они гидролизуют со скоростью, в 40-50 раз большей, чем карбапенемы [30]. Как правило, они не угнетаются клавулановой кислотой.
В России, Беларуси более значимым механизмом устойчивости к карбапенемам у нозокомиальных штаммов Acinetobacter baumannii являлась продукция карбапенемаз класса D, относящихся к группам OXA-23, OXA-40 и OXA-58 [32].
Цефалоспориназы подгруппы 2e гидролизуют цефалоспорины широкого спектра действия и ингибируются клавулановой кислотой и тазобактамом. Чаще всего, эти индуцибельные ß-лактамазы с хромосомной локализацией кодирующих их продукцию генов, обнаруживают у представителей рода Proteus.
Сериновые карбапенемазы класса А входят в подгруппу 2f. Они в большей степени ингибируются тазобактамом, нежели клавулановой кислотой.
Металло-ß-лактамазы группы 3 содержат ион цинка в активном центре. Они гидролизуют все бета-лактамы, за исключением азтреонама. Их активность ингибируется ЭДТА, но не клавуланатом. Первоначально металло-ß— лактамазы (МБЛ) были идентифицированы как хромосомные ферменты у грамположительных и изредка — у грамотрицательных бактерий (как, например, Bacteroides fragilis [33] или Stenotrophomonas maltophilia) [34, 35]. Продукция приобретенных МБЛ встречается у многих видов грамотрицательных неферментирующих бактерий (ГHБ), чаще всего у Pseudomonas aeruginosa, а также у представителей семейства Enterobacteriaceae [36].
В настоящее время известно 10 генетических групп приобретенных МБЛ: VIM, IMP, NDM, SPM, GIM, DIM, SIM, AIM, KHM и TMB [37, 38]. Широкое распространение VIM и IMP ß- лактамаз обусловлено локализацией кодирующих генов в виде кассет в составе интегронов 1 класса, ассоциированных с разнообразными мобильными генетическими элементами (инсерционными элементами и транспозонами) [39]. В последние годы отмечается тенденция стремительного распространения во всем мире штаммов Enterobacteriaceae и Acinetobacter, несущих гены МБЛ нового типа – NDM-1 (New Delphi-metallo-β-lactamase) [40-42].
Результаты исследований МБЛ-продуцирующих штаммов P.aeruginosa, проведенных в России, Казахстане, Беларуси показывают преимущественное клональное распространение VIM-2. Рост доли МБЛ-положительных штаммов в основном был обусловлен распространением эпидемических клонов ST235 и, в меньшей степени, ST234. ST235 является центральным сиквенс-типом клонального комплекса 235 (СС235) и известен как международный эпидемический клон [3].
В этой ситуации своевременная микробиологическая диагностика и строгое соблюдение мер инфекционного контроля в стационарах являются единственным путем сдерживания распространения МБЛ.
СПИСОК ЛИТЕРАТУРЫ
- Сухорукова М. В., Эйдельштейн М. В., Склеенова Е. Ю , Иванчик Н. В., Тимохова А. В., Дехнич А. В., Козлов Р. С. и исследовательская группа «Марафон». Антибиотикорезистентность нозокомиальных штаммов Enterobacteriaceae в стационарах России: результаты многоцентрового эпидемиологического исследования МАРАФОН в 2011 – 2012 гг.// Клин микробиол антимикроб химиотер.- 2014.- №16 (4). – C.254-265.
- Решедько Г. К., Рябкова Е. Л., Кречикова О. И., Сухорукова М. В., Шевченко О. В., Эйдельштейн М. В., Козлов Р. С., Туркутюков В. Б., Нехаева Г. И., Бочкарев Д. Н., Розанова С. М., Боронина Л. Г., Агапова Е. Д., Марусина Н. Е., Мултых И. Г., Тарабан В. К., Здзитовецкий Д. Э., Сарматова Н. И., Тихонов Ю. Г., Поликарпова С. В. и др. Резистентность к антибиотикам грамотрицательных возбудителей нозокомиальных инфекций в ОРИТ многопрофильных стационаров России. //Клин. микробиол. антимикроб химиотер. – 2008.- №10(2). С.96 – 112.
- Эйдельштейн М. В., Склеенова Е. Ю., Шевченко О. В., Тапальский Д. В., Азизов И. С., Дсоуза Д. В., Тимохова А. В., Сухорукова М. В., Козырева В. К.,Сафронова Е. В., Астахова М. В., Карпов И. А., Шамаева С. Х., Абрамова Н. В., Гординская Н. А., Козлов Р. С. Распространенность и молекулярная эпидемиология грамотрицательных бактерий, продуцирующих метало-бета-лактамазы, в России, Беларуси и Казахстане. //Клин микробиол антимикроб химиотер. – 2012. - №14(2). – С.132-152.
- Сидоренко С. В., Эйдельштейн М. В. Механизмы резистентности микроорганизмов. //Практическое руководство по антиинфекционной химиотерапии под ред. Страчунского Л. С., Белоусова Ю. В., Козлова С. Н. – 2007. - С.19 – 31.
- Фурсова Н., Прямчук С. Д., Абаев И. В., Ковалев Ю. Н., Шишкова Н. А., Печерских Э. И. и др. Генетическое окружение генов blaCTX-M, локализованных на коньюгативных плазмидах нозокомиальных изолятов Enterobacteriaceae, выделенных в России в 2003 – 2007гг. //Антибиотики и химиотерапия. – 2010. - №55 (11 – 12). С.3 – 10.
- Сидоренко С. В., Партина И. В., Агеевец В. А. Имипенем: 30 лет терапии. //Антибиотики и химиотерапия. – 2013. - №58 (5 – 6). – С.55 – 61.
- Bush K., Jacoby G. A., Medeiros A. A. A functional classification scheme for β-lactamases and its correlation with molecular structure. //Antimicrob.Agents Chemother. – 1995. – Vol.39 – P.1211 – 1233.
- Bush K., Jacoby G.A. Updated functional classification of blactamases //Antimicrob. Agents Chemother. - 2010. - №54 (3). - Р.969 - 976.
- Jacoby G.A. AmpC blactamases //Clin. Microbiol. Rev. - 2009. - №22. -Р. 161-182.
- Jacoby G.A., Mills D.M., Chow N. Role of blactamases and porins in resistance to ertapenem and other blactams in Klebsiella pneumoniae //Antimicrob. Agents Chemother. - 2004. - №48. – Р.3203-3206.
- Quale J., Bratu S., Gupta J., Landman D. Interplay of efflux system, ampC, and oprD expression in carbapenem resistance of Pseudomonas aeruginosa clinical isolates //Antimicrob. Agents Chemother. - 2006. - №50. - Р.1633-1641.
- Lee S.H., Jeong S.H., Park Y.M. Characterization of blaCMY10, a novel, plasmidencoded AmpCtype blactamase gene in a clinical isolate of Enterobacter aerogenes //J. Appl. Microbiol. - 2003. - №95. - Р. 744-752.
- Wachino J., Kurokawa H., Suzuki S. et al. Horizontal transfer of blaCMYbearing plasmids among clinical Escherichia coli and Klebsiella pneumoniae isolates and emergence of cefepimehydrolyzing CMY19 //Antimicrob. Agents Chemother. - 2006. - №50. - Р.534-541.
- Doi Y., Paterson D.L., AdamsHaduch J.M. et al. Reduced susceptibility to cefepime among Escherichia coli clinical isolates producing novel variants of CMY2 β-lactamase //Antimicrob. Agents Chemother. – 2009 .- №53. - Р. 3159-3161.
- RodríguezMartínez J.M., Poirel L., Nordmann P. Extendedspectrum cephalosporinases in Pseudomonas aeruginosa //Antimicrob. Agents Chemother. - 2009. - №53. – Р. 1766 - 1771.
- Mammeri H., Nordmann P., Berkani A., Eb F. Contribution of extendedspectrum AmpC (ESAC) blactamases to carbapenem resistance in Escherichia coli //FEMS Microbiol. Lett. - 2008. - №282. – Р. 238 - 240.
- Paterson D.L., Bonomo R.A. Extendedspectrum betalactamases: a clinical update //Clin. Microbiol. Rev. - 2005. - №18 (4). – Р. 657-686.
- Pitout J.D.D. Infections with extendedspectrum blactamaseproducing Enterobacteriaceae. Changing epidemiology and drug treatment choices //Drugs. - 2010. - №70 (3). – Р. 313 - 333.
- Matsumoto Y., Ikeda F., Kamimura T. et al. Novel plasmidmediated betalactamase from Escherichia coli that inactivates oxyiminocephalosporins //Antimicrob. Agents Chemother. - 1988. - №32 (8). – Р. 124 - 136.
- Poirel L., Lartigue M.F., Decousser J.W. et al. ISEcp1Bmediated transposition of blaCTXM in Escherichia coli //Antimicrob. Agents Chemother. - 2005. - №49 (1). – Р. 447 - 450.
- Bonnet R. Growing group of extendedspectrum blactamases: the CTXM enzymes //Antimicrob. Agents Chemother. - 2004. - №48. - Р. 11 - 14.
- Poirel L., Naas T., Nordmann P. Genetic support of extendedspectrum betalactamases //Clin. Microbiol. Infect. - 2008. - №14 (Suppl. 1). Р. 75 - 81.
- Poirel L., Gniadkowski M., Nordmann P. Biochemical analysis of the ceftazidimehydrolysing extendedspectrum betalactamase CTXM15 and of its structurally related betalactamase CTXM3 //J. Antimicrob. Chemother. - 2002. - №50 (6). – Р. 103 - 114.
- Степанова М. Н. Мутациоонная изменчивость CTX-M ß-лактамаз и формирование устойчивости к цефтазидиму у клинических и лабораторных штаммов Escherichia coli. //Автореф. уч.степени канд.биол.наук. - 2011. - С.23.
- Сидоренко С. В., Березин А. Г., Иванов Д. В. Молекулярные механизмы устойчивости грамотрицательных бактерий семейства Enterobacteriaceae к цефалоспориновым антибиотикам. //Антибиотики и химиотерапия. - 2011. - №49(3). – С.6 – 16.
- Rossolini G. M., D'Andrea M., Mugnaioli C. The spread of CTX-M-type extended-spectrum β-lactamases. //Clin Microbiol Infect. – 2008. - №14(Suppl.1). – Р. 33 - 41.
- Petroni A., Melano R.G., Saka H.A. et al. CARB9, a carbenicillinase encoded in the VCR region of Vibrio cholerae nonO1, nonO139 belongs to a family of cassetteencoded blactamases //Antimicrob. Agents Chemother. - 2004. - №48. – Р. 4042 - 4046.
- Potron A., Poirel L., Croizé J. et al. Genetic and biochemical characterization of the first extendedspectrum CARBtype blactamase, RTG4, from Acinetobacter baumannii //Antimicrob. Agents Chemother. - 2009. - №53. –Р. 3010 - 3016.
- Bradford P.A. Extendedspectrum blactamases in the 21st century: characterization, epidemiology, and detection of this important resistance threat //Clin. Microbiol. Rev. - 2001. - №14. - Р. 933 - 951.
- WaltherRasmussen J., Hoiby N. OXAtype carbapenemases //J. Antimicrob. Chemother. - 2006. - №57. - Р. 373 - 383.
- Poirel L., Heritier C., Tolun V., Nordmann P. Emergence of oxacillinasemediated resistance to imipenem in Klebsiella pneumoniae //Antimicrob. Agents Chemother. - 2004. - №48. - Р. 15 - 22.
- Martinovich A., Edelstein M., Kozlov R. Multilocus sequence typing of Acinetobacter strains from Russia and Belarus that produce acquired OXA carbapenemases. //49th Interscience Conference on Antimicrobial Agents and Chemotherapy. - 2009 September. - San Francisco, CA, USA.
- Yotsuji A., Minami S., Inoue M., Mitsuhashi S. Properties of novel blactamase produced by Bacteroides fragilis //Antimicrob. Agents Chemother. - 1983. - №24. Р. 925 - 929.
- Livermore D.M., Woodford N. Carbapenemases: a problem in waiting? //Curr. Opin. Microbiol. - 2000. - №3. - Р. 489 - 495.
- Mercuri P.S., Ishii Y., Ma L. et al. Clonal diversity and metalloblactamase production in clinical isolates of Stenotrophomonas maltophilia //Microb. Drug Resist. - 2002. - №8. - Р. 193 - 200.
- Miriagou V., Cornaglia G., Edelstein M., et al. Acquired carbapenemases in Gram-negative bacterial pathogens: detection and surveillance issues. //Clin Microbiol Infect. - 2010. - №16(2). - Р. 112 - 122.
- Cornaglia G., Giamarellou H., Rossolini G. M. Metallo-beta-lactamases: a last frontier for beta-lactams? //Lancet Infect Dis. - 2011. - №11(5). - Р. 381-393.
- El Salabi A., Borra P. S., Toleman M. A., Samuelsen O., Walsh T. R. Genetic and biochemical characterization of a novel metallo-beta- lactamase, TMB-1, from an Achromobacter xylosoxidans strain isolated in Tripoli, Libya. //Antimicrob Agents Chemother. - 2012. - №56(5). - Р. 2241 - 2245.
- Walsh T. R., Toleman M. A., Poirel L., Nordmann P. Metallo-beta-lactamases: the quiet before the storm? //Clin Microbiol Rev. - 2005. - №18(2). - Р. 306 - 325.
- Nordmann P., Poirel L., Walsh T. R., Livermore D. M. The emerging NDM carbapenemases. //Trends Microbiol. - 2011. - №19(12). - Р. 588 - 595.
- Toleman M. A., Spenser J., Jones L., Walsh T. R. blaNDM-1 is a chimera likely constructed in Acinetobacter baumannii. //Antimicrob Agents Chemother - 2012. - №56(5). - Р. 2773 - 2776.
- Giske C. G., Froding I., Hasan C. M., at al. Diverse Sequense Types of Klebsiella pneumoniae Contribute to the Dissemination of blaNDM-1 in India, Sweden and United Kingdom. //Antimicrob Agents Chemother. - 2012. - №56(5). - Р. 2735 - 2738.