Плюрипотентные стволовые клетки ( в том числе индуцированные) могут Дифференцироваться в различные клетки взрослого организма. Наличие плюрипотентных клеток у взрослого организма остается объектом научных Дискуссий, хотя исследования показали, что существует возможность получения плюрипотентных клеток из фибробластов взрослого человека в лабораторных условиях в процессе так называемого репрограммирования клеток.
Существуют как этические, так и технические затруднения, связанные с получением культур клеток из плюрипотентных стволовых клеток. Эти проблемы связаны, в том числе, с практикой испытания лекарственных среДств на культурах клеток животных и человека. Такие проблемы могут быть разрешены при использовании собственных стволовых клеток или путем их клонирования. Возникла необходимость в развитии новых направлении тестирования лекарственных среДств с использованием клеточных культур и клеточных линии, полученных из плюри-мульти-потентных стволовых клеток.
Стратегией правительства РК обозначены основные векторы развития фармацевтической промышленности, основными задачами которой является повышение конкурентоспособности отечественной фармацевтической промышленности, стимулирование разработки и производства инновационых лекарственных средств, увеличение обеспеченности населения жизненно необходимыми и важнейшими лекарственными средствами, подготовка высококвалифицированных кадров в области фармацевтического производства [1].
Конечной целью данной программы является создание устойчивой конкурентоспособной национальной индустрии, способной обеспечить население РК эффективными лекарственными средствами в необходимом количестве.
Несмотря на то, что некоторые препараты, производящиеся в РК, не уступают по качеству западным аналогам, казахстанцы часто предпочитают западную продукцию собственной. На данный момент на внутреннем рынке страны преобладают дженерики-аналоги импортных медикаментов. К сожалению, их качество оставляет желать лучшего, более высокая токсичность и меньшая эффективность существенно вредит здоровью.
Средняя стоимость разработки оригинального препарата — от $1 до 5 млрд. Из 10 тыс. молекул до этапа испытаний на культурах клеток доходит 10-20, до этапа клинических исследований — 2-3, до этапа регистрации — 1 молекула[2]. Если мы не разработали препарат и не предлагаем его миру, то есть ли смысл стремиться к тому, чтобы в своей стране налаживать его производство этих, хоть и дорогих, но все же ориентированных на узкую часть рынка потребляемых препаратов? Может, проще искать пути снижения цены на них (например, за счет современных схем оплаты с разделением рисков в рамках страховой медицины) и увеличивать тем самым доступность этих лекарств для пациентов, которых совсем немного. При этом одновременно направить усилия на поиски лекарств от тех болезней, которые пока не излечиваются и генетические риски для коренной национальности превышают мировые эпидемиологические показатели? Тем более что сейчас приходит время биотехнологий, и в Казахстане это направление стало неплохо развиваться.
Однако здесь есть один технологический нюанс. Если мы будем фокусироваться на производстве аналогов биологических препаратов, то перед нами остро встанет вопрос взаимозаменяемости. Лекарство из одной культуры микробных, гибридомных клеток может действовать хорошо, а точно такое же лекарство из другой культуры может не действовать. Поэтому, когда наши отечественные производители пытаются повторять зарубежные биотехнологические разработки, эти лекарства обязательно должны пройти доклинические и клинические испытания, чтобы больные были уверены в том, что этими препаратами можно заменить исходные.
До недавних пор существовало два основных подхода к доклиническим испытаниям: клеточные технологии и испытания на животных. В настоящее время все лекарственные средства сначала проходят испытания на клеточных культурах, далее - на животных, и только после этого на человеке.
В чем недостаток клеточных технологий? Все-таки они дают несистемный ответ. Тестируют только один или в лучшем случае два типа клеток одновременно и смотрят, как эти клетки реагируют на лекарственные вещества — оценивают токсичность, в некоторых случаях - снижение пролиферативной активности, влияние на дифференциацию, другие факторы.
Второй поход - это испытания на животных. Да, у животных ответ системный. Если мы вводим лекарственное средство перорально, оно попадает сначала в желудочно-кишечный тракт, подвергается действию ферментов и всасывается через стенки кишечника, трансформируется и модифицируется там, потом попадает в печеночный кровоток, где подвергается действию ферментов печени. Идет биотрасформация препарата и в ходе этого процесса могут образоваться токсичные продукты. Но здесь проблема в том, что вещества, которые успешно испытывают на животных, на человеке не всегда показывают аналогичное действие. Исходно фармакологический поиск начинают с большого числа молекул действующих препаратов , первую стадию отбора проходят 10 процентов, дальше остается один процент, и в конце концов из 10 тысяч кандидатных препаратов на рынок выходит одно вещество. В результате испытания на животных обходятся очень дорого. Известно, что сейчас вывести вещество на рынок стоит несколько миллиардов долларов, а от начала испытаний до выхода вещества в качестве лекарственного препарата проходит до 15-20 лет [3].
Одним из новых подходов, предлагаемой мировой наукой является использование микробиореакторов (микробиочипов) в доклинических исследованиях. Это платформа, на базе которой можно исследовать воздействие различных веществ на модели органов человека. Можно одновременно использовать несколько моделей - кожи, печени, нервной ткани, кишечника, почек, моделируя таким образом структурно-функциональную часть конкретной физиологической системы на органно-тканевом уровне. Для решения этой задачи компания Curiox Biosystems (Сингапур) разработала DropArray - платформу для миниатюризации, которая может снизить количество материала, требуемого для проведения исследования на клетках, в 1000 раз, при этом снизив в 10 раз время реакции. Компания утверждает, что время, необходимое для проведения многих экспериментов, может быть уменьшено 60%, причем материальные расходы могут быть снижены до 90%.
Первое направление в использовании микробиореакторов — это токсикологические исследования, то есть тестирование лекарственных, косметических препаратов.Мы можем наносить вещество в разных концентрациях на модель кожи (острая токсичность), смотреть, как оно проникает через кожу, не исключено, при этом оно может как-то трансформироваться (системы детоксикации существуют и в коже). Потом вещество попадает в кровоток и только после этого попадет в модель печени. То есть, это вещество действует на модель печени только после того, как оно уже проникло через кожу, т.е. пройдя молеклярно- биохимическую модификацию в коже и крови. И тогда непонятно, зачем смотреть его токсичность только для печени, если таким путём это вещество до неё не доберётся. Если же вещество проникает, то потенциально может быть токсично.
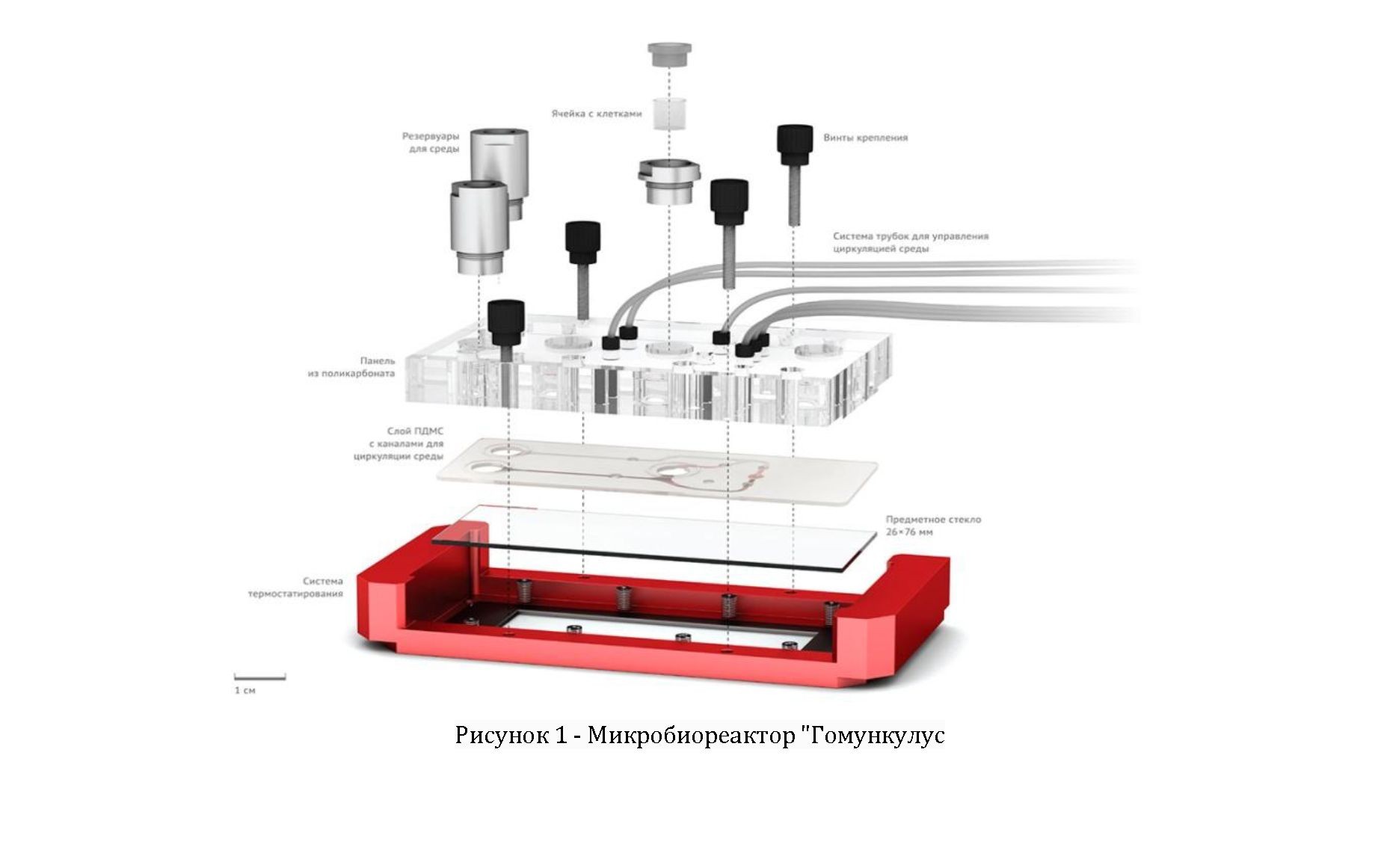
Микробиореактор "Гомункулус" позволяет следить также за развитием хронической токсичности. Для испытания хронической токсичности есть определенный срок, заданный европейскими стандартами - 28 дней. Для создания таких условий необходимо в микробиореакторе периодически менять питательную среду.
Для использования микробиореактора в практике испытаний лекарственных средств в качестве модели предлагается два подхода. Первый подход — модель состоит из клеточных линий, которые стандартизованы и одинаковы во всех лабораториях мира, второй — из материала биопсии, которую получают от конкретного пациента (персонализированная медицина).
Микробиореактор состоит из двух модулей. Первый - одноразовый клеточный блок, в котором происходит культивирование клеток и расположены ключевые датчики для определения их физиологического и функционального состояния. Второй - блок управления, осуществляющий поддержку и регуляцию параметров клеточного блока (температуры, скорости и пути циркуляции питательной среды), а также первичную обработку сигналов от сенсоров, расположенных в сменном клеточном блоке (определение концентрации ключевых клеточных метаболитов). Блок управления будет иметь возможность подключения к персональному компьютеру, на котором с помощью специально разработанного программного обеспечения будет осуществляться управление микробиореактором, а также анализ и интерпретация данных, полученных в процессе культивирования клеток и определения их основных параметров.
Второе направление - это использование микробиореактора для персонализированной медицины. Вот, например, есть пять типов рака молочной железы, их лечат разными лекарствами. Узнать эти типы не всегда представляется возможным, и лекарство может не подействовать. Зачем мучить человека, если мы можем взять пять кусочков биопсии и посмотреть действие пяти лекарств или больше, оценить, какое из них лечит, и конкретно этим лекарством проводить терапию. То есть не брать лекарство, которое, то ли будет работать, то ли нет. Есть типы опухолей гормон- зависимые и гормон-независимые. И вот появляется новый препарат, в частности, антитело герцептин. Казахстан его закупает на миллионы долларов. Примерно треть больных может излечиться, но остальные две трети больных он не поможет, и это, к сожалению, потраченные деньги. Но если заранее правильно подобрать лекарство, то, можно увеличить число тех людей, кто получит правильное лечение. Надо использовать небольшое количество раковых клеток, используя образцы, полученными при помощи прижизненной биопсии. Культивируя их несколько дней в микробиореакторе и воздействуя на эту культуру лекарством, можно получить информацию об отклике на генном уровне (транскриптома) на применяемую терапию. Все исследование на микробиореакторе с использованием одноразового чипа стоит около 100 долларов (для сравнения: иммуногистохимическое определение чувствительности к герцептину в биопсийном материале стоит в 3-4 раза дороже). По сравнению с тем огромным количеством денег (3-5000 долларов США на каждого больного), которые будут потрачены потом, это ничто. Чип одноразовый[4].
Существующая на сегодняшний день методика тестирования лекарственных препаратов не позволяет создать эффективную систему для фармакологического рынка. На испытание одного лекарственного препарата уходит не менее 5 лет, что, является непозволительно долго для современной биомедицины. По правилам, тестирование лекарственных препаратов происходит в два этапа, включающие в себя доклинические и клинические испытания. На первом этапе тестирование лекарственных препаратов проводят на модельных животных, а также на культурах клеток человека. Животные не всегда представляют собой хорошую модель для тестирования препаратов[5]. В самом деле, результаты таких исследований могут вводить в заблуждение, так как препараты, которые доказали свою безопасность для животных в дальнейшем могут оказаться вредными для людей, в то время как ценные лекарства и методы лечения могут быть пропущены, если они не прошли испытания на животных . И это не говоря уже об этической стороне использования животных для этих целей. Клеточные культуры человека являются гораздо более адекватной и удобной моделью для биомедицины, однако, в том виде, в котором данная система разработана и поставлена на сегодняшний день она имеет ряд существенных недостатков. Клеточные культуры получают путем биопсии пораженной ткани или органа и введении данных клеток в культуру. Однако такой способ имеет ряд непреодолимых ограничений. Так, для целого ряда заболеваний просто невозможно получить культуру клеток путем биопсии (клетки мозга, некоторых внутренних органов и т.д.), кроме того сама процедура биопсии является дорогостоящей, болезненной и, даже опасной для жизни пациента. Даже при успешном получении культуры клеток дифференцированных производных встает проблема времени и качества их культивирования. Как правило, такие дифференцированные производные имеют ограниченную способность к пролиферации, что приводит к ограничению количества клеток и времени проведения анализа, что значительно снижает качество испытания лекарственных препаратов. И самая главная проблема - это проблема наличия донора клеток, особенно, если речь идёт о редких наследственных заболеваниях или разновидностях мутаций. Таким образом, существующий подход тестирования лекарственных препаратов требует разработки новой, более эффективно работающей системы. В перспективе мы предлагаем совершенно новую технологию, пригодную для тестирования, разработки и применения лекарственных препаратов, которая позволит преодолеть существующие недостатки. Данная технология предполагает использование в качестве основы плюрипотентные стволовые клетки (ПСК) человека [6].
ПСК сходны по своим свойствам с эмбриональными стволовыми клетками, однако, имеют ряд преимуществ для биомедицинских исследований. Основное преимущество заключается в том, что они ПСК могут быть получены из соматических клеток различного происхождения (фибробласты кожи, кератиноциты, стволовые клетки жировой ткани, клетки периферической крови и другие) в любой период жизни человека. Использование пациент-специфичных ПСК позволяют исследовать болезнь на клеточном и молекулярном уровне, что может дать новые данные о патогенезе заболевания, выбрать молекулы или процессы клетки, являющиеся кандидатами для фармакологического воздействия[7]. Кроме того, из ПСК возможно получить практически все дифференцированные производные. Более того, ПСК возможно культивировать неограниченное время и получать производные в том количестве, в котором они необходимы для качественного исследования лекарственных препаратов. Данный проект направлен на создание эффективной методики использования ПСК в области клинической фармакологии и экспериментальногомоделирования патологических процессов, в основе которых лежит нарушение дифференцировки и развития самих стволовых клеток. Сложность в диагностировании таких видов заболевания, в первую очередь, связано с тем, что известно более десятка генов, и, соответственно, сотни мутаций, ассоциированных с развитием наследственных форм патологии стволовых клеток. Таким образом, найти такое количество доноров клеток, получить культуры клеток в необходимом количестве при различных формах заболевания не представляется возможным. В данном случае мы предлагаем совершенно новую систему, позволяющую избежать данные трудности - это создание панели изогенных линий ПСК человека, несущие мутации, опосредующие развитие различных форм патологии стволовых клеток. Создание такой панели изогенных линий основано на получении ПСК человека и последующем искусственном внесении определенных мутаций, опосредующие развитие различных форм генетических дефектов стволовых клеток. Наличие такой панели позволит провести скрининг сотни лекарственных препаратов в краткие сроки с максимальным результатом и выбрать наиболее эффективно работающие для каждой из патологии. Кроме того, эта система является моделью для подробного изучения патогенеза различных форм генетических заболеваний и использовании её в области клеточных технологий. Современные методы исследований будут включать в себя - молекулярно-генетический и цитологический анализ полученных линий ПСК и анализ экспрессии генов, характерных для плюрипотентности (методами микроэррей, ОТ-ПЦР, иммуноцитохимический метод), анализ метилирования ДНК промоторных областей генов OCT4 и NANOG (бисульфитное секвенирование), анализ активности фермента-теломеразы и Х-хромосом в клетках с набором половых хромосом XX, кариотипирование полученных клонов ПСК, исследование на предмет наличия хромосомных аберраций. Будут получены клоны ПСК, содержащие определенные мутации, опосредующие развитие различных форм заболеваний. Далее такие культуры клеток будут уже пригодны для полномасштабного скрининга лекарственных препаратов для лечения различных форм заболеваний. Таким образом, такая модернизация тестирования лекарственных препаратов приведет к: - увеличению качества лекарственных препаратов для каждого конкретного заболевания за счёт их апробации на более подходящих моделях; - увеличению эффективности лечения данного заболевания; - снижению стоимости лекарственных препаратов; - снижению времени испытания лекарственных препаратов; Данная технология является универсальной и будет пригодна не только для заболеваний, связанных с патологией стволовых клеток, но и для других заболеваний.
СПИСОК ЛИТЕРАТУРЫ
- Постановление Правительства Республики Казахстан Астана, Үкімет Үйі от 31 декабря 2013 года No 1594 «О Стратегическом плане Министерства здравоохранения Республики Казахстан на 2014-2018 годы»
- Huggins, D. J., Venkitaraman, A. R. & Spring, D. R. Rational methods for the
- selection of diverse screening compounds. ACS Chem. Biol.6,208-217 (2011).
- Research, C. for D. E. and. Investigational New Drug (IND) Application. at
- <http://www.fda.gov/drugs/developmentapprovalprocess/howdrugsaredevelopedandapproved/approvalapplications/investigational newdrugindapplication/default.htm#FDA Guidances for Investigational New Drugs>
- Huh D, Hamilton GA, Ingber DE. From 3D cell culture to organs-on-chips. Trends Cell Biol. 2011 Dec;21(12):745-54.
- Balani, S., Miwa, G., Gan, L.-S., Wu, J.-T. & Lee, F. Strategy of Utilizing In Vitro and In Vivo ADME Tools for Lead Optimization and Drug Candidate Selection. Curr. Top. Med. Chem.5,1033-1038.
- Yamanaka S, Blau HM. Nuclear reprogramming to a pluripotent state by three approaches. Nature. - 2010.- 465(7299)Р. 704-712.
- Luni C, Serena E, Elvassore N. Human-on-chip for therapy development and fundamental science. Curr Opin Biotechnol. 2014 Feb;25:45- 50.