Статья посвящена изучению некоторых клинических особенностей тяжелой черепно-мозговой травмы с внутричерепными кровоизлияниями. Материалом исследования служили 167 больных с тяжелыми повреждениями мозга. На основании проведенного анализа результатов лечения были выявлены особенности фомирования длительным посттравматических нарушений сознания, определена их частота. Разработан и внедрен метод электростимуляции стволовых отделов головного мозга при длительных посткоматозных состояниях.
ВВЕДЕНИЕ. Гипертензионно-дислокационный синдром (ГДС) обуславливает развитие витальных нарушений, приводящих к высокой летальности, составляющей по данным различных авторов 56 – 80 % [6, 19]. Кроме этого, травматические стволовые повреждения, по-видимому, имеют важнейшее значение для возникновения еще одного вида неблагоприятных исходов тяжелой ЧМТ – посттравматического вегетативного статуса (ВС) [2, 4, 7, 13]. В связи с ростом черепно-мозгового травматизма, успехами нейрореаниматологии, в последние годы отмечается рост числа этих больных [26]. При этом все пострадавшие из этой категории подвержены стойкой и глубокой инвалидизации, остается высокой смертность [26, 28]. Посттравматический ВС относится к мало изученной области неврологии и нейрохирургии. В частности, неясными являются вопросы о частоте возникновения ВС после черепно-мозговой травмы, влиянии на его формирование степени выраженности и характера травматического повреждения стволовых структур головного мозга в остром периоде травмы. Кроме того, сложнейшей проблемой на сегодняшний день являются и вопросы лечения посттравматического ВС [2, 26, 29]. Согласно мнению Ф. Плам и Дж.Б. Познер (1986) основная роль в развитии вегетативного статуса принадлежит угнетению функций восходящей активирующей ретикулярной формации в поврежденных стволовых отделах головного мозга [11]. В связи с этим, разработка методов лечения, направленных на активизацию ее функций, имеет приоритетное значение.
ЦЕЛЬ: изучение закономерностей формирования вегетативного статуса после интракраниальных посттравматических кровоизлияний и поиски путей улучшения его лечения.
МАТЕРИАЛ И МЕТОДЫ. Материалом исследования были 167 пациентов, перенесших тяжелую ЧМТ среди которых было 136 (81,4 %) мужчин и 31 (18,6 %) женщина в возрасте от 16 до 74 лет (средний возраст 32,8±1,3), которым было проведено комплексное клинико-неврологическое обследование. Диагностический комплекс включал в себя нейрорентгенологическое обследование (КТ и МРТ), электрофизиологическое обследование в динамике (ЭЭГ и регистрация акустических стволовых вызванных потенциалов - АСВП).
Тяжесть состояния больных определялась по степени нарушения сознания, состоянию витальных функций и очаговому неврологическому дефициту. Степень тяжести ЧМТ устанавливалась в соответствии с положениями единой классификации черепно-мозговой травмы [8]. Степень выраженности супратенториального варианта гипертензионно-дислокационного синдрома (ГДС) оценивалась с использованием схемы деления признаков дислокации при опухолях головного мозга супратенториальной локализации [9] в модификации РНХИ им. проф. А.Л. Поленова [5]. Результаты лечения оценивались на момент выписки больного из стационара (до 4 месяцев после ЧМТ) по шкале исходов Глазго (ШИГ) [11].
Для лечения больных в вегетативном состоянии был разработан метод чрезликворной электростимуляции (ЧЛЭС) ствола головного мозга [9, 10], который применялся в шести случаях. Методика заключается в проведении длительной электростимуляции после имплантации электродов в ликворосодержащие пространства головного мозга (боковой желудочек и большая затылочная цистерна). В процессе лечения использовались электростимуляторы «НЕЙРОЭЛЕКТ», разработанные в ФГУП «ВНИИОФИ» - НИИ нейрохирургии им. акад. Н.Н. Бурденко. Клинический эффект после электростимуляции оценивался по динамике восстановления психических функций с помощью шкалы пролонгированного коматозного состояния Tsubokawa T. et. al. [28], согласно которой наличие определенного клинического признака оценивается по 10-балльной шкале (Таблица 1).
Таблица 1 - Шкала пролонгированного коматозного состояния Tsubokawa T. et. al., 1990.
|
Клинический признак |
Баллы |
|
Жизнедеятельность со спонтанным дыханием |
1 |
|
Отдергивание конечностей на боль |
2 |
|
Спонтанное открывание и закрывание глаз |
3 |
|
Спонтанные движения конечностей |
4 |
|
Слежение |
5 |
|
Эмоциональные реакции |
6 |
|
Самостоятельное глотание при кормлении |
7 |
|
Воспроизведение звуков |
8 |
|
Выполнение команд |
9 |
|
Вербальный ответ |
10 |
РЕЗУЛЬТАТЫ. Тяжесть состояния обследованных была обусловлена черепно-мозговой травмой: тяжелое состояние установлено у 58 больных (34,7%), крайне тяжелое у 101 (60,5%), терминальное у 8 (4,8%). Первичная травма стволовых отделов головного мозга (ПТСГМ) диагностирована у 31 (18,6 %) обследованного, дислокационная травма - у 136 (81,4%). Признаки супратенториального ГДС были выявлены у 133 больных (79,6 %). По степени выраженности дислокации больные распределились следующим образом: I степень - 21 (15,8 %) человек, II - 53 (39,8 %), III - 56 (42,2 %), IV - 3 (2,2 %) пострадавших соответственно. Субтенториальные варианты дислокационного синдрома наблюдались в 3 (1,8 %) случаях.
Большинству больных (146 наблюдений - 87,4%) как с первичным, так и с дислокационным повреждением ствола головного мозга было выполнено хирургическое лечение. В табл. 2 представлены различные виды травматического субстрата вызвавшего развитие дислокации. Из таблицы видно, что наиболее часто выраженный ГДС (III и IV степень) выявлен у пациентов с субдуральными гематомами (75,9 %), множественными очагами размозжения головного мозга в сочетании с интракраниальной гематомой (64,3 %).
Таблица 2 - Виды морфологического субстрата, вызвавшего сдавление мозга у обследованных.
|
Морфологический субстрат |
ГДС I |
ГДС II |
ГДС III |
ГДС IV |
Всего |
|
Эпидуральная гематома |
2 (9,5%) |
6 (11,3%) |
5 (8,9%) |
- |
13 (9,8%) |
|
Субдуральная гематома |
2 (9,5%) |
5 (9,4%) |
20 (35,7%) |
2 (66,7%) |
29 (21,8%) |
|
Внутримозговая гематома |
1 (4,8%) |
11 (20,8%) |
4 (7,1%) |
- |
16 (12,0%) |
|
ОРГМ |
4 (19%) |
9 (17%) |
2 (3,6%) |
- |
15 (11,3%) |
|
Контузионные очаги |
3 (14,3%) |
- |
- |
- |
3 (2,3%) |
|
Множественные ОРГМ |
1 (4,8%) |
10 (18,9%) |
8 (14,3%) |
1 (33,3%) |
20 (15,0%) |
|
ОРГМ + интракраниал. гемат. |
4 (19%) |
7 (13,2%) |
8 (14,3%) |
- |
19 (14,3%) |
|
МОРГМ+интракраниал. гемат. |
- |
5 (9,4%) |
9 (16,1%) |
- |
14 (10,5%) |
|
Отек гемисферы |
4 (19%) ¯¯ |
- |
- |
- |
4 (3,0%) |
|
Итого |
21(100%) |
53 (100%) |
56 (100%) |
3 (100%) |
133 (100%) |
Примечание: ОРГМ - очаг размозжения головного мозга; МОРГМ - множественные очаги размозжения головного мозга; МОРГМ - множественные очаги размозжения головного мозга.
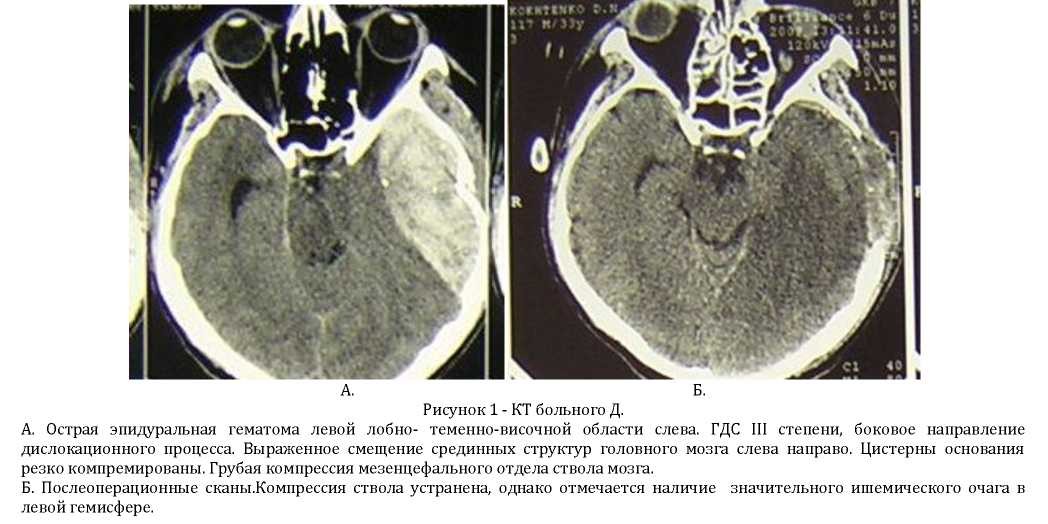
Или без нее (45 %), а также у 8 пациентов (42,1 %) с единичным очагом размозжения и интракраниальной гематомой. При КТ или МРТ исследовании головного мозга у больных этой группы выявлялись смещение срединных структур головного мозга от 5 до 28 мм, сдавление боковых желудочков, базальных цистерн мозга, а также последствия этих процессов (Рисунок 1 А, Б). Менее выраженная дислокация определялась у пострадавших с единичными очагами размозжения, очагами контузии головного мозга и отеком одной из гемисфер мозга. Оперативное вмешательство у больных с дислокационной травмой ствола проводилось в ближайшие часы после поступления в стационар и было направлено на удаление компремирующего субстрата.
При первичной травме ствола головного мозга (31 наблюдение) показаниями к хирургическому лечению служили КТ- и МРТ- признаки внутричерепной гипертензии, возникающие вследствие отека головного мозга. К таким признакам относили компрессию базальных цистерн и боковых желудочков головного мозга. Как правило, в подобных случаях при нейровизуализационном исследовании обнаруживались множественные мелкие контузионные очаги, локализующиеся субкортикально, паравентрикулярно, в области базальных ядер и мозолистого тела. Хирургическое лечение при ПТСГМ проведено в 17 (54,8 %) случаях и было направлено на создание декомпрессии на стороне преобладающего поражения у пациентов с субкомпенсированными витальными функциями.
Результаты лечения больных с тяжелой ЧМТ, в зависимости от характера и выраженности поражения ствола головного мозга представлены в табл. 3. Наиболее благоприятные результаты получены при I и II степенях дислокационного синдрома, а летальные исходы в этих наблюдениях были обусловлены такими осложнениями травмы как менингит, гнойная пневмония, отек легких. У пострадавших с III степенью ГДС летальные исходы составили 91,1%, а благоприятных исходов не было установлено ни в одном наблюдении. При ГДС IV степени все пострадавшие погибали, независимо от объема и сроков проведенных оперативных вмешательств. Благоприятных результатов лечения первичной травмы ствола не наблюдалось, хотя летальность была значительно ниже, чем при III степени дислокационного синдрома.
Такой исход травмы как посттравматический ВС развился у 12 (7,2 %) обследованных – в 5 случаях из 31 первичного и в 7 случаях из 136 дислокационных поражений ствола головного мозга. В процентном отношении это составило 16,1% и 5,1 % соответственно. При анализе частоты развития вегетативного статуса в зависимости от характера повреждения ствола головного мозга у выживших больных (75 человек), было установлено, что это патологическое состояние сформировалось у 41,7 % (5 случаев) пациентов с первичным повреждением ствола (12 наблюдений) и у 11,2 % выживших больных (7 случаев) с дислокационным характером повреждения (63 наблюдения). Таким образом, вегетативный статус развивался практически в 4 раза чаще (p< 0,05) при первичных стволовых повреждениях. При анализе частоты формирования ВС, в зависимости от степени дислокации установлено, что вегетативный статус сформировался у 3 (5,7 %) пациентов с ГДС II степени и у 4 (8,5 %) с ГДС III степени.
Таблица 3 - Исходы тяжелой черепно-мозговой травмы, в зависимости от характера и выраженности травматического поражения
ствола головного мозга по шкале исходов Глазго [16].
|
Исходы по ШИГ |
Степени выраженности ГДС |
МТД |
ПТСГМ |
Итого |
|||
|
J |
II |
III |
IV |
||||
|
V |
8 (38,1%) |
1 (1,9%) |
- |
- |
- |
- |
9 (5,4%) ¯¯ |
|
IV |
11 (52,4%) |
24 (45,3%) |
- |
- |
- |
- |
35 (20,9%) |
|
¯¯īɪɪ |
- |
11 (20,7%) |
1 (1,8%) |
- |
- |
7 (22,6%) |
19 (11,4%) |
|
II |
- |
3 (5,7%) |
4 (7,1%) ¯¯ |
- |
- |
5 (16,1%) ' |
12 (7,2%) ¯¯ |
|
I |
2 (9,5%) |
14 (26,4%) |
51 (91,1%) |
3 (100%) |
¯3 (100%) |
19 (61,3%) |
92 (55,1%) |
|
Всего |
21 (100%) |
53 (100%) |
56 (100%) |
3 (100%) |
3 (100%) |
31 (100%) |
167 (100%) |
Примечание: V- хорошее восстановление, IV - умеренное нарушение функции, III - грубое нарушение функции, II - вегетативное состояние, I – летальный исход. МТД – мозжечково-тенториальная дислокация. ПТСГМ – первичная травма ствола головного мозга.
Для клинико-неврологической симптоматики обследованных с ВС было характерным отсутствие поведенческих реакций на голосовые стимулы, речи и активных движений, плавающие движения глазных яблок или их неподвижность, а также нарушение смены фаз сон- бодрствование. Грубые очаговые неврологические симптомы выявлялись во всех наблюдениях и проявлялись нарушениями функций черепно-мозговых нервов, двигательными нарушениями и расстройствами мышечного тонуса, оральными автоматизмами. Еще одним, наблюдавшимся во всех случаях, проявлением этой патологии было наличие вегетативных нарушений, которые проявлялись нестабильностью артериального давления, лабильностью пульса, потливостью, слюнотечением. У 4 (33,4 %) обследованных вегетативные нарушения носили резко выраженный характер с отмечавшимися периодически вегетативными кризами, у 8 (66,7 %) пациентов - были относительно стабильны. Нарушения мышечного тонуса проявлялись характерными позно- тоническими реакциями - декортикационной или децеребрационной ригидностью, поворотами головы, туловища. Выделение декортикационного или
децеребрационного варианта тонических расстройств было затруднительным вследствие наблюдавшегося их сочетания и сопутствующими пирамидными нарушениями. Однако были отмечены некоторые различия в группе больных с дислокационной травмой (7 наблюдений - 58,4 %) и первичной травмой ствола (5 наблюдений – 41,7 %). Так в 6 случаях с дислокационной травмой наблюдались изменения мышечного тонуса по децеребрационному типу. В 1 наблюдении отмечено сгибание руки с одной стороны и разгибание с другой. В группе больных с первичной травмой ствола наблюдались явные декортикационные реакции, сочетавшиеся с невыраженными децеребрационными проявлениями.
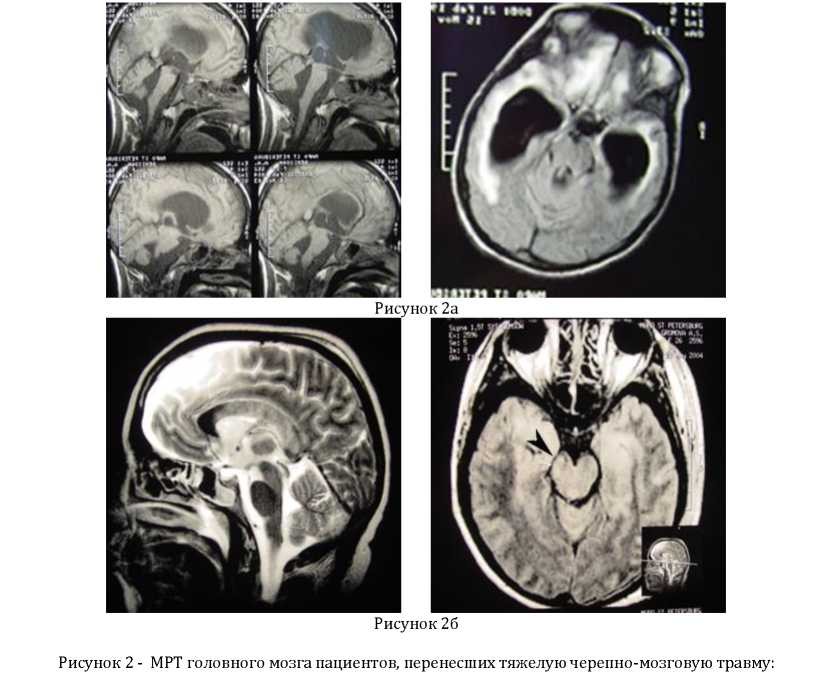
а. МРТ головного мозга пациентки Г., 23 г. с тяжелой закрытой черепно-мозговой травмой и первичным повреждением ствола головного мозга (контузионный очаг в ножке мозга указан стрелкой). Обследование проведено на фоне восстановления психических функций, после выхода из коматозного состояния на 28 сутки после травмы. На томограммах не наблюдается атрофии ствола головного мозга;
Среди методов диагностики, особую ценность представляла МРТ головного мозга, которая позволяла с высокой степенью разрешающей способности диагностировать посттравматические изменения тканей головного мозга и ликворосодержащих пространств, как правило, сопутствующие длительным нарушениям сознания травматической этиологии. Во всех случаях выявлены грубые посттравматические изменения, которые локализовались не только в стволе головного мозга, но и в коре, подкорковых структурах, базальных ганглиях и мозолистом теле. Основным достоинством МРТ при обследовании данной группы пациентов, на наш взгляд, является высокая точность визуализации стволовых структур головного мозга. Характерным является то обстоятельство, что всех наблюдениях, по данным МРТ, наблюдались изменения атрофического характера в различных отделах головного мозга с обязательным наличием атрофических изменений ствола головного мозга. На рис. 2 представлены МР-томограммы двух пациентов – в одном случае (рис. 2 а), обследование проведено у больной на фоне восстановления уровня сознания после выхода из комы, в другом – МРТ головного мозга выполнено
б. МРТ головного мозга пациентки Д., 19 лет, с тяжелой закрытой черепно-мозговой травмой и первичным повреждением ствола головного мозга. Обследование проведено на фоне вегетативного статуса на 63 сутки после травмы. Определяется вентрикуломегалия, атрофические изменения больших полушарий на фоне выраженных атрофических изменений ствола головного мозга.
пациентке в вегетативном статусе (рис. 2 б). Основное отличие МРТ-картины двух обследованных, заключается в наличии и отсутствии признаков атрофии ствола головного мозга.
Разработанный метод чрезликворной элетростимуляции ствола головного мозга применялся шести пациентам в вегетативном статусе. Электроды устанавливались следующим образом: первый электрод подводился в передний рог бокового желудочка через ранее установленный вентрикулярный дренаж. Второй электрод устанавливался транскутанно в большую затылочную цистерну. ЧЛЭС проводилась в сроки от 13 до 96 дней после травмы, в каждом случае ежедневно (три сеанса в сутки), в течение 21 дня. Применялся постоянный ток с прямоугольными импульсами частотой от 30 до 100 Гц, сила тока – 1,5 – 3,5 мА, длина волны – 200 – 600 мкс. Параметры тока (в указанных пределах) подбирались индивидуально с помощью электрофизиологического мониторинга. При этом благоприятными изменениями ЭЭГ считались снижение выраженности дистантной синхронизации, увеличение частоты колебаний, а также повышение амплитудных значений при фоновой «плоской» ЭЭГ. Подобные изменения расценивались как реакция десинхронизации [20].
Продолжительность одного сеанса стимуляции составляла 15 - 20 минут.
У всех пациентов клинически определялась отчетливая реакция на электростимуляцию уже непосредственно в момент начала стимуляции. Она выражалась появлением двигательной активности (открывание глаз, движения глазных яблок, моторная активность в жевательных мышцах и конечностях), умеренным расширением зрачков. После проведения сеанса электростимуляции определялось снижение ранее повышенного тонуса в конечностях. После окончания курса ЧЛЭС у 3 больных наблюдалось восстановление психических функций по шкале Tsubokawa T. et. al. (1990) [28] до 8 и 9 баллов при исходных - 2 и 3 балла (рисунок 3).
У трех пострадавших отмечено восстановление психических функций до 5 и 6 баллов при исходных - 1, 3 и 2 балла (рисунок 3). На рис. 3 представлена диаграмма, отражающая усредненный уровень психических функций у обследованных, оцененный по шкале Tsubokawa Т. et al. (1990) [28] до и после курса электростимуляции.
Паттерны ЭЭГ у всех больных были представлены характерными для травматических стволовых поражений отсутствием основного ритма, доминированием медленной активности, имеющей синхронный характер (Рисунок 4 а).
а. ЭЭГ до электростимуляции - неустойчивость и деформация основного ритма с билатеральными вспышками высокоамплитудных колебаний различного диапазона;
б. ЭЭГ во время электростимуляции - на фоне артефактов («наводки») вызванных активацией электростимулятора определяются перестройки биопотенциалов мозга в виде увеличения частоты колебаний и снижения выраженности дельта активности.
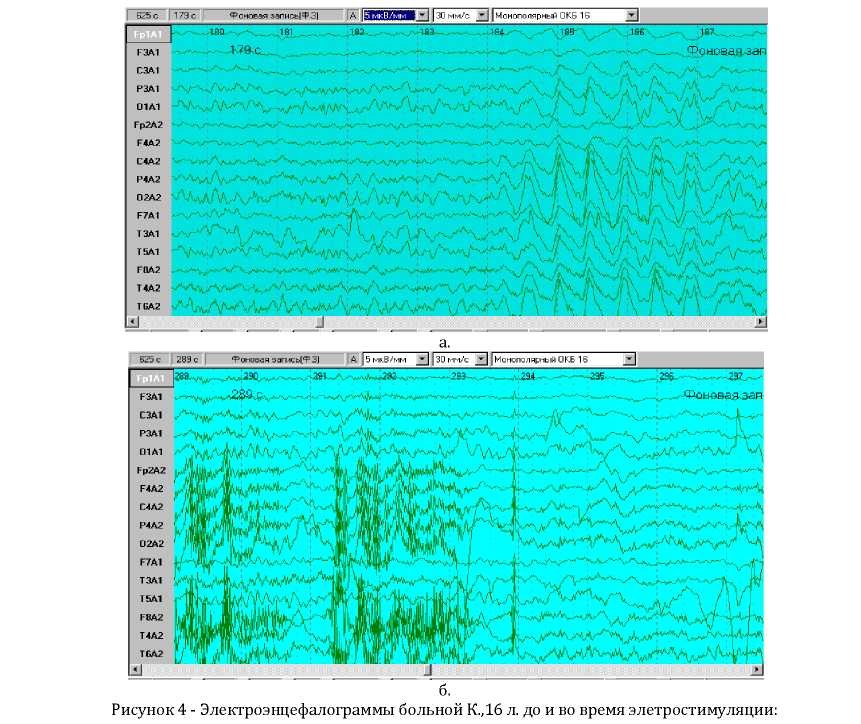
На фоне проведения электростимуляции, во всех случаях были отмечены положительные перестройки биоэлектрической активности, проявляющиеся уменьшением выраженности дистантной синхронизации и увеличением частоты колебаний (Рисунок 4 б). Необходимо также отметить, что ни в одном случае не было выявлено типичных эпилептиформных изменений биоэлектрической активности (пароксизмальные вспышки, комплексы “пик - волна” и др.).
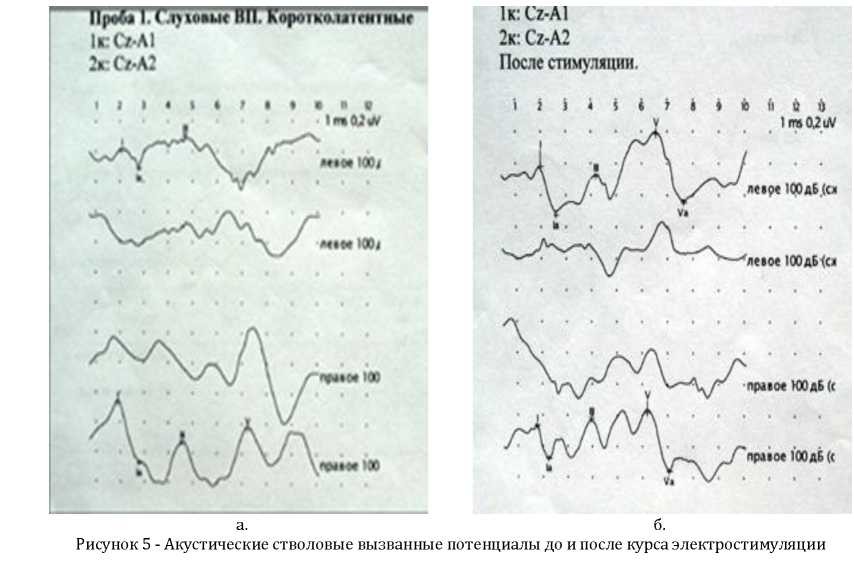
У всех больных до стимуляции в паттернах АСВП наблюдалось увеличение интерпиковых расстояний и латентностей пиков всех волн (Рисунок 5 а), что свидетельствовало о поражении стволовых отделов головного мозга на мезенцефало-понтинном уровне.
П-т. Ш., 38 лет: а. АСВП до начала электростимуляции - слева выявляется отсутствие V пика, удлинение латентных периодов I и III пиков и удлинение интерпикового расстояния I-III слева и I-III, III - V, I-V справа; б. АСВП после курса элетростимуляции - слева выявляется появление V пика, укорочение латентного периода III пика на 25 % от исходного значения и укорочение интерпикового расстояния I-III на 35 % от исходного значения; справа наблюдается укорочение латентных периодов I-III пиков - на 15 %, III-V - на 5 % и I-V - на 25 % от исходных значений. Непосредственно после проведения первых сеансов ЧЛЭС было зарегистрировано укорочение интерпиковых расстояний и латентностей пиков волн на 5 - 62 % от исходного, увеличение амплитуды 1, 3 и 5 пиков на 32 - 78 % (Рисунок 5 б).
При проведении контрольного исследования после окончания курса электростимуляции (в сроки до 1 месяца) результаты, достигнутые в ходе лечения, сохранялись.
ОБСУЖДЕНИЕ. Являясь, по сути, неблагоприятным исходом травмы, с другой стороны вегетативный статус на современном этапе можно рассматривать как нежелательный, но неизбежный исход критической черепно-мозговой травмы с тяжелым травматическим повреждением стволовых отделов мозга, а частота его развития косвенно может служить показателем «класса» нейрореаниматологического отделения клиники. В связи с этим, продолжающийся рост удельного веса тяжелой черепно-мозговой травмы в общей структуре травматизма, развитие нейрореаниматологии, совершенствование методов лечения тяжелой ЧМТ будут приводить к дальнейшему росту числа больных с длительными посттравматическими нарушениями сознания. По- видимому, необходимость изучения этой категории больных, разработка новых методов лечения будет все более актуальной в будущем. Следует сказать, что в наших наблюдениях среди данной группы больных, как правило, наблюдались сочетанные комплексные последствия ЧМТ, как структурного, так и функционально-неврологического характера, основной особенностью которых было то, что они протекали на фоне длительного нарушения уровня сознания. Важным обстоятельством, на наш взгляд является тот факт, что среди больных в вегетативном статусе преобладали пациенты с первичным поражением ствола головного мозга, что на наш взгляд, может быть следствием двух причин: 1) при первичной травме ствола головного мозга летальность несколько ниже, чем при выраженных дислокационных поражениях (ГДС III - IV степеней). Следовательно, среди пострадавших с такой формой повреждения стволовых структур, выживших пациентов больше и у части из них наблюдаются длительные нарушения сознания; 2) возможно, что первичная травма ствола головного мозга, более «избирательно» приводит к нарушению функций активирующей ретикулярной формации ствола головного мозга, основным проявлением которой является нарушение сознания.
Данные исследования свидетельствуют о том, что травматическое повреждение стволовых структур головного мозга имеет кардинальное значение для исхода тяжелой черепно-мозговой травмы. На результаты лечения оказывает влияние не только выраженность травматического поражения ствола, но и его характер (первичный или дислокационный). Эти же факторы влияют и на частоту развития наиболее тяжелой формы последствий черепно-мозговой травмы - вегетативного статуса. Вместе с тем, считаем, что было бы не верно считать травматическое повреждение ствола головного мозга единственной причиной развития ВС. Согласно современным взглядам в формировании длительных бессознательных состояний имеют большое значение такие факторы, как диффузное обширное поражение головного мозга, двустороннее повреждение таламических областей, диффузное аксональное поражение ствола [7, 9, 11, 26]. В наших наблюдениях во всех случаях грубые посттравматические изменения визуализировались (КТ и
МРТ) не только в стволе головного мозга, но и в коре, подкорковых структурах, базальных ганглиях, мозолистом теле. В этой связи именно травматический вегетативный статус, вероятно, является неудачной моделью для установления роли тех или иных структур головного мозга в генезе его развития. Тем не менее, результаты проведенного исследования свидетельствуют о том, что травматическое повреждение ствола головного мозга, его характер и выраженность служит одним из основных факторов, определяющих формирование вегетативного статуса Наблюдающаяся в настоящее время тенденция к поиску и все более широкому применению методов электростимуляции различных структур ЦНС обусловлена наличием многих неврологических расстройств, лечение которых вызывает значительные затруднения. К ним, несомненно, относится и посттравматический вегетативный статус. Учитывая явный дефицитарный характер этого состояния, попытки применения электростимуляционных методов лечения логичны. Среди методов электростимуляции, применяемых при травматическом поражении головного мозга, наибольшее распространение получили транскраниальная электростимуляция [12], электростимуляция на уровне спинного мозга [15, 23, 27], а также метод глубокой интракраниальной электростимуляции (deep brain stimulation), осуществляющийся после имплантации электродов в глубокие структуры головного мозга (таламус или средний мозг) [14, 28]. Все эти методы значительно отличаются друг от друга и обладают как очевидными преимуществами, так и недостатками. Так, основные клинические эффекты транскраниальной электростимуляции связаны с распространением постоянного импульсного тока по ликворным пространствам конвекситальных, в меньшей степени базальных отделов интракраниального пространства с преимущественным воздействием на супратенториальные и на верхнестволовые отделы мозга [1]. При этом, в связи с вариабельной толщиной костей черепа и мягких тканей головы у разных индивидов, невозможно точно рассчитать параметры электрического воздействия на интракраниальные структуры [25], а раздражение обширных областей коры мозга вызывает усиление патологической медленной активности в лобных и лобновисочных отделах больших полушарий [12].
Электростимуляция задних столбов спинного мозга, очевидно, вызывает только опосредованное воздействие на стволовые структуры мозга за счет наличия связей восходящих чувствительных путей задних столбов и медиальной петли (II нейрон) с некоторыми ядрами ретикулярной формации ствола [21].
При стимуляции глубоких образований головного мозга (таламус, мезенцефальные отделы), по-видимому, активируются только те отделы ретикулярной формации, к которым непосредственно подведены биполярные электроды (локальность воздействия). Кроме того, нельзя не отметить, что процедура подведения электродов весьма опасна и сопряжена с деструкцией стволовых структур мозга [29].
В этой связи предлагаемая методика, на наш взгляд, имеет определенные преимущества: 1) простая методика установки электродов; 2) метод не сопровождается введением электродов в стволовые структуры мозга и его базальные ядра; 3) используемая схема расположения электродов и высокая электропроводность ликвора обуславливает воздействие электрического тока на ретикулярную формацию ствола головного мозга на всем её протяжении. Метод применен у 6 больных в вегетативном статусе. При этом основным положительным клиническим эффектом электростимуляции было восстановление психических функций больных, оцененное по шкале Tsubokawa Т. et al. (1990) [28]. Полученные клинические данные подтверждены электрофизиологическим мониторингом, который выявил возникновение реакции десинхронизации на ЭЭГ во время электростимуляции.
Подобные изменения ЭЭГ-кривой впервые в эксперименте были описаны Moruzzi G. и Magoun H. в 1949 году, а в дальнейшем подтверждены многочисленными исследованиями в момент пробуждения спящих обезьян, и получили название реакции десинхронизации или реакции «пробуждения» [20]. По мнению большинства исследователей, возникновение подобных изменений ЭЭГ (реакция десинхронизации) обусловлено активирующим влиянием ретикулярной формации ствола на полушария головного мозга [18, 24]. Кроме того, выявленные после электростимуляции укорочение латентностей пиков и межпиковых интервалов по данным АСВП, служат признаками улучшения синаптической передачи в церебральных структурах. В целом, результаты проведенного исследования свидетельствуют о том, что изменения в состоянии больных и показателях электрофизиологического контроля, по-видимому, являются следствием стимулирующего влияния электрического тока на структуры головного мозга и в первую очередь на ретикулярную формацию.
Предположительный механизм действия ЧЛЭС, по нашему мнению, заключается в следующем. Поскольку электрическое сопротивление ликвора на порядок ниже сопротивления тканей головного мозга, то большая часть электрического тока будет распространяться между электродами по ликворосодержащим пространствам: базальные цистерны → отверстия Люшка и Мажанди → IV желудочек → водопровод мозга → III желудочек → отверстие Монро → один из боковых желудочков мозга (в зависимости от положения электрода). M.L.G. Joy et. al. [17] убедительно показали в эксперименте, что электрический ток, распространяясь по ликвору, в значительной мере воздействует и на мозговые структуры, образующие ликворосодержащие пространства. В связи с этим, вероятно, можно считать, что при проведении ЧЛЭС прохождение тока по ликворным пространствам цистерн основания мозга оказывает непосредственное воздействие на продолговатый мозг и активирует дыхательный и сосудодвигательный центры. Электрический ток оказывает непосредственное активирующее влияние на ретикулярную формацию ствола головного мозга при прохождении через водопровод мозга и III желудочек. Распространение же электрического тока в ликвор бокового желудочка головного мозга обуславливает его воздействие на таламические структуры. Медиальное ядро таламуса имеет двустороннюю проекцию в ассоциативных полях префронтальной коры ростральнее премоторной зоны, т.е. при воздействии на медиальное ядро таламуса происходит активация самых больших долей мозга – лобных. Воздействие электрического тока на переднее ядро таламуса опосредованно поддерживает импульсацию в нейронных структурах лимбической системы, которая, согласно данным литературы, способствует обмену импульсами между структурами среднего и промежуточного мозга, а также отделами новой коры [3, 22].
ВЫВОДЫ:
- Развитие посттравматического вегетативного состояния наблюдается у 7,2% больных, перенесших тяжелую черепномозговую травму. При этом в его формировании определяющее значение имеют характер и выраженность травматического повреждения стволовых структур головного мозга. При первичной травме ствола головного мозга посттравматический вегетативный статус возникает чаще (41,7%), чем при дислокационной (11,2%) (p<0,05), причем в последней группе вегетативное состояние формируется только у больных с II и III степенью гипертензионно-дислокационного синдрома.
- Атрофические изменения в стволовых отделах головного мозга, выявляемые при магнитно-резонансной томографии, являются специфическими признаками, присущими вегетативному статусу травматической этиологии. МРТ- синдром травматического вегетативного статуса характеризуется грубыми посттравматическими изменениями головного мозга, его оболочек, ликворосодержащих пространств и обязательным наличием атрофии ствола мозга.
Чрезликворная электростимуляция ствола головного мозга при посттравматическом вегетативном статусе приводит к возникновению клинического улучшения в состоянии больных, подтверждаемого данными электрофизиологического исследования (ЭЭГ, АСВП), что свидетельствует о перспективности метода для применения в структуре комплексного лечения этой патологии.
СПИСОК ЛИТЕРАТУРЫ
- Джой, М.Л.Дж. Плотности тока и пути его распространения в мозге кролика при транскраниальной электростимуляции: изучение с помощью ядерномагнитнорезонансной томографии. // Транскраниальная электростимуляция. – СПб.: 2001. – С. 128 – 149.
- Доброхотова, Т.А. Обратимые посткоматозные бессознательные состояния. // Социальная и клиническая психиатрия. - 1996. - №3. - C. 26-36.
- Дуус, П. Топический диагноз в неврологии (анатомия, физиология, клиника) / Дуус П. – М.: ИПЦ Вазар-Ферро, 1997. – С. 173 – 179.
- Зайцев, О.С. Психопатология тяжелой черепно-мозговой травмы: дис. …д-р. мед. наук - М., 2004. - 50 с.
- Зотов, Ю.В. Клиническая диагностика гипертензионно-дислокационного синдрома и дифференцированная тактика хирургического лечения пострадавших с черепно-мозговой травмой // Ю.В. Зотов, Р.Д. Касумов, Ю.П. Лапшинов. – СПб.: Изд-во РНХИ им. проф. А.Л. Поленова, 1991. – С. 4-6.
- Зотов, Ю.В. Очаги размозжения головного мозга // Ю.В. Зотов, Р.Д. Касумов, Исмаил Тауфик.. – СПб.: 1996. - С. 40.
- Кондратьева, Е.А. Вегетативное состояние: диагностика, интенсивная терапия, терапия, прогнозирование исхода: дис. … канд. мед. - СПб., 2004. - 21 с.
- Коновалов, А.Н. Градация тяжести состояния пострадавших с черепно-мозговой травмой и унифицированные критерии для их определения // Вопр. нейрохир. - 1982. - № 5. - С. 11- 17.
- Климаш, А.В. Особенности клиники, диагностики и хирургического лечения травматических поражений ствола головного мозга: дис. … канд. мед. наук - СПб., 2005. - 24 с.
- Климаш, А.В. Применение чрезликворной электростимуляции у пациентов с тяжелой черепно-мозговой травмой // VII международный симпозиум «Новые технологии в нейрохирургии». - СПб, 2004. - С. 36-37.
- Ф. Плам, Дж.Б. Познер Диагностика ступора и комы . - 3 изд. - М.: Медицина, 1986. - 544 с.
- Шарова, Е. В. ЭЭГ-эффекты лечебной электростимуляции головного мозга человека при посттравматическом бессознательном // Физиология человека. – 2001. – Т. 27. - № 2 - С. 29 – 39.
- Bricolo A. prolonged posttraumatic unconsciousness. // Neurosurg. - 1980. - V. 52. - p. 625-634.
- Deliac, p. Electrphysiological development under thalamic stimulation of posttraumatic patients // Neurochirurgie. - 1993. - Vol. 39. - № 5. - p. 293.
- Funahashi, K. Spinal cord stimulation on vegetative state – a study of optimal stimulation using EEG – mapping // proceeding of the 2 – st annual meeting of the Society for Treatment of Coma. - Kyoto: 1993. - Vol. 2. - p. 51.
- Jennett B. Assessment of Outcome After Severe Brain Damage // Practical Scale. - Lancet: 1975. - № 1. - Р. 480-484.
- Joy, M.L.G. Low Frequency Current Density Imaging in Rabbits // Annals of Biomedical Engineering. - 1993. - Vol. 21. - №56. - P. 36-41.
- Machne X., Calma I., Magoun H.W. Unit activity of central cephalic brain stem in EEG arousal // J. Neurophysiol. - 1955. - V. 18. - P. 547.
- Marshall LF. The outcome of severe closed head injury // J. Neurosurg. - 1991. - V.75. - P. 28-36.
- Moruzzi G., Magoun H.W. Brain stem reticular formation and activation of EEG // EEG a. Clin. Neurophysiol. - 1949. - V. 1. - P. 455.
- Matsui, T. Clinical experience of spinal cord stimulation in an attempt of treatment of patients with prolonged // Proccedings of the 1-st annual meeting of the Society for trestment of coma. - Kyoto: 1992. - Vol. 1. - P. 107.
- Nieuwenhuys, R. The human central nervous system // 2nd Ed. Berlin-Heidelberg. - New York: Springer Verlag, 1981. - P. 389.
- ohira, T. Effects of spinal cord stimulation on vegetative state // Proceedings of the 1-st annual meeting of the Society for Treatment of Coma. - Kyoto: 1992. - Vol. 1. - P. 101.
- Purpura D.P. A neurogumoral mechanism of reticulo-cortical activation // Am. J. Physiol. - 1956. - V. 186, - P. 250.
- Reynolds, D.V. Voltage Distribution in the Brain during Diffusely Applied Electrical Current in the // In: Neuroelectric Research, Eds. Reynolds D. V., Sjoberg A.E., Thomas C. - Springfield: 1971. - P. 290 - 299.
- Sazbon L. outcome in 134 patients with prolonged posttraumatic unawareness // J. Neurosurg. - 1990. - V. 72. - P. 75-80.
- Takizawa, T. High cervical medullary electric stimulation therapy for prolonged disturbance of cansciousness after diffuse axonal injury // Proceedings of the 1-st annual meeting of the Society for Treatment of Coma. - Kyoto: 1992. - Vol. 1. - P. 107.
- Tsubokawa T. Deep - brain stimulation in a persistent vegetative state: follow - up results and criteria for selection of candidates // Brain Injury. - 1990. - Vol. 4. - P. 315-327.
- Tsubokawa, T. Deep brain stimulation therapy for a persistent vegetative state // J.of Neurotrauma. - 1995. - V. 12. - № 3. - P. 345.